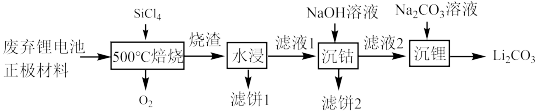
1 . 近几年新能源汽车呈现爆发式增长,对于锂电池的需求量越来越大,而碳酸锂是锂电池的重要原料之一,对废旧锂离子电池进行资源化和无害化处理具有重要的经济和环境效益,利用SiCl4对废弃的锂电池正极材料LiCoO2)进行氧化处理以回收Li等金属的工艺流程如下:
(1)Co在元素周期表的位置是___________ ,Co2+与Co3+的未成对电子数之比为___________ 。
(2)“烧渣”是LiCl、CoCl2和SiO2的混合物。“ 焙烧”反应生成的氧化产物与还原产物的物质的量之比为
焙烧”反应生成的氧化产物与还原产物的物质的量之比为___________ 。
(3)“滤饼2”的主要成分为___________ (填化学式)。利用Li2CO3与CoCO3按n(Li):n(Co)=1:1的比例配合,然后在空气中于 烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为
烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为___________ 。
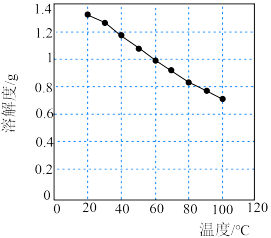
(4)碳酸锂的溶解度随温度变化如图所示。向滤液2中加入Na2CO3溶液,将温度升至90℃是为了提高沉淀反应速率和___________ 。得到碳酸锂沉淀的操作为___________ (填标号)。
(5)常温下,取 “滤液2”,其中
“滤液2”,其中 ,为使锂元素的回收率不低于
,为使锂元素的回收率不低于 ,则至少应加入
,则至少应加入 固体的质量为
固体的质量为___________ g[已知常温下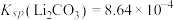 。计算结果保留3位小数。
。计算结果保留3位小数。
(6)由 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。 在晶胞中的位置为
在晶胞中的位置为___________ 。
② 晶体的密度为
晶体的密度为 ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为___________ nm(列出计算式,阿伏加德罗常数的值为 )。
)。
(1)Co在元素周期表的位置是
(2)“烧渣”是LiCl、CoCl2和SiO2的混合物。“
 焙烧”反应生成的氧化产物与还原产物的物质的量之比为
焙烧”反应生成的氧化产物与还原产物的物质的量之比为(3)“滤饼2”的主要成分为
 烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为
烧结可合成锂电池正极材料LiCoO2,反应的化学方程式为(4)碳酸锂的溶解度随温度变化如图所示。向滤液2中加入Na2CO3溶液,将温度升至90℃是为了提高沉淀反应速率和
(5)常温下,取
 “滤液2”,其中
“滤液2”,其中 ,为使锂元素的回收率不低于
,为使锂元素的回收率不低于 ,则至少应加入
,则至少应加入 固体的质量为
固体的质量为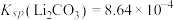 。计算结果保留3位小数。
。计算结果保留3位小数。(6)由
 进一步制得的
进一步制得的 具有反萤石结构,晶胞如图所示。
具有反萤石结构,晶胞如图所示。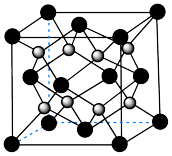
 在晶胞中的位置为
在晶胞中的位置为②
 晶体的密度为
晶体的密度为 ,则晶胞参数(棱长)为
,则晶胞参数(棱长)为 )。
)。
您最近半年使用:0次
2 . 在苯甲酸重结晶与粗盐提纯的实验操作过程中,均不需要用到的玻璃仪器为
| A.烧杯 | B.玻璃棒 | C.漏斗 | D.温度计 |
您最近半年使用:0次
名校
3 . 高纯二氧化硅是一种纯度极高的精细化工产品。一种利用氟硅酸( )制备高纯
)制备高纯 的工艺流程如图所示,请回答下列问题:
的工艺流程如图所示,请回答下列问题:
②“制备 ”时发生的反应为
”时发生的反应为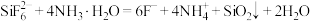 。
。
(1)氨水中含有的分子有 、
、________ (填化学式);“中和”时发生反应的化学方程式为________ ;“制备 ”时,常常加热至60℃以加快反应速率,不选择更高温度的原因可能是
”时,常常加热至60℃以加快反应速率,不选择更高温度的原因可能是________ 。
(2)“过滤分离”所得的滤液中,溶质的主要成分属于盐类的是________ (填化学式);“水洗”时,将滤饼放入烧杯中,加蒸馏水,搅拌热洗1h,减压抽滤(装置如图所示)分离,重复操作两到三次,下列说法正确的是________ (填标号)。
B.带磨口玻璃塞的试剂瓶常用于盛装强酸溶液、强碱溶液
C.“水洗”时,热水洗涤的目的是提高滤饼表面部分杂质的溶解度和溶解速率,提高洗涤效果
D.与普通过滤操作相比,“减压抽滤”可加快过滤速度,并获得较干燥的固体
E.“水洗”时,往最后一次洗涤液中滴加NaOH溶液,试管口放置的湿润的红色石蕊试纸不变蓝,说明滤饼已经洗涤干净
(3)“煅烧”时的温度控制在1000~1300℃之间,以降低产物中杂质含量。“煅烧”需要用到的仪器有________ (填标号);某工厂用2.4吨氟硅酸(其余试剂均过量)按上述方法制备高纯二氧化硅,最终获得0.95吨高纯二氧化硅(纯度视为100%),则 的产率为
的产率为________ (产率= )。
)。
 )制备高纯
)制备高纯 的工艺流程如图所示,请回答下列问题:
的工艺流程如图所示,请回答下列问题:
②“制备
 ”时发生的反应为
”时发生的反应为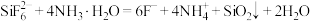 。
。(1)氨水中含有的分子有
 、
、 ”时,常常加热至60℃以加快反应速率,不选择更高温度的原因可能是
”时,常常加热至60℃以加快反应速率,不选择更高温度的原因可能是(2)“过滤分离”所得的滤液中,溶质的主要成分属于盐类的是

B.带磨口玻璃塞的试剂瓶常用于盛装强酸溶液、强碱溶液
C.“水洗”时,热水洗涤的目的是提高滤饼表面部分杂质的溶解度和溶解速率,提高洗涤效果
D.与普通过滤操作相比,“减压抽滤”可加快过滤速度,并获得较干燥的固体
E.“水洗”时,往最后一次洗涤液中滴加NaOH溶液,试管口放置的湿润的红色石蕊试纸不变蓝,说明滤饼已经洗涤干净
(3)“煅烧”时的温度控制在1000~1300℃之间,以降低产物中杂质含量。“煅烧”需要用到的仪器有
 的产率为
的产率为 )。
)。
您最近半年使用:0次
4 . 下列实验操作能达到实验目的的是
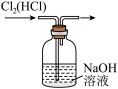 | 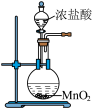 | 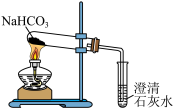 | 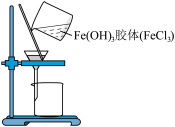 |
| A.提纯Cl2 | B.制备Cl2 | C. 证明NaHCO3受热分解 | D.提纯Fe(OH)3胶体 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
名校
解题方法
5 .  是生活中常用的消毒剂。工业制备方法之一为
是生活中常用的消毒剂。工业制备方法之一为
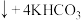 ,下列叙述正确的是
,下列叙述正确的是
 是生活中常用的消毒剂。工业制备方法之一为
是生活中常用的消毒剂。工业制备方法之一为
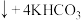 ,下列叙述正确的是
,下列叙述正确的是A. 是该反应的催化剂 是该反应的催化剂 |
| B.氧化剂、还原剂的物质的量之比为2∶1 |
C.锰酸钾在水中的电离方程式: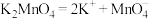 |
D.实验结束,可以采用“过滤”操作分离出 |
您最近半年使用:0次
2024-03-22更新
|
84次组卷
|
2卷引用:河北省沧州市2023-2024学年高一上学期12月联考化学试题
名校
解题方法
6 . 由含硒废料(主要含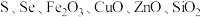 等)制取硒的流程如下:
等)制取硒的流程如下:
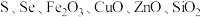 等)制取硒的流程如下:
等)制取硒的流程如下: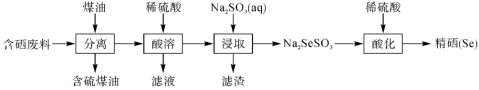

| A.流程中的“分离”的方法是过滤 |
B.“滤液”中主要存在的阴离子是 |
C.“酸化”时发生反应的离子方程式为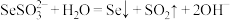 |
D. 晶胞如上图所示,1个 晶胞如上图所示,1个 晶胞中有16个 晶胞中有16个 原子 原子 |
您最近半年使用:0次
2024-03-03更新
|
175次组卷
|
2卷引用:河北省衡水董子高级中学等校2023-2024学年高三下学期2月 入校考试 化学试题
名校
解题方法
7 . 下列实验操作中选用仪器正确的是
| A | B | C | D |
 |  |  |  |
| 量取10.00mL盐酸 | 配制一定物质的量浓度的NaCl溶液 | 分离乙醇和水的混合物 | 分离碘和四氯化碳的混合物 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2024-02-26更新
|
80次组卷
|
2卷引用:河北省唐山市2023-2024学年高一上学期1月期末考试化学试题
8 . 我国传统酿老陈醋工艺的主要步骤有蒸、酵、沥、陈。
蒸——将大米、高粱、小米等原料蒸熟后放至冷却;
酵——拌酶曲入坛发酵,经糖化、成醇后,在醋酸菌作用下成酸;
沥——除去糟,闻到酒、醋香味;
陈——陈放1~3年,闻到果香味。
上述主要步骤中,涉及过滤操作的是
蒸——将大米、高粱、小米等原料蒸熟后放至冷却;
酵——拌酶曲入坛发酵,经糖化、成醇后,在醋酸菌作用下成酸;
沥——除去糟,闻到酒、醋香味;
陈——陈放1~3年,闻到果香味。
上述主要步骤中,涉及过滤操作的是
| A.“蒸” | B.“酵” | C.“沥” | D.“陈” |
您最近半年使用:0次
9 . 下列混合物的分离(或除杂)方法正确的是
| A.除去 FeCl2溶液中混有的FeCl3:加入足量Cu粉后,过滤 |
| B.除去KCl中的MnO2:加入水中充分溶解,过滤、洗涤、干燥 |
| C.除去 CO2中的CO:与足量氧气混合后点燃 |
| D.除去 Fe2O3中的Al2O3:加入过量氢氧化钠溶液,过滤、洗涤、干燥 |
您最近半年使用:0次
名校
解题方法
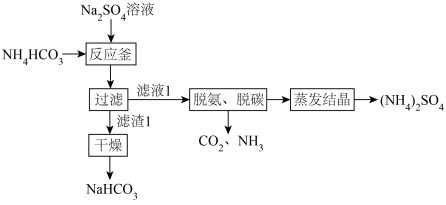
10 . 一种以芒硝和碳酸氢铵为原料联合生产 和
和 的方法如图所示,反应釜中发生的反应为复分解反应。已知
的方法如图所示,反应釜中发生的反应为复分解反应。已知 在60℃可迅速分解,
在60℃可迅速分解, 在100℃以上会缓慢分解,下列说法错误的是
在100℃以上会缓慢分解,下列说法错误的是
 和
和 的方法如图所示,反应釜中发生的反应为复分解反应。已知
的方法如图所示,反应釜中发生的反应为复分解反应。已知 在60℃可迅速分解,
在60℃可迅速分解, 在100℃以上会缓慢分解,下列说法错误的是
在100℃以上会缓慢分解,下列说法错误的是
| A.实验室进行过滤操作时,需要用到漏斗、烧杯、玻璃棒 |
B.“干燥”获取 时,可采用常温风干的方法 时,可采用常温风干的方法 |
| C.“脱氨、脱碳”的温度需控制在100℃以上 |
D.可以用稀盐酸来区分 和 和 |
您最近半年使用:0次
2023-12-01更新
|
69次组卷
|
2卷引用:河北省邢台市质检联盟2023-2024学年高一上学期11月月考化学试题



