解题方法
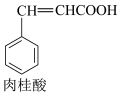
1 . 肉桂酸是白色单斜晶体,在生产生活中有重要应用。实验室常用如下方法制备肉桂酸:


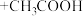
实验步骤:
【步骤1】分别量取6.0mL苯甲醛和12.0mL的乙酸酐 于100mL干燥的圆底烧瓶中,再加入少许无水碳酸钾,加热回流45分钟。
于100mL干燥的圆底烧瓶中,再加入少许无水碳酸钾,加热回流45分钟。
【步骤2】反应结束,趁热迅速转入长颈圆底烧瓶(水蒸气蒸馏用)中,进行水蒸气蒸馏。
【步骤3】蒸馏一段时间后,将长颈圆底烧瓶中的剩余物转入烧杯中,冷却,加入约30mL10%氢氧化钠溶液中和至溶液呈碱性。
【步骤4】再加入一定量水,并加入适量活性炭,煮沸5min,趁热过滤。滤液冷却后,用稀盐酸酸化至酸性,冷却,待晶体全部析出后抽滤,洗涤沉淀,抽干后,粗产品在80℃烘箱中烘干,得产品7.548g。
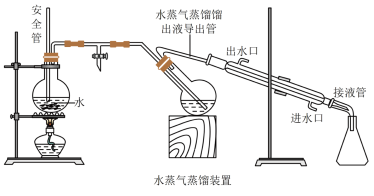
已知:①水蒸气蒸馏的原理是将水蒸气通入有机混合物中,使易挥发的有机成分随水蒸气一起被蒸馏出来,从而达到分离提纯的目的,装置如图所示。
②相关物质的性质如下表:
回答下列问题:
(1)安全管的作用是___________ 。
(2)步骤2中水蒸气蒸馏的目的是___________ 。
(3)步骤3中加氢氧化钠发生反应的主要化学方程式为___________ 。
(4)步骤4中抽滤按如图所示装置,经过一系列操作完成抽滤,请选择合适的编号,按正确的操作顺序补充完整___________ 。

在布氏漏斗中加入润湿的滤纸→微开水龙头→___________→___________→___________→___________。
①开大水龙头;②转移固液混合物;③关闭水龙头;④确认抽干
(5)简述步骤4中沉淀洗涤的方法:___________ 。
(6)该实验采用“抽滤”,与普通过滤相比,“抽滤”的优点是___________ 。
(7)该实验所得肉桂酸的产率为___________ 。



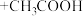
实验步骤:
【步骤1】分别量取6.0mL苯甲醛和12.0mL的乙酸酐
 于100mL干燥的圆底烧瓶中,再加入少许无水碳酸钾,加热回流45分钟。
于100mL干燥的圆底烧瓶中,再加入少许无水碳酸钾,加热回流45分钟。【步骤2】反应结束,趁热迅速转入长颈圆底烧瓶(水蒸气蒸馏用)中,进行水蒸气蒸馏。
【步骤3】蒸馏一段时间后,将长颈圆底烧瓶中的剩余物转入烧杯中,冷却,加入约30mL10%氢氧化钠溶液中和至溶液呈碱性。
【步骤4】再加入一定量水,并加入适量活性炭,煮沸5min,趁热过滤。滤液冷却后,用稀盐酸酸化至酸性,冷却,待晶体全部析出后抽滤,洗涤沉淀,抽干后,粗产品在80℃烘箱中烘干,得产品7.548g。
已知:①水蒸气蒸馏的原理是将水蒸气通入有机混合物中,使易挥发的有机成分随水蒸气一起被蒸馏出来,从而达到分离提纯的目的,装置如图所示。
②相关物质的性质如下表:
| 名称 | 相对分子质量 | 密度g/mL | 熔点℃ | 沸点℃ | 溶解度 |
| 苯甲醛 | 106 | 1.06 | -26 | 179.6 | 微溶于水,可溶于乙醇、乙醚等 |
| 乙酸酐 | 102 | 1.08 | -73.1 | 138.6 | 缓慢地溶于水形成乙酸 |
| 肉桂酸 | 148 | 1.25 | 135 | 300 | 不溶于冷水,可溶于乙醇、乙醚 |

回答下列问题:
(1)安全管的作用是
(2)步骤2中水蒸气蒸馏的目的是
(3)步骤3中加氢氧化钠发生反应的主要化学方程式为
(4)步骤4中抽滤按如图所示装置,经过一系列操作完成抽滤,请选择合适的编号,按正确的操作顺序补充完整

在布氏漏斗中加入润湿的滤纸→微开水龙头→___________→___________→___________→___________。
①开大水龙头;②转移固液混合物;③关闭水龙头;④确认抽干
(5)简述步骤4中沉淀洗涤的方法:
(6)该实验采用“抽滤”,与普通过滤相比,“抽滤”的优点是
(7)该实验所得肉桂酸的产率为
您最近半年使用:0次
解题方法
2 . 次磷酸钠(NaH2PO2)在食品工业中用作防腐剂、抗氧化剂,也是一种很好的化学镀剂。
(1)NaH2PO2中P的化合价为_____ 。
(2)将待镀零件浸泡在NiSO4和NaH2PO2的混合溶液中,可达到化学镀镍的目的,该过程中H2PO 被氧化为二元弱酸H3PO3,写出该反应的离子方程式
被氧化为二元弱酸H3PO3,写出该反应的离子方程式_____ 。
(3)次磷酸钠的制备将黄磷(P4)和过量烧碱溶液混合加热,生成NaH2PO2和PH3(气体),PH3与NaClO溶液反应可生成次磷酸(H3PO2),实验装置如图:
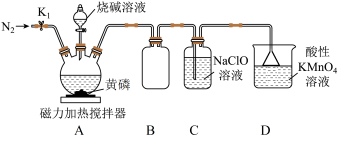
①装置A中盛放烧碱溶液的仪器名称为_____ 。
②装置B的作用为_____ 。
③装置C中发生反应的化学方程式为_____ 。
④已知相关物质的溶解度如表:
充分反应后,将A、C中溶液混合,再将混合液(含极少量NaOH)加热浓缩,有大量杂质晶体析出,然后_____ (填操作名称),得到含NaH2PO2的溶液,进一步处理得到粗产品。
(4)产品纯度的计算
取1.00g粗产品配成100mL溶液,取25.00mL于锥形瓶中,酸化后加入30.00mL0.100mol•L-1碘水,充分反应。然后以淀粉溶液作指示剂,用0.100mol•L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液24.00mL,有关反应的方程式为:H2PO +H2O+I2=H2PO
+H2O+I2=H2PO +2H++2I—,2S2O
+2H++2I—,2S2O +I2=S4O
+I2=S4O +2I-,则产品纯度为
+2I-,则产品纯度为_____ (NaH2PO2式量88)。
(1)NaH2PO2中P的化合价为
(2)将待镀零件浸泡在NiSO4和NaH2PO2的混合溶液中,可达到化学镀镍的目的,该过程中H2PO
 被氧化为二元弱酸H3PO3,写出该反应的离子方程式
被氧化为二元弱酸H3PO3,写出该反应的离子方程式(3)次磷酸钠的制备将黄磷(P4)和过量烧碱溶液混合加热,生成NaH2PO2和PH3(气体),PH3与NaClO溶液反应可生成次磷酸(H3PO2),实验装置如图:

①装置A中盛放烧碱溶液的仪器名称为
②装置B的作用为
③装置C中发生反应的化学方程式为
④已知相关物质的溶解度如表:
| 溶解度/g 物质 | 25℃ | 100℃ |
| NaCl | 37 | 39 |
| NaH2PO2 | 100 | 667 |
(4)产品纯度的计算
取1.00g粗产品配成100mL溶液,取25.00mL于锥形瓶中,酸化后加入30.00mL0.100mol•L-1碘水,充分反应。然后以淀粉溶液作指示剂,用0.100mol•L-1Na2S2O3溶液滴定至终点,消耗Na2S2O3溶液24.00mL,有关反应的方程式为:H2PO
 +H2O+I2=H2PO
+H2O+I2=H2PO +2H++2I—,2S2O
+2H++2I—,2S2O +I2=S4O
+I2=S4O +2I-,则产品纯度为
+2I-,则产品纯度为
您最近半年使用:0次
3 . 2021年10月河南省地矿局发现一特大型金矿。下图为纯化黄金(纯度>90%,含铁、铜化合物等杂质)的工艺流程图。下列说法不正确的是


A.往四氯金酸中加入 溶液,当 溶液,当 被氧化时,反应转移1.5mol电子 被氧化时,反应转移1.5mol电子 |
B.王水溶金生成 和NO的化学方程式为 和NO的化学方程式为 |
| C.实验室进行操作A用到的玻璃仪器有漏斗、玻璃棒、烧杯 |
| D.操作A所得金粉会吸附铁的化合物,加盐酸的目的是为了将吸附的杂质溶解除去 |
您最近半年使用:0次
2022-04-11更新
|
622次组卷
|
4卷引用:湖南省新高考教学教研联盟2021-2022学年高三下学期第二次联考化学试题
4 . 锌电解阳极泥(主要成分为MnO2、PbSO4和ZnO,还有少量锰铅氧化物Pb2Mn8O16和Ag)是冶锌过程中产生的废渣,一种回收锌电解阳极泥中金属元素锌、锰、铅和银的工艺如图。回答下列问题:

已知:①MnSO4∙H2O易溶于水,不溶于乙醇。
②在较高温度及酸性催化条件下,葡萄糖能发生如下反应:

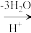
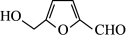

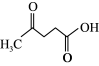 +HCOOH
+HCOOH
(1)已知Pb2Mn8O16中Pb为+2价,Mn为+2价和+4价,则氧化物中+2价和+4价Mn的个数比为____ 。
(2)“还原酸浸”过程中主要反应的离子方程式为____ 。
(3)实际锰浸出最适宜的葡萄糖加入量远大于理论加入量,其原因是____ ,为提高葡萄糖的有效利用率,除充分搅拌外还可采取的措施为____ 。
(4)整个流程中可循环利用的物质是____ 。获得MnSO4∙H2O晶体的一系列操作是指蒸发结晶、趁热过滤、洗涤、干燥,其中洗涤的具体操作是____ 。
(5)加入Na2CO3溶液的目的是将PbSO4转化为PbCO3,Na2CO3溶液的最小浓度为____ mol·L–1(保留两位小数)。判断沉淀转化能否彻底进行并说明理由____ 。[已知:20℃时Ksp(PbSO4)=1.6×10-8mol2·L-2,Ksp(PbCO3)=7.4×10-14mol2·L-2,1.262≈1.6]

已知:①MnSO4∙H2O易溶于水,不溶于乙醇。
②在较高温度及酸性催化条件下,葡萄糖能发生如下反应:

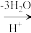


 +HCOOH
+HCOOH(1)已知Pb2Mn8O16中Pb为+2价,Mn为+2价和+4价,则氧化物中+2价和+4价Mn的个数比为
(2)“还原酸浸”过程中主要反应的离子方程式为
(3)实际锰浸出最适宜的葡萄糖加入量远大于理论加入量,其原因是
(4)整个流程中可循环利用的物质是
(5)加入Na2CO3溶液的目的是将PbSO4转化为PbCO3,Na2CO3溶液的最小浓度为
您最近半年使用:0次
2022-03-12更新
|
1156次组卷
|
5卷引用:山东省烟台市、德州市2021-2022学年下学期高三一模化学试题
解题方法
5 . 天然气是绿色、优质的能源。开采的天然气中通常会含有杂质H2S和CO2。实验室利用如下装置除去杂质并测定H2S的含量。

已知: FeS 难溶于水可溶于稀硫酸,CuS 既不溶于水又不溶于稀硫酸。
可供选择的试剂有: FeSO4溶液、CuSO4溶液、NaOH溶液、NaCl溶液。
回答下列问题:
(1)A中的试剂是___________ 。
(2)为测量H2S的含量,停止通气后,对洗气瓶中混合物应进行的操作是___________ 、______ 、干燥、称量。其中第一步操作用到的玻璃仪器有玻璃棒、烧杯、___________ 。
(3)若通入22.4L标准状况下的气体,测得生成3.84g沉淀, 则此天然气中H2S的体积分数为___________ %。
(4)室温下,氢硫酸(H2S)和碳酸的电离平衡常数如下表所示:
H2S与碳酸钠溶液反应的化学方程式是________ ,是否能用碳酸钠溶液替代A中的试剂?___________ (填“是”或“否”)。原因是________ 。
(5)工业上也可使用醇胺吸收H2S, 反应原理为(HOCH2CH2)2NH+H2S=(HOCH2CH2)2NH2HS,上述反应说明(HOCH2CH2)2NH中,___________ (填基团结构简式)具有碱性。

已知: FeS 难溶于水可溶于稀硫酸,CuS 既不溶于水又不溶于稀硫酸。
可供选择的试剂有: FeSO4溶液、CuSO4溶液、NaOH溶液、NaCl溶液。
回答下列问题:
(1)A中的试剂是
(2)为测量H2S的含量,停止通气后,对洗气瓶中混合物应进行的操作是
(3)若通入22.4L标准状况下的气体,测得生成3.84g沉淀, 则此天然气中H2S的体积分数为
(4)室温下,氢硫酸(H2S)和碳酸的电离平衡常数如下表所示:
| Kal | Ka2 | |
| H2S | 1.1×10-7 | 1.3×10-13 |
| H2CO3 | 4.5×107 | 4.7×10-11 |
(5)工业上也可使用醇胺吸收H2S, 反应原理为(HOCH2CH2)2NH+H2S=(HOCH2CH2)2NH2HS,上述反应说明(HOCH2CH2)2NH中,
您最近半年使用:0次
名校
6 . 某工厂的工业废水中含有大量的 和
和 ,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收
,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收 和金属
和金属 。请回答相关问题:
。请回答相关问题:
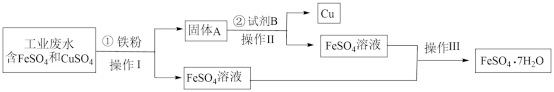
(1)操作I分离方法的名称是___________ 。
(2)实验室模拟操作II使用的主要玻璃仪器有___________ 种。
(3)为得到纯净的铜需要进行洗涤,请简述如何证明洗涤干净___________ 。
(4)从 溶液中得到
溶液中得到 的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为
的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为___________ 。
(5)流程图中, 溶液只含有
溶液只含有 而不含
而不含 ,可证明该事实的实验方法是
,可证明该事实的实验方法是______ (填序号)。
①先加氯水,后加 溶液后显红色
溶液后显红色
②先加 溶液,不显红色,再加氯水后显红色
溶液,不显红色,再加氯水后显红色
③只滴加 溶液不显红色
溶液不显红色
 和
和 ,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收
,为了减少污染并变废为宝,工厂拟定用以下流程从该废水中回收 和金属
和金属 。请回答相关问题:
。请回答相关问题:
(1)操作I分离方法的名称是
(2)实验室模拟操作II使用的主要玻璃仪器有
(3)为得到纯净的铜需要进行洗涤,请简述如何证明洗涤干净
(4)从
 溶液中得到
溶液中得到 的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为
的操作是加热浓缩→冷却结晶→过滤→洗涤,该过程特别需要注意的事项为(5)流程图中,
 溶液只含有
溶液只含有 而不含
而不含 ,可证明该事实的实验方法是
,可证明该事实的实验方法是①先加氯水,后加
 溶液后显红色
溶液后显红色②先加
 溶液,不显红色,再加氯水后显红色
溶液,不显红色,再加氯水后显红色③只滴加
 溶液不显红色
溶液不显红色
您最近半年使用:0次
2022-01-24更新
|
138次组卷
|
2卷引用:山东省枣庄滕州市2021-2022学年高一上学期期末考试化学试题
解题方法
7 . 银系列产品广泛地应用于化工、电子电镀材料和工业催化等领域。与原矿相比,含银废料中银含量较高,成分单一,回收简单,污染少。从含银废料中(主要含Ag,其他金属微量,忽略不计)回收银已成为各国贵金属银系列产品的重要来源。下图为从含银废料中回收并制得纯Ag的工业流程。回答下列问题:

(1)N2H4的电子式为_______ 。
(2)操作I的名称为_______ ,简述利用“操作I”的装置洗涤难溶物的实验操作:_______ 。
(3)还原过程中的氧化产物为环境友好产物,请补充并配平还原过程的化学方程式:_______ 。
 _____=_____
_____=_____ _____
_____

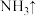
(4)已知: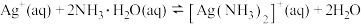 的平衡常数
的平衡常数 ;
; 的
的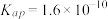 。写出
。写出 溶于氨水的离子方程式:
溶于氨水的离子方程式:_______ ,该反应的平衡常数K=_______ 。在氯化银溶于氨水后的溶液中滴加稀硝酸,会再产生白色氯化银沉淀,原因是_______ 。
(5)工业上经常会用过量的NaClO溶液替代HNO3在80℃条件下氧化单质银,产物为 、NaOH和O2用NaClO溶液替换HNO3溶液的好处是
、NaOH和O2用NaClO溶液替换HNO3溶液的好处是_______ 。

(1)N2H4的电子式为
(2)操作I的名称为
(3)还原过程中的氧化产物为环境友好产物,请补充并配平还原过程的化学方程式:
 _____=_____
_____=_____ _____
_____

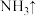
(4)已知:
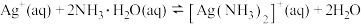 的平衡常数
的平衡常数 ;
; 的
的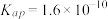 。写出
。写出 溶于氨水的离子方程式:
溶于氨水的离子方程式:(5)工业上经常会用过量的NaClO溶液替代HNO3在80℃条件下氧化单质银,产物为
 、NaOH和O2用NaClO溶液替换HNO3溶液的好处是
、NaOH和O2用NaClO溶液替换HNO3溶液的好处是
您最近半年使用:0次
解题方法
8 . 硫酸镍(NiSO4)主要用于电镀工业,是电镀镍和化学镍的主要镍盐。某矿渣的主要成分是NiFe2O4(铁酸镍)、NiO、FeO、CaO、SiO2等,从该矿渣中回收NiSO4的工艺流程如下:

(1)“焙烧”时发生多个反应,其中NiFe2O4生成NiSO4、Fe2(SO4)3,发生该反应的化学方程式为___________ 。
(2)“浸泡”时用“95℃热水”的目的是___________ ,“浸泡”过程中Fe2(SO4)3生成FeO(OH)的离子方程式为___________ 。
(3)“浸渣”的成分除Fe2O3、FeO(OH)外还含有___________ (填化学式),为检验浸出液中是否含有Fe3+,可选用的化学试剂是___________ 。
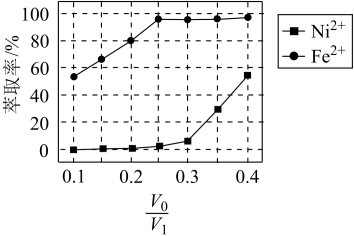
(4)“萃取"过程中发生反应Fe2+(水相)+2RH(有机相) FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如下图所示,V0/VA的最佳取值为
FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如下图所示,V0/VA的最佳取值为___________ ;在___________ (填“强碱性”“强酸性”或“中性”)介质中“反萃取”能使有机相再生而循环利用。

(1)“焙烧”时发生多个反应,其中NiFe2O4生成NiSO4、Fe2(SO4)3,发生该反应的化学方程式为
(2)“浸泡”时用“95℃热水”的目的是
(3)“浸渣”的成分除Fe2O3、FeO(OH)外还含有
(4)“萃取"过程中发生反应Fe2+(水相)+2RH(有机相)
 FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如下图所示,V0/VA的最佳取值为
FeR(有机相)+2H+(水相)。萃取剂与溶液的体积比(V0/VA)对溶液中Ni2+、Fe2+的萃取率影响如下图所示,V0/VA的最佳取值为
您最近半年使用:0次
解题方法
9 . 过氧化钙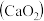 是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备
是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备 过程如下。
过程如下。
Ⅰ.制备
利用反应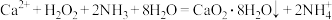 ,在碱性环境下制取
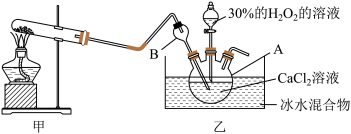
,在碱性环境下制取 的装置如图:
的装置如图:
(1) 的电子式为
的电子式为_______ 。
(2)写出甲装置中反应的化学方程式_______ 。
(3)仪器A的名称为_______ ;仪器B的作用是_______ 。
(4)乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低有利于提高 的产率和
的产率和_______ 。
(5)反应结束后,分离提纯 的过程中,洗涤的操作为
的过程中,洗涤的操作为_______ 。
Ⅱ.制得产品并定量检测
(6) 脱水干燥即得
脱水干燥即得 产品。经检测知某
产品。经检测知某 产品中含有
产品中含有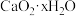 和
和 ,已知
,已知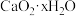 受热分解有
受热分解有 、
、 和
和 生成。①称取
生成。①称取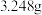 产品,加热,在标准状况下生成
产品,加热,在标准状况下生成 气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的
气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的 溶液得到沉淀
溶液得到沉淀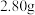 ,则该产品中
,则该产品中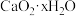 的x值为
的x值为_______ 。
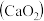 是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备
是一种用途广泛的优良供氧剂,常温下为白色固体,能溶于酸,难溶于水、乙醇,且本身无毒,不污染环境,某实验小组制备 过程如下。
过程如下。Ⅰ.制备

利用反应
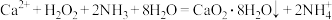 ,在碱性环境下制取
,在碱性环境下制取 的装置如图:
的装置如图:
(1)
 的电子式为
的电子式为(2)写出甲装置中反应的化学方程式
(3)仪器A的名称为
(4)乙中反应温度需控制在0℃左右的原因是该反应是放热反应,温度低有利于提高
 的产率和
的产率和(5)反应结束后,分离提纯
 的过程中,洗涤的操作为
的过程中,洗涤的操作为Ⅱ.制得产品并定量检测
(6)
 脱水干燥即得
脱水干燥即得 产品。经检测知某
产品。经检测知某 产品中含有
产品中含有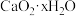 和
和 ,已知
,已知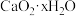 受热分解有
受热分解有 、
、 和
和 生成。①称取
生成。①称取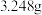 产品,加热,在标准状况下生成
产品,加热,在标准状况下生成 气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的
气体。②另取等量产品,溶于适量的稀盐酸后,加入足量的 溶液得到沉淀
溶液得到沉淀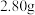 ,则该产品中
,则该产品中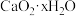 的x值为
的x值为
您最近半年使用:0次
解题方法
10 . 镁将成为21世纪重要的轻型环保材料。
(1)海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
海水中MgCl2 →Mg(OH)2→ MgCl2•6H2O →MgCl2→ Mg
①在实验室进行过滤操作时需要用到玻璃棒,其作用是___________ 。
②电解熔融氯化镁的过程中,___________ 能转化为___________ 能。
(2)①金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧。燃烧的化学方程式为2Mg+CO2=C+2MgO,此反应类型属于___________
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
②金属镁在高温下与氮气反应生成氮化镁,在氮化镁中氮元素的化合价为﹣3.据此写出氮化镁的化学式___________ 。
(3)镁铝合金广泛用于火箭、导弹和飞机制造业等。某兴趣小组为探究镁铝合金的组成,取16g镁铝合金样品,把60g氢氧化钠溶液平均分成三份依次加入样品中,充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
从以上数据可知,该合金中,镁元素与铝元素的质量比为___________ 。所用氢氧化钠溶液的溶质质量分数为___________ 。
(4)老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属。但拿出的镁条总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是MgO;小赵认为可能是 Mg2(OH)2CO3;小花认为可能是Mg(OH)2 。
小花认为小明的猜想是错误的,其理由是___________ 。
实验探究:小赵按如图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体。

实验分析:实验后,小赵认为小花的猜想也是错误的,其理由是___________ 。
查阅资料得出结论: Mg(OH)2和 Mg2(OH)2CO3都可以加热分解,产物均为氧化物,据此请你写出 Mg2(OH)2CO3加热分解的化学方程式___________ 。
(1)海洋是天然的镁元素宝库,从海水中提取镁的流程如下:
海水中MgCl2 →Mg(OH)2→ MgCl2•6H2O →MgCl2→ Mg
①在实验室进行过滤操作时需要用到玻璃棒,其作用是
②电解熔融氯化镁的过程中,
(2)①金属镁是一种较活泼金属,在二氧化碳气体中也能燃烧。燃烧的化学方程式为2Mg+CO2=C+2MgO,此反应类型属于
A.分解反应 B.化合反应 C.置换反应 D.复分解反应
②金属镁在高温下与氮气反应生成氮化镁,在氮化镁中氮元素的化合价为﹣3.据此写出氮化镁的化学式
(3)镁铝合金广泛用于火箭、导弹和飞机制造业等。某兴趣小组为探究镁铝合金的组成,取16g镁铝合金样品,把60g氢氧化钠溶液平均分成三份依次加入样品中,充分反应后,过滤出固体,将其洗涤、干燥、称量,得实验数据如下:
| 所加氢氧化钠溶液的次数 | 第一次 | 第二次 | 第三次 |
| 剩余固体的质量/g | 10.6 | 5.2 | 4.0 |
(4)老师每次做有关镁的实验时都会强调:镁是一种银白色有金属光泽的金属。但拿出的镁条总是有一层灰黑色的“外衣”,这层灰黑色的外衣是什么物质呢?
猜想:小明认为可能是MgO;小赵认为可能是 Mg2(OH)2CO3;小花认为可能是Mg(OH)2 。
小花认为小明的猜想是错误的,其理由是
实验探究:小赵按如图所示装置进行实验,发现试管口有液滴出现,澄清石灰水变浑浊,同时试管内生成白色固体。

实验分析:实验后,小赵认为小花的猜想也是错误的,其理由是
查阅资料得出结论: Mg(OH)2和 Mg2(OH)2CO3都可以加热分解,产物均为氧化物,据此请你写出 Mg2(OH)2CO3加热分解的化学方程式
您最近半年使用:0次



