1 . 硼酸( )是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含
)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含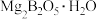 、
、 及少量
及少量 、
、 )为原料生产硼酸及轻质氧化镁的工艺流程如下:
)为原料生产硼酸及轻质氧化镁的工艺流程如下:
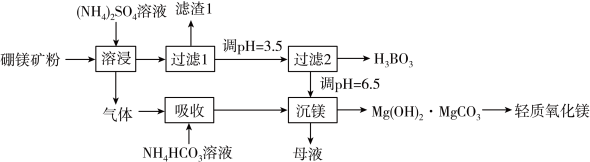
已知:
回答下列问题:
(1)在95℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式___________ 。
(2)“滤渣1”的主要成分有___________ (填化学式)。为检验“过滤1”后的滤液中是否含有 离子,可选用的化学试剂是
离子,可选用的化学试剂是___________ (填化学式)。
(3)已知 的电离方程式为
的电离方程式为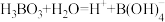 ,可知
,可知 为
为___________ 元弱酸,请写出 与足量
与足量 溶液反应的离子方程式
溶液反应的离子方程式___________ ;“过滤2”前,将溶液pH调节至3.5的目的是___________ 。
(4)“沉镁”后分离生成的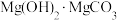 沉淀的操作为
沉淀的操作为___________ ,母液经加热后可返回___________ (填“溶浸”“吸收”或“沉镁”)工序循环使用。高温焙烧碱式碳酸镁可制备轻质氧化镁,写出化学方程式___________ 。
 )是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含
)是一种重要的化工原料,广泛应用于玻璃、医药、肥料等工艺。一种以硼镁矿(含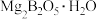 、
、 及少量
及少量 、
、 )为原料生产硼酸及轻质氧化镁的工艺流程如下:
)为原料生产硼酸及轻质氧化镁的工艺流程如下:
已知:

回答下列问题:
(1)在95℃“溶浸”硼镁矿粉,产生的气体在“吸收”中反应的化学方程式
(2)“滤渣1”的主要成分有
 离子,可选用的化学试剂是
离子,可选用的化学试剂是(3)已知
 的电离方程式为
的电离方程式为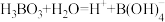 ,可知
,可知 为
为 与足量
与足量 溶液反应的离子方程式
溶液反应的离子方程式(4)“沉镁”后分离生成的
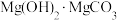 沉淀的操作为
沉淀的操作为
您最近一年使用:0次
名校
2 . 回答下列问题:
(1)控制变量法是化学实验的一种常用方法,如表是稀硫酸与某金属反应的实验数据。
分析上述数据,回答下列问题:
①V1=_____ mL,t1_____ 125(填“>”、“<”或“=”)。
②实验2和3的目的是_____ 。
(2)纯碳酸钙广泛应用于精密电子陶瓷、医药等的生产,某兴趣小组按图所示实验步骤,模拟工业流程制备高纯碳酸钙,请回答下列问题。
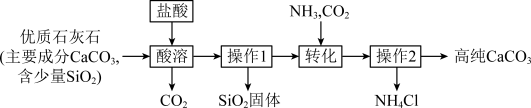
①“酸溶”过程中,提前将石灰石粉碎,并进行搅拌,目的是_____ ,“操作1”的名称_____ 。
②实验室制取、收集干燥的NH3

需选用上述仪器装置的接口连接顺序是(填字母):a接_____、_____接_____,_____接h。_____ 。
③制备碳酸钙通入NH3和CO2气体时,应先通入的气体是_____ ,写出流程中制碳酸钙的化学方程式_____ 。
(1)控制变量法是化学实验的一种常用方法,如表是稀硫酸与某金属反应的实验数据。
| 实验序号 | 金属质量/g | 金属状态 | c(H2SO4)/mol•L-1 | V(H2SO4)/mL | 溶液温度/℃ | 金属消失的时间/s | |
| 反应前 | 反应后 | ||||||
| 1 | 0.10 | 粉末 | 0.5 | V1 | 20 | 35 | 50 |
| 2 | 0.10 | 块状 | 0.8 | 50 | 20 | 35 | t1 |
| 3 | 0.10 | 粉末 | 0.8 | 50 | 20 | 36 | 25 |
| 4 | 0.10 | 块状 | 1.0 | 50 | 20 | 35 | 125 |
①V1=
②实验2和3的目的是
(2)纯碳酸钙广泛应用于精密电子陶瓷、医药等的生产,某兴趣小组按图所示实验步骤,模拟工业流程制备高纯碳酸钙,请回答下列问题。

①“酸溶”过程中,提前将石灰石粉碎,并进行搅拌,目的是
②实验室制取、收集干燥的NH3

需选用上述仪器装置的接口连接顺序是(填字母):a接_____、_____接_____,_____接h。
③制备碳酸钙通入NH3和CO2气体时,应先通入的气体是
您最近一年使用:0次
名校
解题方法
3 . 高铁酸钾(K2FeO4)是一种环保、高效饮水处理剂,利用铁屑制备的简略流程如图所示:

请回答下列问题:
(1)反应Ⅰ的生成物中可能含有的金属阳离子是___________ (用离子符号表示),如何检验该离子___________ 。
(2)操作A和操作B相同,其操作名称是___________ ;由操作B判断该生产条件下物质的溶解性:Na2FeO4___________ K2FeO4 (填“>”或“<”)。
(3)溶液C可与氯气反应制取漂白液,其离子方程式为___________ 。
(4)当生产过程中制得2mol的K2FeO4时,反应Ⅱ中转移的电子数为___________ 。
(5)反应Ⅱ中用到NaOH,若某同学做实验时要用到200mL 0.1mol/L NaOH溶液,现进行配制,则:
①配制该浓度的溶液需用托盘天平称量NaOH固体的质量为___________ g;
②配制过程中,下列操作导致所配溶液浓度偏大的是___________ (填标号)。
a.转移溶液时有少许液体溅出
b.溶解后,将溶液直接转移到容量瓶中
c.定容时俯视刻度线
d.定容摇匀后,发现液面下降,继续加水至刻度线

请回答下列问题:
(1)反应Ⅰ的生成物中可能含有的金属阳离子是
(2)操作A和操作B相同,其操作名称是
(3)溶液C可与氯气反应制取漂白液,其离子方程式为
(4)当生产过程中制得2mol的K2FeO4时,反应Ⅱ中转移的电子数为
(5)反应Ⅱ中用到NaOH,若某同学做实验时要用到200mL 0.1mol/L NaOH溶液,现进行配制,则:
①配制该浓度的溶液需用托盘天平称量NaOH固体的质量为
②配制过程中,下列操作导致所配溶液浓度偏大的是
a.转移溶液时有少许液体溅出
b.溶解后,将溶液直接转移到容量瓶中
c.定容时俯视刻度线
d.定容摇匀后,发现液面下降,继续加水至刻度线
您最近一年使用:0次
名校
4 .  是一种常见的氧化剂,工业上利用软锰矿
是一种常见的氧化剂,工业上利用软锰矿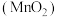 制备高锰酸钾的流程如下,在实验室中模拟该流程制备
制备高锰酸钾的流程如下,在实验室中模拟该流程制备 ,并对产物纯度进行测定。
,并对产物纯度进行测定。
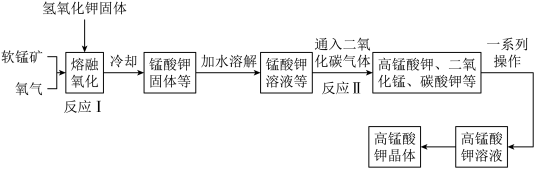
回答下列问题:
(1)反应Ⅰ需要的温度约为400℃,应选择的加热仪器为_______ 。
A酒精灯 B.电磁炉 C.电吹风
(2)加水溶解步骤必须要用到的玻璃仪器有_______。
(3)若要除去 、
、 溶液中的
溶液中的 ,应进行操作
,应进行操作_______ (填操作名称)。
(4)由 溶液获的
溶液获的 晶体的一系列操作为:蒸发浓缩至饱和、
晶体的一系列操作为:蒸发浓缩至饱和、_______ 、过滤、洗涤、干燥(填操作名称)。
(5)研究表明,反应Ⅰ分两步进行:
第一步反应生成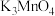 ,反应方程式为
,反应方程式为_______ 。
第二步反应方程式为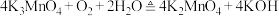
(6)写出反应Ⅱ的离子方程式_______ 。
(7)所得产品中只含有杂质 ,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为_______ %(保留两位小数)。
 是一种常见的氧化剂,工业上利用软锰矿
是一种常见的氧化剂,工业上利用软锰矿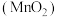 制备高锰酸钾的流程如下,在实验室中模拟该流程制备
制备高锰酸钾的流程如下,在实验室中模拟该流程制备 ,并对产物纯度进行测定。
,并对产物纯度进行测定。
回答下列问题:
(1)反应Ⅰ需要的温度约为400℃,应选择的加热仪器为
A酒精灯 B.电磁炉 C.电吹风
(2)加水溶解步骤必须要用到的玻璃仪器有_______。
| A.烧杯 | B.玻璃棒 | C.量筒 | D.酒精灯 |
 、
、 溶液中的
溶液中的 ,应进行操作
,应进行操作(4)由
 溶液获的
溶液获的 晶体的一系列操作为:蒸发浓缩至饱和、
晶体的一系列操作为:蒸发浓缩至饱和、(5)研究表明,反应Ⅰ分两步进行:
第一步反应生成
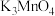 ,反应方程式为
,反应方程式为第二步反应方程式为
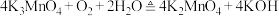
(6)写出反应Ⅱ的离子方程式
(7)所得产品中只含有杂质
 ,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
,通过元素分析仪测定出产品中所有氧原子的质量分数为40.48%,产品的纯度为
您最近一年使用:0次
名校
5 . 某固体混合物,可能含有CaO、 、
、 、
、 、NaCl中的几种,为检验其成分,做了如下实验:
、NaCl中的几种,为检验其成分,做了如下实验:
①取一定量固体溶于足量水,搅拌后得到无色透明溶液和白色沉淀,过滤得到滤液Ⅰ和沉淀Ⅰ,沉淀质量为10.00g。
②向滤液Ⅰ中加入过量的 溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。
溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。
③向沉淀Ⅱ中加入过量的盐酸,仍有固体未溶解,过滤得到沉淀Ⅲ,沉淀质量为23.30g。
④向滤液Ⅱ中加入硝酸酸化后,再加入过量的 溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。
溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。
已知:溶液中有 、
、 时,
时, 更容易和
更容易和 形成沉淀。
形成沉淀。
回答下列问题:
(1)通过实验①可知,一定不存在的是_______ (填化学式,下同)。
(2)沉淀Ⅰ、沉淀Ⅱ分别是_______ 、_______ 。
(3)本实验需要多次过滤,过滤需要用到得玻璃仪器有_______。
(4)写出实验④反应的离子方程式_______ 。
(5)该固体中一定含有_______ (填化学式),质量之比为_______ 。
 、
、 、
、 、NaCl中的几种,为检验其成分,做了如下实验:
、NaCl中的几种,为检验其成分,做了如下实验:①取一定量固体溶于足量水,搅拌后得到无色透明溶液和白色沉淀,过滤得到滤液Ⅰ和沉淀Ⅰ,沉淀质量为10.00g。
②向滤液Ⅰ中加入过量的
 溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。
溶液,产生白色沉淀,过滤得到滤液Ⅱ和沉淀Ⅱ,沉淀质量为43.00g。③向沉淀Ⅱ中加入过量的盐酸,仍有固体未溶解,过滤得到沉淀Ⅲ,沉淀质量为23.30g。
④向滤液Ⅱ中加入硝酸酸化后,再加入过量的
 溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。
溶液,得到大量白色沉淀,过滤得到沉淀Ⅳ,沉淀质量为71.75g。已知:溶液中有
 、
、 时,
时, 更容易和
更容易和 形成沉淀。
形成沉淀。回答下列问题:
(1)通过实验①可知,一定不存在的是
(2)沉淀Ⅰ、沉淀Ⅱ分别是
(3)本实验需要多次过滤,过滤需要用到得玻璃仪器有_______。
| A.烧杯 | B.玻璃棒 | C.漏斗 | D.酒精灯 |
(5)该固体中一定含有
您最近一年使用:0次
名校
6 . 某工业废水中存在大盘的Na+、 、Cu2+、
、Cu2+、 ,欲除去其中的Cu2+、
,欲除去其中的Cu2+、 ,设计的工艺流程如图所示:
,设计的工艺流程如图所示:

(1)加入NaOH溶液时反应的离子方程式:_______ 。
(2)试剂a为_______ ,试剂b为_______ 。
(3)流程图中操作X为_______ 。
(4)检验废水中的 已沉淀完全的方法为
已沉淀完全的方法为_______ 。
 、Cu2+、
、Cu2+、 ,欲除去其中的Cu2+、
,欲除去其中的Cu2+、 ,设计的工艺流程如图所示:
,设计的工艺流程如图所示:
(1)加入NaOH溶液时反应的离子方程式:
(2)试剂a为
(3)流程图中操作X为
(4)检验废水中的
 已沉淀完全的方法为
已沉淀完全的方法为
您最近一年使用:0次
解题方法
7 . 某工厂的废水中含有较多的 和
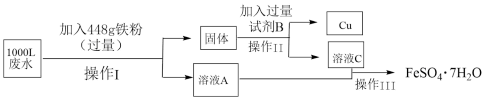
和 。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收
。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收 和金属铜。
和金属铜。
请回答下列问题:
(1)向废水中加入铁粉,所发生的主要反应的离子方程式为___________ 。
(2)操作Ⅰ和操作Ⅱ的名称是___________ ,所用到的玻璃仪器有___________ 。
(3)流程中“固体”的主要成分是___________ (填化学式);加入试剂B所发生反应的化学方程式为___________ 。
(4)操作Ⅲ包括蒸发浓缩、___________ 、过滤、___________ 、干燥。
(5)设计实验方案检验废水中是否含有 :
:___________ 。
(6)若废水中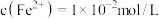 ,
,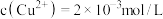 ,上述1000L废水经处理后,理论上可获得
,上述1000L废水经处理后,理论上可获得 的质量是
的质量是___________ g。
 和
和 。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收
。为了减少污染并变废为宝, 用如图所示的工艺流程从废水中回收 和金属铜。
和金属铜。
请回答下列问题:
(1)向废水中加入铁粉,所发生的主要反应的离子方程式为
(2)操作Ⅰ和操作Ⅱ的名称是
(3)流程中“固体”的主要成分是
(4)操作Ⅲ包括蒸发浓缩、
(5)设计实验方案检验废水中是否含有
 :
:(6)若废水中
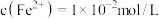 ,
,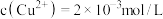 ,上述1000L废水经处理后,理论上可获得
,上述1000L废水经处理后,理论上可获得 的质量是
的质量是
您最近一年使用:0次
8 . 我国化学家侯德榜发明了联合制碱法(又称侯氏制碱法),对世界制碱工业做出了巨大贡献。侯氏制碱法的主要过程如下图所示(部分物质已略去)。

回答下列问题:
(1)①~③所涉及的操作中,属于过滤的是___________ (填序号)。
(2)将下列化学方程式补充完整___________ :NH3+CO2+___________+___________=NaHCO3↓+NH4Cl
(3)写出操作②发生反应的化学方程式___________ 。
(4)下列说法中正确的是___________ (填字母序号)。
a.NH3与CO2的通入顺序为先通入CO2,再通入NH3
b.副产物NH4Cl可用作肥料
c.CO2可循环使用

回答下列问题:
(1)①~③所涉及的操作中,属于过滤的是
(2)将下列化学方程式补充完整
(3)写出操作②发生反应的化学方程式
(4)下列说法中正确的是
a.NH3与CO2的通入顺序为先通入CO2,再通入NH3
b.副产物NH4Cl可用作肥料
c.CO2可循环使用
您最近一年使用:0次
2022-01-18更新
|
90次组卷
|
2卷引用:重庆市缙云教育联盟2023-2024学年高三下学期8月月考化学试题
名校
解题方法
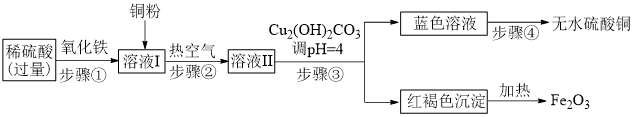
9 . 工业上以稀硫酸、氧化铁、铜粉为原料制备硫酸铜的流程如下:
已知:①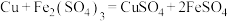 ;
;
②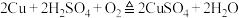 ;
;
③Fe2+易被氧化成Fe3+。
(1)步骤①发生的化学方程式是_______ 。
(2)溶液Ⅱ中溶质的成分是_______ (填化学式)。
(3)步骤③的名称是_______ ,用到的玻璃仪器有烧杯、_______ 、玻璃棒。
(4)上述流程中可以循环使用的物质是_______ (填名称)。

已知:①
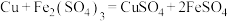 ;
;②
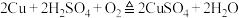 ;
;③Fe2+易被氧化成Fe3+。
(1)步骤①发生的化学方程式是
(2)溶液Ⅱ中溶质的成分是
(3)步骤③的名称是
(4)上述流程中可以循环使用的物质是
您最近一年使用:0次
10 . 某工厂生产硼砂产生的固体废料,主要含有MgCO3、CaCO3、SiO2、Al2O3和Fe2O3等,其中MgCO3质量分数为84%。采用以下工艺流程可回收固体废料中的镁资源。
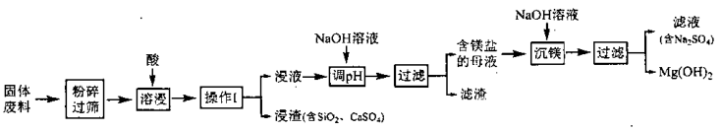
该工艺条件下,溶液中金属离子开始生成氢氧化物沉淀和完全沉淀的pH如下表所示:
回答下列问题:
(1)将固体废料“粉碎过筛”后再进入“溶浸”环节的目的是______________________ 。
(2)“溶浸”时MgCO3发生反应的化学方程式为______________________ 。
(3) 下图是某学生在实验室模拟进行“操作I”的示意图,其操作不规范的是_______ (填标号)。
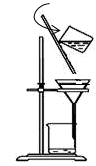
a.漏斗末端颈尖未紧靠烧杯壁 b. 玻璃棒用作引流
c. 将滤纸湿润,使其紧贴漏斗壁 d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(4)在“调pH”之前,“浸液”的pH______ 7 (填“>”、“<”或“=”);将该溶液的pH范围应调节为_____ ~8.9之间, 所得“滤渣”的主要成分是________ (填化学式)。
(5)写出“沉镁”的化学方程式_________________________ 。
(6)已知固体废料质量为m g,理论上可生产Mg(OH)2的质量为___ g。

该工艺条件下,溶液中金属离子开始生成氢氧化物沉淀和完全沉淀的pH如下表所示:
| 金属离子 | Fe3+ | Al3+ | Mg2+ |
| 开始沉淀pH | 1.9 | 3.0 | 8.9 |
| 完全沉淀pH | 3.2 | 4.7 | 10.9 |
回答下列问题:
(1)将固体废料“粉碎过筛”后再进入“溶浸”环节的目的是
(2)“溶浸”时MgCO3发生反应的化学方程式为
(3) 下图是某学生在实验室模拟进行“操作I”的示意图,其操作不规范的是

a.漏斗末端颈尖未紧靠烧杯壁 b. 玻璃棒用作引流
c. 将滤纸湿润,使其紧贴漏斗壁 d.滤纸边缘高出漏斗
e.用玻璃棒在漏斗中轻轻搅动以加快过滤速度
(4)在“调pH”之前,“浸液”的pH
(5)写出“沉镁”的化学方程式
(6)已知固体废料质量为m g,理论上可生产Mg(OH)2的质量为
您最近一年使用:0次



