名校
解题方法
1 . 类比是化学学习的重要方法之一,过氧化钙( )与
)与 在结构和性质上相似。
在结构和性质上相似。 是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室制备流程如下:
是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室制备流程如下:
Ⅰ. 的制备
的制备
已知:① 是一种白色晶体,微溶于水,不溶于乙醇,易与酸反应;
是一种白色晶体,微溶于水,不溶于乙醇,易与酸反应;
② 在0℃时稳定,加热至130℃时变为无水
在0℃时稳定,加热至130℃时变为无水 ,在350℃时能迅速分解,生成
,在350℃时能迅速分解,生成 和
和 。
。

回答下列问题:
(1) 中阳离子和阴离子的个数之比为
中阳离子和阴离子的个数之比为___________ 。
(2) 可用于长途运输鱼苗,请用化学方程式解释
可用于长途运输鱼苗,请用化学方程式解释___________ 。
(3)“操作Ⅰ”的名称是___________ 。
(4)“洗涤”工序中应选择的洗涤液为___________ 。“沉淀”工序中为了提高产品产率应在___________ 浴中进行。
Ⅱ. 纯度的测定
纯度的测定
(5)取一定质量的产品,按照图装置(加热装置已省略)进行实验。实验结束读取体积时,若水准管中液面高于量气管中液面,会使测得的 纯度
纯度___________ (填“偏大”、“偏小”、“无影响”)。若有影响,应向___________ (填“上”或“下”)移动水准管,使两管液面相平(注:若第一格填无影响,第二格不用填写)。
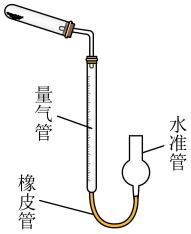
(6)已知:样品质量 ,标况下测得气体体积为VmL,样品中
,标况下测得气体体积为VmL,样品中 的纯度为
的纯度为___________ %。
 )与
)与 在结构和性质上相似。
在结构和性质上相似。 是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室制备流程如下:
是一种新型水产养殖增氧剂,常用于鲜活水产品的运输。实验室制备流程如下:Ⅰ.
 的制备
的制备已知:①
 是一种白色晶体,微溶于水,不溶于乙醇,易与酸反应;
是一种白色晶体,微溶于水,不溶于乙醇,易与酸反应;②
 在0℃时稳定,加热至130℃时变为无水
在0℃时稳定,加热至130℃时变为无水 ,在350℃时能迅速分解,生成
,在350℃时能迅速分解,生成 和
和 。
。
回答下列问题:
(1)
 中阳离子和阴离子的个数之比为
中阳离子和阴离子的个数之比为(2)
 可用于长途运输鱼苗,请用化学方程式解释
可用于长途运输鱼苗,请用化学方程式解释(3)“操作Ⅰ”的名称是
(4)“洗涤”工序中应选择的洗涤液为
Ⅱ.
 纯度的测定
纯度的测定(5)取一定质量的产品,按照图装置(加热装置已省略)进行实验。实验结束读取体积时,若水准管中液面高于量气管中液面,会使测得的
 纯度
纯度
(6)已知:样品质量
 ,标况下测得气体体积为VmL,样品中
,标况下测得气体体积为VmL,样品中 的纯度为
的纯度为
您最近一年使用:0次
解题方法
2 .  是一种重要的有机化工原料,是一种金黄色液体,沸点为138℃。学习小组在实验室利用下述装置制备
是一种重要的有机化工原料,是一种金黄色液体,沸点为138℃。学习小组在实验室利用下述装置制备 并测定其纯度(加热和夹持装置略)。
并测定其纯度(加热和夹持装置略)。

已知:①单质硫沸点为445℃;
② 能被
能被 氧化为
氧化为 ,
, (是一种暗红色液体)沸点为59℃;
(是一种暗红色液体)沸点为59℃;
③ 和
和 均易水解,
均易水解, 水解生成S、
水解生成S、 和HCl,
和HCl, 水解生成S和两种强酸。
水解生成S和两种强酸。
回答下列问题:
(1)组装仪器,装置合理的连接顺序是a→___________ (按气流顺序填各接口编号)。仪器m的作用为___________ 。
(2)检查装置气密性后开始实验:①打开 ,通
,通 一段时间;②关闭
一段时间;②关闭 ,加热装置B,控制温度为140℃;③加热A处蒸馏烧瓶,当观察到F处U形管内出现大量金黄色液体,停止加热A;④打开
,加热装置B,控制温度为140℃;③加热A处蒸馏烧瓶,当观察到F处U形管内出现大量金黄色液体,停止加热A;④打开 ,继续通一段时间
,继续通一段时间 。
。
加热装置B采用的加热方式为___________ ,当B处三颈烧瓶内充满黄绿色气体时,停止加热B,反应仍可以继续进行,可能的原因是___________ ,停止加热A后继续通一段时间 的目的是
的目的是___________ 。
(3)学习小组若长时间未观察到F处有金黄色液体生成,可以采取的措施为___________ ;最终所得粗产品需经过___________ (填操作名称)进一步提纯。
(4)测定粗产品纯度:称量mg产品,加稀盐酸振荡保证反应充分,通水蒸气将 和HCl全部蒸出后,配成100mL溶液,取25mL于锥形瓶中,用
和HCl全部蒸出后,配成100mL溶液,取25mL于锥形瓶中,用 溶液滴定至终点,消耗VmLNaOH溶液。则样品中
溶液滴定至终点,消耗VmLNaOH溶液。则样品中 纯度的表达式为
纯度的表达式为___________ 。
 是一种重要的有机化工原料,是一种金黄色液体,沸点为138℃。学习小组在实验室利用下述装置制备
是一种重要的有机化工原料,是一种金黄色液体,沸点为138℃。学习小组在实验室利用下述装置制备 并测定其纯度(加热和夹持装置略)。
并测定其纯度(加热和夹持装置略)。
已知:①单质硫沸点为445℃;
②
 能被
能被 氧化为
氧化为 ,
, (是一种暗红色液体)沸点为59℃;
(是一种暗红色液体)沸点为59℃;③
 和
和 均易水解,
均易水解, 水解生成S、
水解生成S、 和HCl,
和HCl, 水解生成S和两种强酸。
水解生成S和两种强酸。回答下列问题:
(1)组装仪器,装置合理的连接顺序是a→
(2)检查装置气密性后开始实验:①打开
 ,通
,通 一段时间;②关闭
一段时间;②关闭 ,加热装置B,控制温度为140℃;③加热A处蒸馏烧瓶,当观察到F处U形管内出现大量金黄色液体,停止加热A;④打开
,加热装置B,控制温度为140℃;③加热A处蒸馏烧瓶,当观察到F处U形管内出现大量金黄色液体,停止加热A;④打开 ,继续通一段时间
,继续通一段时间 。
。加热装置B采用的加热方式为
 的目的是
的目的是(3)学习小组若长时间未观察到F处有金黄色液体生成,可以采取的措施为
(4)测定粗产品纯度:称量mg产品,加稀盐酸振荡保证反应充分,通水蒸气将
 和HCl全部蒸出后,配成100mL溶液,取25mL于锥形瓶中,用
和HCl全部蒸出后,配成100mL溶液,取25mL于锥形瓶中,用 溶液滴定至终点,消耗VmLNaOH溶液。则样品中
溶液滴定至终点,消耗VmLNaOH溶液。则样品中 纯度的表达式为
纯度的表达式为
您最近一年使用:0次
3 . 碱式硫酸铁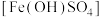 难溶于水,可做净水剂、媒染剂、颜料和药物。可由硫酸亚铁与稀硝酸共热制得。某实验小组欲用如图所示装置进行实验,回答下列问题:
难溶于水,可做净水剂、媒染剂、颜料和药物。可由硫酸亚铁与稀硝酸共热制得。某实验小组欲用如图所示装置进行实验,回答下列问题:
(1)锥形瓶中发生反应的化学方程式为___________ ;某同学认为用 溶液代替稀硝酸更好,理由是
溶液代替稀硝酸更好,理由是___________ 。
(2)酸性高锰酸钾溶液可除去一氧化氮,反应的离子方程式为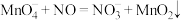 。
。
该反应分两步进行。第一步是高锰酸钾把一氧化氮氧化为二氧化氮,反应的离子方程式为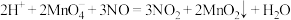 ,则第二步反应的离子方程式为
,则第二步反应的离子方程式为___________ 。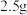 产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用
产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用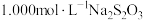 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 (涉及的反应方程式为
(涉及的反应方程式为 、
、 )。
)。
①盛装 标准溶液的滴定管应选用
标准溶液的滴定管应选用___________ (填“酸式”或“碱式”)滴定管。
②判断达到滴定终点的方法为___________ 。
③该产品的纯度为___________  ,滴定过程中,如果滴定速度过慢,可能导致所测结果
,滴定过程中,如果滴定速度过慢,可能导致所测结果___________ (填“偏高”“偏低”或“无影响”)。
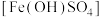 难溶于水,可做净水剂、媒染剂、颜料和药物。可由硫酸亚铁与稀硝酸共热制得。某实验小组欲用如图所示装置进行实验,回答下列问题:
难溶于水,可做净水剂、媒染剂、颜料和药物。可由硫酸亚铁与稀硝酸共热制得。某实验小组欲用如图所示装置进行实验,回答下列问题:(1)锥形瓶中发生反应的化学方程式为
 溶液代替稀硝酸更好,理由是
溶液代替稀硝酸更好,理由是(2)酸性高锰酸钾溶液可除去一氧化氮,反应的离子方程式为
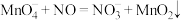 。
。该反应分两步进行。第一步是高锰酸钾把一氧化氮氧化为二氧化氮,反应的离子方程式为
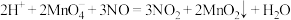 ,则第二步反应的离子方程式为
,则第二步反应的离子方程式为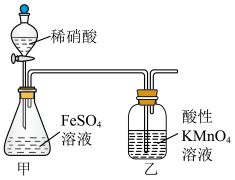
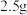 产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用
产物溶于适量稀硫酸中,加入足量KI溶液,充分反应后,滴入几滴淀粉溶液,用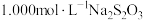 标准溶液滴定至终点,消耗标准液
标准溶液滴定至终点,消耗标准液 (涉及的反应方程式为
(涉及的反应方程式为 、
、 )。
)。①盛装
 标准溶液的滴定管应选用
标准溶液的滴定管应选用②判断达到滴定终点的方法为
③该产品的纯度为
 ,滴定过程中,如果滴定速度过慢,可能导致所测结果
,滴定过程中,如果滴定速度过慢,可能导致所测结果
您最近一年使用:0次
2023-12-21更新
|
94次组卷
|
2卷引用:山东省级联考2023-2024学年高二上学期12月月考化学试题
解题方法
4 . 通过测定加热样品产生的 质量,测量碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,设计装置如下图所示:
质量,测量碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,设计装置如下图所示:

下列说法错误的是:
 质量,测量碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,设计装置如下图所示:
质量,测量碳酸钠和碳酸氢钠混合物中碳酸钠的质量分数,设计装置如下图所示:
下列说法错误的是:
A.加热样品前,先通一段时间X,X可以是 |
B.装置a的作用是防止空气中的 和 和 进入U型管 进入U型管 |
| C.该装置的缺陷导致碳酸钠的质量分数偏高 |
D.改进C选项中缺陷后,U型管增重n g,则碳酸钠的质量分数为 |
您最近一年使用:0次
解题方法
5 . 某化学研究小组,用杂铜(含有较多杂质的铜粉),通过不同的途径制取胆矾并测定胆矾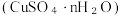 中结晶水的n值,实验过程如下:
中结晶水的n值,实验过程如下:
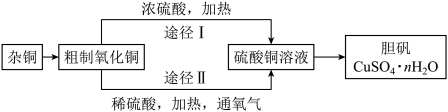
胆矾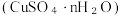 中结晶水n值的测定步骤如下:
中结晶水n值的测定步骤如下:
i.称量坩埚的质量,记为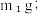
ii.称量坩埚和胆矾的质量,记为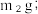
iii.加热、冷却、称量坩埚和固体的质量,记为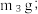
iv.再次加热、冷却、称量坩埚和固体的质量,记为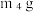 (注:上述过程无
(注:上述过程无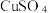 分解)。
分解)。
在胆矾(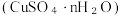 中结晶水n值的测定实验中,下列不规范操作会导致测定结果偏大的是
中结晶水n值的测定实验中,下列不规范操作会导致测定结果偏大的是
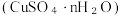 中结晶水的n值,实验过程如下:
中结晶水的n值,实验过程如下:
胆矾
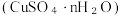 中结晶水n值的测定步骤如下:
中结晶水n值的测定步骤如下:i.称量坩埚的质量,记为
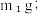
ii.称量坩埚和胆矾的质量,记为
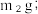
iii.加热、冷却、称量坩埚和固体的质量,记为
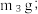
iv.再次加热、冷却、称量坩埚和固体的质量,记为
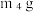 (注:上述过程无
(注:上述过程无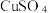 分解)。
分解)。在胆矾(
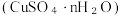 中结晶水n值的测定实验中,下列不规范操作会导致测定结果偏大的是
中结晶水n值的测定实验中,下列不规范操作会导致测定结果偏大的是| A.加热后放在空气中冷却 | B.胆矾晶体的颗粒较大 |
| C.加热温度过高 | D.粉末未完全变白就停止加热 |
您最近一年使用:0次
名校
6 . 实验室使用标准 溶液测定补铁剂硫酸亚铁片中
溶液测定补铁剂硫酸亚铁片中 的含量,发生反应为
的含量,发生反应为 。加入无色、被氧化后变为紫红色的二苯胺磺酸钠做指示剂。下列说法错误的是
。加入无色、被氧化后变为紫红色的二苯胺磺酸钠做指示剂。下列说法错误的是
 溶液测定补铁剂硫酸亚铁片中
溶液测定补铁剂硫酸亚铁片中 的含量,发生反应为
的含量,发生反应为 。加入无色、被氧化后变为紫红色的二苯胺磺酸钠做指示剂。下列说法错误的是
。加入无色、被氧化后变为紫红色的二苯胺磺酸钠做指示剂。下列说法错误的是| A.将硫酸亚铁片研碎,置于稀硫酸中溶解后过滤 |
| B.标准重铬酸钾液应用酸式滴定管取用 |
C.由实验可知酸性溶液中还原性: 二苯胺磺酸钠 二苯胺磺酸钠 |
D.酸性 溶液与乙醇生成乙酸的离子方程式为: 溶液与乙醇生成乙酸的离子方程式为: |
您最近一年使用:0次
解题方法
7 . 铁的化合物在生产生活中应用广泛,回答下列问题:
(1) 是一种重要的铁盐,常用于金属蚀刻。某同学向盛有黄色
是一种重要的铁盐,常用于金属蚀刻。某同学向盛有黄色 溶液的烧杯中加入石灰石粉末,发现有无色气泡产生。静置24小时,可观察到烧杯内液体变为透明的红褐色,猜想得到了
溶液的烧杯中加入石灰石粉末,发现有无色气泡产生。静置24小时,可观察到烧杯内液体变为透明的红褐色,猜想得到了 胶体。
胶体。
①证明该猜想正确的实验方法是_______ ,此反应的离子方程式为_______ 。
②分离该红褐色液体与烧杯底部石灰石的方法是_______ (填操作名称,下同):除去红褐色液体中混有的 的方法是
的方法是_______ 。
(2)硫酸铁铵常用作分析试剂和媒染剂。实验室利用废铁屑(含 、
、 等杂质)制备硫酸铁铵晶体[
等杂质)制备硫酸铁铵晶体[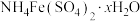 ]的实验流程如下。
]的实验流程如下。

①用离子方程式表示 的作用
的作用_______ 。
②硫酸铁铵晶体中结晶水含量的测定:准确称量9.640g硫酸铁铵晶体配成100 溶液,向该溶液中加入过量0.5
溶液,向该溶液中加入过量0.5
 溶液,充分反应后,过滤、洗涤、干燥、称量,得9.320g白色固体。判断
溶液,充分反应后,过滤、洗涤、干燥、称量,得9.320g白色固体。判断 溶液已过量的操作是
溶液已过量的操作是_______ ;硫酸铁铵晶体中
_______ 。
(1)
 是一种重要的铁盐,常用于金属蚀刻。某同学向盛有黄色
是一种重要的铁盐,常用于金属蚀刻。某同学向盛有黄色 溶液的烧杯中加入石灰石粉末,发现有无色气泡产生。静置24小时,可观察到烧杯内液体变为透明的红褐色,猜想得到了
溶液的烧杯中加入石灰石粉末,发现有无色气泡产生。静置24小时,可观察到烧杯内液体变为透明的红褐色,猜想得到了 胶体。
胶体。①证明该猜想正确的实验方法是
②分离该红褐色液体与烧杯底部石灰石的方法是
 的方法是
的方法是(2)硫酸铁铵常用作分析试剂和媒染剂。实验室利用废铁屑(含
 、
、 等杂质)制备硫酸铁铵晶体[
等杂质)制备硫酸铁铵晶体[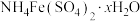 ]的实验流程如下。
]的实验流程如下。
①用离子方程式表示
 的作用
的作用②硫酸铁铵晶体中结晶水含量的测定:准确称量9.640g硫酸铁铵晶体配成100
 溶液,向该溶液中加入过量0.5
溶液,向该溶液中加入过量0.5
 溶液,充分反应后,过滤、洗涤、干燥、称量,得9.320g白色固体。判断
溶液,充分反应后,过滤、洗涤、干燥、称量,得9.320g白色固体。判断 溶液已过量的操作是
溶液已过量的操作是
您最近一年使用:0次
8 . 根据钠的价-类二维图回答下列问题:

(1)NaH在野外可用作生氢剂,其化学反应原理为 。该反应中体现了NaH的
。该反应中体现了NaH的_____ (填“氧化性”、“还原性”或“氧化性和还原性”)。
(2)写出二维图中缺失①中某种淡黄色固体与水反应的离子方程式_____ 。
(3)实验室模拟工业制备①中淡黄色固体并检验其纯度的实验流程如图所示。
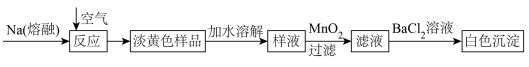
样液中加入 后产生一种无色无味的气体单质,该气体的名称为
后产生一种无色无味的气体单质,该气体的名称为_____ ,已知白色沉淀为 ,说明
,说明 样品中含有的杂质是
样品中含有的杂质是_____ 。
(4)我国科学家研发了一种室温下“可呼吸”的 充电电池。电池的总反应为
充电电池。电池的总反应为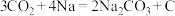 ,该电池消耗6.72L(标准状况)
,该电池消耗6.72L(标准状况) 气体时,转移电子数为
气体时,转移电子数为_____  。
。
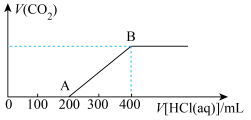
(5)向500mL某NaOH溶液中缓慢通入一定量的 (忽略溶液体积的变化),充分反应。向上述所得溶液中逐滴滴加
(忽略溶液体积的变化),充分反应。向上述所得溶液中逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示,则原NaOH溶液的物质的量浓度为
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示,则原NaOH溶液的物质的量浓度为_____ 。

(1)NaH在野外可用作生氢剂,其化学反应原理为
 。该反应中体现了NaH的
。该反应中体现了NaH的(2)写出二维图中缺失①中某种淡黄色固体与水反应的离子方程式
(3)实验室模拟工业制备①中淡黄色固体并检验其纯度的实验流程如图所示。

样液中加入
 后产生一种无色无味的气体单质,该气体的名称为
后产生一种无色无味的气体单质,该气体的名称为 ,说明
,说明 样品中含有的杂质是
样品中含有的杂质是(4)我国科学家研发了一种室温下“可呼吸”的
 充电电池。电池的总反应为
充电电池。电池的总反应为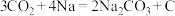 ,该电池消耗6.72L(标准状况)
,该电池消耗6.72L(标准状况) 气体时,转移电子数为
气体时,转移电子数为 。
。(5)向500mL某NaOH溶液中缓慢通入一定量的
 (忽略溶液体积的变化),充分反应。向上述所得溶液中逐滴滴加
(忽略溶液体积的变化),充分反应。向上述所得溶液中逐滴滴加 的盐酸,所得气体的体积与所加盐酸的体积关系如图所示,则原NaOH溶液的物质的量浓度为
的盐酸,所得气体的体积与所加盐酸的体积关系如图所示,则原NaOH溶液的物质的量浓度为
您最近一年使用:0次
解题方法
9 . 铁黄( )是一种无机颜料,也是重要的化工产品。某小组在实验室制备少量铁黄,并测定其纯度。回答下列问题:
)是一种无机颜料,也是重要的化工产品。某小组在实验室制备少量铁黄,并测定其纯度。回答下列问题:
(1)向 溶液中滴加氨水并持续通入空气可制得铁黄,反应的离子方程式为
溶液中滴加氨水并持续通入空气可制得铁黄,反应的离子方程式为___________ 。
(2)为测定铁黄产品的纯度,进行如下实验:
Ⅰ.准确称取2.000g样品,向其中加入50 1.000
1.000 稀硫酸(杂质不参与反应),加热溶解;
稀硫酸(杂质不参与反应),加热溶解;
Ⅱ.向Ⅰ所得溶液中加入 溶液,发生反应:
溶液,发生反应: ;
;
Ⅲ.将Ⅱ所得溶液稀释至100 ,量取25.00
,量取25.00 于锥形瓶中,滴入2滴酚酞溶液,用0.5000
于锥形瓶中,滴入2滴酚酞溶液,用0.5000 标准
标准 溶液滴定,达终点时消耗
溶液滴定,达终点时消耗 溶液20.00
溶液20.00 [滴定过程中,
[滴定过程中, 与
与 溶液不反应]。
溶液不反应]。
①下列关于滴定管的使用,说法正确的是___________ (填标号)。
A.滴定管使用前需检查是否漏水
B.滴定管用蒸馏水洗净后,不可使用烘箱快速烘干
C.润洗滴定管时,应将洗涤液从滴定管上口倒出
D.滴定管装液时,应借助漏斗、胶头滴管等玻璃仪器转移
E.滴定读数时,应双手一上一下持滴定管
②步骤Ⅲ量取25.00 溶液应选用
溶液应选用___________ (填“酸式”或“碱式”)滴定管;在规格为50.00 的滴定管中,若溶液起始读数为12.00
的滴定管中,若溶液起始读数为12.00 ,此时滴定管中溶液的实际体积为
,此时滴定管中溶液的实际体积为___________ (填标号)。
A.12.00 B.38.00
B.38.00 C.小于12.00
C.小于12.00 D.大于38.00
D.大于38.00
③步骤Ⅲ中判断反应达到滴定终点的方法是___________ ;产品中 的纯度为
的纯度为___________ 。
④若步骤Ⅲ滴定达终点时,发现滴定管尖嘴内有气泡生成,会导致测定的产品纯度___________ (填“偏大”、“偏小”或“无影响”,下同);若步骤Ⅱ加入的 溶液过量,过量
溶液过量,过量 能与稀硫酸反应生成二元弱酸
能与稀硫酸反应生成二元弱酸 ,会导致测定的产品纯度
,会导致测定的产品纯度___________ 。已知:25℃时, 的
的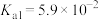 ,
,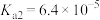 。
。
 )是一种无机颜料,也是重要的化工产品。某小组在实验室制备少量铁黄,并测定其纯度。回答下列问题:
)是一种无机颜料,也是重要的化工产品。某小组在实验室制备少量铁黄,并测定其纯度。回答下列问题:(1)向
 溶液中滴加氨水并持续通入空气可制得铁黄,反应的离子方程式为
溶液中滴加氨水并持续通入空气可制得铁黄,反应的离子方程式为(2)为测定铁黄产品的纯度,进行如下实验:
Ⅰ.准确称取2.000g样品,向其中加入50
 1.000
1.000 稀硫酸(杂质不参与反应),加热溶解;
稀硫酸(杂质不参与反应),加热溶解;Ⅱ.向Ⅰ所得溶液中加入
 溶液,发生反应:
溶液,发生反应: ;
;Ⅲ.将Ⅱ所得溶液稀释至100
 ,量取25.00
,量取25.00 于锥形瓶中,滴入2滴酚酞溶液,用0.5000
于锥形瓶中,滴入2滴酚酞溶液,用0.5000 标准
标准 溶液滴定,达终点时消耗
溶液滴定,达终点时消耗 溶液20.00
溶液20.00 [滴定过程中,
[滴定过程中, 与
与 溶液不反应]。
溶液不反应]。①下列关于滴定管的使用,说法正确的是
A.滴定管使用前需检查是否漏水
B.滴定管用蒸馏水洗净后,不可使用烘箱快速烘干
C.润洗滴定管时,应将洗涤液从滴定管上口倒出
D.滴定管装液时,应借助漏斗、胶头滴管等玻璃仪器转移
E.滴定读数时,应双手一上一下持滴定管
②步骤Ⅲ量取25.00
 溶液应选用
溶液应选用 的滴定管中,若溶液起始读数为12.00
的滴定管中,若溶液起始读数为12.00 ,此时滴定管中溶液的实际体积为
,此时滴定管中溶液的实际体积为A.12.00
 B.38.00
B.38.00 C.小于12.00
C.小于12.00 D.大于38.00
D.大于38.00
③步骤Ⅲ中判断反应达到滴定终点的方法是
 的纯度为
的纯度为④若步骤Ⅲ滴定达终点时,发现滴定管尖嘴内有气泡生成,会导致测定的产品纯度
 溶液过量,过量
溶液过量,过量 能与稀硫酸反应生成二元弱酸
能与稀硫酸反应生成二元弱酸 ,会导致测定的产品纯度
,会导致测定的产品纯度 的
的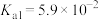 ,
,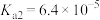 。
。
您最近一年使用:0次
解题方法
10 . 实验室利用TiO2、TiCl4、H2制备半导体材料Ti2O3的装置如图所示(加热及夹持装置略)。

已知:I.高温时Ti2O3易被空气中O2氧化;TiCl4易水解,易挥发。
II.部分物质的物理性质:
回答下列问题:
(1)制备Ti2O3时进行操作:(i)连接装置,(ii)……;(iii)加入药品;(iv)……;(v)加热开始反应。操作(ii)为___________ 。操作(iv)__________ 。
(2)C装置的作用是___________ 。
(3)在880℃时反应生成Ti2O3的化学方程式为2TiCl4+H2=2TiCl3+2HCl,2TiCl3+6TiO2+3H2=4Ti2O3+6HCl,判断TiO2已经反应结束的实验现象是___________ 。
(4)将1.440gTi2O3在空气中加热,固体的质量随温度变化如图所示

T1→T2℃时,反应的化学方程式为___________ 。

已知:I.高温时Ti2O3易被空气中O2氧化;TiCl4易水解,易挥发。
II.部分物质的物理性质:
| Ti2O3 | TiCl3 | TiCl4 | |
| 颜色 | 暗紫色 | 紫红色 | 无色 |
| 熔点(℃) | 2130 | 440 | -25 |
| 沸点(℃) | —— | 600 | 135 |
(1)制备Ti2O3时进行操作:(i)连接装置,(ii)……;(iii)加入药品;(iv)……;(v)加热开始反应。操作(ii)为
(2)C装置的作用是
(3)在880℃时反应生成Ti2O3的化学方程式为2TiCl4+H2=2TiCl3+2HCl,2TiCl3+6TiO2+3H2=4Ti2O3+6HCl,判断TiO2已经反应结束的实验现象是
(4)将1.440gTi2O3在空气中加热,固体的质量随温度变化如图所示

T1→T2℃时,反应的化学方程式为
您最近一年使用:0次



