1 . 锂和铍是重要的稀有金属,被国内外视为战略性资源。一种从尾矿(主要含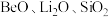 及
及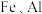 元素)中回收锂、铍、铝的工艺流程如图:
元素)中回收锂、铍、铝的工艺流程如图:
(1)“浸渣”中主要成分的晶体类型为_____ 。
(2)“沉铁”中生成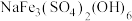 沉淀,其中
沉淀,其中 元素的化合价为
元素的化合价为_____ ,该反应的离子方程式为_____ 。
(3)“萃取”时,以 为萃取剂、
为萃取剂、 为协萃剂,溶液中的
为协萃剂,溶液中的 可与
可与 结合成
结合成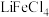 而被
而被 萃取。“反萃取”时,加入浓盐酸,发生
萃取。“反萃取”时,加入浓盐酸,发生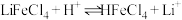 。
。
①“萃取”时还需要加入 ,其作用是
,其作用是_____ 。
②取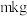 尾矿(其中
尾矿(其中 的质量分数为
的质量分数为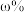 ),“反萃取”后所得
),“反萃取”后所得 水相中
水相中 ,则该过程
,则该过程 的回收率为
的回收率为_____ (用含相关物理量字母的代数式表示)。
(4)实验室提纯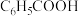 的方法是
的方法是_____ 。
(5)为了得到较高的空间利用率,离子晶体中的阴离子(通常半径较大)会尽可能紧密堆积,阳离子(通常半径较小)填入阴离子形成的空隙中,这种模型称为离子晶体的“堆积-填隙模型”。
已知常见的 型离子晶体的离子半径比和配位数的关系如下表:
型离子晶体的离子半径比和配位数的关系如下表:
表中离子半径比的临界值是由“堆积—填隙模型”中阴阳离子的几何关系确定的,例如配位数为8时,阳离子进入阴离子形成的正方体空隙,正方体8个顶点处的阴离了相切,空隙处(正方体体心)的阳离子与8个阴离子也相切,此时可由相关几何关系求得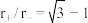 。
。
①
_____ 。
② 晶胞为立方
晶胞为立方 型,而
型,而 等的晶胞为
等的晶胞为 型。请结合上表,解释出现此结果的原因:
型。请结合上表,解释出现此结果的原因:_____ 。
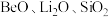 及
及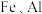 元素)中回收锂、铍、铝的工艺流程如图:
元素)中回收锂、铍、铝的工艺流程如图: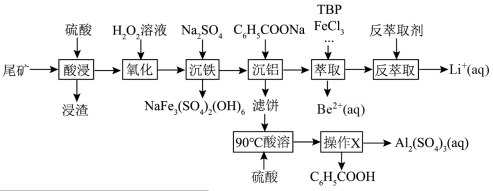
(1)“浸渣”中主要成分的晶体类型为
(2)“沉铁”中生成
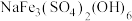 沉淀,其中
沉淀,其中 元素的化合价为
元素的化合价为(3)“萃取”时,以
 为萃取剂、
为萃取剂、 为协萃剂,溶液中的
为协萃剂,溶液中的 可与
可与 结合成
结合成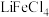 而被
而被 萃取。“反萃取”时,加入浓盐酸,发生
萃取。“反萃取”时,加入浓盐酸,发生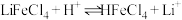 。
。①“萃取”时还需要加入
 ,其作用是
,其作用是②取
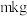 尾矿(其中
尾矿(其中 的质量分数为
的质量分数为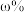 ),“反萃取”后所得
),“反萃取”后所得 水相中
水相中 ,则该过程
,则该过程 的回收率为
的回收率为(4)实验室提纯
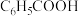 的方法是
的方法是(5)为了得到较高的空间利用率,离子晶体中的阴离子(通常半径较大)会尽可能紧密堆积,阳离子(通常半径较小)填入阴离子形成的空隙中,这种模型称为离子晶体的“堆积-填隙模型”。
已知常见的
 型离子晶体的离子半径比和配位数的关系如下表:
型离子晶体的离子半径比和配位数的关系如下表: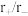 | 配位数 | 晶胞类型 |
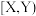 | 4 | 立方 |
 | 6 |  |
 | 8 |  |
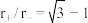 。
。①

②
 晶胞为立方
晶胞为立方 型,而
型,而 等的晶胞为
等的晶胞为 型。请结合上表,解释出现此结果的原因:
型。请结合上表,解释出现此结果的原因:
您最近一年使用:0次
昨日更新
|
94次组卷
|
2卷引用:2024届河南省信阳高级中学高三下学期考前最后一卷理科综合试题-高中化学
2 . 硫酰氯( )是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用
)是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用 和
和 反应合成
反应合成 。
。
已知:① 。
。
② 的熔点为
的熔点为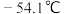 ,沸点为
,沸点为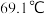 ;
; 以上会分解;遇水能发生剧烈反应,并产生白雾。
以上会分解;遇水能发生剧烈反应,并产生白雾。
回答下列问题:
(1)从甲~戊中选择合适的装置(可以重复选用)制备 ,正确的连接顺序是
,正确的连接顺序是
_______ 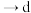 (用小写字母表示)。
(用小写字母表示)。_______ ;仪器Y中盛放的试剂为_______ (填名称),其作用为_______ 。
(3)装置丙中发生反应的离子方程式为_______ 。
(4)装置丁的作用有除去少量 气体、平衡气压和
气体、平衡气压和_______ 。
(5)硫酰氯纯度的测定:取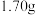 硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为
硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为 溶液,取
溶液,取 该溶液于锥形瓶中,调
该溶液于锥形瓶中,调 为
为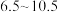 ,加入少量
,加入少量 作指示剂,用
作指示剂,用 的
的 标准溶液滴定(滴定过程中
标准溶液滴定(滴定过程中 不参与反应),平行滴定三次,平均消耗
不参与反应),平行滴定三次,平均消耗 标准溶液
标准溶液 。
。
①下列操作使测定结果偏低的是_______ (填字母)。
A.调节 过低
过低
B.滴定终点时,俯视标准液液面读数
C.锥形瓶未用待测液润洗
②该硫酰氯产品的纯度为_______ 。
(6)亚硫酰氯( )易水解,被广泛应用于结晶水合物的脱水。将
)易水解,被广泛应用于结晶水合物的脱水。将 与
与 混合并加热,可得到无水
混合并加热,可得到无水 ,写出该反应的化学方程式:
,写出该反应的化学方程式:_______ 。
 )是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用
)是一种重要的化工试剂,被广泛应用于制造医药品、染料、表面活性剂等。某兴趣小组在实验室利用 和
和 反应合成
反应合成 。
。已知:①
 。
。②
 的熔点为
的熔点为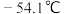 ,沸点为
,沸点为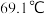 ;
; 以上会分解;遇水能发生剧烈反应,并产生白雾。
以上会分解;遇水能发生剧烈反应,并产生白雾。回答下列问题:
(1)从甲~戊中选择合适的装置(可以重复选用)制备
 ,正确的连接顺序是
,正确的连接顺序是
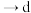 (用小写字母表示)。
(用小写字母表示)。
(3)装置丙中发生反应的离子方程式为
(4)装置丁的作用有除去少量
 气体、平衡气压和
气体、平衡气压和(5)硫酰氯纯度的测定:取
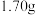 硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为
硫酰氯产品在密闭条件下溶于烧碱溶液,最后定容为 溶液,取
溶液,取 该溶液于锥形瓶中,调
该溶液于锥形瓶中,调 为
为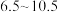 ,加入少量
,加入少量 作指示剂,用
作指示剂,用 的
的 标准溶液滴定(滴定过程中
标准溶液滴定(滴定过程中 不参与反应),平行滴定三次,平均消耗
不参与反应),平行滴定三次,平均消耗 标准溶液
标准溶液 。
。①下列操作使测定结果偏低的是
A.调节
 过低
过低B.滴定终点时,俯视标准液液面读数
C.锥形瓶未用待测液润洗
②该硫酰氯产品的纯度为
(6)亚硫酰氯(
 )易水解,被广泛应用于结晶水合物的脱水。将
)易水解,被广泛应用于结晶水合物的脱水。将 与
与 混合并加热,可得到无水
混合并加热,可得到无水 ,写出该反应的化学方程式:
,写出该反应的化学方程式:
您最近一年使用:0次
2024-05-30更新
|
99次组卷
|
3卷引用:2024届河南省安阳市高三下学期第三次模拟考试理科综合试题-高中化学
3 .  的捕集和利用是实现“碳中和”的有效途径。
的捕集和利用是实现“碳中和”的有效途径。
(1)CaO可在较高温度下捕集 。工业制备CaO的工艺有两种:
。工业制备CaO的工艺有两种:
ⅰ. 热分解制备
热分解制备
ⅱ. 热分解制备
热分解制备
其中 在隔绝空气加热升温过程中固体残留率的变化如图1所示(
在隔绝空气加热升温过程中固体残留率的变化如图1所示( )。
)。_______ (填化学式,下同)转化为_______ 。
②已知分解反应放出的气体越多,制得的固体越疏松多孔,则工艺_______ (填“ⅰ”或“ⅱ”)得到的CaO具有更好的 捕集性能。
捕集性能。
(2)在恒容密闭反应器中充入物质的量之比为1:1的 和
和 的混合气体,可发生以下反应:
的混合气体,可发生以下反应:
ⅰ.
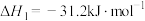
ⅱ.

在相同时间内, 的转化率、HCOOH的选择性与温度的关系如图2所示。
的转化率、HCOOH的选择性与温度的关系如图2所示。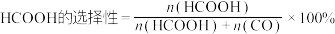 ,CO的选择性与HCOOH的选择性的计算方式相似。
,CO的选择性与HCOOH的选择性的计算方式相似。
①反应ⅰ在相对_______ (填“较低”或“较高”)温度下易自发进行;温度低于673K时,CO的选择性随温度升高而_______ (填字母)。
a.减小 b.增大 c.不变 d.无法判断
②温度高于673K时,随温度升高,HCOOH的选择性减小的原因可能是_______ (已知反应均未达到平衡状态)。
③平衡时再充入0.1mol 和0.1mol
和0.1mol  ,再次平衡时
,再次平衡时 的转化率
的转化率_______ (填“减小”“增大”或“不变”)。
(3)一定温度时,将一定量的 和
和 (物质的量之比为1:1)充入某恒容密闭容器中发生(2)中反应ⅰ和ⅱ,达到平衡时
(物质的量之比为1:1)充入某恒容密闭容器中发生(2)中反应ⅰ和ⅱ,达到平衡时 的转化率为y,CO的选择性为x,体系中氢气的分压为
的转化率为y,CO的选择性为x,体系中氢气的分压为 ,则反应ⅰ的压强平衡常数
,则反应ⅰ的压强平衡常数
_______  (用含x、y、
(用含x、y、 的代数式表示)。
的代数式表示)。
(4)研究发现,用氮化铁作催化材料,对 选择性加氢制烃类具有重要意义。某氮化铁的晶胞结构如图3所示,沿z轴方向的投影如图4所示,A原子的分数坐标为(0,0,0),B原子的分数坐标为
选择性加氢制烃类具有重要意义。某氮化铁的晶胞结构如图3所示,沿z轴方向的投影如图4所示,A原子的分数坐标为(0,0,0),B原子的分数坐标为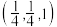 ,则C原子的分数坐标为
,则C原子的分数坐标为_______ (用含b、c的代数式表示);设阿伏加德罗常数的值为 ,该晶体的密度为
,该晶体的密度为_______ g· (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。
 的捕集和利用是实现“碳中和”的有效途径。
的捕集和利用是实现“碳中和”的有效途径。(1)CaO可在较高温度下捕集
 。工业制备CaO的工艺有两种:
。工业制备CaO的工艺有两种:ⅰ.
 热分解制备
热分解制备ⅱ.
 热分解制备
热分解制备其中
 在隔绝空气加热升温过程中固体残留率的变化如图1所示(
在隔绝空气加热升温过程中固体残留率的变化如图1所示( )。
)。
②已知分解反应放出的气体越多,制得的固体越疏松多孔,则工艺
 捕集性能。
捕集性能。(2)在恒容密闭反应器中充入物质的量之比为1:1的
 和
和 的混合气体,可发生以下反应:
的混合气体,可发生以下反应:ⅰ.

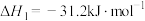
ⅱ.


在相同时间内,
 的转化率、HCOOH的选择性与温度的关系如图2所示。
的转化率、HCOOH的选择性与温度的关系如图2所示。
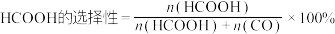 ,CO的选择性与HCOOH的选择性的计算方式相似。
,CO的选择性与HCOOH的选择性的计算方式相似。①反应ⅰ在相对
a.减小 b.增大 c.不变 d.无法判断
②温度高于673K时,随温度升高,HCOOH的选择性减小的原因可能是
③平衡时再充入0.1mol
 和0.1mol
和0.1mol  ,再次平衡时
,再次平衡时 的转化率
的转化率(3)一定温度时,将一定量的
 和
和 (物质的量之比为1:1)充入某恒容密闭容器中发生(2)中反应ⅰ和ⅱ,达到平衡时
(物质的量之比为1:1)充入某恒容密闭容器中发生(2)中反应ⅰ和ⅱ,达到平衡时 的转化率为y,CO的选择性为x,体系中氢气的分压为
的转化率为y,CO的选择性为x,体系中氢气的分压为 ,则反应ⅰ的压强平衡常数
,则反应ⅰ的压强平衡常数
 (用含x、y、
(用含x、y、 的代数式表示)。
的代数式表示)。(4)研究发现,用氮化铁作催化材料,对
 选择性加氢制烃类具有重要意义。某氮化铁的晶胞结构如图3所示,沿z轴方向的投影如图4所示,A原子的分数坐标为(0,0,0),B原子的分数坐标为
选择性加氢制烃类具有重要意义。某氮化铁的晶胞结构如图3所示,沿z轴方向的投影如图4所示,A原子的分数坐标为(0,0,0),B原子的分数坐标为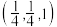 ,则C原子的分数坐标为
,则C原子的分数坐标为 ,该晶体的密度为
,该晶体的密度为 (用含a、b、
(用含a、b、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
2024-05-30更新
|
58次组卷
|
2卷引用:2024届河南省名校联盟高三考前模拟大联考(三模)理综试题-高中化学
4 . 葡萄糖酸锌 是一种有机补锌剂,易溶于热水,不溶于乙醇,温度高于100℃即开始分解。化学间接合成法制备葡萄糖酸锌的过程如下图所示。
是一种有机补锌剂,易溶于热水,不溶于乙醇,温度高于100℃即开始分解。化学间接合成法制备葡萄糖酸锌的过程如下图所示。
称取ag产品配成溶液置于锥形瓶中,加入铬黑T指示剂,用 的EDTA进行滴定,消耗EDTA的体积平均为VmL。[
的EDTA进行滴定,消耗EDTA的体积平均为VmL。[ 代表EDTA,EDTA与
代表EDTA,EDTA与 形成无色的配合物
形成无色的配合物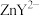 ,铬黑T离子
,铬黑T离子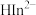 (蓝色)能与
(蓝色)能与 形成紫红色的
形成紫红色的 。滴定原理为:
。滴定原理为: (紫红色)
(紫红色) (蓝色)
(蓝色)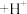 ]
]
已知: 的溶解度如下表:
的溶解度如下表:
回答以下问题:
(1)Ⅰ处稀释浓硫酸时不需要用到下列物品中的________ (填标号)。
(2)Ⅱ处葡萄糖酸钙和稀硫酸反应时需保持温度为90℃,其加热方式为________ 。分离出“滤渣”的操作是________ 。Ⅲ处将滤液通过强酸性离子交换树脂的目的是________ 。
(3)生成葡萄糖酸锌的化学方程式是________ 。
(4)抽滤前加入乙醇,充分搅拌并冷却,析出葡萄糖酸锌固体。加入乙醇的目的是________ ,从而降低产品的溶解度而使其析出。抽滤时滤纸用乙醇湿润,而不能用水湿润的原因是________ 。
(5)滴定终点时溶液的颜色变化为________ 。
(6)产品中Zn的含量为________ 。
 是一种有机补锌剂,易溶于热水,不溶于乙醇,温度高于100℃即开始分解。化学间接合成法制备葡萄糖酸锌的过程如下图所示。
是一种有机补锌剂,易溶于热水,不溶于乙醇,温度高于100℃即开始分解。化学间接合成法制备葡萄糖酸锌的过程如下图所示。
称取ag产品配成溶液置于锥形瓶中,加入铬黑T指示剂,用
 的EDTA进行滴定,消耗EDTA的体积平均为VmL。[
的EDTA进行滴定,消耗EDTA的体积平均为VmL。[ 代表EDTA,EDTA与
代表EDTA,EDTA与 形成无色的配合物
形成无色的配合物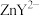 ,铬黑T离子
,铬黑T离子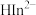 (蓝色)能与
(蓝色)能与 形成紫红色的
形成紫红色的 。滴定原理为:
。滴定原理为: (紫红色)
(紫红色) (蓝色)
(蓝色)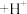 ]
]已知:
 的溶解度如下表:
的溶解度如下表:温度/℃ | 40 | 50 | 60 | 70 |
| 0.210 | 0.207 | 0.201 | 0.193 |
(1)Ⅰ处稀释浓硫酸时不需要用到下列物品中的
|
|
|
|
| A.实验服 | B.护目镜 | C.医用橡胶手套 | D.防毒面具 |
(3)生成葡萄糖酸锌的化学方程式是
(4)抽滤前加入乙醇,充分搅拌并冷却,析出葡萄糖酸锌固体。加入乙醇的目的是
(5)滴定终点时溶液的颜色变化为
(6)产品中Zn的含量为
您最近一年使用:0次
名校
解题方法
5 . 某学习小组为探究化合物 [化学式为
[化学式为 ]的性质,设计并完成如下实验:
]的性质,设计并完成如下实验:
I.取少量固体 ,加入稀盐酸,固体溶解,有无色气体逸出,且生成蓝色溶液。
,加入稀盐酸,固体溶解,有无色气体逸出,且生成蓝色溶液。
Ⅱ.取 固体
固体 ,按如图装置进行实验(夹持装置略,装置
,按如图装置进行实验(夹持装置略,装置 和
和 中为常见药品):
中为常见药品):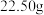 残渣
残渣 ,装置c增重
,装置c增重 ;
;
Ⅲ.将Ⅱ中的残渣B加入到水中,部分溶解,离心分离出 红色固体
红色固体 (单一成分),向溶解液中继续加水至
(单一成分),向溶解液中继续加水至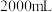 得到溶液
得到溶液 ;
;
IV.测定溶液 的
的 ,再取
,再取 溶液
溶液 加入足量的稀硫酸,得到
加入足量的稀硫酸,得到 白色沉淀
白色沉淀 。
。
V.将红色固体 溶于稀硝酸得到蓝色溶液,加入过量的氨水生成深蓝色溶液
溶于稀硝酸得到蓝色溶液,加入过量的氨水生成深蓝色溶液 。
。
回答下列问题:
(1)步骤Ⅱ中:
①装置 用石英管,而不用普通玻璃管的原因是
用石英管,而不用普通玻璃管的原因是___________ ,装置 中的前段和后段分别盛有一种试剂,有检测气体产物中某一成分的作用,装置
中的前段和后段分别盛有一种试剂,有检测气体产物中某一成分的作用,装置 中盛放药品的方法是
中盛放药品的方法是___________ ;装置 的作用是
的作用是___________ 。
②停止加热后的实验操作是___________ 。
(2)步骤Ⅲ中向溶解液继续加水至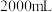 得到溶液
得到溶液 时,一定未用到下列仪器中的
时,一定未用到下列仪器中的___________ (填名称)。 的
的 的实验操作是
的实验操作是___________ ;溶液 是
是___________ (填“单一溶质”或“混合溶质”),理由是___________ 。
(4)步骤V中红色固体 溶于稀硝酸发生反应的离子方程式是
溶于稀硝酸发生反应的离子方程式是___________ 。
(5) 中的z:w=
中的z:w=___________ 。
 [化学式为
[化学式为 ]的性质,设计并完成如下实验:
]的性质,设计并完成如下实验:I.取少量固体
 ,加入稀盐酸,固体溶解,有无色气体逸出,且生成蓝色溶液。
,加入稀盐酸,固体溶解,有无色气体逸出,且生成蓝色溶液。Ⅱ.取
 固体
固体 ,按如图装置进行实验(夹持装置略,装置
,按如图装置进行实验(夹持装置略,装置 和
和 中为常见药品):
中为常见药品):
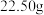 残渣
残渣 ,装置c增重
,装置c增重 ;
;Ⅲ.将Ⅱ中的残渣B加入到水中,部分溶解,离心分离出
 红色固体
红色固体 (单一成分),向溶解液中继续加水至
(单一成分),向溶解液中继续加水至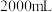 得到溶液
得到溶液 ;
;IV.测定溶液
 的
的 ,再取
,再取 溶液
溶液 加入足量的稀硫酸,得到
加入足量的稀硫酸,得到 白色沉淀
白色沉淀 。
。V.将红色固体
 溶于稀硝酸得到蓝色溶液,加入过量的氨水生成深蓝色溶液
溶于稀硝酸得到蓝色溶液,加入过量的氨水生成深蓝色溶液 。
。回答下列问题:
(1)步骤Ⅱ中:
①装置
 用石英管,而不用普通玻璃管的原因是
用石英管,而不用普通玻璃管的原因是 中的前段和后段分别盛有一种试剂,有检测气体产物中某一成分的作用,装置
中的前段和后段分别盛有一种试剂,有检测气体产物中某一成分的作用,装置 中盛放药品的方法是
中盛放药品的方法是 的作用是
的作用是②停止加热后的实验操作是
(2)步骤Ⅲ中向溶解液继续加水至
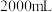 得到溶液
得到溶液 时,一定未用到下列仪器中的
时,一定未用到下列仪器中的
 的
的 的实验操作是
的实验操作是 是
是(4)步骤V中红色固体
 溶于稀硝酸发生反应的离子方程式是
溶于稀硝酸发生反应的离子方程式是(5)
 中的z:w=
中的z:w=
您最近一年使用:0次
6 . 碘酸钙[ ]为白色结晶性粉末,微溶于水,不溶于乙醇,主要用作防臭剂、药物和食品添加剂。某同学在实验室制备
]为白色结晶性粉末,微溶于水,不溶于乙醇,主要用作防臭剂、药物和食品添加剂。某同学在实验室制备 实验步骤如下:
实验步骤如下:
Ⅰ.将一定质量的 、
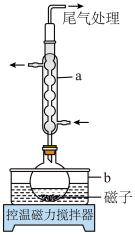
、 和45mL水加入圆底烧瓶中,再加入几滴盐酸,使溶液的pH≈1,控制温度在85℃回流大约1h;
和45mL水加入圆底烧瓶中,再加入几滴盐酸,使溶液的pH≈1,控制温度在85℃回流大约1h;
Ⅱ.步骤Ⅰ反应完毕后,将烧瓶内的混合液倒入烧杯中,滴入KOH溶液调节pH=10,然后用滴管逐滴加入1 的
的 溶液,至沉淀完全。经一系列操作,得到碘酸钙粗品;
溶液,至沉淀完全。经一系列操作,得到碘酸钙粗品;
Ⅲ.碘酸钙粗品纯度:准确称取a g碘酸钙粗品于烧杯中,加入10mL 将其溶解,转移至250mL容量瓶中定容,移取25.00 mL溶液于锥形瓶中,再加入1mL
将其溶解,转移至250mL容量瓶中定容,移取25.00 mL溶液于锥形瓶中,再加入1mL  、20mL KI溶液,在避光处放置3min,加入50mL水,用淀粉作指示剂,用
、20mL KI溶液,在避光处放置3min,加入50mL水,用淀粉作指示剂,用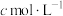 的
的 溶液滴定,平行三次,平均消耗
溶液滴定,平行三次,平均消耗 溶液的体积为V mL(
溶液的体积为V mL( )
)
(1)仪器a的名称为___________ ,b中应盛放的最佳传热介质是___________ 。
(2)步骤Ⅰ中反应生成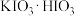 、
、 等,写出反应的化学方程式:
等,写出反应的化学方程式:___________ 。反应过程中,在烧瓶瓶颈或仪器a下口处可能会看到___________ (填物质名称)析出,其原因是___________ 。
(3)步骤Ⅱ“一系列操作”包括静置、___________ 、洗涤、干燥,其中洗涤所用较佳试剂为___________ (填“水”或“乙醇”)。
(4)碘酸钙粗晶纯度为___________ %(用含a、c、V的代数式表示),下列情况导致产品纯度测定结果偏低的是___________ (填字母)。
A.所配待测溶液中含有 少量沉淀 B.定容时俯视读数
少量沉淀 B.定容时俯视读数
C.盛放 溶液的滴定管未润洗 D.滴定后俯视读数
溶液的滴定管未润洗 D.滴定后俯视读数
 ]为白色结晶性粉末,微溶于水,不溶于乙醇,主要用作防臭剂、药物和食品添加剂。某同学在实验室制备
]为白色结晶性粉末,微溶于水,不溶于乙醇,主要用作防臭剂、药物和食品添加剂。某同学在实验室制备 实验步骤如下:
实验步骤如下:Ⅰ.将一定质量的
 、
、 和45mL水加入圆底烧瓶中,再加入几滴盐酸,使溶液的pH≈1,控制温度在85℃回流大约1h;
和45mL水加入圆底烧瓶中,再加入几滴盐酸,使溶液的pH≈1,控制温度在85℃回流大约1h;Ⅱ.步骤Ⅰ反应完毕后,将烧瓶内的混合液倒入烧杯中,滴入KOH溶液调节pH=10,然后用滴管逐滴加入1
 的
的 溶液,至沉淀完全。经一系列操作,得到碘酸钙粗品;
溶液,至沉淀完全。经一系列操作,得到碘酸钙粗品;Ⅲ.碘酸钙粗品纯度:准确称取a g碘酸钙粗品于烧杯中,加入10mL
 将其溶解,转移至250mL容量瓶中定容,移取25.00 mL溶液于锥形瓶中,再加入1mL
将其溶解,转移至250mL容量瓶中定容,移取25.00 mL溶液于锥形瓶中,再加入1mL  、20mL KI溶液,在避光处放置3min,加入50mL水,用淀粉作指示剂,用
、20mL KI溶液,在避光处放置3min,加入50mL水,用淀粉作指示剂,用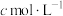 的
的 溶液滴定,平行三次,平均消耗
溶液滴定,平行三次,平均消耗 溶液的体积为V mL(
溶液的体积为V mL( )
)
(1)仪器a的名称为
(2)步骤Ⅰ中反应生成
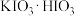 、
、 等,写出反应的化学方程式:
等,写出反应的化学方程式:(3)步骤Ⅱ“一系列操作”包括静置、
(4)碘酸钙粗晶纯度为
A.所配待测溶液中含有
 少量沉淀 B.定容时俯视读数
少量沉淀 B.定容时俯视读数C.盛放
 溶液的滴定管未润洗 D.滴定后俯视读数
溶液的滴定管未润洗 D.滴定后俯视读数
您最近一年使用:0次
2024-05-27更新
|
180次组卷
|
3卷引用:2024届河南省九师联盟2023-2024学年高三下学期4月联考理综试题-高中化学
7 . 硫酸亚硝酰合铁(Ⅱ)在现代化工行业有着广泛的应用,其一种工业制备流程如图所示。回答下列问题:

(1)“洗涤”的具体操作是将废铁屑置于 溶液中并加热至沸腾一段时间,加热至沸腾的好处是
溶液中并加热至沸腾一段时间,加热至沸腾的好处是___________ ,请写出“酸浸”副产物的一种用途:___________ 。
(2)“合成”阶段可在如图所示的装置中完成(加热及夹持装置略)。___________ ,向圆底烧瓶中加入稀硫酸前需要先通入一段时间的 ,否则易出现的不良后果是
,否则易出现的不良后果是___________ 。
②装置 中有
中有 生成,反应的离子方程式为
生成,反应的离子方程式为___________ ,装置 的作用是
的作用是___________ 。
③硫酸亚硝酰合铁(Ⅱ)化学式的确定。
(3)取一定量产品溶于水配制成 溶液,进行实验:
溶液,进行实验:
ⅰ.取 配制的溶液于试管中,加入足量
配制的溶液于试管中,加入足量 溶液,最终可得到
溶液,最终可得到 干燥纯净的白色沉淀。
干燥纯净的白色沉淀。
ⅱ.取 配制的溶液于试管中,用
配制的溶液于试管中,用 酸性
酸性 溶液滴定,滴定至终点时消耗酸性
溶液滴定,滴定至终点时消耗酸性 溶液
溶液 (最终氮元素全部以
(最终氮元素全部以 形式存在)。
形式存在)。
①“步骤ⅱ”滴定终点时的现象为___________ ,产品中
___________ 。
②若要确定产品化学式,则还需要获得一个数据,该数据是___________ 。

(1)“洗涤”的具体操作是将废铁屑置于
 溶液中并加热至沸腾一段时间,加热至沸腾的好处是
溶液中并加热至沸腾一段时间,加热至沸腾的好处是(2)“合成”阶段可在如图所示的装置中完成(加热及夹持装置略)。

 ,否则易出现的不良后果是
,否则易出现的不良后果是②装置
 中有
中有 生成,反应的离子方程式为
生成,反应的离子方程式为 的作用是
的作用是③硫酸亚硝酰合铁(Ⅱ)化学式的确定。
(3)取一定量产品溶于水配制成
 溶液,进行实验:
溶液,进行实验:ⅰ.取
 配制的溶液于试管中,加入足量
配制的溶液于试管中,加入足量 溶液,最终可得到
溶液,最终可得到 干燥纯净的白色沉淀。
干燥纯净的白色沉淀。ⅱ.取
 配制的溶液于试管中,用
配制的溶液于试管中,用 酸性
酸性 溶液滴定,滴定至终点时消耗酸性
溶液滴定,滴定至终点时消耗酸性 溶液
溶液 (最终氮元素全部以
(最终氮元素全部以 形式存在)。
形式存在)。①“步骤ⅱ”滴定终点时的现象为

②若要确定产品化学式,则还需要获得一个数据,该数据是
您最近一年使用:0次
解题方法
8 . 葡萄糖酸锌 (相对分子质量为455)作为有机补锌剂,易溶于热水,具有良好的抗氧化性能。可以通过葡萄糖酸钙与硫酸锌直接反应制备,具体步骤如下:
(相对分子质量为455)作为有机补锌剂,易溶于热水,具有良好的抗氧化性能。可以通过葡萄糖酸钙与硫酸锌直接反应制备,具体步骤如下:
 .取200mL烧杯,加水,加热至80~90℃,加入
.取200mL烧杯,加水,加热至80~90℃,加入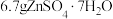 ,用玻璃棒搅拌至完全溶解。
,用玻璃棒搅拌至完全溶解。
 .将烧杯置于90℃水浴中,逐渐加入10.0g葡萄糖酸钙,搅拌至完全溶解,静置保温20min。
.将烧杯置于90℃水浴中,逐渐加入10.0g葡萄糖酸钙,搅拌至完全溶解,静置保温20min。
 .趁热减压过滤,弃去滤渣;滤液转入烧杯,加热近沸,用小火加热浓缩至黏稠状,将滤液冷却到室温,加入95%乙醇20mL,此时有大量的胶状葡萄糖酸锌析出,搅拌,用倾析法去除清液。再加20mL95%乙醇,充分搅拌后,慢慢析出晶体,抽滤至干,得到葡萄糖酸锌粗品。
.趁热减压过滤,弃去滤渣;滤液转入烧杯,加热近沸,用小火加热浓缩至黏稠状,将滤液冷却到室温,加入95%乙醇20mL,此时有大量的胶状葡萄糖酸锌析出,搅拌,用倾析法去除清液。再加20mL95%乙醇,充分搅拌后,慢慢析出晶体,抽滤至干,得到葡萄糖酸锌粗品。
 .取粗品经重结晶并干燥得到无色晶体,准确称取2.3g样品,配成100mL溶液。
.取粗品经重结晶并干燥得到无色晶体,准确称取2.3g样品,配成100mL溶液。
 .纯度测定:移取25.00mL溶液于锥形瓶中,加10mL氨-氯化铵缓冲液、4滴铬黑T(EBT)指示剂,用
.纯度测定:移取25.00mL溶液于锥形瓶中,加10mL氨-氯化铵缓冲液、4滴铬黑T(EBT)指示剂,用 标准溶液滴定至终点,三次滴定平均消耗EDTA标准溶液的体积为24.79mL。
标准溶液滴定至终点,三次滴定平均消耗EDTA标准溶液的体积为24.79mL。
已知:滴定中的反应原理为
回答下列问题:
(1)葡萄糖酸钙与硫酸锌反应的化学方程式为___________ 。
(2)本实验中___________ (填“能”或“不能”)用氯化锌替代硫酸锌,理由是___________ 。
(3)步骤 中用到的倾析法通常用于所得沉淀的结晶颗粒较大或比重较大,静置后易沉降的固、液间的分离,在该操作方法中除了使用烧杯外,还需要使用的一种玻璃仪器是
中用到的倾析法通常用于所得沉淀的结晶颗粒较大或比重较大,静置后易沉降的固、液间的分离,在该操作方法中除了使用烧杯外,还需要使用的一种玻璃仪器是___________ 。实验中加入95%乙醇,其作用是___________ 。
(4)步骤 重结晶时,需进行的操作有①加入10mL95%乙醇,搅拌;②加入10mL90℃热水,搅拌;③待结晶析出后,减压过滤;④趁热减压过滤,滤液冷却至室温。正确的顺序为
重结晶时,需进行的操作有①加入10mL95%乙醇,搅拌;②加入10mL90℃热水,搅拌;③待结晶析出后,减压过滤;④趁热减压过滤,滤液冷却至室温。正确的顺序为___________ (填标号)。
(5)为了测定葡萄糖酸锌的纯度,步骤 采用了络合置换滴定法。
采用了络合置换滴定法。
①下列关于滴定分析的实验操作错误的是___________ 。
A.平行滴定时,需重新装液并调节液面至“0”刻度或“0”刻度以下某一刻度
B.排出酸式滴定管中的气泡时,应控制活塞使液体快速流下
C.在接近滴定终点时,改为滴加半滴液可提高测量的准确度
D.滴定时左手控制活塞,右手摇动锥形瓶,眼晴注视滴定管中溶液体积的变化
②用EDTA溶液滴定,标志滴定终点的现象是___________ 。
(6)样品中葡萄糖酸锌的含量为___________ %(保留四位有效数字)。
 (相对分子质量为455)作为有机补锌剂,易溶于热水,具有良好的抗氧化性能。可以通过葡萄糖酸钙与硫酸锌直接反应制备,具体步骤如下:
(相对分子质量为455)作为有机补锌剂,易溶于热水,具有良好的抗氧化性能。可以通过葡萄糖酸钙与硫酸锌直接反应制备,具体步骤如下: .取200mL烧杯,加水,加热至80~90℃,加入
.取200mL烧杯,加水,加热至80~90℃,加入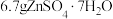 ,用玻璃棒搅拌至完全溶解。
,用玻璃棒搅拌至完全溶解。 .将烧杯置于90℃水浴中,逐渐加入10.0g葡萄糖酸钙,搅拌至完全溶解,静置保温20min。
.将烧杯置于90℃水浴中,逐渐加入10.0g葡萄糖酸钙,搅拌至完全溶解,静置保温20min。 .趁热减压过滤,弃去滤渣;滤液转入烧杯,加热近沸,用小火加热浓缩至黏稠状,将滤液冷却到室温,加入95%乙醇20mL,此时有大量的胶状葡萄糖酸锌析出,搅拌,用倾析法去除清液。再加20mL95%乙醇,充分搅拌后,慢慢析出晶体,抽滤至干,得到葡萄糖酸锌粗品。
.趁热减压过滤,弃去滤渣;滤液转入烧杯,加热近沸,用小火加热浓缩至黏稠状,将滤液冷却到室温,加入95%乙醇20mL,此时有大量的胶状葡萄糖酸锌析出,搅拌,用倾析法去除清液。再加20mL95%乙醇,充分搅拌后,慢慢析出晶体,抽滤至干,得到葡萄糖酸锌粗品。 .取粗品经重结晶并干燥得到无色晶体,准确称取2.3g样品,配成100mL溶液。
.取粗品经重结晶并干燥得到无色晶体,准确称取2.3g样品,配成100mL溶液。 .纯度测定:移取25.00mL溶液于锥形瓶中,加10mL氨-氯化铵缓冲液、4滴铬黑T(EBT)指示剂,用
.纯度测定:移取25.00mL溶液于锥形瓶中,加10mL氨-氯化铵缓冲液、4滴铬黑T(EBT)指示剂,用 标准溶液滴定至终点,三次滴定平均消耗EDTA标准溶液的体积为24.79mL。
标准溶液滴定至终点,三次滴定平均消耗EDTA标准溶液的体积为24.79mL。已知:滴定中的反应原理为

回答下列问题:
(1)葡萄糖酸钙与硫酸锌反应的化学方程式为
(2)本实验中
(3)步骤
 中用到的倾析法通常用于所得沉淀的结晶颗粒较大或比重较大,静置后易沉降的固、液间的分离,在该操作方法中除了使用烧杯外,还需要使用的一种玻璃仪器是
中用到的倾析法通常用于所得沉淀的结晶颗粒较大或比重较大,静置后易沉降的固、液间的分离,在该操作方法中除了使用烧杯外,还需要使用的一种玻璃仪器是(4)步骤
 重结晶时,需进行的操作有①加入10mL95%乙醇,搅拌;②加入10mL90℃热水,搅拌;③待结晶析出后,减压过滤;④趁热减压过滤,滤液冷却至室温。正确的顺序为
重结晶时,需进行的操作有①加入10mL95%乙醇,搅拌;②加入10mL90℃热水,搅拌;③待结晶析出后,减压过滤;④趁热减压过滤,滤液冷却至室温。正确的顺序为(5)为了测定葡萄糖酸锌的纯度,步骤
 采用了络合置换滴定法。
采用了络合置换滴定法。①下列关于滴定分析的实验操作错误的是
A.平行滴定时,需重新装液并调节液面至“0”刻度或“0”刻度以下某一刻度
B.排出酸式滴定管中的气泡时,应控制活塞使液体快速流下
C.在接近滴定终点时,改为滴加半滴液可提高测量的准确度
D.滴定时左手控制活塞,右手摇动锥形瓶,眼晴注视滴定管中溶液体积的变化
②用EDTA溶液滴定,标志滴定终点的现象是
(6)样品中葡萄糖酸锌的含量为
您最近一年使用:0次
2024-05-23更新
|
74次组卷
|
2卷引用:2024届河南省平许济洛四市高三下学期第四次质量检测理科综合试题-高中化学
9 . 某化学兴趣小组探究一种硫酸盐晶体的组成,其实验过程如图所示。下列说法正确的是
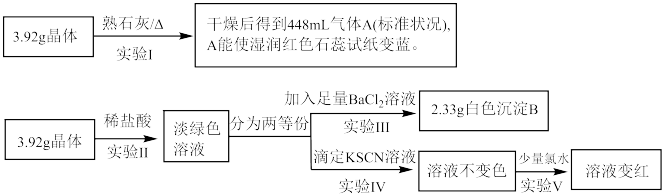
A.该硫酸盐的化学式为 |
| B.实验Ⅲ的操作包括过滤、洗涤、干燥、称量 |
C.由实验Ⅲ数据可知3.92g晶体中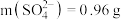 |
D.上述实验过程可证明该晶体中含有 |
您最近一年使用:0次
解题方法
10 . 闪锌矿的主要成分为ZnS,其中含有大量的铁元素以及少量的CuO等。湿法浸取闪锌矿制备 和
和 的工艺流程如下图所示。请回答以下问题。
的工艺流程如下图所示。请回答以下问题。 的价电子排布图为
的价电子排布图为________ 。同周期和基态Cu原子具有相同未成对电子数目的元素还有________ 种。
(2)酸浸时 的作用为
的作用为________ 。铜元素在滤渣中的存在形式为________ 。
(3)加入铁粉还原脱酸的优点是________ 。
(4)浓缩结晶时,溶液蒸发至________ 即停止加热。
(5)针铁矿法除铁是在常温下将 缓慢氧化,使铁元素以针铁矿形式形成沉淀而达到除铁的目的。针铁矿法除铁的离子方程式为
缓慢氧化,使铁元素以针铁矿形式形成沉淀而达到除铁的目的。针铁矿法除铁的离子方程式为________ 。
(6)把 放到密闭容器内,缓缓抽去其中的水气,
放到密闭容器内,缓缓抽去其中的水气, 分三次脱水。各步脱水过程为一系列动态平衡。剩余固体质量占原来总质量的百分比(η)与容器中水蒸气的压强变化关系如下图所示。
分三次脱水。各步脱水过程为一系列动态平衡。剩余固体质量占原来总质量的百分比(η)与容器中水蒸气的压强变化关系如下图所示。________ ;第三步反应的压强平衡常数为________ Pa;M点时所对应反应的转化率为________ 。
 和
和 的工艺流程如下图所示。请回答以下问题。
的工艺流程如下图所示。请回答以下问题。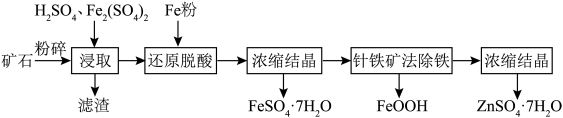
 的价电子排布图为
的价电子排布图为(2)酸浸时
 的作用为
的作用为(3)加入铁粉还原脱酸的优点是
(4)浓缩结晶时,溶液蒸发至
(5)针铁矿法除铁是在常温下将
 缓慢氧化,使铁元素以针铁矿形式形成沉淀而达到除铁的目的。针铁矿法除铁的离子方程式为
缓慢氧化,使铁元素以针铁矿形式形成沉淀而达到除铁的目的。针铁矿法除铁的离子方程式为(6)把
 放到密闭容器内,缓缓抽去其中的水气,
放到密闭容器内,缓缓抽去其中的水气, 分三次脱水。各步脱水过程为一系列动态平衡。剩余固体质量占原来总质量的百分比(η)与容器中水蒸气的压强变化关系如下图所示。
分三次脱水。各步脱水过程为一系列动态平衡。剩余固体质量占原来总质量的百分比(η)与容器中水蒸气的压强变化关系如下图所示。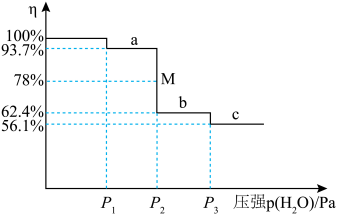
您最近一年使用:0次







