名校
1 . 吸烟有害健康,香烟烟雾中含有CO、CO2、SO2、H2O等气体,用下列物质可将其一一检出:
a.无水硫酸铜b.澄清石灰水c.红热氧化铜d.生石灰e.酸性高锰酸钾溶液f.品红溶液
检出的正确顺序是
a.无水硫酸铜b.澄清石灰水c.红热氧化铜d.生石灰e.酸性高锰酸钾溶液f.品红溶液
检出的正确顺序是
| A.混合气→a→e→b→f→d→c |
| B.混合气→c→d→e→e→a |
| C.混合气→a→e→f→b→d→c |
| D.混合气→b→e→a-→d→c |
您最近半年使用:0次
2023-03-24更新
|
225次组卷
|
3卷引用:河北省石家庄市第二中学西校区2022-2023学年高一下学期3月月考化学试题
2 . 草酸亚铁(FeC2O4)可作为生产电池正极材料磷酸铁锂的原料,受热容易分解,为探究草酸亚铁的热分解产物,按下面所示装置进行实验。下列说法不正确的是
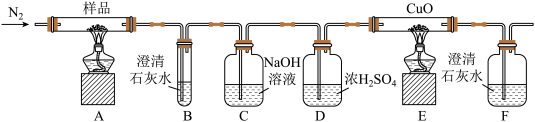
| A.装置D的作用只是除去混合气中的水蒸气,由于草酸亚铁的热分解产物没有水,不用除去水蒸气,所以装置D可以省略 |
| B.实验中观察到装置B、F中石灰水变浑浊,E中固体变为红色,则证明分解产物中有CO2和CO |
| C.实验开始时,应先通入N2,再点燃装置A、E的酒精灯 |
| D.反应结束后,取A中固体溶于稀硫酸,向其中滴加1~2滴KSCN溶液,溶液无颜色变化,证明分解产物中不含Fe2O3 |
您最近半年使用:0次
2023-03-21更新
|
290次组卷
|
3卷引用:重庆市育才中学2022-2023学年高三上学期开学考试化学试题
解题方法
3 . 用石墨作电极电解稀 溶液的装置(如图),电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的pH范围是6.8~8.0,酸性溶液中呈红色,碱性溶液中呈黄色)。下列判断正确的是
溶液的装置(如图),电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的pH范围是6.8~8.0,酸性溶液中呈红色,碱性溶液中呈黄色)。下列判断正确的是
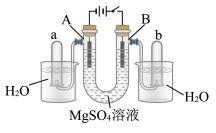
 溶液的装置(如图),电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的pH范围是6.8~8.0,酸性溶液中呈红色,碱性溶液中呈黄色)。下列判断正确的是
溶液的装置(如图),电解液中事先加有指示剂,此时溶液呈红色(指示剂变色的pH范围是6.8~8.0,酸性溶液中呈红色,碱性溶液中呈黄色)。下列判断正确的是
| A.电解过程中,A管溶液由红色变为黄色 |
| B.电解过程中,B管溶液由红色变为黄色 |
C.A管中发生的电极反应为 |
| D.用拇指堵住b管口,取出b管,靠近火焰,移开拇指,有爆鸣声,管口有蓝色火焰 |
您最近半年使用:0次
名校
解题方法
4 .  (三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:
(1)探究三草酸合铁酸钾的热分解产物。
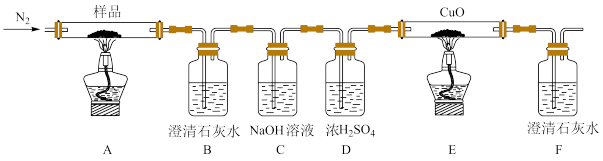
按如上图所示装置进行实验:观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色。
①装置C的作用是_______ 。
②装置E中发生反应的化学方程式为_______ 。
(2)测定三草酸合铁酸钾中铁的含量。
测定原理:

①配制溶液:实验中配制100mL1.0
 溶液,需要的仪器有烧杯、玻璃棒、量筒、
溶液,需要的仪器有烧杯、玻璃棒、量筒、_______ (从下图中选择,写出名称)。

②测定:称量10.00g晶体样品,加1.0
 溶解后配成100
溶解后配成100 溶液。
溶液。
步骤Ⅰ 取20.00 配制好的溶液于锥形瓶中,滴加0.2000
配制好的溶液于锥形瓶中,滴加0.2000
 溶液至恰好完全反应。该操作的目的是
溶液至恰好完全反应。该操作的目的是_______ 。
步骤Ⅱ 向上述溶液中加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中,加稀 酸化,用0.2000
酸化,用0.2000
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液20.00
溶液20.00 。
。
该晶体样品中铁的质量分数为_______ (写出计算过程)。
 (三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:
(三草酸合铁酸钾)为亮绿色晶体,可用于工艺设计和生产科研中晒制蓝图。回答下列问题:(1)探究三草酸合铁酸钾的热分解产物。

按如上图所示装置进行实验:观察到装置B、F中澄清石灰水均变浑浊,装置E中固体变为红色。
①装置C的作用是
②装置E中发生反应的化学方程式为
(2)测定三草酸合铁酸钾中铁的含量。
测定原理:


①配制溶液:实验中配制100mL1.0

 溶液,需要的仪器有烧杯、玻璃棒、量筒、
溶液,需要的仪器有烧杯、玻璃棒、量筒、
②测定:称量10.00g晶体样品,加1.0

 溶解后配成100
溶解后配成100 溶液。
溶液。步骤Ⅰ 取20.00
 配制好的溶液于锥形瓶中,滴加0.2000
配制好的溶液于锥形瓶中,滴加0.2000
 溶液至恰好完全反应。该操作的目的是
溶液至恰好完全反应。该操作的目的是步骤Ⅱ 向上述溶液中加入过量铜粉至反应完全后,过滤、洗涤,将滤液及洗涤液全部收集到锥形瓶中,加稀
 酸化,用0.2000
酸化,用0.2000
 溶液滴定至终点,消耗
溶液滴定至终点,消耗 溶液20.00
溶液20.00 。
。该晶体样品中铁的质量分数为
您最近半年使用:0次
名校
解题方法
5 . 已知硫酸亚铁铵[ ](俗称莫尔盐)可溶于水,在
](俗称莫尔盐)可溶于水,在 时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
Ⅰ. 探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是_______ ,由此可知分解产物中有_______ (填化学式)。
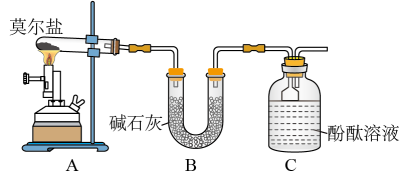
(2)乙同学认为莫尔盐晶体分解的产物中还可能含有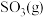 、
、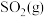 及
及 。为验证产物的存在,用下列装置进行实验。
。为验证产物的存在,用下列装置进行实验。
①乙同学的实验中,装置依次连按的合理顺序为:A→H→→→→G。_______
②证明含有 的实验现象是
的实验现象是_______ 。
Ⅱ. 为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成 溶液。甲、乙两位同学设计了如下两个实验方案。
溶液。甲、乙两位同学设计了如下两个实验方案。
甲方案:取 样品溶液用
样品溶液用 的酸性
的酸性 溶液分三次进行测定。
溶液分三次进行测定。
乙方案(通过 测定):实验设计装置如图所示。取
测定):实验设计装置如图所示。取 样品溶液进行该实验。
样品溶液进行该实验。
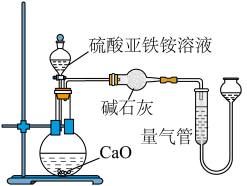
请回答:
(3)乙方案中量气管中最佳试剂是_______ 。
a. 水 b. 饱和 溶液 c.
溶液 c.  d. 饱和
d. 饱和 溶液
溶液
(4)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是_______ 。
(5)若测得 为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
为VL(已折算为标准状况下),则硫酸亚铁铵纯度为_______ (列出计算式)。
 ](俗称莫尔盐)可溶于水,在
](俗称莫尔盐)可溶于水,在 时分解,其探究其化学性质,甲、乙两同学设计了如下实验。
时分解,其探究其化学性质,甲、乙两同学设计了如下实验。Ⅰ. 探究莫尔盐晶体加热时的分解产物。
(1)甲同学设计如图所示的装置进行实验。装置C中可观察到的现象是

(2)乙同学认为莫尔盐晶体分解的产物中还可能含有
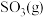 、
、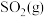 及
及 。为验证产物的存在,用下列装置进行实验。
。为验证产物的存在,用下列装置进行实验。 | 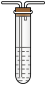 |  | 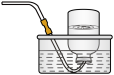 |  |
| D. 品红溶液 | E.  溶液 溶液 | F.  溶液和足量盐酸 溶液和足量盐酸 | G. 排水集气法 | H.安全瓶 |
②证明含有
 的实验现象是
的实验现象是Ⅱ. 为测定硫酸亚铁铵纯度,称取mg莫尔盐样品,配成
 溶液。甲、乙两位同学设计了如下两个实验方案。
溶液。甲、乙两位同学设计了如下两个实验方案。甲方案:取
 样品溶液用
样品溶液用 的酸性
的酸性 溶液分三次进行测定。
溶液分三次进行测定。乙方案(通过
 测定):实验设计装置如图所示。取
测定):实验设计装置如图所示。取 样品溶液进行该实验。
样品溶液进行该实验。
请回答:
(3)乙方案中量气管中最佳试剂是
a. 水 b. 饱和
 溶液 c.
溶液 c.  d. 饱和
d. 饱和 溶液
溶液(4)乙方案中收集完气体并恢复至室温,为了减小实验误差,读数前应进行的操作是
(5)若测得
 为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
为VL(已折算为标准状况下),则硫酸亚铁铵纯度为
您最近半年使用:0次
2023-01-21更新
|
752次组卷
|
3卷引用:山东省青岛第五十八中学2022-2023学年高一上学期期末考试化学试题
解题方法
6 . 氯元素能与许多元素形成种类繁多的化合物,这些含氯化合物在生活及工农业生产中发挥着重要的作用。
(1)从海水中获取粗盐的方法是_______ 。
(2)利用电解饱和食盐水可以制备氢气、氯气、氢氧化钠。电解时阳极产物为_______ ,该产物的检验方法为_______ 。
(3)工业上用氯气和消石灰反应制备漂白粉,其有效成分是_______ (填化学式);写出漂白粉露置在空气中失效过程中所涉及的化学方程式:_______ 、_______ 。
(4)H2与Cl2在点燃条件下可以制取HCl。某同学对HCl性质进行如下预测:
①从物质类别上看,HCl属于酸,其水溶液能与碳酸钙反应,相应的离子方程式为_______ 。
②从化合价角度看,HCl中的Cl元素显-1价,处于氯元素的最低价,因此-1价的Cl元素在反应中可以被_______ (选填“氧化”或“还原”),在一定条件下能与_______ 发生氧化还原反应(填编号)。
a.KI b.NaOH c.KMnO4
(5)已知HClO4是强酸,HClO4在水中的电离方程式为_______ 。
(1)从海水中获取粗盐的方法是
(2)利用电解饱和食盐水可以制备氢气、氯气、氢氧化钠。电解时阳极产物为
(3)工业上用氯气和消石灰反应制备漂白粉,其有效成分是
(4)H2与Cl2在点燃条件下可以制取HCl。某同学对HCl性质进行如下预测:
①从物质类别上看,HCl属于酸,其水溶液能与碳酸钙反应,相应的离子方程式为
②从化合价角度看,HCl中的Cl元素显-1价,处于氯元素的最低价,因此-1价的Cl元素在反应中可以被
a.KI b.NaOH c.KMnO4
(5)已知HClO4是强酸,HClO4在水中的电离方程式为
您最近半年使用:0次
名校
解题方法
7 . 硫酸亚铁在工农业生产中具有广泛的应用。该物质不稳定,受热易分解产生氧化物,具有较强的还原性。某学习小组利用如下装置来探究FeSO4受热分解的产物。
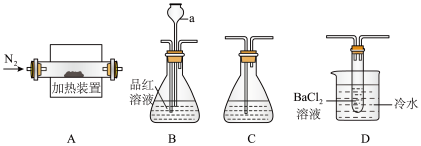
(1)甲组同学利用“A接B接C”的装置来验证产物中含有SO2气体。
①连接好装置后,接下来的操作是_______ 。
②仪器a的名称是_______ ;其作用是_______ 。
(2)乙组同学查阅资料得:硫酸亚铁分解的气体产物中除SO2外还有SO3;SO3的熔点为16.8℃,沸点是46.8℃,溶于水放出大量的热,易形成酸雾。为此设计了“A接D接C”的装置验证产物中含有SO3。
①装置D中的现象是_______ ,BaCl2溶液不能用Ba(NO3)2溶液代替的原因是_______ 。
②装置A中固体变为红棕色,结合两组同学的实验,写出硫酸亚铁分解的化学方程式_______ ;

(1)甲组同学利用“A接B接C”的装置来验证产物中含有SO2气体。
①连接好装置后,接下来的操作是
②仪器a的名称是
(2)乙组同学查阅资料得:硫酸亚铁分解的气体产物中除SO2外还有SO3;SO3的熔点为16.8℃,沸点是46.8℃,溶于水放出大量的热,易形成酸雾。为此设计了“A接D接C”的装置验证产物中含有SO3。
①装置D中的现象是
②装置A中固体变为红棕色,结合两组同学的实验,写出硫酸亚铁分解的化学方程式
您最近半年使用:0次
名校
8 . SO2虽是大气污染物之一,但也是重要的工业原料。某同学在实验室设计了如下实验,对SO2的部分性质进行了探究。
I.二氧化硫的水溶性
(1) SO2易溶于水,溶于水有H2SO3生成。向SO2饱和溶液中加入NaHSO3固体,有气体冒出,原因是_______ (结合有关平衡方程式简要说明)。
II.验证SO2能否与BaCl2溶液反应
某同学设计了如图装置,且所配制的溶液均使用了无氧蒸馏水,检验SO2在无氧干扰时,是否与氯化钡反应生成沉淀。
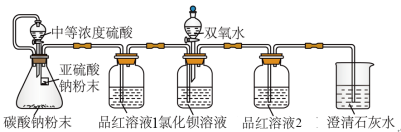
(2)加入碳酸钠粉末的目的是_______ 。
(3)当_______ 时,氯化钡溶液中没有沉淀出现,说明二氧化硫不与氯化钡溶液反应,此时滴加双氧水,出现了白色沉淀。
(4)装置中选用澄清石灰水而不用氢氧化钠溶液的目的是_______ 。
III.二氧化硫的还原性
已知SO2具有还原性,可以还原I2,也可以与Na2O2发生反应。
(5)将SO2通入装有过氧化钠的硬质试管中,将带火星的木条放在试管口处。
①若木条不复燃,则说明SO2与Na2O2反应无O2生成,可能发生反应的化学方程式为_______ 。
②若木条复燃,则说明SO2与Na2O2反应有O2生成,发生反应的化学方程式为2Na2O2+2SO2=2Na2SO3+O2。
(6)将SO2通入装有碘水(含淀粉)的洗气瓶中,若_______ ,说明还原性:SO2>I-,写出该反应的离子方程式:_______ 。
I.二氧化硫的水溶性
(1) SO2易溶于水,溶于水有H2SO3生成。向SO2饱和溶液中加入NaHSO3固体,有气体冒出,原因是
II.验证SO2能否与BaCl2溶液反应
某同学设计了如图装置,且所配制的溶液均使用了无氧蒸馏水,检验SO2在无氧干扰时,是否与氯化钡反应生成沉淀。

(2)加入碳酸钠粉末的目的是
(3)当
(4)装置中选用澄清石灰水而不用氢氧化钠溶液的目的是
III.二氧化硫的还原性
已知SO2具有还原性,可以还原I2,也可以与Na2O2发生反应。
(5)将SO2通入装有过氧化钠的硬质试管中,将带火星的木条放在试管口处。
①若木条不复燃,则说明SO2与Na2O2反应无O2生成,可能发生反应的化学方程式为
②若木条复燃,则说明SO2与Na2O2反应有O2生成,发生反应的化学方程式为2Na2O2+2SO2=2Na2SO3+O2。
(6)将SO2通入装有碘水(含淀粉)的洗气瓶中,若
您最近半年使用:0次
2022-12-31更新
|
305次组卷
|
2卷引用:广东省梅州市名校2022-2023学年高三上学期期末考试化学试题
9 . 铁与水蒸气反应的实验装置如图所示,下列有关该实验的说法不正确 的是
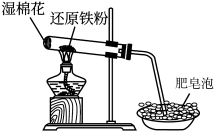

| A.湿棉花的作用是提供水蒸气 |
B.每消耗3mol ,生成4mol ,生成4mol |
| C.点燃酒精灯产生肥皂泡,证明发生了反应 |
D.铁与水蒸气反应生成的固体产物是 |
您最近半年使用:0次
解题方法
10 . 电解原理在化学工业中有广泛应用。如图表示一个电解池,装有电解液a;X、Y是两块电极板,通过导线与直流电源相连。
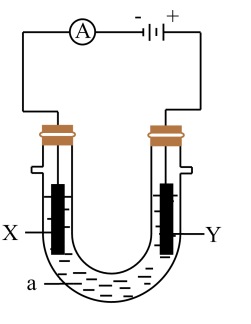
请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:Y电极上的电极反应式为_______ ,检验该电极反应产物的方法是_______ 。
(2)如要用电解方法精炼粗铜,则:X电极的材料是_______ ,电极反应式是_______ 。电解液a可以选用_______ 。

请回答以下问题:
(1)若X、Y都是惰性电极,a是饱和NaCl溶液,实验开始时,同时在两边各滴入几滴酚酞试液,则:Y电极上的电极反应式为
(2)如要用电解方法精炼粗铜,则:X电极的材料是
您最近半年使用:0次



