1 . 下列关于物质或离子检验的叙述正确的是
| A.在溶液中加KSCN,溶液显红色,证明原溶液中有Fe3+,无Fe2+ |
| B.气体通过无水CuSO4,粉末变蓝,证明原气体中含有水蒸气 |
| C.加入AgNO3溶液,生成白色沉淀,加稀盐酸沉淀不溶解时,可确定有Cl-存在 |
| D.将气体通入澄清石灰水,溶液变浑浊,证明原气体是CO2 |
您最近半年使用:0次
解题方法
2 . Na2O2具有强氧化性,H2具有还原性,某实验小组同学推测Na2O2与H2可以发生氧化还原反应,并设计了如下的实验验证自己的推测。
I.实验探究:

(1)装置B名称为___________ ,盛放的试剂是___________ (填选项),其作用是___________ 。
A.浓硫酸 B.碱石灰 C.无水氯化钙 D.无水硫酸铜
(2)以下是实验过程中的主要步骤,正确的操作顺序为___________ ⑤___________ (补全序号)
①组装好实验装置,检查装置的气密性
②停止加热,充分冷却后,关闭止水夹K1和K2
③加热装有Na2O2的硬质玻璃管,使其逐渐熔化,反应一段时间
④打开止水夹K1和K2,通过分液漏斗向A中滴加稀盐酸
⑤用小试管在装置D右侧导管处收集H2,并检验其纯度
(3)在实验过程中观察到C中淡黄色固体逐渐变成白色,无水硫酸铜未变成蓝色,则Na2O2与H2反应的化学方程式为___________ 。
(4)实验结束后,小组同学猜测C中Na2O2可能未完全反应。他们设计了如下实验验证:取少量固体溶于水后,再滴加2-3滴酚酞溶液,能证明Na2O2未完全反应的现象是___________ 。
II.数据处理:
(5)实验结束以后,该小组的同学还测定了C装置内白色固体中未完全反应的Na2O2质量。操作流程如下:

①则白色固体中Na2O2的质量为___________ g(用含m1和m2的代数式表示)。
②若在转移溶液的过程中,不小心将溶液溅到蒸发皿外面,则测得的Na2O2的质量___________ (填“偏大”、“偏小”或“不变”)
I.实验探究:

(1)装置B名称为
A.浓硫酸 B.碱石灰 C.无水氯化钙 D.无水硫酸铜
(2)以下是实验过程中的主要步骤,正确的操作顺序为
①组装好实验装置,检查装置的气密性
②停止加热,充分冷却后,关闭止水夹K1和K2
③加热装有Na2O2的硬质玻璃管,使其逐渐熔化,反应一段时间
④打开止水夹K1和K2,通过分液漏斗向A中滴加稀盐酸
⑤用小试管在装置D右侧导管处收集H2,并检验其纯度
(3)在实验过程中观察到C中淡黄色固体逐渐变成白色,无水硫酸铜未变成蓝色,则Na2O2与H2反应的化学方程式为
(4)实验结束后,小组同学猜测C中Na2O2可能未完全反应。他们设计了如下实验验证:取少量固体溶于水后,再滴加2-3滴酚酞溶液,能证明Na2O2未完全反应的现象是
II.数据处理:
(5)实验结束以后,该小组的同学还测定了C装置内白色固体中未完全反应的Na2O2质量。操作流程如下:

①则白色固体中Na2O2的质量为
②若在转移溶液的过程中,不小心将溶液溅到蒸发皿外面,则测得的Na2O2的质量
您最近半年使用:0次
3 . 固体化合物X由3种元素组成。某学习小组进行了如下实验:
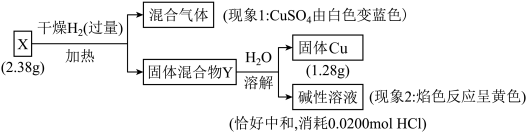
下列推断不正确 的是

下列推断
| A.由现象1得出化合物X含有O元素 |
B.X的化学式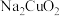 |
C.固体混合物Y的成分可能是 和 和 |
D.若X与浓盐酸反应产生氯气( )气体,则反应中X作氧化剂 )气体,则反应中X作氧化剂 |
您最近半年使用:0次
解题方法
4 . 下列实验操作能达到实验目的的是
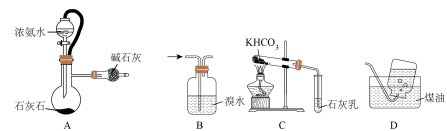
| A.制备干燥氨气 | B.除去乙炔中 |
| C.探究碳酸氢钾稳定性 | D.收集氯化氢 |
您最近半年使用:0次
名校
解题方法
5 . 过硫酸钾(K2S2O8)可用作破胶剂、聚合促进剂、氧化剂、分析试剂等,100℃时分解。实验小组对过硫酸钾进行相关探究,回答下列问题:
(1)K2S2O8中硫元素化合价为___________ 价,K2S2O8可用于检验酸性溶液中的Mn2+,在催化剂的作用下可发生氧化还原反应,溶液变为紫红色,写出该反应的离子方程式___________ 。
(2)小组同学预测过硫酸钾的分解产物有K2SO4、SO3、SO2和O2,并用下图所示装置验证分解产物中含有SO3和SO2 (部分夹持及加热仪器已省略)。
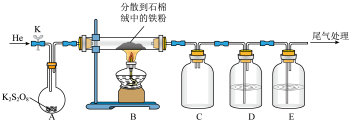
①装置E中盛放的试剂为___________ (填字母)。装置D中有气泡冒出,还观察到的现象是___________ 。
a.品红溶液 b.NaOH溶液 c.BaCl2溶液 d. Ba(NO3)2溶液 e.浓硫酸
②实验时,通入He排尽装置中的空气后,应先加热装置___________ (填“A”或“B”),其中装置A适合的加热方式为___________ 。
③装置B中石棉线的作用为___________ 。
(3)工业上利用K2S2O8能将低价氮氧化为 ,来测定废水中氮元素的含量。取100mL含NH4NO3的废水,用c mol/L的K2S2O8标准溶液滴定(杂质不参加反应),达到滴定终点时消耗标准溶液的体积为VmL,则废水中氮元素的含量为
,来测定废水中氮元素的含量。取100mL含NH4NO3的废水,用c mol/L的K2S2O8标准溶液滴定(杂质不参加反应),达到滴定终点时消耗标准溶液的体积为VmL,则废水中氮元素的含量为___________ mg/L。
(1)K2S2O8中硫元素化合价为
(2)小组同学预测过硫酸钾的分解产物有K2SO4、SO3、SO2和O2,并用下图所示装置验证分解产物中含有SO3和SO2 (部分夹持及加热仪器已省略)。

①装置E中盛放的试剂为
a.品红溶液 b.NaOH溶液 c.BaCl2溶液 d. Ba(NO3)2溶液 e.浓硫酸
②实验时,通入He排尽装置中的空气后,应先加热装置
③装置B中石棉线的作用为
(3)工业上利用K2S2O8能将低价氮氧化为
 ,来测定废水中氮元素的含量。取100mL含NH4NO3的废水,用c mol/L的K2S2O8标准溶液滴定(杂质不参加反应),达到滴定终点时消耗标准溶液的体积为VmL,则废水中氮元素的含量为
,来测定废水中氮元素的含量。取100mL含NH4NO3的废水,用c mol/L的K2S2O8标准溶液滴定(杂质不参加反应),达到滴定终点时消耗标准溶液的体积为VmL,则废水中氮元素的含量为
您最近半年使用:0次
名校
解题方法
6 . FeSO4·7H2O 广泛用于医药和工业领域。下面是以工业废铁屑为原料生产FeSO4·7H2O 的流程图。

(1)加适量碳酸钠溶液的目的是___________ ,反应Ⅰ需要加热数分钟,其原因是___________ 。
(2)判断反应Ⅱ完成的现象是___________ 。反应Ⅱ需要 100mL1mol/L 的稀硫酸,用 98.3%,ρ=1.84g/cm3 的浓硫酸配制。所用的仪器除量筒、烧杯、玻璃棒外,还需要玻璃仪器___________ 。
(3)测定 FeSO4·7H2O 产品中 Fe2+含量的方法是用 KMnO4溶液滴定法(5Fe2++MnO +8H+= 5Fe3++Mn2++4H2O),步骤为:
+8H+= 5Fe3++Mn2++4H2O),步骤为:
Ⅰ.称取 2.8500g FeSO4·7H2O 产品,配制成 250mL 溶液;
Ⅱ.量取 25.00mL 待测溶液于锥形瓶中;
Ⅲ.用硫酸酸化的 0.0100moL/L KMnO4溶液滴定至终点,消耗 KMnO4溶液体积的平均值为 20.00mL。
①判断此滴定实验达到终点的现象是___________ ;
②计算上述样品中 FeSO4·7H2O 的质量分数为___________ (用小数表示,保留三位小数);
(4)已知 FeSO4·7H2O 晶体在加热条件下发生如下反应:2FeSO4·7H2O Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。

①仪器的连接顺序为 a___________ 。
②装置 C 中的 X 为___________ ;该装置中冷水的作用是___________ 。

(1)加适量碳酸钠溶液的目的是
(2)判断反应Ⅱ完成的现象是
(3)测定 FeSO4·7H2O 产品中 Fe2+含量的方法是用 KMnO4溶液滴定法(5Fe2++MnO
 +8H+= 5Fe3++Mn2++4H2O),步骤为:
+8H+= 5Fe3++Mn2++4H2O),步骤为:Ⅰ.称取 2.8500g FeSO4·7H2O 产品,配制成 250mL 溶液;
Ⅱ.量取 25.00mL 待测溶液于锥形瓶中;
Ⅲ.用硫酸酸化的 0.0100moL/L KMnO4溶液滴定至终点,消耗 KMnO4溶液体积的平均值为 20.00mL。
①判断此滴定实验达到终点的现象是
②计算上述样品中 FeSO4·7H2O 的质量分数为
(4)已知 FeSO4·7H2O 晶体在加热条件下发生如下反应:2FeSO4·7H2O
 Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
Fe2O3+SO2↑+SO3↑+14H2O↑。利用下图装置可检验该反应的气体产物。
①仪器的连接顺序为 a
②装置 C 中的 X 为
您最近半年使用:0次
名校
解题方法
7 . 某校化学兴趣小组,通过下列装置探究Na2CO3和NaHCO3的热稳定性,设计如下的探究方案,请你参与并完成该探究方案。
提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(1)设计实验:
①利用如图装置分别对一定量的Na2CO3和NaHCO3进行加热:
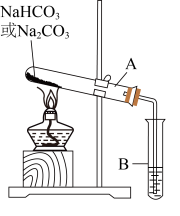
②为了检验CO2的生成,试管B中应加入的物质是________ (填“澄清石灰水”或“NaOH溶液”);并发生反应________ (写出化学方程式)。
(2)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生,且有________ 沉淀生成(填沉淀的颜色),说明Na2CO3和NaHCO3的热稳定性是:Na2CO3________ NaHCO3(填“>”或“<”)。
(3)请写出NaHCO3受热分解的化学方程式_________ 。
(4)某同学在探究NaHCO3的热稳定性时,称取了16.8gNaHCO3,充分加热,请你计算理论上可产生CO2气体的质量为________ g。
(5)在加热后的A试管中仍留有少量白色固体,冷却后加少量水溶解,再滴加1~2滴酚酞试液,可观察到的现象是________ 。
提出假设:Na2CO3或NaHCO3加热分解时可能有CO2生成。
(1)设计实验:
①利用如图装置分别对一定量的Na2CO3和NaHCO3进行加热:

②为了检验CO2的生成,试管B中应加入的物质是
(2)现象与结论:同学们发现只有在加热NaHCO3时,试管B中才有气泡产生,且有
(3)请写出NaHCO3受热分解的化学方程式
(4)某同学在探究NaHCO3的热稳定性时,称取了16.8gNaHCO3,充分加热,请你计算理论上可产生CO2气体的质量为
(5)在加热后的A试管中仍留有少量白色固体,冷却后加少量水溶解,再滴加1~2滴酚酞试液,可观察到的现象是
您最近半年使用:0次
名校
8 . 用如图所示实验装置进行相关实验探究,实验设计合理并能达到实验目的的是
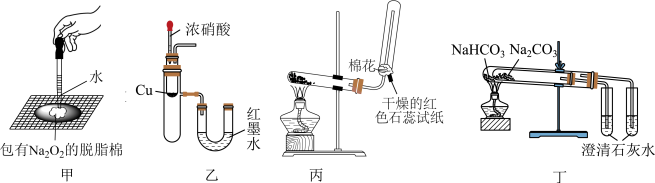

| A.装置甲验证Na2O2与水反应放热 |
| B.装置乙验证Cu与浓硝酸反应的热量变化 |
| C.装置丙制取并收集、检验氨气 |
| D.装置丁比较Na2CO3与NaHCO3的稳定性 |
您最近半年使用:0次
2023-09-15更新
|
382次组卷
|
2卷引用:山东省枣庄市第八中学2022-2023学年高一上学期期末考试化学试题
名校
解题方法
9 . 区分下列物质的方法不正确的是
| 选项 | 物质 | 方法 |
| A | 金刚石和石墨 | 比较硬度 |
| B | 一氧化碳和甲烷 | 观察颜色 |
| C | 氧气和氮气 | 用带火星的木条检验 |
| D | 氢氧化钠和硝酸铵 | 溶于水测温度 |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
10 . 化学兴趣小组课外实验时,取出镁条,发现久置的镁条有一层灰黑色的“外衣”他们把该镁条放入试管中,倒入一定浓度的盐酸,观察到有气泡产生,试管壁发烫。同学们对此气体成分产生了兴趣。
【提出问题】产生的气体是什么?
【查阅资料】i.灰黑色“外衣”中含有
ii.无水 遇水由白色变为蓝色
遇水由白色变为蓝色
【猜想假设】猜想一: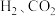
猜想二: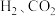 和水蒸气
和水蒸气
猜想三: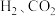 、水蒸气和HCl气体
、水蒸气和HCl气体
(1)猜想三中有HCl气体的理由是___________ 。
【设计实验】为检测产生的气体成分,同学们设计如图所示装置进行实验(部分固定装置略去)
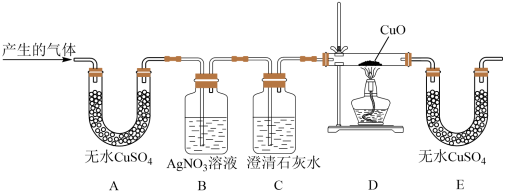
(2)B装置中出现白色沉淀,证明产生的气体中含有___________ ,写出有关的化学方程式___________ 。
(3)C装置的作用是___________ 。
(4)甲同学观察到E装置中无水 由白色变为蓝色,于是得出结论:产生的气体中一定含有H2。乙同学对此提出质疑,理由是
由白色变为蓝色,于是得出结论:产生的气体中一定含有H2。乙同学对此提出质疑,理由是___________ 。
(5)若颠倒B装置和C装置的安装顺序,___________ (填“能”或“不能”)达到实验目的,原因是___________ 。
【反思与评价】
(6)从安全角度考虑,你认为实验时应注意___________ 。
【提出问题】产生的气体是什么?
【查阅资料】i.灰黑色“外衣”中含有

ii.无水
 遇水由白色变为蓝色
遇水由白色变为蓝色【猜想假设】猜想一:
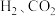
猜想二:
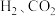 和水蒸气
和水蒸气猜想三:
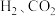 、水蒸气和HCl气体
、水蒸气和HCl气体(1)猜想三中有HCl气体的理由是
【设计实验】为检测产生的气体成分,同学们设计如图所示装置进行实验(部分固定装置略去)

(2)B装置中出现白色沉淀,证明产生的气体中含有
(3)C装置的作用是
(4)甲同学观察到E装置中无水
 由白色变为蓝色,于是得出结论:产生的气体中一定含有H2。乙同学对此提出质疑,理由是
由白色变为蓝色,于是得出结论:产生的气体中一定含有H2。乙同学对此提出质疑,理由是(5)若颠倒B装置和C装置的安装顺序,
【反思与评价】
(6)从安全角度考虑,你认为实验时应注意
您最近半年使用:0次



