1 . 用下列实验装置(部分夹持装置略去)进行相应的实验,能达到实验目的的是
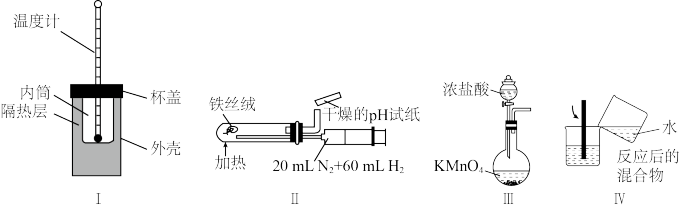

| A.I是中和热的测定 |
| B.利用装置II合成氨并检验氨的生成 |
| C.利用装置III制备少量的氯气 |
| D.用图IV装置向Cu和浓硫酸反应后的混合物中加水稀释 |
您最近半年使用:0次
解题方法
2 . 下列实验所选择的装置(部分夹持装置略去)正确的是
| 选项 | A | B | C | D |
| 实验 | 制取少量的乙酸乙酯 | 检验反应有乙烯气体生成 | 检验葡萄糖具有还原性 | 除去乙醇中的苯酚 |
| 装置 |  | 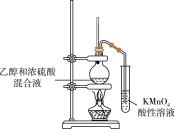 |  |  |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
3 . 蛋白质是生命的物质基础。某学习小组实验探究一种蛋白质的元素组成。
I.确定该蛋白质中的某些组成元素
(1)为确定该蛋白质中含氮元素,将样品中有机氮转化成铵盐,能证明铵盐存在的实验方法是_______ 。
(2)为确定该蛋白质中含碳、氢、硫三种元素,采用如图装置进行探究,通入氧气使样品在装置A中 充分燃烧,并使其产物依次缓缓通过其余装置。
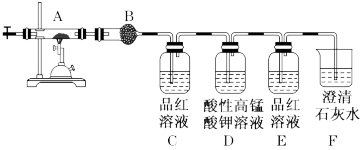
①装置B中的试剂是_______ 。
②装置D的作用是_______ 。
③当装置B、C、E、F依次出现下列现象:_______ ,品红溶液褪色,_______ ,出现白色浑浊;可证明燃烧产物中含有H2O,SO2>CO2,结论:该蛋白质中含碳、氢、硫、氮等元素。
II.为测定该蛋白质中硫元素的质量分数,小组取蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫, 再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。已知:2 +I2=
+I2= +2I-
+2I-
(3)写出二氧化硫与碘水反应的化学方程式:_______ 。
(4)滴定终点的现象为_______ 。
(5)取蛋白质样品m g进行测定,采用c1 mol·L-1的碘水V1 mL进行吸收,滴定过量的碘样时消耗c2 mol·L-1硫代硫酸钠溶液V2mL。该蛋白质中的硫元素的质量分数为_______ 。
(6)若燃烧时过量氧气进入吸收液中,可能会导致该蛋白质中的硫元素的质量分数测定值_______ (填“偏大*偏小”或“无影响”)。
I.确定该蛋白质中的某些组成元素
(1)为确定该蛋白质中含氮元素,将样品中有机氮转化成铵盐,能证明铵盐存在的实验方法是
(2)为确定该蛋白质中含碳、氢、硫三种元素,采用如图装置进行探究,通入氧气使样品在装置A中 充分燃烧,并使其产物依次缓缓通过其余装置。

①装置B中的试剂是
②装置D的作用是
③当装置B、C、E、F依次出现下列现象:
II.为测定该蛋白质中硫元素的质量分数,小组取蛋白质样品充分燃烧,先用足量碘水吸收二氧化硫, 再取吸收液,以淀粉为指示剂,用硫代硫酸钠溶液滴定过量的碘。已知:2
 +I2=
+I2= +2I-
+2I-(3)写出二氧化硫与碘水反应的化学方程式:
(4)滴定终点的现象为
(5)取蛋白质样品m g进行测定,采用c1 mol·L-1的碘水V1 mL进行吸收,滴定过量的碘样时消耗c2 mol·L-1硫代硫酸钠溶液V2mL。该蛋白质中的硫元素的质量分数为
(6)若燃烧时过量氧气进入吸收液中,可能会导致该蛋白质中的硫元素的质量分数测定值
您最近半年使用:0次
名校
解题方法
4 . 高氯酸铵(NH4ClO4)为白色晶体且不稳定,受热易分解产生多种气体。某化学兴趣小组同学利用如图所示装置探究NH4ClO4的分解产物。(假设装置内药品均足量。)
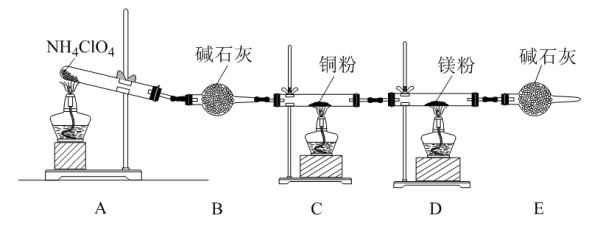
(1)在实验过程中发现_______ ,说明产物中有氧气生成。
(2)实验完毕后,取D中硬质玻璃管中的固体物质于试管中,滴加蒸馏水,产生能使湿润的红色石蕊试纸变蓝色的气体,该气体化学式为_______ ,则原来D中发生反应的化学方程式为_______ 。
(3)为了证明H2O和Cl2的存在,用下图提供的装置进行实验(不重复使用):
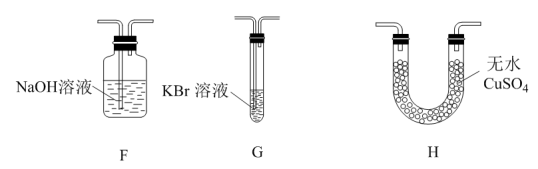
①按气流从左至右,装置的连接顺序为A→_______ ;实验过程中H中的现象为__________ 。
②写出F中发生反应的离子方程式:_______ 。
(4)NH4ClO4分解时产生了,上述几种物质,则高氯酸铵分解的化学方程式为_______ 。

(1)在实验过程中发现
(2)实验完毕后,取D中硬质玻璃管中的固体物质于试管中,滴加蒸馏水,产生能使湿润的红色石蕊试纸变蓝色的气体,该气体化学式为
(3)为了证明H2O和Cl2的存在,用下图提供的装置进行实验(不重复使用):

①按气流从左至右,装置的连接顺序为A→
②写出F中发生反应的离子方程式:
(4)NH4ClO4分解时产生了,上述几种物质,则高氯酸铵分解的化学方程式为
您最近半年使用:0次
名校
5 . 下列实验仪器或装置的选择正确的是
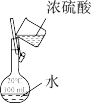 |  |  |  |
| 配制1mol/L的稀硫酸 | 制备少量的 | 除氯气中的氯化氢气体 | 检验过氧化钠与水反应产物的气体 |
| A | B | C | D |
| A.A | B.B | C.C | D.D |
您最近半年使用:0次
2022-03-07更新
|
226次组卷
|
2卷引用:陕西省渭南市大荔县2021-2022学年高一上学期期末考试化学试题
2022高三·全国·专题练习
解题方法
6 . 某草酸钙晶体(CaC2O4·xH2O)热分解研究
(提示:CaC2O4·xH2O受热会失去结晶水成为CaC2O4;白色硫酸铜粉末遇水会变蓝。)
按下图装置将草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设装置中各试剂均足量)
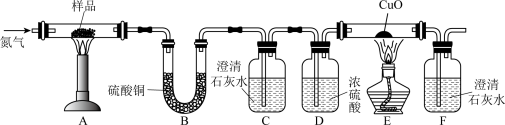
(1)①反应开始前通入氮气的目的是___________ ,装置C的作用是___________ 。
②装置B中硫酸铜粉末变蓝,C、F中澄清石灰水均变浑浊,E中CuO变红,说明产物有___________ ,经检验A中残留固体为氧化物。
③对上述装置从环保角度提一个改进建议___________ 。
(2)某研究所利用SDT Q600热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,
获得相关数据,绘制成固体质量—分解温度的关系如图。

①800℃以上时,固体成分的化学式为___________ 。
②残留固体为CaC2O4时的温度范围___________ 。
③写出固体质量由12.8 g变为10.0 g时的化学方程式___________ 。
(提示:CaC2O4·xH2O受热会失去结晶水成为CaC2O4;白色硫酸铜粉末遇水会变蓝。)
按下图装置将草酸钙晶体样品高温加热,使其完全分解,对所得气体产物进行探究(假设装置中各试剂均足量)

(1)①反应开始前通入氮气的目的是
②装置B中硫酸铜粉末变蓝,C、F中澄清石灰水均变浑浊,E中CuO变红,说明产物有
③对上述装置从环保角度提一个改进建议
(2)某研究所利用SDT Q600热分析仪对草酸钙晶体(CaC2O4·xH2O)进行热分解,
获得相关数据,绘制成固体质量—分解温度的关系如图。

①800℃以上时,固体成分的化学式为
②残留固体为CaC2O4时的温度范围
③写出固体质量由12.8 g变为10.0 g时的化学方程式
您最近半年使用:0次
7 . 下列实验及相关叙述正确的是
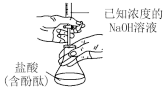 ① ① | 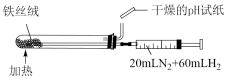 ② ② |
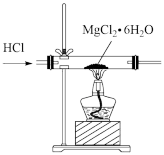 ③ ③ | 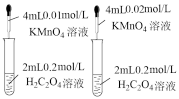 ④ ④ |
| A.滴定法用装置①测定盐酸的浓度 |
| B.可用装置②来合成氨并检验氨气的生成 |
| C.用装置③能制取无水MgCl2 |
| D.装置④依据单位时间内颜色变化来比较浓度对反应速率的影响 |
您最近半年使用:0次
2022-01-19更新
|
222次组卷
|
3卷引用:四川省眉山市2021-2022学年高二上学期期末教学质量检测化学试题
名校
解题方法
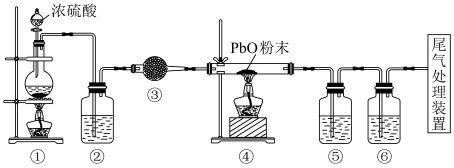
8 . 氧化铅(PbO)是黄色固体。实验室用草酸在浓硫酸作用F分解制备CO,其原理为H2C2O4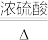 CO↑+CO2↑+H2O。某学习小组设计实验探究CO还原氧化铅并检验氧化产物的装置如图所示(已知CO通入银氨溶液产生黑色银粒)。下列说法不正确的是
CO↑+CO2↑+H2O。某学习小组设计实验探究CO还原氧化铅并检验氧化产物的装置如图所示(已知CO通入银氨溶液产生黑色银粒)。下列说法不正确的是
 CO↑+CO2↑+H2O。某学习小组设计实验探究CO还原氧化铅并检验氧化产物的装置如图所示(已知CO通入银氨溶液产生黑色银粒)。下列说法不正确的是
CO↑+CO2↑+H2O。某学习小组设计实验探究CO还原氧化铅并检验氧化产物的装置如图所示(已知CO通入银氨溶液产生黑色银粒)。下列说法不正确的是
| A.实验时,先点燃①处酒精灯,等装置⑥中出现较多黑色银粒且有连续气泡后再点燃④处酒精灯 |
| B.实验完毕时,先熄灭④处酒精灯,再熄灭①处酒精灯 |
| C.尾气处理装置可选用盛NaOH溶液的洗气瓶 |
D.当装置④中固体质量减轻了0.16g时,装置①中消耗的 的物质的量为0.01mol 的物质的量为0.01mol |
您最近半年使用:0次
2021-12-04更新
|
237次组卷
|
3卷引用:湖南省190多所名校2021-2022学年高三上学期12月联考化学试题
湖南省190多所名校2021-2022学年高三上学期12月联考化学试题(已下线)专题35 物质的检验、分离和提纯(限时精炼)-2022年高三毕业班化学常考点归纳与变式演练湖南省株洲市第四中学2022-2023学年高三上学期第一次月考化学试题
9 . 为检验二氧化碳气体中是否混有一氧化碳,某课外兴趣小组的同学设计了如图所示的实验装置,根据如图装置回答问题:

(1)实验时,在点燃C处时酒精灯前必须先通一会儿气体,其目的是___________ 。
(2)A装置的作用是___________ ,B装置的作用是___________ 。
(3)若实验后需要对尾气进行处理,则处理的方法___________ ,发生反应的化学方程式为___________ 。
(4)若实验时观察到___________ 现象,则证明原气体中一定含有一氧化碳。

(1)实验时,在点燃C处时酒精灯前必须先通一会儿气体,其目的是
(2)A装置的作用是
(3)若实验后需要对尾气进行处理,则处理的方法
(4)若实验时观察到
您最近半年使用:0次
10 . 下列操作中,能鉴别空气、氧气和二氧化碳三瓶气体的是
| A.插入燃着的木条 | B.观察气体颜色 |
| C.闻气体的气味 | D.倒入澄清石灰水 |
您最近半年使用:0次



