名校
解题方法
1 . 某课外小组探究Cu(Ⅱ)盐与Na2S2O3溶液的反应。
【查阅资料】
ⅰ. 2 +Cu2+
+Cu2+ [Cu(S2O3)2]2-(绿色),2
[Cu(S2O3)2]2-(绿色),2 +Cu+
+Cu+ [Cu(S2O3)2]3-(无色):
[Cu(S2O3)2]3-(无色):
ⅱ. 2NH3+Cu+ [Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+ (蓝色);
[Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+ (蓝色);
ⅲ. 易被氧化为
易被氧化为 或
或 。
。
【猜想假设】
同学们根据资料认为Cu(Ⅱ)盐与Na2S2O3可能会发生两种反应:
假设1:Cu2+与 在溶液中发生配合反应生成[Cu(S2O3)2]2-;
在溶液中发生配合反应生成[Cu(S2O3)2]2-;
假设2:Cu(Ⅱ)有氧化性,Cu2+与 在溶液中发生氧化还原反应。
在溶液中发生氧化还原反应。
【实验操作及现象分析】
实验一:探究CuSO4与Na2S2O3溶液的反应。
(1)根据实验a的现象可推测溶液中生成的含Cu微粒是___________ (填化学式)。
(2)甲同学认为实验一可证明假设2成立,他的理由是___________ 。
实验二:探究CuCl2与Na2S2O3的反应。___________ (补全实验方案),则说明含Cu(Ⅰ)。
(4)经检验白色沉淀中含CuCl,请写出继续加Na2S2O3溶液后CuCl沉淀溶解的离子方程式:___________ 。
(5)经检验氧化产物以 形式存在,写出Cu2+与
形式存在,写出Cu2+与 发生氧化还原反应得到无色溶液的离子方程式:
发生氧化还原反应得到无色溶液的离子方程式:___________ 。
【获得结论】
(6)综合以上实验,同学们认为Cu(Ⅱ)盐与Na2S2O3在溶液中的反应与多种因素有关,得到实验结论,选择合适的选项填入下面的横线中。
A配合反应 B.氧化还原反应 C.置换反应 D.复分解反应
①随n( ):n(Cu2+)的增大,二者发生
):n(Cu2+)的增大,二者发生___________ 的趋势减弱;
②Cu(Ⅱ)盐的阴离子为Cl-时能增大Cu2+和 发生
发生___________ 的趋势。
【查阅资料】
ⅰ. 2
 +Cu2+
+Cu2+ [Cu(S2O3)2]2-(绿色),2
[Cu(S2O3)2]2-(绿色),2 +Cu+
+Cu+ [Cu(S2O3)2]3-(无色):
[Cu(S2O3)2]3-(无色):ⅱ. 2NH3+Cu+
 [Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+ (蓝色);
[Cu(NH3)2]+(无色),[Cu(NH3)2]+遇空气容易被氧化成[Cu(NH3)4]2+ (蓝色);ⅲ.
 易被氧化为
易被氧化为 或
或 。
。【猜想假设】
同学们根据资料认为Cu(Ⅱ)盐与Na2S2O3可能会发生两种反应:
假设1:Cu2+与
 在溶液中发生配合反应生成[Cu(S2O3)2]2-;
在溶液中发生配合反应生成[Cu(S2O3)2]2-;假设2:Cu(Ⅱ)有氧化性,Cu2+与
 在溶液中发生氧化还原反应。
在溶液中发生氧化还原反应。【实验操作及现象分析】
实验一:探究CuSO4与Na2S2O3溶液的反应。
| 实验操作 | 实验序号 | V1(mL) | V2(mL) | 逐滴加入Na2S2O3溶液时的实验现象 |
| a | 1.5 | 0.5 | 溶液逐渐变为绿色,静置无变化 |
| b | 1.0 | 1.0 | 溶液先变为绿色,后逐渐变成浅绿色,静置无变化 | |
| c | 0 | 2.0 | 溶液先变为绿色,后逐渐变浅至无色,静置无变化 |
(1)根据实验a的现象可推测溶液中生成的含Cu微粒是
(2)甲同学认为实验一可证明假设2成立,他的理由是
实验二:探究CuCl2与Na2S2O3的反应。
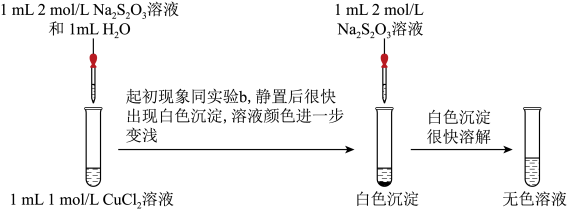
(4)经检验白色沉淀中含CuCl,请写出继续加Na2S2O3溶液后CuCl沉淀溶解的离子方程式:
(5)经检验氧化产物以
 形式存在,写出Cu2+与
形式存在,写出Cu2+与 发生氧化还原反应得到无色溶液的离子方程式:
发生氧化还原反应得到无色溶液的离子方程式:【获得结论】
(6)综合以上实验,同学们认为Cu(Ⅱ)盐与Na2S2O3在溶液中的反应与多种因素有关,得到实验结论,选择合适的选项填入下面的横线中。
A配合反应 B.氧化还原反应 C.置换反应 D.复分解反应
①随n(
 ):n(Cu2+)的增大,二者发生
):n(Cu2+)的增大,二者发生②Cu(Ⅱ)盐的阴离子为Cl-时能增大Cu2+和
 发生
发生
您最近一年使用:0次
2 . 氧化还原反应可拆分为氧化和还原两个“半反应”,某小组同学从“半反应”的角度探究反应规律。
(1)已知: 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。
①该转化的还原半反应是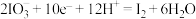 ,则相应的氧化半反应是
,则相应的氧化半反应是___________ 。
②分析上述还原半反应可知:增大 可促进
可促进 得到电子,使其
得到电子,使其___________ 性增强,进而与 发生反应。
发生反应。
(2)探究 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。
①有同学认为 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是___________ 。
用如下装置进行实验【硫酸与浓盐酸中 接近】。
接近】。
②甲实验的目的是___________ 。
③a.丙中气球变鼓是因为生成了___________ 气体(填化学式)。
b.经检测,丙中反应后溶液中存在 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:___________ 。
(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧 电极表面有
电极表面有 析出。
析出。
①该装置中左侧  电极作
电极作___________ (填“正”或“负”)极。
②写出该装置右侧 烧杯中的电极反应式___________ 。
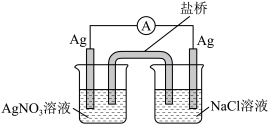
对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池__________ 。
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
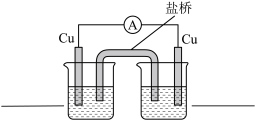
a.若能,在右装置图中填写烧杯中的试剂,并标出电子的移动方向 。
b.若不能,说明原因。
(1)已知:
 的转化在酸性条件下才能发生。
的转化在酸性条件下才能发生。①该转化的还原半反应是
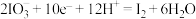 ,则相应的氧化半反应是
,则相应的氧化半反应是②分析上述还原半反应可知:增大
 可促进
可促进 得到电子,使其
得到电子,使其 发生反应。
发生反应。(2)探究
 与浓盐酸能否发生反应。
与浓盐酸能否发生反应。①有同学认为
 与浓盐酸不能发生反应产生氢气,其依据是
与浓盐酸不能发生反应产生氢气,其依据是用如下装置进行实验【硫酸与浓盐酸中
 接近】。
接近】。| 装置 | 序号 | 试管内药品 | 现象 |
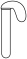 | 甲 | 浓盐酸 | 24小时后仍无明显变化 |
| 乙 |  粉+硫酸 粉+硫酸 | 24小时后仍无明显变化 | |
| 丙 |  粉+浓盐酸 粉+浓盐酸 | 24小时后气球变鼓 |
③a.丙中气球变鼓是因为生成了
b.经检测,丙中反应后溶液中存在
 。从物质性质角度分析丙中反应能够发生的原因:
。从物质性质角度分析丙中反应能够发生的原因:(3)探究以下原电池的工作原理。
实验结果:产生电流,左侧
 电极表面有
电极表面有 析出。
析出。①该装置中
 电极作
电极作②写出该装置

对该原电池的电极反应和总反应的反应类型进行分析,发现两极上分别发生氧化和还原反应,而总反应不一定是氧化还原反应。
③结合上述实验思考,仅由以下实验用品能否设计成原电池
 片、
片、 浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
浓溶液、蒸馏水、烧杯、盐桥、导线、电流表(选做下列a或b,若两个都作答,按a计分)
a.若能,在右装置图中填写烧杯中的试剂,
b.若不能,说明原因。
您最近一年使用:0次
3 . 兴趣小组查阅文献后,设计实验对苯酚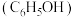 的性质进行探究,回答以下问题。
的性质进行探究,回答以下问题。
已知:ⅰ. 25℃,相关弱酸的电离平衡常数如下:Ka1(H2CO3)=4.2×10−7,Ka2(H2CO3)=5.6×10−11,Ka(C6H5OH)=1.3×10−10。
ⅱ.苯酚与 显色反应的化学方程式为:Fe3++6C6H5OH
显色反应的化学方程式为:Fe3++6C6H5OH [Fe(C6H5O)6]3−(紫色)+6H+。
[Fe(C6H5O)6]3−(紫色)+6H+。
Ⅰ.探究苯酚酸性的强弱
(1)苯酚的电离方程式为___________ 。
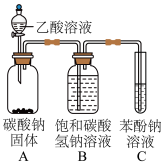
(2)兴趣小组按如图装置进行实验,证明酸性强弱顺序为CH3COOH>H2CO3> C6H5OH,所依据的实验现象为___________ ,C中反应的化学方程式为___________ 。
兴趣小组对以上实验的现象提出猜想。
猜想1: 对铁离子与苯酚的反应有促进作用。
对铁离子与苯酚的反应有促进作用。
猜想2: 对铁离子与苯酚的反应有抑制作用。
对铁离子与苯酚的反应有抑制作用。
(3)向实验1反应后溶液中继续加入 固体,若溶液颜色无变化,则可得出的结论是
固体,若溶液颜色无变化,则可得出的结论是___________ 。
(4)向实验1反应后溶液中加入___________ 固体(填化学式),若溶液颜色变为浅紫色,说明猜想2成立。
(5)兴趣小组同学提出猜想3:溶液的 会影响显色效果,并设计如下实验进行验证。
会影响显色效果,并设计如下实验进行验证。
①实验4中生成的红褐色沉淀是___________ (填化学式)。
②实验5中滴加盐酸至过量,溶液由紫色变为浅黄色,结合平衡移动原理解释原因___________ 。
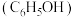 的性质进行探究,回答以下问题。
的性质进行探究,回答以下问题。已知:ⅰ. 25℃,相关弱酸的电离平衡常数如下:Ka1(H2CO3)=4.2×10−7,Ka2(H2CO3)=5.6×10−11,Ka(C6H5OH)=1.3×10−10。
ⅱ.苯酚与
 显色反应的化学方程式为:Fe3++6C6H5OH
显色反应的化学方程式为:Fe3++6C6H5OH [Fe(C6H5O)6]3−(紫色)+6H+。
[Fe(C6H5O)6]3−(紫色)+6H+。Ⅰ.探究苯酚酸性的强弱
(1)苯酚的电离方程式为
(2)兴趣小组按如图装置进行实验,证明酸性强弱顺序为CH3COOH>H2CO3> C6H5OH,所依据的实验现象为
| 实验1 | 实验2 |
|
|
猜想1:
 对铁离子与苯酚的反应有促进作用。
对铁离子与苯酚的反应有促进作用。猜想2:
 对铁离子与苯酚的反应有抑制作用。
对铁离子与苯酚的反应有抑制作用。(3)向实验1反应后溶液中继续加入
 固体,若溶液颜色无变化,则可得出的结论是
固体,若溶液颜色无变化,则可得出的结论是(4)向实验1反应后溶液中加入
(5)兴趣小组同学提出猜想3:溶液的
 会影响显色效果,并设计如下实验进行验证。
会影响显色效果,并设计如下实验进行验证。| 实验 | 操作 | 现象 |
| 3 | 向2mL苯酚溶液(调节 )中滴加0.1mol/LFeCl3溶液 )中滴加0.1mol/LFeCl3溶液 | 溶液显紫色 |
| 4 | 向2mL苯酚溶液(调节 )中滴加0.1mol/LFeCl3溶液 )中滴加0.1mol/LFeCl3溶液 | 生成红褐色沉淀 |
| 5 | 向实验4所得悬浊液中逐滴加入0.1mol/L盐酸至过量 | 沉淀逐渐溶解,溶液变为紫色;继续滴加盐酸,溶液由紫色变为浅黄色 |
②实验5中滴加盐酸至过量,溶液由紫色变为浅黄色,结合平衡移动原理解释原因
您最近一年使用:0次
2024-04-26更新
|
186次组卷
|
2卷引用:北京市北京大学附属中学2023-2024学年高二下学期期中考试化学试题
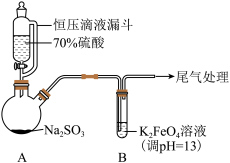
4 . 某实验小组探究SO2与K2FeO4的反应,实验如下。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;
(1)A中产生SO2的化学方程式为___________ 。
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO 、SO
、SO ,检验如下:
,检验如下:
实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在___________ 。另取少量溶液滴加BaCl2溶液,产生白色沉淀,但不能确认含有SO ,原因是
,原因是___________ 。
实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO 。
。
实验三中用H2C2O4溶液溶解沉淀的目的是:___________ 。
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:___________ 。
(3)查阅资料:a.Fe3+、SO 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是___________ 。
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:___________ 。
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
资料:i.K2FeO4为紫色固体,微溶于KOH溶液;具有强氧化性,在酸性或中性溶液中快速产生O2,在碱性溶液中较稳定。
ii.Fe3+可以与C2O
 形成[Fe(C2O4)3]3-;
形成[Fe(C2O4)3]3-;| 装置 | 操作及现象 |
| 实验一:向B中通入SO2,产生暗红褐色沉淀X和溶液Y(略显红色);继续通入SO2一段时间后,溶液呈红色,继而变为橙色,最终沉淀消失,溶液几乎无色。 |
(1)A中产生SO2的化学方程式为
(2)暗红褐色沉淀X可能含Fe3+、OH-、SO
 、SO
、SO ,检验如下:
,检验如下:实验二:向X中加入足量盐酸,沉淀溶解。取少量溶液,滴加KSCN溶液后变红。证明溶液中存在
 ,原因是
,原因是实验三:向X中加入H2C2O4溶液,沉淀溶解。继续滴加BaCl2溶液,产生白色沉淀,过滤后,向沉淀中加入盐酸,白色沉淀溶解。确认X中不含SO
 。
。实验三中用H2C2O4溶液溶解沉淀的目的是:
实验四:向X中加入足量盐酸,沉淀溶解。加入几滴碘水(含淀粉),蓝色立即褪去。静置,一段时间后蓝色复现,振荡,不褪色。
结合离子方程式解释沉淀溶解后的现象:
(3)查阅资料:a.Fe3+、SO
 、H2O(或OH﹣)会形成配合物HOFeOSO2。
、H2O(或OH﹣)会形成配合物HOFeOSO2。
 和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
和O2在金属离子的催化作用下产生具有强氧化性的过一硫酸(HSO
①向溶液Y中滴加2滴KSCN溶液,未见红色;再加几滴6mol·L-1盐酸,溶液变红。溶液Y中存在Fe(Ⅲ),但直接滴加KSCN溶液未见红色的原因是
②取出部分实验一中的橙色溶液,久置不褪色。结合资料a中过程ii分析实验一中溶液最终“几乎无色”的原因:
总结:SO2与K2FeO4发生了氧化还原反应和复分解反应,并且遵循化学反应速率和限度规律。
您最近一年使用:0次
2024-04-15更新
|
634次组卷
|
3卷引用:北京市朝阳区2023-2024学年高三下学期一模化学试题
北京市朝阳区2023-2024学年高三下学期一模化学试题(已下线)压轴题12?化学实验综合题(5大题型+方法总结+压轴题速练)-2024年高考化学压轴题专项训练(新高考通用)辽宁省大连市大连第二十四中学2023-2024学年高一下学期期中考试化学试卷
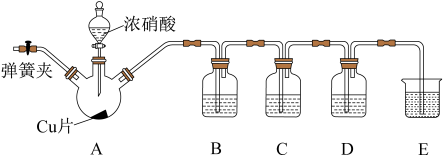
5 . 某小组通过实验探究NO的某些性质,实验装置图如下:___________ 。
(2)判断NO既有氧化性又有还原性的理论依据是___________ 。
资料:i.NO与 溶液会发生氧化还原反应,NO被还原为
溶液会发生氧化还原反应,NO被还原为 。
。
ii.醋酸银易溶于水,硫酸银微溶于水, 是不溶于水的黄色固体。
是不溶于水的黄色固体。
iii.浓硝酸能将NO氧化成 ,而稀硝酸不能氧化NO。
,而稀硝酸不能氧化NO。
iv.NaOH溶液不与NO反应,能与 反应:
反应: 。
。
可选药品: 溶液、浓
溶液、浓 、3mo/L稀
、3mo/L稀 、蒸馏水、浓
、蒸馏水、浓 、NaOH溶液及
、NaOH溶液及 。
。
(3)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹后,通入一段时间 ,关闭弹簧夹,其目的是
,关闭弹簧夹,其目的是___________ 。
(4)装置B的作用是___________ (用化学方程式表示)。
(5)装置C中装有 溶液,实验探究NO的氧化性。
溶液,实验探究NO的氧化性。
①甲同学检验 的转化产物。取少量反应后装置C中的溶液,
的转化产物。取少量反应后装置C中的溶液,___________ (填操作和实验现象)。
②乙同学认为即使甲同学检验出有 ,也不能说明NO具有氧化性,理由是
,也不能说明NO具有氧化性,理由是___________ (用离子方程式说明)。
③丙同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验I:取饱和 溶液,加入少量醋酸,再滴加5滴0.1mol/L的
溶液,加入少量醋酸,再滴加5滴0.1mol/L的 溶液,无明显变化。
溶液,无明显变化。
实验Ⅱ:取少量装置C中反应后的溶液,加入少量醋酸,再滴加5滴0.1mol/L的 溶液,
溶液,___________ (填实验现象)。
实验I的目的是___________ 。
上述实验证明NO有氧化性。
(6)实验探究NO的还原性。
装置D中,实验得出NO具有还原性的实验现象是___________ 。
(7)装置E的作用是___________ 。
(2)判断NO既有氧化性又有还原性的理论依据是
资料:i.NO与
 溶液会发生氧化还原反应,NO被还原为
溶液会发生氧化还原反应,NO被还原为 。
。ii.醋酸银易溶于水,硫酸银微溶于水,
 是不溶于水的黄色固体。
是不溶于水的黄色固体。iii.浓硝酸能将NO氧化成
 ,而稀硝酸不能氧化NO。
,而稀硝酸不能氧化NO。iv.NaOH溶液不与NO反应,能与
 反应:
反应: 。
。可选药品:
 溶液、浓
溶液、浓 、3mo/L稀
、3mo/L稀 、蒸馏水、浓
、蒸馏水、浓 、NaOH溶液及
、NaOH溶液及 。
。(3)滴加浓硝酸之前的操作是检验装置的气密性,加入药品,打开弹簧夹后,通入一段时间
 ,关闭弹簧夹,其目的是
,关闭弹簧夹,其目的是(4)装置B的作用是
(5)装置C中装有
 溶液,实验探究NO的氧化性。
溶液,实验探究NO的氧化性。①甲同学检验
 的转化产物。取少量反应后装置C中的溶液,
的转化产物。取少量反应后装置C中的溶液,②乙同学认为即使甲同学检验出有
 ,也不能说明NO具有氧化性,理由是
,也不能说明NO具有氧化性,理由是③丙同学认为,需通过进一步实验验证NO的氧化性,补充以下实验:
实验I:取饱和
 溶液,加入少量醋酸,再滴加5滴0.1mol/L的
溶液,加入少量醋酸,再滴加5滴0.1mol/L的 溶液,无明显变化。
溶液,无明显变化。实验Ⅱ:取少量装置C中反应后的溶液,加入少量醋酸,再滴加5滴0.1mol/L的
 溶液,
溶液,实验I的目的是
上述实验证明NO有氧化性。
(6)实验探究NO的还原性。
装置D中,实验得出NO具有还原性的实验现象是
(7)装置E的作用是
您最近一年使用:0次
名校
解题方法
6 . 某小组同学探究不同条件下氯气与二价锰化合物的反应
资料:i. 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。
ii.浓碱条件下, 可被
可被 还原为
还原为 。
。
iii. 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
实验装置如图(夹持装置略)
(1)B中试剂是___________ 。
(2)通入 前,II、III中沉淀由白色
前,II、III中沉淀由白色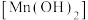 变为棕黑色,补全发生反应的化学方程式:
变为棕黑色,补全发生反应的化学方程式:___________ 。

(3)对比实验I、II通入 后的实验现象,对于二价锰化合物还原性的认识是:
后的实验现象,对于二价锰化合物还原性的认识是:
①___________ ;
②在碱性条件下二价锰可以被氧化到更高价态。
(4)根据资料ii,II中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入 导致溶液的碱性减弱。
导致溶液的碱性减弱。
原因二:可能是氧化剂过量,氧化剂将 氧化为
氧化为 。
。
①用化学方程式表示可能导致溶液碱性减弱的原因___________ ,但通过实验测定,溶液的碱性变化很小。
②针对原因二小组同学做如下探究:
IV中溶液紫色迅速变为绿色的离子方程式为___________ ,溶液绿色缓慢加深,原因是 被
被___________ (填“化学式”)氧化,可证明III的悬浊液中氧化剂过量。
③分析IV、V实验现象不同的原因是___________ 。
资料:i.
 在一定条件下被
在一定条件下被 或
或 氧化成
氧化成 (棕黑色)、
(棕黑色)、 (绿色)、
(绿色)、 (紫色)。
(紫色)。ii.浓碱条件下,
 可被
可被 还原为
还原为 。
。iii.
 的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。
的氧化性与溶液的酸碱性无关,NaClO的氧化性随碱性增强而减弱。实验装置如图(夹持装置略)

| 序号 | I | II | III |
| 物质a | 水 | 5%NaOH溶液 | 40%NaOH溶液 |
通入 前C中实验现象 前C中实验现象 | 得到无色溶液 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 | 产生白色沉淀,在空气中缓慢变成棕黑色沉淀 |
通入 后C中实验现象 后C中实验现象 | 产生棕黑色沉淀,且放置后不发生变化 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 | 棕黑色沉淀增多,放置后溶液变为紫色,仍有沉淀 |
(1)B中试剂是
(2)通入
 前,II、III中沉淀由白色
前,II、III中沉淀由白色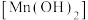 变为棕黑色,补全发生反应的化学方程式:
变为棕黑色,补全发生反应的化学方程式:
(3)对比实验I、II通入
 后的实验现象,对于二价锰化合物还原性的认识是:
后的实验现象,对于二价锰化合物还原性的认识是:①
②在碱性条件下二价锰可以被氧化到更高价态。
(4)根据资料ii,II中应得到绿色溶液,实验中得到紫色溶液,分析现象与资料不符的原因:
原因一:可能是通入
 导致溶液的碱性减弱。
导致溶液的碱性减弱。原因二:可能是氧化剂过量,氧化剂将
 氧化为
氧化为 。
。①用化学方程式表示可能导致溶液碱性减弱的原因
②针对原因二小组同学做如下探究:
| 序号 | IV | V |
| 操作 | 取III中放置后的1mL悬浊液,加入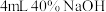 溶液 溶液 | 取III中放置后的1mL悬浊液,加入4mL水 |
| 现象 | 溶液紫色迅速变为绿色,且绿色缓慢加深 | 溶液紫色缓慢加深 |
 被
被③分析IV、V实验现象不同的原因是
您最近一年使用:0次
7 . 探究铜与浓硫酸的反应。
加热铜与浓硫酸,在反应过程中,有刺激性气味的气体产生,溶液逐渐变为墨绿色浊液,试管底部有灰白色沉淀;继续加热,试管中出现“白雾”,浊液逐渐变澄清,溶液颜色慢慢变为浅蓝色,试管底部灰白色沉淀增多。
资料:ⅰ.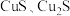 均为黑色固体。
均为黑色固体。
ⅱ.
Ⅰ.沉淀成分探究。
(1)经检验灰白色沉淀中含有无水硫酸铜,结合化学方程式解释原因_______ 。
继续探究沉淀成分:取沉淀,用蒸馏水多次洗涤,干燥,得到沉淀样品,取少量样品于试管中,分别进行如下3个实验。
(2)根据实验①,推测沉淀中含有还原性物质,经检验有 ,反应初期生成
,反应初期生成 可能原因是
可能原因是_______ 。
(3)②中浅蓝色溶液变深的反应原理是(用离子方程式表示)_______ 。
(4)由以上实验推断沉淀成分主要有_______ 。
Ⅱ.溶液颜色探究。
猜测1:查阅资料:若铜丝不纯(含有铁),导致体系中含有 和
和 ,与水合铜离子调和成墨绿色。
,与水合铜离子调和成墨绿色。
猜测2:铜丝表面常常涂一层聚氯乙烯薄膜,聚氯乙烯在加热条件下易分解产生 ,导致反应体系中形成
,导致反应体系中形成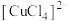 (黄色),与水合铜离子混合溶液呈绿色。
(黄色),与水合铜离子混合溶液呈绿色。
(5)④中加入的试剂是_______ ;⑤中实验现象_______ 。
(6)总结:铜与浓硫酸反应的多样性与_______ 有关。
加热铜与浓硫酸,在反应过程中,有刺激性气味的气体产生,溶液逐渐变为墨绿色浊液,试管底部有灰白色沉淀;继续加热,试管中出现“白雾”,浊液逐渐变澄清,溶液颜色慢慢变为浅蓝色,试管底部灰白色沉淀增多。
资料:ⅰ.
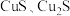 均为黑色固体。
均为黑色固体。
ⅱ.

Ⅰ.沉淀成分探究。
(1)经检验灰白色沉淀中含有无水硫酸铜,结合化学方程式解释原因
继续探究沉淀成分:取沉淀,用蒸馏水多次洗涤,干燥,得到沉淀样品,取少量样品于试管中,分别进行如下3个实验。
| 编号 | 试剂 | 实验操作 | 实验现象 | |
 | ① | 浓硝酸 | 滴加适量浓硝酸 | 沉淀逐渐溶解,产生大量红棕色气体 |
| ② | 氨水 | 滴加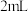 氨水,振荡,在空气中放置一段时间 氨水,振荡,在空气中放置一段时间 | 滴加氨水后,溶液呈极浅蓝色;静置后逐渐变深,呈深蓝色 | |
| ③ | 酒精 | 滴加 酒精,充分振荡,静置、过滤,将滤液移入盛有水的试管中,稍加振荡 酒精,充分振荡,静置、过滤,将滤液移入盛有水的试管中,稍加振荡 | 酒精与水的界面呈现乳白色 |
(2)根据实验①,推测沉淀中含有还原性物质,经检验有
 ,反应初期生成
,反应初期生成 可能原因是
可能原因是(3)②中浅蓝色溶液变深的反应原理是(用离子方程式表示)
(4)由以上实验推断沉淀成分主要有
Ⅱ.溶液颜色探究。
猜测1:查阅资料:若铜丝不纯(含有铁),导致体系中含有
 和
和 ,与水合铜离子调和成墨绿色。
,与水合铜离子调和成墨绿色。猜测2:铜丝表面常常涂一层聚氯乙烯薄膜,聚氯乙烯在加热条件下易分解产生
 ,导致反应体系中形成
,导致反应体系中形成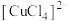 (黄色),与水合铜离子混合溶液呈绿色。
(黄色),与水合铜离子混合溶液呈绿色。| 编号 | 实验操作 | 实验现象 | 实验结论 |
| ④ | 取铜丝与浓硫酸反应后的混合液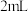 于试管中,滴入2滴 于试管中,滴入2滴 ,再加入____ ,再加入____ | 溶液未变红 | 混合液中不含 |
| ⑤ | 取一段铜丝放入大试管中,加入 浓硫酸,加热 浓硫酸,加热 | _______ | 铜丝表面含有氯元素 |
| ⑥ | 另取一段铜丝,在酒精灯上灼烧除去铜丝表面薄膜;放入大试管中,加入 浓硫酸,加热 浓硫酸,加热 | 溶液慢慢变蓝色、蓝黑色 |
(5)④中加入的试剂是
(6)总结:铜与浓硫酸反应的多样性与
您最近一年使用:0次
8 . 化学小组同学探究铜与过量浓硝酸反应后溶液呈绿色的原因。
资料:ⅰ.铜与浓硝酸反应过程中可生成 ,
, 易分解产生无色气体。
易分解产生无色气体。
ⅱ. 是一种弱酸。
是一种弱酸。 电离出
电离出 ,
, 与
与 发生如下反应:
发生如下反应: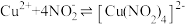 (绿色)
(绿色)
下列说法不正确 的是
资料:ⅰ.铜与浓硝酸反应过程中可生成
 ,
, 易分解产生无色气体。
易分解产生无色气体。ⅱ.
 是一种弱酸。
是一种弱酸。 电离出
电离出 ,
, 与
与 发生如下反应:
发生如下反应: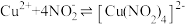 (绿色)
(绿色)| 编号 | 操作 | 现象 |
| ① | 分别向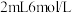  和 和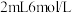  溶液中通入稳定的 溶液中通入稳定的 气流 气流 |  溶液变黄 溶液变黄 溶液不变黄 溶液不变黄 |
| ② | 将实验①的黄色溶液与蓝色 溶液混合 溶液混合 | 溶液呈绿色 |
| ③ | 将  溶液与 溶液与  溶液混合 溶液混合 | 溶液呈绿色 |
| ④ | 向实验③所得溶液中加入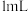 浓硝酸 浓硝酸 | 溶液变蓝 |
A.依据实验①,向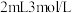  通入稳定的 通入稳定的 气流,溶液可能会变黄 气流,溶液可能会变黄 |
B.实验④加入浓硝酸后可能发生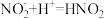 ,使 ,使 浓度下降,绿色消失 浓度下降,绿色消失 |
C.铜与过量浓硝酸反应溶液呈绿色可能原因是:浓硝酸中溶解了生成的 呈黄色,黄色与蓝色叠加呈绿色 呈黄色,黄色与蓝色叠加呈绿色 |
D.铜与过量浓硝酸反应溶液呈绿色可能原因是:铜与浓硝酸反应过程中,生成 使溶液呈绿色 使溶液呈绿色 |
您最近一年使用:0次
名校
解题方法
9 . 某化学小组研究硝酸与金属的反应。下列实验中硝酸与金属的反应均在注射器中完成,实验操作及实验现象记录如表:
(1)铜与浓HNO3反应产生红棕色气体的化学方程式是___________ 。
(2)对实验1所得溶液呈绿色,而实验2所得溶液呈蓝色的原因提出猜想。
查阅资料:
i.NO2溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;
ⅱ.NO2与水反应时会有部分发生反应: ,HNO2是弱酸,无色,不稳定。
,HNO2是弱酸,无色,不稳定。
ⅲ. 离子颜色为绿色。
离子颜色为绿色。
猜想1:NO2溶于浓硝酸,与蓝色 溶液混合而呈现绿色。
溶液混合而呈现绿色。
猜想2:HNO2电离出的 与
与 结合为
结合为 (绿色)。
(绿色)。
①向浓硝酸中通入NO2,溶液呈黄色,加入___________ (填试剂)后呈绿色,证实猜想1合理。
②研究猜想2是否为实验I所得溶液呈绿色的主要原因,实验如下。
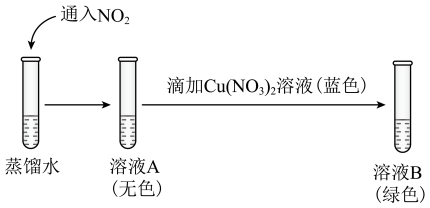
a.证明溶液A中含有HNO2的证据是___________ 。
b.向溶液B中滴加少量硝酸,溶液由绿色变为蓝色。结果表明,猜想2不是实验I所得溶液呈绿色的主要原因,说明理由:___________ 。
(3)实验2中充入O2后气体变为红棕色的反应的化学方程式是___________ 。
(4)查阅文献:铁粉与稀硝酸反应会生成H2.由实验3中的实验现象可知,过量的铁粉与0.5mol/L稀HNO3反应的还原产物中除了H2外,还有___________ 生成。写出白色沉淀迅速变为灰绿色,最后变成红褐色的化学方程式___________ 。
(5)甲同学对实验3产生H2的原因提出假设:该浓度的硝酸中H+的氧化性大于 。乙同学认为该假设不合理。依据是实验2中观察到了
。乙同学认为该假设不合理。依据是实验2中观察到了___________ (填实验现象),该现象能说明假设不合理。
(6)结合以上实验可知,金属与硝酸反应的产物与___________ 等因素有关。
| 序号 | 实验操作与实验现象 |
| 实验1 | 加入适量铜片与2mL的浓硝酸。反应剧烈,产生红棕色气体,溶液立即呈绿色。 |
| 实验2 | 加入过量的铜片与2mL0.5mol/LHNO3溶液。产生无色气泡,溶液逐渐变为蓝色。注射器中的气体始终无色。反应结束后,向注射器中充入一定量的O2,气体迅速变为红棕色 |
| 实验3 | 加入过量的铁粉与2mL0.5mol/LHNO3溶液,立即有无色气体生成,溶液为很浅的绿色,反应结束后将气体通入有空气的容器无明显变化,点燃,有尖锐的爆鸣声,容器壁出现无色液滴;取反应后溶液,加入足量NaOH溶液,立刻得到白色沉淀,迅速变为灰绿色,最后变成红褐色,加热后产生能使湿润红色石蕊试纸变蓝的气体。 |
(1)铜与浓HNO3反应产生红棕色气体的化学方程式是
(2)对实验1所得溶液呈绿色,而实验2所得溶液呈蓝色的原因提出猜想。
查阅资料:
i.NO2溶于稀硝酸会反应:而溶于浓硝酸不反应,使溶液呈黄色;
ⅱ.NO2与水反应时会有部分发生反应:
 ,HNO2是弱酸,无色,不稳定。
,HNO2是弱酸,无色,不稳定。ⅲ.
 离子颜色为绿色。
离子颜色为绿色。猜想1:NO2溶于浓硝酸,与蓝色
 溶液混合而呈现绿色。
溶液混合而呈现绿色。猜想2:HNO2电离出的
 与
与 结合为
结合为 (绿色)。
(绿色)。①向浓硝酸中通入NO2,溶液呈黄色,加入
②研究猜想2是否为实验I所得溶液呈绿色的主要原因,实验如下。

a.证明溶液A中含有HNO2的证据是
b.向溶液B中滴加少量硝酸,溶液由绿色变为蓝色。结果表明,猜想2不是实验I所得溶液呈绿色的主要原因,说明理由:
(3)实验2中充入O2后气体变为红棕色的反应的化学方程式是
(4)查阅文献:铁粉与稀硝酸反应会生成H2.由实验3中的实验现象可知,过量的铁粉与0.5mol/L稀HNO3反应的还原产物中除了H2外,还有
(5)甲同学对实验3产生H2的原因提出假设:该浓度的硝酸中H+的氧化性大于
 。乙同学认为该假设不合理。依据是实验2中观察到了
。乙同学认为该假设不合理。依据是实验2中观察到了(6)结合以上实验可知,金属与硝酸反应的产物与
您最近一年使用:0次
10 . 某校化学实验兴趣小组同学设计了如图所示的实验装置,利用如下原理探究氯气的某些性质反应原理: .
.
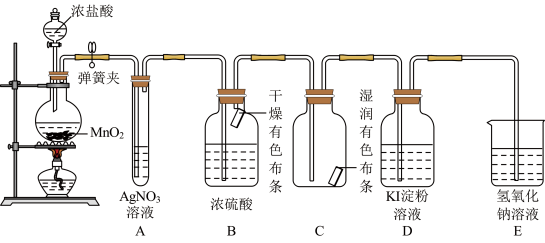
(1)A中产生现象是______ ,甲同学认为是 与水反应产生某新物质的结果,写出其中发生的两个反应的化学方程式
与水反应产生某新物质的结果,写出其中发生的两个反应的化学方程式______ 、______ ,乙同学则认为A中的现象不足以说明白色沉淀是 与水反应产生新物质的结果,理由是
与水反应产生新物质的结果,理由是______ .
(2)B和C中出现的不同现象可得出的结论是______ .
(3)装置D中产生的现象是______ ,该反应的基本反应类型是______ .
(4)E是尾气吸收装置,写出其中发生反应的离子方程式:______ ,丙同学将充分吸收了尾气之后的吸收液拿来做实验,向吸收液中滴加盐酸,产生了有刺激性气味的气体,写出该反应的离子方程式______ .
(5)工业上用氯气和石灰乳反应可制漂白粉,该反应方程式为:______ ,漂白粉需要密闭保存,原因是(用化学方程式表示)______ ,丁同学取漂白粉的溶液来做实验,向其中滴加碳酸钠溶液,观察到产生白色沉淀,请推测白色沉淀为______ (填化学式).
 .
.
(1)A中产生现象是
 与水反应产生某新物质的结果,写出其中发生的两个反应的化学方程式
与水反应产生某新物质的结果,写出其中发生的两个反应的化学方程式 与水反应产生新物质的结果,理由是
与水反应产生新物质的结果,理由是(2)B和C中出现的不同现象可得出的结论是
(3)装置D中产生的现象是
(4)E是尾气吸收装置,写出其中发生反应的离子方程式:
(5)工业上用氯气和石灰乳反应可制漂白粉,该反应方程式为:
您最近一年使用:0次