名校
解题方法
1 . 下列实验的操作、现象和结论正确的是
| 选项 | 实验目的 | 实验操作 | 现象和结论 |
| A | 鉴别食盐与亚硝酸钠 | 分别取少量溶液于试管中,再滴加少量酸性 溶液 溶液 | 若溶液的紫红色不褪去,则该溶液为 溶液 溶液 |
| B | 检验海带中是否含有碘元素 | 将海带灼烧、溶解、过滤、酸化,加入少量新制氯水后加入淀粉溶液 | 溶液变蓝,则证明海带中含有碘元素 |
| C | 比较难溶物的 大小 大小 | 向等浓度的 和 和 混合溶液中逐滴滴入氢氧化钠溶液 混合溶液中逐滴滴入氢氧化钠溶液 | 先产生红褐色沉淀,说明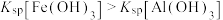 |
| D | 探究温度对水解平衡的影响 | 将25℃  溶液加热到40℃,用pH计测量溶液pH变化 溶液加热到40℃,用pH计测量溶液pH变化 | pH逐渐减小,说明温度升高,促进 溶液水解 溶液水解 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
解题方法
2 . 海洋中蕴含着丰富的化学元素,是人类资源的宝库。
I.某学校兴趣小组在实验室按如下实验流程提取海带中的碘。

(1)海带灼烧的目的是___________ 。海带灰中含有的其他可溶性无机盐,是在___________ (从以上流程中选填实验操作名称)中实现与碘分离。上述实验流程中不需要用到的仪器是___________ (从下列图中选择,写出名称)。

(2)“氧化”时加入3mol·L-1H2SO4和3%H2O2溶液,发生反应的离子方程式为___________ 。
(3)加碘食盐中的碘以KIO3形式存在,证明食盐中存在IO ,必须使用的物质是
,必须使用的物质是___________ (填序号)。
①pH试纸 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④蒸馏水 ⑤食醋 ⑥醇
Ⅱ.某学校兴趣小组从海水晒盐后的盐卤(含MgCl2、NaCl、KCl、MgSO4等)中模拟工业生产来提取镁,主要过程如图甲:
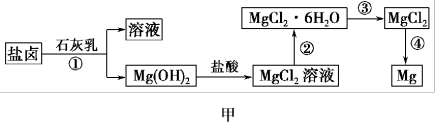
(4)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到T2℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是___________ 。步骤③的具体操作为___________ 。
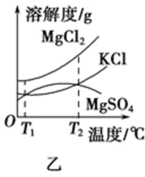
(5)写出步骤④制备金属镁的化学方程式:___________ 。该过程得到的镁蒸气需要在特定的循环中冷却,可选用___________ (填字母)作冷却剂。
A.Ar B.CO2 C.空气 D.O2 E.水蒸气
I.某学校兴趣小组在实验室按如下实验流程提取海带中的碘。

(1)海带灼烧的目的是

(2)“氧化”时加入3mol·L-1H2SO4和3%H2O2溶液,发生反应的离子方程式为
(3)加碘食盐中的碘以KIO3形式存在,证明食盐中存在IO
 ,必须使用的物质是
,必须使用的物质是①pH试纸 ②蓝色石蕊试纸 ③碘化钾淀粉试纸 ④蒸馏水 ⑤食醋 ⑥醇
Ⅱ.某学校兴趣小组从海水晒盐后的盐卤(含MgCl2、NaCl、KCl、MgSO4等)中模拟工业生产来提取镁,主要过程如图甲:

(4)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到T2℃以上,根据溶解度曲线,首先从盐卤中分离出来的晶体是

(5)写出步骤④制备金属镁的化学方程式:
A.Ar B.CO2 C.空气 D.O2 E.水蒸气
您最近一年使用:0次
3 . 我国拥有很长的海岸线,具有丰富的海洋资源。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。
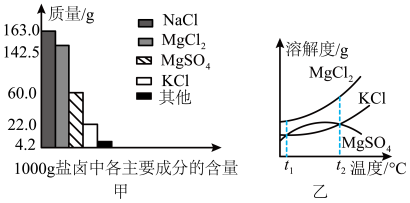
(1)根据图甲所示,写出盐卤中含量最多的盐为__________ 。(填化学式)
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到 以上,根据溶解度曲线,首先析出的晶体应是
以上,根据溶解度曲线,首先析出的晶体应是__________ 。(填化学式)
(3)如图是常用于混合物的分离和提纯的装置:
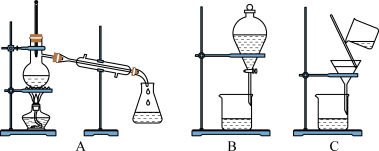
粗盐的提纯应选择图__________ (填字母,下同)装置,若实验中为了除去粗盐中的 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是__________ 。
A.NaOH、 、
、 、HCl B.NaOH、
、HCl B.NaOH、 、
、 、HCl
、HCl
C. 、
、 、NaOH、HCl D.
、NaOH、HCl D. 、NaOH、
、NaOH、 、HCl
、HCl
Ⅱ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的__________ (填字母)
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中 的存在,
的存在,______________________________ 。
(6)“提取碘”存在以下两种方案。
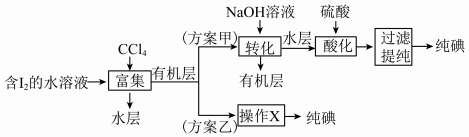
①方案乙中“操作X”的名称是__________ 。
②该流程可循环利用的物质是__________ 。
③采用方案乙得到纯碘的产率较低,原因是______________________________ 。
Ⅰ.盐卤是海水晒盐后的富含镁盐的溶液,其中除含镁盐外,还含有其他盐类(如图甲所示)。

(1)根据图甲所示,写出盐卤中含量最多的盐为
(2)图乙是盐卤中某些物质的溶解度曲线,将盐卤加热到
 以上,根据溶解度曲线,首先析出的晶体应是
以上,根据溶解度曲线,首先析出的晶体应是(3)如图是常用于混合物的分离和提纯的装置:

粗盐的提纯应选择图
 、
、 、
、 等杂质离子加入试剂的顺序可以是
等杂质离子加入试剂的顺序可以是A.NaOH、
 、
、 、HCl B.NaOH、
、HCl B.NaOH、 、
、 、HCl
、HClC.
 、
、 、NaOH、HCl D.
、NaOH、HCl D. 、NaOH、
、NaOH、 、HCl
、HClⅡ.海带是一种含碘量很高的海藻,从中提取的碘广泛应用于医药、食品和化工。实验室里从海带中提取碘的流程如图。

(4)实验步骤①会用到下列仪器中的
a.酒精灯 b.蒸发皿 c.坩埚 d.泥三角
(5)设计实验证明第③步操作后滤液中
 的存在,
的存在,(6)“提取碘”存在以下两种方案。

①方案乙中“操作X”的名称是
②该流程可循环利用的物质是
③采用方案乙得到纯碘的产率较低,原因是
您最近一年使用:0次
2023-12-27更新
|
159次组卷
|
2卷引用:河北省保定市1+3联考2023-2024学年高一上学期12月月考化学试题
名校
解题方法
4 . 下列方案设计、现象和结论正确的是
| 目的 | 方案设计 | 现象和结论 | |
| A | 探究H2SO3和 的酸性强弱 的酸性强弱 | 将SO2气体通入Ca(ClO)2溶液中 | 若产生白色沉淀,则说明酸性:H2SO3>HClO |
| B | 验证某红棕色气体是否为 NO2 | 将气体通入淀粉碘化钾溶液 | 若溶液变蓝,则说明气体为NO2 |
| C | 探究碘在纯水和CCl4中溶解性 | 向碘的四氯化碳溶液中加入 1mL 浓KI 溶液,振荡试管。 | 若碘的四氯化碳溶液紫色变浅,说明碘在纯水中的溶解性更好 |
| D | 检验海带中是否含有碘元素 | 将海带灰溶解过滤后,取适量滤液于试管中,酸化后加入少量双氧水,充分反应后加入1~2 滴淀粉溶液 | 溶液变蓝,则证明海带中含有碘元素 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
名校
5 . 海洋是一座巨大的化学资源宝库,如图是从海水中或海产品中提取若干种化学物质的流程图。
Ⅰ.海水提溴的流程如图所示:
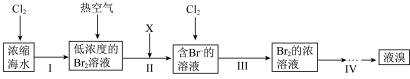
(1)X可用 气体,该反应的离子方程式为
气体,该反应的离子方程式为___________ 。
(2)步骤Ⅳ包含蒸馏,该操作不需要下列仪器中的___________ (填字母)。
a.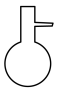 b.
b. c.
c.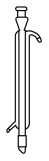 d.
d.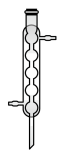 e.
e.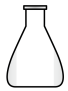 f.
f.
Ⅱ.兴趣小组同学按如图实验过程,证明海带中存在碘元素。
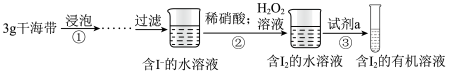
(3)实验时需要将干海带放入___________ 中灼烧(填仪器名称)
(4) 的作用是
的作用是___________ (用离子方程式解释)
(5)试剂a不能选择的是(填序号)___________。
(6)操作③的名称是___________ 。
(7)操作③中需要振荡排放气体,放气时分液漏斗的状态是___________。
Ⅰ.海水提溴的流程如图所示:

(1)X可用
 气体,该反应的离子方程式为
气体,该反应的离子方程式为(2)步骤Ⅳ包含蒸馏,该操作不需要下列仪器中的
a.
 b.
b. c.
c. d.
d. e.
e. f.
f.
Ⅱ.兴趣小组同学按如图实验过程,证明海带中存在碘元素。

(3)实验时需要将干海带放入
(4)
 的作用是
的作用是(5)试剂a不能选择的是(填序号)___________。
A. | B.苯 | C.酒精 | D.裂化汽油 |
(7)操作③中需要振荡排放气体,放气时分液漏斗的状态是___________。
A.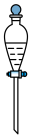 | B. | C.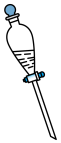 | D.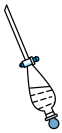 |
您最近一年使用:0次
解题方法
6 . 下列有关实验操作能达到相应实验目的的是
| 选项 | 实验操作 | 实验目的 |
| A | 将干海带灼烧、浸取、过滤 | 获得含 的水溶液 的水溶液 |
| B | 将表面积相同的镁条和铝条放入相同浓度相同温度的稀盐酸中 | 比较镁铝的失电子能力 |
| C | 将 固体高温加热成熔融,测其熔融态导电性 固体高温加热成熔融,测其熔融态导电性 | 证明 中含有离子键 中含有离子键 |
| D | 取相同体积不同浓度的 溶液于两试管中,分别向两试管中加入等体积等浓度的 溶液于两试管中,分别向两试管中加入等体积等浓度的 | 探究浓度对化学反应速率的影响 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
解题方法
7 . 碘和碘的化合物在有机化学中十分重要,另外在医药和照相方面的用途也很广泛。海带提碘的相关流程如下所示,已知 ,请回答下列问题:
,请回答下列问题:
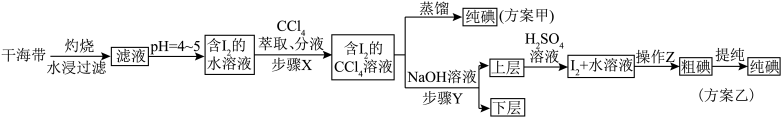
(1)海带灼烧的目的是_______ ;实验室进行此操作用到的主要仪器名称为_______ 。
(2)滤液得到含 的水溶液,除了调节
的水溶液,除了调节 ,还需要加入臭氧或过氧化氢,所加试剂在反应中作
,还需要加入臭氧或过氧化氢,所加试剂在反应中作_______ 剂(填“氧化”或“还原”),写出加入过氧化氢时发生反应的离子方程式:_______ 。
(3)步骤 是否可以用酒精代替
是否可以用酒精代替 ,并说明理由
,并说明理由_______ 。
(4)步骤 的操作为
的操作为_______ 。
(5)上层液体加入 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为_______ 。
(6)以上流程中可以循环使用的试剂是_______ 。
(7)加碘食盐中的碘以碘酸钾 形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在
形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在 。可供选用的物质有:①
。可供选用的物质有:① 试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是
试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是_______ (填序号)。
 ,请回答下列问题:
,请回答下列问题:
(1)海带灼烧的目的是
(2)滤液得到含
 的水溶液,除了调节
的水溶液,除了调节 ,还需要加入臭氧或过氧化氢,所加试剂在反应中作
,还需要加入臭氧或过氧化氢,所加试剂在反应中作(3)步骤
 是否可以用酒精代替
是否可以用酒精代替 ,并说明理由
,并说明理由(4)步骤
 的操作为
的操作为(5)上层液体加入
 溶液后发生反应的离子方程式为
溶液后发生反应的离子方程式为(6)以上流程中可以循环使用的试剂是
(7)加碘食盐中的碘以碘酸钾
 形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在
形式存在,根据以上信息,可用试纸和一些常见试剂进行检验,证明食盐中存在 。可供选用的物质有:①
。可供选用的物质有:① 试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是
试纸、②蓝色石蕊试纸、③碘化钾淀粉试纸、④蒸馏水、⑤食醋、⑥醇,进行上述实验时必须使用的物质是
您最近一年使用:0次
解题方法
8 . 海洋是巨大的资源宝库,孕育着丰富的矿产。海水资源的综合利用对人类的生产生活有重要意义。回答下列问题:
Ⅰ.从海带中提取碘的工艺流程如图所示:

(1)灼烧干海带需在仪器________ (填“蒸发皿”“坩埚”或“烧杯”)内进行。
(2)用蒸馏水浸取海带灰时,为提高浸取率,可采用的方法有_________ (填一种即可);
(3)将溶液中的I-氧化成I2,最佳选用试剂为_________(填标号)。
(4)欲证明水溶液中含有I2,实验方法为________________ 。
Ⅱ.空气吹出法是目前“海水提溴”的主要方法之一,其主要工艺流程如图所示:

(5)步骤①的离子方程式为___________ 。
(6)步骤②说明溴单质具有_________ 性,步骤③④的目的是______________ 。
(7)步骤③的还原剂若为 溶液,则其离子方程式为
溶液,则其离子方程式为____________ 。
Ⅰ.从海带中提取碘的工艺流程如图所示:

(1)灼烧干海带需在仪器
(2)用蒸馏水浸取海带灰时,为提高浸取率,可采用的方法有
(3)将溶液中的I-氧化成I2,最佳选用试剂为_________(填标号)。
| A.稀硝酸 | B.酸性 | C.浓硫酸 | D.稀硫酸、 |
Ⅱ.空气吹出法是目前“海水提溴”的主要方法之一,其主要工艺流程如图所示:

(5)步骤①的离子方程式为
(6)步骤②说明溴单质具有
(7)步骤③的还原剂若为
 溶液,则其离子方程式为
溶液,则其离子方程式为
您最近一年使用:0次
名校
解题方法
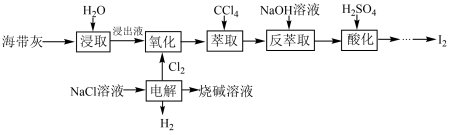
9 . 海带中含有丰富的碘,某校化学兴趣小组的同学们设计联合氯碱工业,以海带灰为原料提碘的工艺流程如图:
回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是_____ ;请你设计实验证明“浸取”已经进行完全:_____ (需要用到的实验药品有:淀粉溶液、硫酸酸化的H2O2溶液,写出具体实验操作和现象)。
(2)“电解”反应的化学方程式为_____ 。
(3)“萃取”时,CCl4层的颜色为______ 色;“反萃取”时生成NaI和NaIO3,写出该反应的离子方程式:______ 。
(4)“酸化”后生成含I2的悬浊液,需要经过_____ (填操作名称)操作得到I2。
(5)该工艺流程实际操作中,碘的损失率为23.8%。若以2.5t海带灰为原料,最终制得I2物质的量为3×103mol,则该原料中含碘量为______ %
(6)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有_____ (填化学式)。

回答下列问题:
(1)“浸取”操作需要进行2~3次,将所得浸取液合并后进入下一流程,其目的是
(2)“电解”反应的化学方程式为
(3)“萃取”时,CCl4层的颜色为
(4)“酸化”后生成含I2的悬浊液,需要经过
(5)该工艺流程实际操作中,碘的损失率为23.8%。若以2.5t海带灰为原料,最终制得I2物质的量为3×103mol,则该原料中含碘量为
(6)该工艺流程中,除了H2O和NaCl以外,可以循环利用的物质有
您最近一年使用:0次
名校
解题方法
10 . 海洋是一座巨大的化学资源宝库,如图是从海水中或海产品中提取若干种化学物质的流程图。
I.试剂级NaCl可用海盐(含泥沙、海藻、Ca2+、Mg2+、Fe3+、SO 等杂质)为原料制备。
等杂质)为原料制备。

(1)焙炒海盐的目的是______ 。
(2)根据除杂原理,填写合适的试剂③,并选择每步 预期沉淀的离子。
离子:a.Ca2+ b.Mg2+ c.Fe3+ d.SO
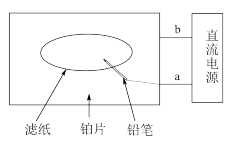
(3)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是______ 。
II.国家海洋局科研学者考察了从浓海水中提溴的一种新型方法:聚四氟乙烯(PTFE)气态膜法提溴。本方法关键是采用了PTFE中空纤维膜,在该膜中,水不可以通过,而溴分子可以自主进入和脱离。
将氧化后的浓海水加入气态膜设备预处理,用NaOH溶液作为吸收液配合处理。处理过程的俯视截面示意图如图所示。经流出液氧化后的流出液检验,流出液中含BrO 离子。
离子。
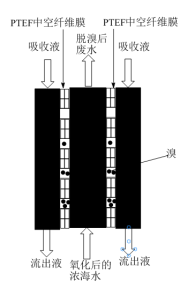
(4)浓海水中溴元素的存在形式是______ ,氧化浓海水时可选用的氧化剂是______ 。
(5)流出液中另外一种含溴物质是______ 。
(6)说明聚四氟乙烯(PTFE)气态膜是如何在上述过程中起到富集作用______ 。
III.小淳同学按如图实验过程,证明海带中存在碘元素。
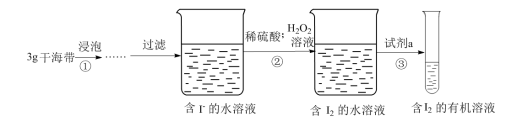
(7)H2O2的作用是______ 。
(8)试剂a不能选择的是(填序号)______ 。
(9)操作③的名称是______ 。
(10)操作③中需要振荡排放气体,放气时分液漏斗的状态是______ 。
小桢同学欲探究I-的性质,进行如图实验:
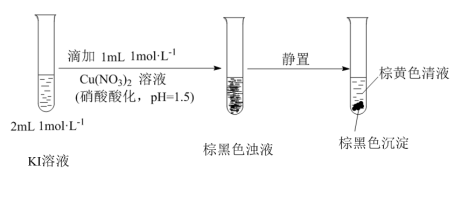
(11)该小组同学推测反应生成了I2。设计实施了如下方案,证实了推测。请将方案补充完整:取棕色清液,______ 。
进一步探究发现:棕黑色沉淀中含有CuI。
(12)由此推知:Cu(NO3)2与KI反应过程中,一定发生的反应的离子方程式为______ 。
I.试剂级NaCl可用海盐(含泥沙、海藻、Ca2+、Mg2+、Fe3+、SO
 等杂质)为原料制备。
等杂质)为原料制备。
(1)焙炒海盐的目的是
(2)根据除杂原理,填写合适的试剂③,并
离子:a.Ca2+ b.Mg2+ c.Fe3+ d.SO

| 实验步骤 | 试剂 | 预期沉淀的离子 |
| 步骤1 | 适量NaOH溶液 | ① |
| 步骤2 | 适量BaCl2溶液 | ② |
| 步骤3 | 适量③ | ④ |
(3)以氯化钠为原料设计了“黑笔写红字”的趣味实验。滤纸先用氯化钠、无色酚酞的混合液浸湿,然后平铺在一块铂片上,接通电源后,用铅笔在滤纸上写字,会出现红色字迹。下列叙述正确的是

| A.b极发生还原反应 | B.铂片端作阴极 |
| C.铅笔端有少量的氯气产生 | D.a处是负极 |
II.国家海洋局科研学者考察了从浓海水中提溴的一种新型方法:聚四氟乙烯(PTFE)气态膜法提溴。本方法关键是采用了PTFE中空纤维膜,在该膜中,水不可以通过,而溴分子可以自主进入和脱离。
将氧化后的浓海水加入气态膜设备预处理,用NaOH溶液作为吸收液配合处理。处理过程的俯视截面示意图如图所示。经流出液氧化后的流出液检验,流出液中含BrO
 离子。
离子。
(4)浓海水中溴元素的存在形式是
(5)流出液中另外一种含溴物质是
(6)说明聚四氟乙烯(PTFE)气态膜是如何在上述过程中起到富集作用
III.小淳同学按如图实验过程,证明海带中存在碘元素。

(7)H2O2的作用是
(8)试剂a不能选择的是(填序号)
| A.CCl4 | B.苯 | C.酒精 | D.直馏汽油 |
(9)操作③的名称是
(10)操作③中需要振荡排放气体,放气时分液漏斗的状态是
A.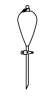 | B.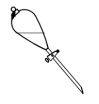 | C.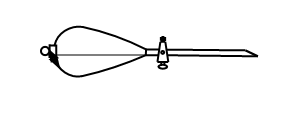 | D. |
小桢同学欲探究I-的性质,进行如图实验:

(11)该小组同学推测反应生成了I2。设计实施了如下方案,证实了推测。请将方案补充完整:取棕色清液,
进一步探究发现:棕黑色沉淀中含有CuI。
(12)由此推知:Cu(NO3)2与KI反应过程中,一定发生的反应的离子方程式为
您最近一年使用:0次



