河北省邯郸市馆陶县第一中学2019-2020学年高一下学期期中考试化学试卷
河北
高一
期中
2020-05-08
446次
整体难度:
容易
考查范围:
常见无机物及其应用、化学与STSE、物质结构与性质、化学反应原理、化学实验基础、有机化学基础、认识化学科学
一、单选题 添加题型下试题
| A.铊比铝的金属性更强 |
| B.氢氧化铊一定具有两性 |
| C.铊在化合物中可以是+3价 |
| D.铊能与盐酸反应放出氢气 |
【知识点】 同主族元素性质递变规律理解及应用解读
| A.液氨是纯净物 |
| B.实验室制氨气的方法是加热NH4Cl |
| C.氨易液化,因此可用来作制冷剂 |
| D.氨极易溶于水,因此可用来作喷泉实验 |
| A.铝热反应 | B.灼热的炭与二氧化碳反应 |
| C.Ba(OH)2·8H2O 晶体和NH4Cl晶体混合 | D.碳酸钙的分解 |
 2Z2在反应过程中的反应速率)(v)与时间(t)的关系曲线,下列叙述正确的是
2Z2在反应过程中的反应速率)(v)与时间(t)的关系曲线,下列叙述正确的是
| A.t1时,只有正反应方向 | B.T1时,反应到达限度 |
| C.t2-t3,反应不再发生 | D.t2-t3,各物质的浓度不再发生变化 |
【知识点】 可逆反应及反应限度解读 化学平衡状态的判断方法解读
①SiO2和SO3 ②晶体硼和HCl ③CO2和SO2 ④晶体硅和金刚石 ⑤晶体氖和晶体氮 ⑥硫黄和碘
| A.①②③ | B.④⑤⑥ | C.③④⑥ | D.①③⑤ |
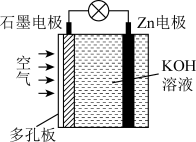
| A.石墨为正极 |
| B.电池放电时Zn电极逐渐溶解 |
| C.电子由石墨经导线流向Zn片 |
| D.电池放电时实现了化学能向电能的转化 |
| A.加入少量铁粉 |
| B.加NaCl溶液 |
| C.滴入几滴硫酸铜溶液 |
| D.改用10 mL 0.1 mol·L-1盐酸 |
A.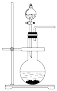 装置甲可作为制取NO2的发生装置 装置甲可作为制取NO2的发生装置 |
B.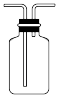 装置乙可作为制取NO的收集装置 装置乙可作为制取NO的收集装置 |
C. 装置丙可作为制取Cl2的尾气吸收装置 装置丙可作为制取Cl2的尾气吸收装置 |
D.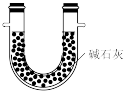 装置丁可用于除去NH3中H2O 装置丁可用于除去NH3中H2O |
【知识点】 氨气 常见气体的制备与收集解读
| A.a-c=m-n | B.a-b=n-m | C.c-d=m+n | D.b-d=n+m |
| A.v(A)=15mol·(L·min)−1 | B.v(B)=18mol·(L·min)−1 |
| C.v(C)=0.8mol·(L·s)−1 | D.v(D)=1mol·(L·s)−1 |
【知识点】 化学反应速率与化学计量数之间的关系解读

| A.原子半径:W>Z>Y>X |
| B.最高价氧化物对应水化物的酸性:X>W>Z |
| C.最简单气态氢化物的热稳定性:Y>X>W>Z |
| D.元素X、Z、W的最高化合价分别与其主族序数相等 |
a.
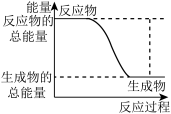 b.
b.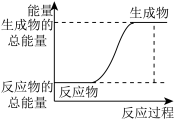
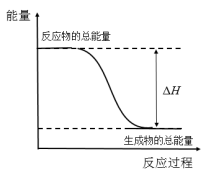
| A.图a表示的是吸热反应的能量变化 |
| B.图a不需要加热就能发生,图b一定需要加热才能发生 |
| C.图a可以表示C与CO2反应生成CO的能量变化 |
| D.图b中反应物比生成物稳定 |
【知识点】 化学反应中能量变化的原因 吸热反应和放热反应解读
 3Fe2+,能实现该反应的原电池是
3Fe2+,能实现该反应的原电池是| A.正极为Cu,负极为Fe,电解质为FeCl3溶液 |
| B.正极为C,负极为Fe,电解质为FeSO4溶液 |
| C.正极为Fe,负极为Zn,电解质为Fe2(SO4)3溶液 |
| D.正极为Ag,负极为Cu,电解质为CuSO4溶液 |
| A.N2、H2的和NH3的质量分数不再改变 |
| B.c(N2):c(H2):c(NH3)=1:3:2 |
| C.N2和H2的物质的量之和NH3的物质的量的2倍 |
| D.单位时间内每增加1molN2,同时增加3molH2 |
【知识点】 化学平衡状态的判断方法解读
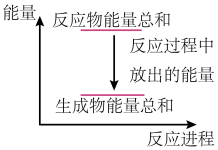
| A.Zn和H2SO4的总能量大于ZnSO4和H2的总能量 |
| B.反应过程中能量关系可用上图表示 |
| C.若将该反应设计成原电池,则Zn为负极 |
| D.若将该反应设计成原电池,当有32.5g锌溶解时正极放出22.4 L气体 |
【知识点】 反应热与焓变概念比较解读 原电池概念及组成 原电池有关计算解读
| A.3种 | B.4种 | C.5种 | D.6种 |
| A.原子半径:r(X) < r(Y) < r(Z) < r(W) |
| B.W的最高价氧化物的水化物是一种弱碱 |
| C.Y氢化物的稳定性比Z的氢化物的稳定性强 |
| D.X、Y、Z 三种元素可以组成共价化合物或离子化合物 |
| A.a>b>c>d |
| B.a>c>d>b |
| C.c>a>b>d |
| D.b>d>c>a |
【知识点】 原电池 利用原电池原理比较金属活动性强弱解读
| A.由于H—O键比H—S键牢固,所以水的熔沸点比H2S高 |
| B.HF的沸点在同族元素的氢化物中出现反常,是因为HF分子间存在氢键 |
| C.F2、Cl2、Br2、I2熔沸点逐渐升高,是因为它们的组成结构相似,分子间的范德华力增大 |
| D.氯化铵固体受热分解破坏了离子键 |
 2HI(g),生成2molHI(g)反应放出热量akJ,已知(a、b、c均大于零),下列说法正确的是( )
2HI(g),生成2molHI(g)反应放出热量akJ,已知(a、b、c均大于零),下列说法正确的是( )
| A.反应物的总能量低于生成物的总能量 |
| B.断开1molH—H键和1molI—I键所需能量大于断开2molH—I键所需能量 |
| C.向密闭容器中加入2molH2和2molI2,充分反应后放出的热量等于2akJ |
| D.断开2molH—I键所需能量为(c+b+a)kJ |
| 步骤 |
|
| |
| 现象 | Fe表面产生大量无色气泡,液面上方变为红棕色 | Fe表面产生少量红棕色气泡后,迅速停止 | Fe、Cu接触后,其表面均产生红棕色气泡 |
| A.Ⅰ中气体由无色变红棕色的化学方程式:2NO+O2=2NO2 |
| B.Ⅱ中的现象说明Fe表面形成致密的氧化膜,阻止Fe进一步反应 |
| C.对比Ⅰ、Ⅱ中现象,说明稀HNO3的氧化性强于浓HNO3 |
| D.针对Ⅲ中现象,在Fe、Cu之间连接电流计,可判断Fe是否被氧化 |
 2Z,已知反应中X、Y、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到化学平衡时,各物质的浓度可能是
2Z,已知反应中X、Y、Z的起始浓度分别为0.1mol/L、0.3mol/L、0.2mol/L,在一定条件下,当反应达到化学平衡时,各物质的浓度可能是| A.X为0.2mol/L | B.Y为0.5mol/L | C.Z为0.35mol/L | D.Y为0.10mol/L |
| A.0.3 | B.0.225 | C.0.6 | D.0.45 |
二、填空题 添加题型下试题
① O2和O3 ; ②12C 与14C; ③ CH3 (CH2) 3 CH3和
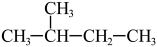
④
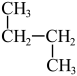 和
和 ;
;(1)互为同位素的是
(3)互为同分异构体的是
①O2 ②H2O2 ③MgCl2 ④H2SO4 ⑤Na2CO3⑥NH4Cl ⑦CO2 ⑧Ne ⑨Na2O2 ⑩NaOH
(1)这些物质中,属于共价化合物的是
(2)写出下列物质的结构式:
①O2
(3)写出下列物质的电子式
⑥NH4Cl
【知识点】 有关粒子结构的化学用语 离子键 共价键 化学键与物质类别关系的判断解读
(1)X、Y、Z、W四种元素的符号: X
(2)由以上元素中的两种元素组成的能溶于水且水溶液显碱性的化合物的电子式分别为
(3)由X、Y、Z所形成的离子化合物是
 xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2molB,并测得C的浓度为1.2mol/L。
xC(g)+2D(s),2min后反应达到平衡状态,此时剩余1.2molB,并测得C的浓度为1.2mol/L。(1)从开始反应至达到平衡状态,生成C的平均反应速率为
(2)x=
(3)下列各项可作为该反应达到平衡状态的标志是
A.气体密度不再变化
B.压强不再变化
C.A的消耗速率与B的消耗速率之比为2:1
D.气体平均相对分子质量不再变化
【知识点】 化学反应速率计算解读 化学平衡状态的判断方法解读
(l)该反应生成物的能量总和
(2)若2mol氢气完全燃烧生成水蒸气,则放出的热量

根据要求回答相关问题:
(1)通入氢气的电极为
(2)石墨电极(C)电极为
(3)反应一段时间后,乙装置中生成氢氧化钠主要在
(4)如果粗铜中含有锌、银等杂质,则丙装置中反应一段时间后,硫酸铜溶液浓度将
(5)若在标准状况下,有4.48L氧气参加反应,则乙装置中铁电极上生成的气体的分子数为
试卷分析
试卷题型(共 31题)
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 二氧化氮 大气污染来源及危害 | |
| 2 | 0.94 | 同主族元素性质递变规律理解及应用 | |
| 3 | 0.94 | 氨的物理性质 氨的喷泉实验 氨气的实验室制法 | |
| 4 | 0.85 | 常见能量转化形式 吸热反应和放热反应 | |
| 5 | 0.85 | 可逆反应及反应限度 化学平衡状态的判断方法 | |
| 6 | 0.65 | 晶体类型判断 化学键类别与晶体类别间的关系 分子晶体 原子晶体(旧教材) | |
| 7 | 0.94 | 原电池原理理解 原电池电子流向判断及应用 原电池正负极判断 | |
| 8 | 0.85 | 浓度对化学反应速率的影响 影响化学反应速率的其他因素 原电池原理对化学反应速率的影响 | |
| 9 | 0.65 | 氨气 常见气体的制备与收集 | |
| 10 | 0.65 | 原子序数与元素在周期表中的位置的关系分析及利用 | |
| 11 | 0.65 | 化学反应速率与化学计量数之间的关系 | |
| 12 | 0.65 | 元素周期律、元素周期表的推断 元素非金属性强弱的比较方法 微粒半径大小的比较方法 | |
| 13 | 0.94 | 化学反应中能量变化的原因 吸热反应和放热反应 | |
| 14 | 0.85 | 原电池 原电池原理的应用 原电池的结构 | |
| 15 | 0.65 | 化学平衡状态的判断方法 | |
| 16 | 0.65 | 反应热与焓变概念比较 原电池概念及组成 原电池有关计算 | |
| 17 | 0.65 | 化学键与分子间作用力 化学键类别与晶体类别间的关系 不同晶体的结构微粒及微粒间作用的区别 | |
| 18 | 0.65 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 “位构性”关系理解及应用 | |
| 19 | 0.85 | 原电池 利用原电池原理比较金属活动性强弱 | |
| 20 | 0.65 | 化学键与物质类别关系的判断 范德华力对物质性质的影响 化学键与分子间作用力 含有氢键的物质 | |
| 21 | 0.65 | 化学反应热的计算 根据△H=反应物的键能之和-生成物的键能之和进行计算 | |
| 22 | 0.65 | 硝酸的强氧化性 原电池原理 电极材料的特殊性质对原电池正负极判断的影响 | |
| 23 | 0.85 | 可逆反应及反应限度 | |
| 24 | 0.65 | 硝酸的强氧化性 有关酸性环境下硝酸根氧化性的有关计算 铜与强氧化性酸的反应 | |
| 二、填空题 | |||
| 25 | 0.85 | “四同”的相关比较 几组常见同素异形体 “四素”比较 | |
| 26 | 0.94 | 有关粒子结构的化学用语 离子键 共价键 化学键与物质类别关系的判断 | |
| 27 | 0.65 | 共价型分子结构式、电子式 元素周期律的应用 根据原子结构进行元素种类推断 | |
| 28 | 0.65 | 化学反应速率计算 化学平衡状态的判断方法 | |
| 29 | 0.65 | 化学反应热的计算 热化学方程式书写及正误判断 依据热化学方程式的计算 | |
| 30 | 0.85 | 根据△H=生成物的总能量之和-反应物的总能量之和进行计算 反应热大小比较 | |
| 31 | 0.65 | 电解原理的应用 原电池、电解池综合考查 电解池电极反应式及化学方程式的书写与判断 利用电子守恒法进行多池串联相关计算 | |





