18. 柴油汽车排放的主要污染物为氮氧化物(NO
x)和颗粒物(PM2.5)。
(1)NO
x的处理与监测。
①汽车尾气中的NO、NO
2和CO可在催化剂存在下反应并转化为参与大气循环的气体,写出NO与CO反应的化学方程式:
__。
②根据下列反应,计算①所写反应的反应热
△H=
_kJ/mol。
已知:N
2(g)+O
2(g)=2NO(g)
△H=+180.5kJ•mol
-1C(g)+O
2(g)=CO
2(g)
△H=-393.5kJ•mol
-12C(g)+O
2(g)=2CO(g)
△H=-221kJ•mol
-1③监测空气中的氮氧化物(假设为NO
2),采集50.00mL含有NO
2的空气,加入适量酸化的H
2O
2的溶液中,使NO
2完全被氧化为NO

,则发生反应的化学方程式为
__,除去所得溶液中过量的过氧化氢后,将其稀释至100.0mL,取出20.00mL.稀释后的溶液,向其中加入足量的稀硫酸和铜粉,使所有NO

还原为NO,消耗的铜粉的质量为1.92mg,则原空气中的NO
2含量为
__mg/L。
(2)氮氧化物(NO
x)主要用SCR技术(选择性催化还原)处理,SCR技术是使用32%尿素[CO(NH
2)]
2作为NH
3的载体,发生的反应如下:
Ⅰ.[CO(NH
2)
2]+H
2O→2NH
3+CO
2Ⅱ.4NH
3+4NO+O
2→4N
2+6H
2O
Ⅲ.4NH
3+2NO+2NO
2→4N
2+6H
2O
Ⅳ.8NH
3+6NO
2→7N
2+12H
2O
Ⅴ.8NH
3+6NO
2→7N
2+12H
2O(过量的氨气可通过反应V转化为氮气)。
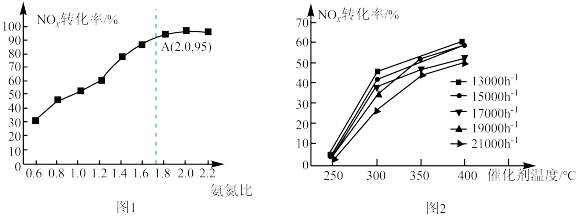
①一定温度下NO
x转化率随着氨氮比(NH
3与NO
x体积比)的变化如图1。当氨氮比为1时,不同空速(单位时间里通过催化剂的空气的量)下NO
x转化率随催化剂温度的变化规律如图2。由图2可知催化剂最低活性温度为
__;图中250℃~300℃时,空速升高,NO
x转化率呈下降的趋势,分析其中的原因可能为
___(写出一条)。
②理论喷射尿素水溶液的质量流量的计算式为Q
urea=

×Q
mass×C
NOx。其中,Q
urea为尿素水溶液喷射的质量流量;R
AN为NH
3与NO
x的化学计量数之比;M
urea为尿素分子的摩尔质量;ω
mass为尿素水溶液的质量分数;M
mass为排气的摩尔质量;Q
mass为排气的质量流量;C
NOx为排气中NO
x的体积分数。已知在空转15000h
-1下,排出气体的平均摩尔质量约为32g/mol,其中NO的体积分数约为0.2%,排气的质量流量约为9.2g·s
-1,按题意选择优化条件,以反应Ⅳ为例计算理论喷射尿素水溶液的质量流量为
__(保留三位有效数字)g·s
-1。