24. 现用盐酸标准溶液来测定NaOH溶液的浓度。实验操作如下:
①向溶液中加入2~3滴指示剂,②取20.00 mL标准溶液放入锥形瓶中,③用氢氧化钠溶液滴定至终点,④重复以上操作,⑤配制250 mL盐酸标准溶液,⑥根据实验数据计算氢氧化钠溶液的物质的量浓度。
(1)实验过程中正确的操作顺序是
_______(填序号),用
_______作指示剂;滴定终点的现象是什么
_______。
(2)滴定并记录V(NaOH)的初、终读数。数据记录如表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| V(HCl)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH) /mL(初读数) | 0.10 | 0.30 | 0.00 | 0.20 |
| V(NaOH) /mL (终读数) | 20.08 | 20.30 | 20.80 | 20.22 |
| V(NaOH) /mL (消耗) | 19.98 | 20.00 | 20.80 | 20.02 |
某同学在处理数据过程中计算得到平均消耗NaOH溶液的体积为
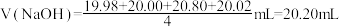
,他的计算结果
_______(填“合理”或“不合理”),理由是
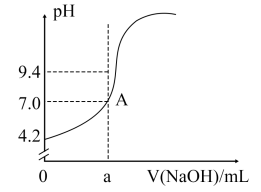
_______。通过仪器测得第4次滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如图所示,则a
_______(填“>”“<”或“=”)20.02。