安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
安徽
高三
阶段练习
2022-10-26
236次
整体难度:
容易
考查范围:
化学与STSE、初中衔接知识点、认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础
安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
安徽
高三
阶段练习
2022-10-26
236次
整体难度:
容易
考查范围:
化学与STSE、初中衔接知识点、认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础
一、单选题 添加题型下试题
单选题
|
较易(0.85)
名校
解题方法
1. 葛洪《抱朴子》云:扶南出金刚(金刚石),生水底石上,如钟乳状,体似紫石英,可以刻玉,人没水取之,虽铁椎击之亦不能伤。下列说法不正确的是
| A.金刚石的硬度大,可以雕刻玉石 | B.金刚石在空气中可以燃烧 |
| C.金刚石是一种特殊的金属材料 | D.石墨在一定条件下可以转化成金刚石 |
【知识点】 化学科学对人类文明发展的意义解读 身边的化学物质
您最近一年使用:0次
2022-10-14更新
|
135次组卷
|
3卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
单选题
|
适中(0.65)
解题方法
2. 常温下,下列各组离子在指定溶液中一定能大量共存的是
A. 的 的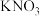 溶液: 溶液: 、 、 、 、 、 、 |
B.能溶解 的溶液: 的溶液: 、 、 、 、 、 、 |
C.无色透明溶液中: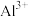 、 、 、 、 、 、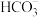 |
D.使甲基橙变红色的溶液: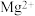 、 、 、 、 、 、 |
【知识点】 限定条件下的离子共存解读 盐类双水解反应解读
您最近一年使用:0次
2022-10-14更新
|
185次组卷
|
2卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
单选题
|
较易(0.85)
名校
解题方法
3. 下列有关钠、铝、铁单质及其化合物的性质的说法中正确的是
| A.钠表面自然形成的氧化层能够保护内层金属不被空气氧化 |
B.可用氢氧化钙溶液鉴别 溶液和 溶液和 溶液 溶液 |
C. 、 、 、 、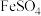 均能通过化合反应制得 均能通过化合反应制得 |
D.Al、 、 、 、 、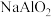 均能与NaOH溶液发生反应 均能与NaOH溶液发生反应 |
您最近一年使用:0次
2022-10-14更新
|
184次组卷
|
3卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
单选题
|
较易(0.85)
解题方法
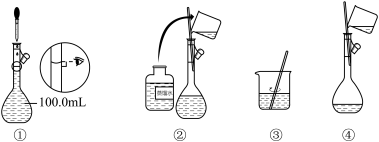
4. 如图是配制100mL
 溶液过程示意图中的几步。其中正确的先后顺序是
溶液过程示意图中的几步。其中正确的先后顺序是

 溶液过程示意图中的几步。其中正确的先后顺序是
溶液过程示意图中的几步。其中正确的先后顺序是
| A.①②③④ | B.③②④① | C.③④②① | D.④③②① |
【知识点】 配制一定物质的量浓度的溶液的步骤、操作解读
您最近一年使用:0次
2022-10-14更新
|
141次组卷
|
3卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题安徽省六安市舒城育才学校2022-2023学年高三上学期12月月考化学试题(已下线)实验01 配制一定物质的量浓度的溶液-【同步实验课】2023-2024学年高一化学教材实验大盘点(人教版2019必修第一册)
单选题
|
较易(0.85)
解题方法
5. 下列有关物质的性质与应用的对应关系正确的是
| A.NaClO具有氧化性,可用于杀灭新型冠状病毒 |
B. 水解显酸性,可用作铜制线路板的蚀刻剂 水解显酸性,可用作铜制线路板的蚀刻剂 |
C. 具有漂白性,常用 具有漂白性,常用 的水溶液作 的水溶液作 蒸气的吸收剂 蒸气的吸收剂 |
D. 具有氧化性,可用于与酸性 具有氧化性,可用于与酸性 溶液反应制取 溶液反应制取 |
您最近一年使用:0次
2022-10-14更新
|
121次组卷
|
3卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题安徽省六安市舒城育才学校2022-2023学年高三上学期12月月考化学试题(已下线)山东省济南市2022届高三3月高考模拟考试(一模)(选择题1-5)
单选题
|
适中(0.65)
名校
解题方法
6. 海洋碳循环在整个地球气候系统中具有重要地位。下列叙述错误的是
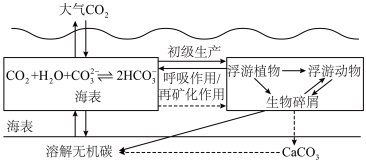

| A.塑料颗粒中含有的碳也会进入海洋碳循环缓慢降解,不会造成污染 |
B.大气中 浓度上升导致海洋酸化,海洋吸收 浓度上升导致海洋酸化,海洋吸收 的能力减弱 的能力减弱 |
C.温室效应导致的海表温度上升,会减少海洋对 的吸收 的吸收 |
D.该循环涉及反应 |
您最近一年使用:0次
2022-10-14更新
|
146次组卷
|
2卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
单选题
|
适中(0.65)
名校
解题方法
7. 氮是各种生物体生命活动中不可缺少的重要元素。自然界中的氮循环为生物体提供了氮元素。下列有关氮元素说法不正确的是
| A.铵态氮肥被植物吸收的过程属于氮的固定 |
B.雷雨发庄稼的起因是打雷时空气中 与 与 化合成NO 化合成NO |
| C.城市空气中的氮氧化物主要来源是燃油汽车产生的尾气 |
D.工业利用 和 和 合成 合成 ,其中 ,其中 的来源是空气 的来源是空气 |
您最近一年使用:0次
2022-10-14更新
|
185次组卷
|
4卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
单选题
|
适中(0.65)
8. 用 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是
 表示阿伏加德罗常数的值。下列说法正确的是
表示阿伏加德罗常数的值。下列说法正确的是A. 的 的 溶液中 溶液中 的数目为0.1 的数目为0.1 |
B.标准状况下,11.2L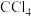 所含氯原子数目为2 所含氯原子数目为2 |
C.2.8g 中含共用电子对的数目为0.6 中含共用电子对的数目为0.6 |
D.0.1molFe与硝酸反应失去的电子数一定为0.3 |
您最近一年使用:0次
2022-10-14更新
|
78次组卷
|
2卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
单选题
|
适中(0.65)
您最近一年使用:0次
2022-10-14更新
|
121次组卷
|
2卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
单选题
|
容易(0.94)
解题方法
10. 实验室中采用如图所示装置(夹持仪器已省略)制备气体,合理的是
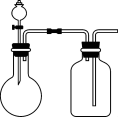
| 选项 | 化学药品 | 制备的气体 |
| A | 浓氨水+熟石灰 |  |
| B | 稀硝酸+铜片 | NO |
| C | 稀硫酸+锌粒 |  |
| D | 浓硫酸+亚硫酸钠 |  |
| A.A | B.B | C.C | D.D |
【知识点】 氨气的实验室制法解读 常见气体的制备与收集解读
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
11. 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向某溶液中滴加 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 溶液中一定含 |
| B | 向 溶液中滴加稀硫酸酸化,再滴加 溶液中滴加稀硫酸酸化,再滴加 溶液,溶液变成血红色 溶液,溶液变成血红色 |  溶液已变质 溶液已变质 |
| C | 向 溶液中逐滴加入少量稀盐酸,无现象 溶液中逐滴加入少量稀盐酸,无现象 | 酸性: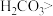 盐酸 盐酸 |
| D | 在足量 溶液中滴入几滴 溶液中滴入几滴 溶液有白色沉淀生成,再滴入 溶液有白色沉淀生成,再滴入 溶液,沉淀变为黑色 溶液,沉淀变为黑色 | 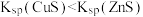 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-08-22更新
|
315次组卷
|
6卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
容易(0.94)
名校
解题方法
12. 某溶液中含有 、
、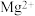 、
、 、
、 、
、 中的几种,向溶液中滴加
中的几种,向溶液中滴加 溶液有白色沉淀生成,过滤、洗涤,再将沉淀加入到足量稀盐酸中,沉淀部分溶解且有气泡产生,下列判断错误的是
溶液有白色沉淀生成,过滤、洗涤,再将沉淀加入到足量稀盐酸中,沉淀部分溶解且有气泡产生,下列判断错误的是
 、
、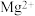 、
、 、
、 、
、 中的几种,向溶液中滴加
中的几种,向溶液中滴加 溶液有白色沉淀生成,过滤、洗涤,再将沉淀加入到足量稀盐酸中,沉淀部分溶解且有气泡产生,下列判断错误的是
溶液有白色沉淀生成,过滤、洗涤,再将沉淀加入到足量稀盐酸中,沉淀部分溶解且有气泡产生,下列判断错误的是A.不能确定是否含有 | B.一定不存在的离子有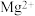 |
C.是否含有 需通过焰色反应确定 需通过焰色反应确定 | D.一定存在的离子有 、 、 、 、 |
【知识点】 离子反应在化合物组成的分析、鉴定的应用解读
您最近一年使用:0次
2022-10-14更新
|
209次组卷
|
3卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
单选题
|
适中(0.65)
解题方法
13. 常温下,氯化铁为棕黑色固体,易升华。实验室欲证明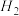 能在加热的条件下还原
能在加热的条件下还原 ,设计了如下实验。
,设计了如下实验。
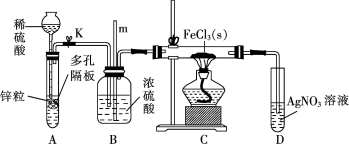
下列说法错误的是
 能在加热的条件下还原
能在加热的条件下还原 ,设计了如下实验。
,设计了如下实验。
下列说法错误的是
| A.装置A中发生的反应为置换反应 |
B.装置D中产生白色沉淀,可证明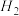 能还原 能还原 |
| C.实验结束后,应先熄灭酒精灯,待硬质玻璃管冷却后再关闭K |
| D.导管m的作用是平衡压强,可观察装置C中导管口是否堵塞 |
【知识点】 铁盐 化学实验方案的设计与评价 化学实验
您最近一年使用:0次
2022-10-14更新
|
234次组卷
|
2卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
单选题
|
较易(0.85)
名校
解题方法
14. 据统计,城市机动车辆每年以15%至20%的速度增长,汽车在剧烈碰撞时,安全气囊中发生反应: 。下列判断正确的是
。下列判断正确的是
 。下列判断正确的是
。下列判断正确的是| A.还原剂与氧化产物的物质的量之比为3:2 |
B. 是只含有离子键的离子化合物 是只含有离子键的离子化合物 |
C.当转移1mol电子时,可以得到35.84L |
D.每生成3.2mol ,则有0.4mol ,则有0.4mol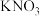 被还原 被还原 |
【知识点】 氧化还原反应的几组概念解读 电子转移计算
您最近一年使用:0次
2022-10-14更新
|
165次组卷
|
3卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
解题方法
15. 某实验小组设计如下实验装置(夹持仪器已省略)制备干燥的 ,并在碱性条件下制备
,并在碱性条件下制备 (反应原理:
(反应原理: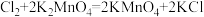 ,
, 溶液为绿色)。回答下列问题:
溶液为绿色)。回答下列问题:
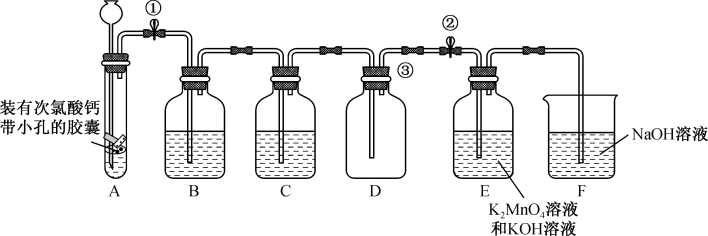
(1)设计次氯酸钙装入带有小孔的胶囊的目的是_______ 。
(2)B、C中盛放的试剂分别为_______ 、_______ (填名称)。
(3)实验时,首先组装装置,然后_______ ,再将各装置中加入相应的试剂后,将浓盐酸从_______ (填仪器名称)加入试管中,写出试管中反应的化学方程式:_______ 。
(4)装置E中反应已完成的现象是_______ 。
(5)装置F的作用是_______ (用离子方程式表示)。
(6)从装置E的溶液中获取 固体的方法是蒸发浓缩、
固体的方法是蒸发浓缩、_______ 、过滤、洗涤干燥。
(7)采用紫外一可见分光光度法测试高锰酸钾样品的纯度。准确称取0.70g高锰酸钾样品配制1000mL 溶液,进行吸光度测试。在525nm处的吸光度A与高锰酸钾溶液浓度之间关系如下表所示。已知高锰酸钾吸光度的标准曲线方程为
溶液,进行吸光度测试。在525nm处的吸光度A与高锰酸钾溶液浓度之间关系如下表所示。已知高锰酸钾吸光度的标准曲线方程为 (式中A为吸光度,C为高锰酸钾浓度,单位为
(式中A为吸光度,C为高锰酸钾浓度,单位为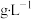 ,a、b为常数)。
,a、b为常数)。
根据上表相关数据可计算出高锰酸钾样品的纯度为_______ %(保留三位有效数字)。
 ,并在碱性条件下制备
,并在碱性条件下制备 (反应原理:
(反应原理: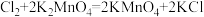 ,
, 溶液为绿色)。回答下列问题:
溶液为绿色)。回答下列问题:
(1)设计次氯酸钙装入带有小孔的胶囊的目的是
(2)B、C中盛放的试剂分别为
(3)实验时,首先组装装置,然后
(4)装置E中反应已完成的现象是
(5)装置F的作用是
(6)从装置E的溶液中获取
 固体的方法是蒸发浓缩、
固体的方法是蒸发浓缩、(7)采用紫外一可见分光光度法测试高锰酸钾样品的纯度。准确称取0.70g高锰酸钾样品配制1000mL
 溶液,进行吸光度测试。在525nm处的吸光度A与高锰酸钾溶液浓度之间关系如下表所示。已知高锰酸钾吸光度的标准曲线方程为
溶液,进行吸光度测试。在525nm处的吸光度A与高锰酸钾溶液浓度之间关系如下表所示。已知高锰酸钾吸光度的标准曲线方程为 (式中A为吸光度,C为高锰酸钾浓度,单位为
(式中A为吸光度,C为高锰酸钾浓度,单位为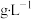 ,a、b为常数)。
,a、b为常数)。 | 0.50 | 0.70 | 待测溶液 |
| A(吸光度) | 0.30 | 0.40 | 0.39 |
您最近一年使用:0次
解答题-工业流程题
|
较难(0.4)
名校
16. 高纯氮化铝( )是一种理想的半导体物质。一种以含铝废料(主要成分为
)是一种理想的半导体物质。一种以含铝废料(主要成分为 ,含有少量
,含有少量 、
、 、
、 、
、 )为原料制备
)为原料制备 的工艺流程如下:
的工艺流程如下:
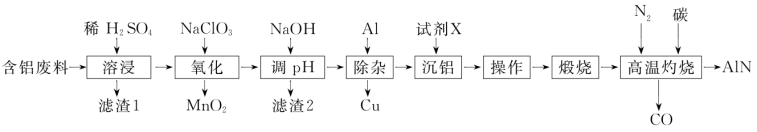
回答下列问题:
(1)“溶浸”过程中发生的基本反应类型为___________ ,滤渣1的主要成分是___________ (填化学式)。
(2)写出“氧化”时生成 的离子方程式:
的离子方程式:___________ 。
(3)常温下,“氧化”后溶液中 ,若“调
,若“调 ”,是否有
”,是否有 沉淀生成?
沉淀生成?___________ {写出计算过程,已知常温下, }。
}。
(4)“沉铝”时,加入试剂X的名称是___________ 。
(5)“操作”步骤包含___________ 。
(6)写出“高温灼烧”时反应的化学方程式:___________ ;该步骤反应后期需通入一定量的空气,其目的是___________ (从提高 纯度角度考虑)。
纯度角度考虑)。
 )是一种理想的半导体物质。一种以含铝废料(主要成分为
)是一种理想的半导体物质。一种以含铝废料(主要成分为 ,含有少量
,含有少量 、
、 、
、 、
、 )为原料制备
)为原料制备 的工艺流程如下:
的工艺流程如下:
回答下列问题:
(1)“溶浸”过程中发生的基本反应类型为
(2)写出“氧化”时生成
 的离子方程式:
的离子方程式:(3)常温下,“氧化”后溶液中
 ,若“调
,若“调 ”,是否有
”,是否有 沉淀生成?
沉淀生成? }。
}。(4)“沉铝”时,加入试剂X的名称是
(5)“操作”步骤包含
(6)写出“高温灼烧”时反应的化学方程式:
 纯度角度考虑)。
纯度角度考虑)。
您最近一年使用:0次
2021-12-31更新
|
654次组卷
|
3卷引用:八省八校(T8联考)2021-2022学年高三上学期第一次联考化学试题(石家庄二中)
解答题-实验探究题
|
适中(0.65)
解题方法
17.  化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究
化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究 与
与 的反应机理,实验步骤如下:
的反应机理,实验步骤如下:
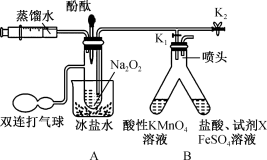
i.打开 、
、 ,通过注射器注入适量蒸馏水,使固体全部溶解;
,通过注射器注入适量蒸馏水,使固体全部溶解;
ii.将部分液体转移至B中;
iii.向A中剩余的溶液中滴加几滴酚酞试液。
回答下列问题:
(1)“步骤ii”B中左侧溶液褪色且有气泡产生,右侧溶液变为红色。
①将部分液体转移至B中的具体操作为_______ 。
②试剂X是_______ (填化学式)溶液,右侧与“溶液变红”有关反应的离子方程式为_______ 、 。
。
③左侧 参与反应的离子方程式为
参与反应的离子方程式为_______ ;②、③涉及的氧化还原反应中,若消耗等物质的量的还原剂,则理论上消耗氧化剂的物质的量之比为_______ 。
(2)若向“步骤iii”A中剩余的溶液中加入 时,有大量气泡产生。
时,有大量气泡产生。
① 在该反应中的作用为
在该反应中的作用为_______ 。
②“步骤iii”的现象为_______ , 与
与 反应的机理是
反应的机理是_______ (用化学方程式表示,第一步)。
(3)向包裹着适量 的脱脂棉(放在石棉网上)上滴加3~4滴水,结果脱脂棉剧烈燃烧。由此可得出与该反应相关的结论是
的脱脂棉(放在石棉网上)上滴加3~4滴水,结果脱脂棉剧烈燃烧。由此可得出与该反应相关的结论是_______ 。
 化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究
化学性质活泼,能与许多物质反应。某实验小组利用下列装置(夹持装置已省略)探究 与
与 的反应机理,实验步骤如下:
的反应机理,实验步骤如下:
i.打开
 、
、 ,通过注射器注入适量蒸馏水,使固体全部溶解;
,通过注射器注入适量蒸馏水,使固体全部溶解;ii.将部分液体转移至B中;
iii.向A中剩余的溶液中滴加几滴酚酞试液。
回答下列问题:
(1)“步骤ii”B中左侧溶液褪色且有气泡产生,右侧溶液变为红色。
①将部分液体转移至B中的具体操作为
②试剂X是
 。
。③左侧
 参与反应的离子方程式为
参与反应的离子方程式为(2)若向“步骤iii”A中剩余的溶液中加入
 时,有大量气泡产生。
时,有大量气泡产生。①
 在该反应中的作用为
在该反应中的作用为②“步骤iii”的现象为
 与
与 反应的机理是
反应的机理是(3)向包裹着适量
 的脱脂棉(放在石棉网上)上滴加3~4滴水,结果脱脂棉剧烈燃烧。由此可得出与该反应相关的结论是
的脱脂棉(放在石棉网上)上滴加3~4滴水,结果脱脂棉剧烈燃烧。由此可得出与该反应相关的结论是
您最近一年使用:0次
2022-10-14更新
|
198次组卷
|
3卷引用:安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
三、填空题 添加题型下试题
填空题
|
适中(0.65)
18. 中学化学教材中涉及许多金属和非金属元素,掌握它们的单质及其化合物的性质是学好化学的基础。回答下列问题:
(1) 的结构式为
的结构式为___________ ,过氧化钠的电子式为___________ 。
(2)黄磷(P4)与过量浓NaOH溶液反应,产生PH3和次磷酸钠( ),该反应的化学方程式为
),该反应的化学方程式为___________ ,其中还原剂和氧化剂的质量比为___________ ;根据题意可判断 是
是___________ 元酸(填“一”“二”或“三”)。
(3)向含有1mol 和1mol
和1mol 的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。
的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。

①写出生成a的离子方程式:___________ 。
②n1=___________ 。
③向P点溶液中加入铜粉,反应的离子方程式为___________ ,最多可溶解铜粉___________ g。
(1)
 的结构式为
的结构式为(2)黄磷(P4)与过量浓NaOH溶液反应,产生PH3和次磷酸钠(
 ),该反应的化学方程式为
),该反应的化学方程式为 是
是(3)向含有1mol
 和1mol
和1mol 的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。
的混合溶液中逐渐加入铁粉至过量,溶液中金属阳离子a、b与所加铁粉的物质的量的关系如图所示(已知稀硝酸的还原产物只有NO)。
①写出生成a的离子方程式:
②n1=
③向P点溶液中加入铜粉,反应的离子方程式为
您最近一年使用:0次
2021-12-07更新
|
241次组卷
|
3卷引用:湖北省部分学校2021-2022学年高三上学期11月质量检测化学试题
湖北省部分学校2021-2022学年高三上学期11月质量检测化学试题(已下线)第14练 化学键-2022年【寒假分层作业】高一化学(人教版2019)安徽省皖优联盟2023届高三上学期第一次阶段测试化学试题
试卷分析
整体难度:适中
考查范围:化学与STSE、初中衔接知识点、认识化学科学、化学反应原理、常见无机物及其应用、化学实验基础
试卷题型(共 18题)
题型
数量
单选题
14
解答题
3
填空题
1
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.85 | 化学科学对人类文明发展的意义 身边的化学物质 | |
| 2 | 0.65 | 限定条件下的离子共存 盐类双水解反应 | |
| 3 | 0.85 | 钠的化学性质 碳酸钠与碳酸氢钠性质的比较 氢氧化铝与强碱反应 氢氧化亚铁 | |
| 4 | 0.85 | 配制一定物质的量浓度的溶液的步骤、操作 | |
| 5 | 0.85 | 氧化还原反应基本概念 次氯酸及其性质 二氧化硫与其他强氧化剂的反应 盐类水解规律理解及应用 | |
| 6 | 0.65 | 化学科学对人类文明发展的意义 “白色污染”危害及防治 绿色化学与可持续发展 | |
| 7 | 0.65 | 自然界氮的固定 硫、氮氧化物对人体、环境的危害 酸雨 人工固氮——合成氨 | |
| 8 | 0.65 | 阿伏加德罗常数的求算 22.4L/mol适用条件 结合物质结构基础知识与NA相关推算 硝酸的强氧化性 | |
| 9 | 0.65 | 酸性氧化物通性 二氧化硅的化学性质 氧化铝与碱溶液反应 常见金属的冶炼 | |
| 10 | 0.94 | 氨气的实验室制法 常见气体的制备与收集 | |
| 11 | 0.65 | 铁盐的检验 沉淀转化 常见阴离子的检验 物质性质实验方案的设计 | |
| 12 | 0.94 | 离子反应在化合物组成的分析、鉴定的应用 | |
| 13 | 0.65 | 铁盐 化学实验方案的设计与评价 化学实验 | |
| 14 | 0.85 | 氧化还原反应的几组概念 电子转移计算 | |
| 二、解答题 | |||
| 15 | 0.65 | 氯气的实验室制法 物质分离、提纯综合应用 物质含量的测定 物质制备的探究 | 实验探究题 |
| 16 | 0.4 | 氧化还原反应方程式的配平 铝三角转化 溶度积常数相关计算 物质分离、提纯综合应用 | 工业流程题 |
| 17 | 0.65 | 氧化还原反应方程式的配平 过氧化钠与水的反应 铁盐的检验 物质性质的探究 | 实验探究题 |
| 三、填空题 | |||
| 18 | 0.65 | 共价型分子结构式、电子式 硝酸的强氧化性 铁盐 探究物质组成或测量物质的含量 | |







