安徽省2023届高三第一次教学质量检测联考化学试题
安徽
高三
开学考试
2022-08-27
375次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、有机化学基础、物质结构与性质、常见无机物及其应用、化学实验基础、化学反应原理
安徽省2023届高三第一次教学质量检测联考化学试题
安徽
高三
开学考试
2022-08-27
375次
整体难度:
适中
考查范围:
认识化学科学、化学与STSE、有机化学基础、物质结构与性质、常见无机物及其应用、化学实验基础、化学反应原理
一、单选题 添加题型下试题
单选题
|
适中(0.65)
名校
解题方法
1. 化学与生活、环境密切相关。下列说法正确的是
A. 跨临界制冰技术的过程发生了化学变化 跨临界制冰技术的过程发生了化学变化 |
| B.纳米纤维素气凝胶具有吸附性 |
| C.将煤炭转化为甲醇再燃烧,可实现“碳中和” |
| D.聚乙烯和聚氯乙烯均是热固性塑料 |
您最近一年使用:0次
2022-08-22更新
|
210次组卷
|
3卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
适中(0.65)
名校
2. 图中实验基本操作正确的是
| A | B | C | D |
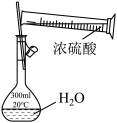 | 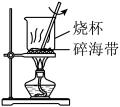 | 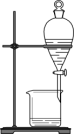 |  |
| 配制溶液 | 灼烧海带 | 分离溴和苯 | 检查气密性 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-08-22更新
|
173次组卷
|
3卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
适中(0.65)
3. 三甲基镓 是应用最广泛的一种金属有机化合物,可通过如下反应制备:
是应用最广泛的一种金属有机化合物,可通过如下反应制备: 。下列说法错误的是
。下列说法错误的是
 是应用最广泛的一种金属有机化合物,可通过如下反应制备:
是应用最广泛的一种金属有机化合物,可通过如下反应制备: 。下列说法错误的是
。下列说法错误的是A.金属性: | B.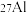 原子的中子数为14 原子的中子数为14 |
C. 结构示意图 结构示意图 | D. 位于周期表中第四周期Ⅲ A族 位于周期表中第四周期Ⅲ A族 |
您最近一年使用:0次
单选题
|
适中(0.65)
4. 设 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是
 为阿伏加德罗常数的值。下列说法正确的是
为阿伏加德罗常数的值。下列说法正确的是A.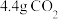 中氧原子数目为 中氧原子数目为 |
B.标准状况下,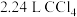 中 中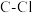 键数目为 键数目为 |
C.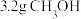 中 中 的数目为 的数目为 |
D.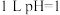 的 的 溶液中 溶液中 数目为 数目为 |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
6. 没食子酸是一种有机酸,可用作显影剂,其结构简式如图所示。下列有关说法错误的是
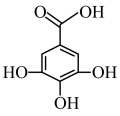

A.能与 溶液发生显色反应 溶液发生显色反应 |
| B.能发生酯化反应、氧化反应 |
| C.苯环上一氯代物有两种(不含立体异构) |
D.等质量的没食子酸分别与 和 和 反应,最多消耗两者的物质的量之比为 反应,最多消耗两者的物质的量之比为 |
您最近一年使用:0次
2022-08-22更新
|
134次组卷
|
2卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
较易(0.85)
名校
解题方法
7. 下列过程涉及氧化还原反应的是
A.用 制备纳米级 制备纳米级 |
| B.以氨气、二氧化碳和饱和食盐水制备小苏打 |
C.高铁酸钾 用作新型水处理剂 用作新型水处理剂 |
D.用 溶液除去铜制品表面的铜绿 溶液除去铜制品表面的铜绿 |
【知识点】 氧化还原反应基本概念 氧化还原反应定义、本质及特征解读
您最近一年使用:0次
2022-08-22更新
|
174次组卷
|
5卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
较易(0.85)
名校
8. 短周期主族元素X、Y、Z、M原子序数依次增大,Z是空气中含量最高的元素,M的最高正价与最低负价绝对值之差为4,它们组成的一种分子结构如图所示。下列说法正确的是
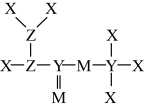
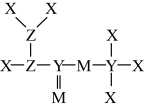
A.最高价氧化物对应水化物的酸性: |
B.原子半径: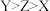 |
| C.分子中Y原子只形成非极性键 |
| D.Y、Z、M的氧化物均为酸性氧化物 |
您最近一年使用:0次
2022-08-22更新
|
181次组卷
|
4卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
适中(0.65)
名校
解题方法
9. 以某钢铁厂烟灰(主要成分为 ,并含少量的
,并含少量的 、
、 、
、 等)为原料制备氧化锌的工艺流程如图:
等)为原料制备氧化锌的工艺流程如图:
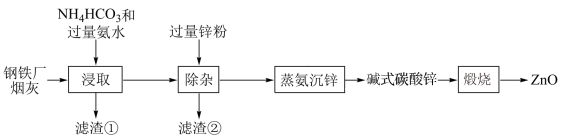
已知:“浸取”后的溶液中阳离子主要是 、
、 。下列说法错误的是
。下列说法错误的是
 ,并含少量的
,并含少量的 、
、 、
、 等)为原料制备氧化锌的工艺流程如图:
等)为原料制备氧化锌的工艺流程如图:
已知:“浸取”后的溶液中阳离子主要是
 、
、 。下列说法错误的是
。下列说法错误的是A.“浸取”时,可以用过量 代替氨水 代替氨水 |
| B.滤渣①为红黑色固体 |
| C.滤渣②中,至少有两种物质 |
D.“煅烧”时,每生成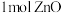 ,转移 ,转移 电子 电子 |
您最近一年使用:0次
2022-08-22更新
|
215次组卷
|
4卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
安徽省2023届高三第一次教学质量检测联考化学试题福建省龙岩第一中学2022-2023学年高三上学期第二次月考化学试题(已下线)2022年福建省高考真题变式题(选择题6-10)河南省焦作市博爱县第一中学2022-2023学年高二下学期4月月考化学试题
单选题
|
适中(0.65)
名校
10. 下列涉及含氯物质反应的离子方程式正确的是
A.向次氯酸钠溶液中通入过量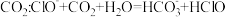 |
B.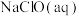 中通入少量 中通入少量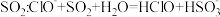 |
C.氯气通入水中: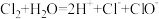 |
D.电解 水溶液: 水溶液: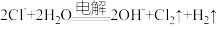 |
您最近一年使用:0次
2022-08-22更新
|
424次组卷
|
5卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
安徽省2023届高三第一次教学质量检测联考化学试题福建省龙岩第一中学2022-2023学年高三上学期第二次月考化学试题(已下线)易错点09 氯元素及其化合物-备战2023年高考化学考试易错题河南省焦作市博爱县第一中学2022-2023学年高二下学期4月月考化学试题辽宁省朝阳市建平县2022-2023学年高三上学期11月期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
11. 在“碳中和”背景下,开发以CO2为原料,通过电化学方法,将其转化为CO利国利民。某科研团队设计的一种电化学装置如图所示,下列说法正确的是
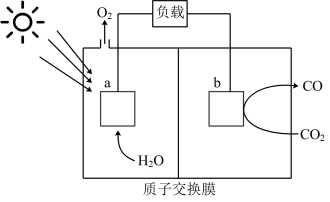

| A.该装置能量转化方式只有太阳能→化学能→电能 |
| B.该电池的总反应为CO2+H2O=CO+H2+O2 |
| C.电极b表面发生反应CO2+2e-+2H+=CO+H2O |
| D.标准状况下,电极a生成1.12 L O2时,两极电解质溶液质量相差1.6 g |
您最近一年使用:0次
2022-08-22更新
|
214次组卷
|
2卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
适中(0.65)
名校
解题方法
12. 用还原法可以将硝酸厂烟气中的大量氮氧化物 转化为无害物质。常温下,将NO与
转化为无害物质。常温下,将NO与 的混合气体通入
的混合气体通入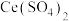 与
与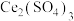 的混合溶液中,其物质的转化过程如图所示。下列说法错误的是
的混合溶液中,其物质的转化过程如图所示。下列说法错误的是

 转化为无害物质。常温下,将NO与
转化为无害物质。常温下,将NO与 的混合气体通入
的混合气体通入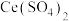 与
与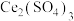 的混合溶液中,其物质的转化过程如图所示。下列说法错误的是
的混合溶液中,其物质的转化过程如图所示。下列说法错误的是
A.反应Ⅱ的离子方程式为 |
B.反应Ⅰ中氧化剂与还原剂的物质的量之比为 |
C. 为该转化过程的中间产物 为该转化过程的中间产物 |
D.反应前后溶液中 和 和 的总数保持不变 的总数保持不变 |
您最近一年使用:0次
2022-08-22更新
|
392次组卷
|
4卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
适中(0.65)
名校
13. 已知一定条件下,氢气与一氧化碳发生反应的热化学方程式为
 。向体积为2L的恒容容器中充入
。向体积为2L的恒容容器中充入 和
和 ,2h后,测得CO的转化率随温度变化关系如图。下列选项中正确的是
,2h后,测得CO的转化率随温度变化关系如图。下列选项中正确的是


 。向体积为2L的恒容容器中充入
。向体积为2L的恒容容器中充入 和
和 ,2h后,测得CO的转化率随温度变化关系如图。下列选项中正确的是
,2h后,测得CO的转化率随温度变化关系如图。下列选项中正确的是
A.正反应为吸热反应, |
| B.a、c两点对应条件下,反应进行的平均速率相等 |
| C.延长反应时间至3h,c点对应条件下CO的转化率升高 |
D.b点对应条件下,向容器中继续通入 、 、 和 和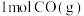 ,达到平衡状态后, ,达到平衡状态后, |
您最近一年使用:0次
2022-08-22更新
|
274次组卷
|
3卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
适中(0.65)
名校
解题方法
14. 根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向某溶液中滴加 溶液,有白色沉淀生成 溶液,有白色沉淀生成 | 溶液中一定含 |
| B | 向 溶液中滴加稀硫酸酸化,再滴加 溶液中滴加稀硫酸酸化,再滴加 溶液,溶液变成血红色 溶液,溶液变成血红色 |  溶液已变质 溶液已变质 |
| C | 向 溶液中逐滴加入少量稀盐酸,无现象 溶液中逐滴加入少量稀盐酸,无现象 | 酸性: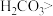 盐酸 盐酸 |
| D | 在足量 溶液中滴入几滴 溶液中滴入几滴 溶液有白色沉淀生成,再滴入 溶液有白色沉淀生成,再滴入 溶液,沉淀变为黑色 溶液,沉淀变为黑色 | 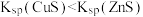 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2022-08-22更新
|
315次组卷
|
6卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
单选题
|
适中(0.65)
解题方法
15. 已知常温下,向20 mL0.1 mol/LHA溶液中滴入0.1 mol/L的NaOH溶液,所得滴定曲线如图所示,下列说法正确的是


| A.HA为一元弱酸,其电离平衡常数的数量级为10-5 |
B.b点各微粒物质的量浓度的关系是: |
C.c点存在关系式: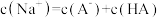 |
D.若d点溶液的pH=8.4,则水电离出的 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-工业流程题
|
较难(0.4)
名校
解题方法
16. 废催化剂(含WO3、Al2O3、MoO3、FeO)为原料制备(NH4)2WO4的工艺流程如图所示。

已知:①钠化焙烧后钨钼的存在形态为WO 和MoO
和MoO ;
;
②MoS 在化学反应中主要表现S2-的性质,受热易分解生成MoS3和S2-,其中MoS3易溶于热水和Na2S溶液中;
在化学反应中主要表现S2-的性质,受热易分解生成MoS3和S2-,其中MoS3易溶于热水和Na2S溶液中;
③pH=2~3时,WO 会聚合成(H2W12O40)6-。
会聚合成(H2W12O40)6-。
回答下列问题:
(1)“钠化焙烧”时WO3发生反应的化学方程式为____ 。
(2)浸出液的主要成分有NaAlO2、____ 、____ ;浸出渣的主要成分为____ 。
(3)将石灰乳加入钨酸钠碱性溶液中可得到钨酸钙,已知某温度时,Ksp(CaWO4)=1×10-10,Ksp[Ca(OH)2]=4×10-7,当溶液中WO 恰好沉淀完全(离子浓度等于10-5mol·L-1)时,溶液中c(OH-)=
恰好沉淀完全(离子浓度等于10-5mol·L-1)时,溶液中c(OH-)=____ 。
(4)如图为“硫化除钼”过程中,各物质的去除率与温度的关系。加入硫化剂NaHS溶液可将钼最终转化为MoS ,加入的除钼剂中含有Cu2+,其中Cu2+的作用是
,加入的除钼剂中含有Cu2+,其中Cu2+的作用是____ ;温度升高,除铝率升高而除钼率降低的原因是____ 。

(5)叔胺(R3N)萃取钨的过程中,胺与硫酸形成胺盐[(R3NH)2SO4]后才能萃取金属配合阴离子,反应方程式如下:5(R3NH)2SO4+2(H2W12O40)6-+2H+=2(R3NH)5H(H2W12O40)+5SO 。加入氨水进行反萃取时,发生的反应无化合价变化,其化学方程式为
。加入氨水进行反萃取时,发生的反应无化合价变化,其化学方程式为____ 。

已知:①钠化焙烧后钨钼的存在形态为WO
 和MoO
和MoO ;
;②MoS
 在化学反应中主要表现S2-的性质,受热易分解生成MoS3和S2-,其中MoS3易溶于热水和Na2S溶液中;
在化学反应中主要表现S2-的性质,受热易分解生成MoS3和S2-,其中MoS3易溶于热水和Na2S溶液中;③pH=2~3时,WO
 会聚合成(H2W12O40)6-。
会聚合成(H2W12O40)6-。回答下列问题:
(1)“钠化焙烧”时WO3发生反应的化学方程式为
(2)浸出液的主要成分有NaAlO2、
(3)将石灰乳加入钨酸钠碱性溶液中可得到钨酸钙,已知某温度时,Ksp(CaWO4)=1×10-10,Ksp[Ca(OH)2]=4×10-7,当溶液中WO
 恰好沉淀完全(离子浓度等于10-5mol·L-1)时,溶液中c(OH-)=
恰好沉淀完全(离子浓度等于10-5mol·L-1)时,溶液中c(OH-)=(4)如图为“硫化除钼”过程中,各物质的去除率与温度的关系。加入硫化剂NaHS溶液可将钼最终转化为MoS
 ,加入的除钼剂中含有Cu2+,其中Cu2+的作用是
,加入的除钼剂中含有Cu2+,其中Cu2+的作用是
(5)叔胺(R3N)萃取钨的过程中,胺与硫酸形成胺盐[(R3NH)2SO4]后才能萃取金属配合阴离子,反应方程式如下:5(R3NH)2SO4+2(H2W12O40)6-+2H+=2(R3NH)5H(H2W12O40)+5SO
 。加入氨水进行反萃取时,发生的反应无化合价变化,其化学方程式为
。加入氨水进行反萃取时,发生的反应无化合价变化,其化学方程式为
您最近一年使用:0次
2022-05-08更新
|
1222次组卷
|
3卷引用:黑龙江省绥化市普通高中2022届高三模拟联合考试理综化学试题
解答题-实验探究题
|
适中(0.65)
名校
17. 高纯 可用于钽电容器的制造,某同学设计实验制备高纯
可用于钽电容器的制造,某同学设计实验制备高纯 。实验步骤如下:
。实验步骤如下:
Ⅰ.配制 溶液;
溶液;
Ⅱ.称取适量废干电池中的粗 加入烧杯中,依次加入
加入烧杯中,依次加入 溶液、适量的水,微热,在不断搅拌下慢慢分批次加入
溶液、适量的水,微热,在不断搅拌下慢慢分批次加入 溶液;
溶液;
Ⅲ.过滤,得到含有 的溶液;
的溶液;
Ⅳ.滴入 溶液,产生大量黑色沉淀;
溶液,产生大量黑色沉淀;
Ⅴ.过滤、洗涤及干燥后得到高纯 。
。
回答下列问题:
(1)步骤Ⅰ由98%的浓硫酸配制 溶液,图中仪器中不需要的是
溶液,图中仪器中不需要的是_______ (填仪器名称)。

(2)步骤Ⅱ所使用仪器如图:

①仪器a中支管的作用为_______ ,仪器b的名称为_______ 。
②写出仪器b中发生反应生成 和
和 的化学方程式:
的化学方程式:_______ 。
(3)步骤Ⅳ发生反应的离子方程式为_______ ;电解硫酸锰溶液也可以制备 ,则电解时在
,则电解时在_______ 极生成 ,该电极反应式为
,该电极反应式为_______ 。
 可用于钽电容器的制造,某同学设计实验制备高纯
可用于钽电容器的制造,某同学设计实验制备高纯 。实验步骤如下:
。实验步骤如下:Ⅰ.配制
 溶液;
溶液;Ⅱ.称取适量废干电池中的粗
 加入烧杯中,依次加入
加入烧杯中,依次加入 溶液、适量的水,微热,在不断搅拌下慢慢分批次加入
溶液、适量的水,微热,在不断搅拌下慢慢分批次加入 溶液;
溶液;Ⅲ.过滤,得到含有
 的溶液;
的溶液;Ⅳ.滴入
 溶液,产生大量黑色沉淀;
溶液,产生大量黑色沉淀;Ⅴ.过滤、洗涤及干燥后得到高纯
 。
。回答下列问题:
(1)步骤Ⅰ由98%的浓硫酸配制
 溶液,图中仪器中不需要的是
溶液,图中仪器中不需要的是
(2)步骤Ⅱ所使用仪器如图:

①仪器a中支管的作用为
②写出仪器b中发生反应生成
 和
和 的化学方程式:
的化学方程式:(3)步骤Ⅳ发生反应的离子方程式为
 ,则电解时在
,则电解时在 ,该电极反应式为
,该电极反应式为【知识点】 配制一定物质的量浓度的溶液实验的仪器解读 物质含量的测定
您最近一年使用:0次
2022-08-22更新
|
174次组卷
|
4卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
解答题-有机推断题
|
适中(0.65)
解题方法
18. 以有机物A为原料合成K的路线如图:
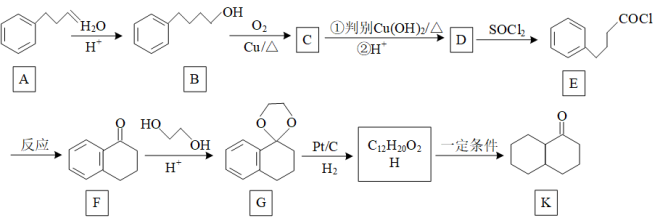
已知: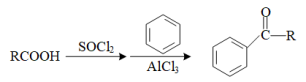 ,R为烃基。
,R为烃基。
回答下列问题:
(1)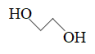 的化学名称是
的化学名称是_______
(2)H的结构简式为_______ ;其分子中的官能团名称为_______
(3)写出由C生成D第①步反应的化学方程式:_______ 。
(4)A→B、D→E的反应类型分别为_______ 、_______ 。
(5)上述路线设计F→G的目的是_______ 。
(6)同时满足下列条件的F的同分异构体有_______ 种(不含立体异构),其中核磁共振氢谱显示有五组氢(氢原子数量比为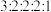 )的结构简式为
)的结构简式为_______ (写出一种即可)。
a.含有一个苯环且苯环上有两个取代基;
b.能与 溶液发生显色反应;
溶液发生显色反应;
c.分子中含有碳碳三键。

已知:
 ,R为烃基。
,R为烃基。回答下列问题:
(1)
 的化学名称是
的化学名称是(2)H的结构简式为
(3)写出由C生成D第①步反应的化学方程式:
(4)A→B、D→E的反应类型分别为
(5)上述路线设计F→G的目的是
(6)同时满足下列条件的F的同分异构体有
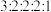 )的结构简式为
)的结构简式为a.含有一个苯环且苯环上有两个取代基;
b.能与
 溶液发生显色反应;
溶液发生显色反应;c.分子中含有碳碳三键。
您最近一年使用:0次
2022-08-22更新
|
164次组卷
|
2卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
解答题-原理综合题
|
适中(0.65)
名校
解题方法
19. 工业上,一氧化碳是一碳化学的基础,可由焦炭氧气法等方法制得,主要用于生产二甲醚、甲醇和光气等。回答下列问题:
(1)在工业上可用CO和 合成二甲醚
合成二甲醚 ,反应的化学方程式为
,反应的化学方程式为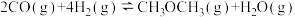
 。下列能说明该反应已达平衡状态的是_______(填字母)。
。下列能说明该反应已达平衡状态的是_______(填字母)。
(2)已知:Ⅰ.
 ;
;
Ⅱ.
 ;
;
①反应 的
的
_______ (用含 、
、 的代数式表示)。
的代数式表示)。
②已知 ,对于反应Ⅰ,图象正确的是
,对于反应Ⅰ,图象正确的是_______ (填字母)。
A. B.
B. C.
C. D.
D.
③为了探究反应条件对反应Ⅱ的影响,某活动小组设计了三个实验,实验曲线如图所示。

请依据实验曲线图补充完整表格中的实验条件:X=_______ ,Y=_______ ;对比实验Ⅱ和实验Ⅲ可知,升高温度,CO的转化率_______ (填“增大”“减小”或“不变”),
_______ (填“>”或“<”)0,理由是_______ 。编号Ⅰ实验中,反应达平衡时, 的转化率为50%,则530℃时该反应的平衡常数
的转化率为50%,则530℃时该反应的平衡常数
_______ (以分压表示,分压 总压
总压 物质的量分数)。
物质的量分数)。
(1)在工业上可用CO和
 合成二甲醚
合成二甲醚 ,反应的化学方程式为
,反应的化学方程式为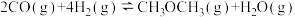
 。下列能说明该反应已达平衡状态的是_______(填字母)。
。下列能说明该反应已达平衡状态的是_______(填字母)。A.单位时间内生成 的同时消耗了 的同时消耗了 |
| B.在恒温恒容的容器中,混合气体的密度保持不变 |
| C.在绝热恒容的容器中,容器内的温度不再变化 |
| D.在恒温恒容的容器中,气体的平均摩尔质量不再变化 |

 ;
;Ⅱ.

 ;
;①反应
 的
的
 、
、 的代数式表示)。
的代数式表示)。②已知
 ,对于反应Ⅰ,图象正确的是
,对于反应Ⅰ,图象正确的是A.
 B.
B. C.
C. D.
D.
③为了探究反应条件对反应Ⅱ的影响,某活动小组设计了三个实验,实验曲线如图所示。
| 编号 | 温度 | 压强 | 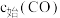 |  |
| Ⅰ | 530℃ |  |  |  |
| Ⅱ | X |  | Y |  |
| Ⅲ | 630℃ |  |  |  |

请依据实验曲线图补充完整表格中的实验条件:X=

 的转化率为50%,则530℃时该反应的平衡常数
的转化率为50%,则530℃时该反应的平衡常数
 总压
总压 物质的量分数)。
物质的量分数)。
【知识点】 化学反应原理综合考查解读
您最近一年使用:0次
2022-08-22更新
|
287次组卷
|
2卷引用:安徽省2023届高三第一次教学质量检测联考化学试题
试卷分析
整体难度:适中
考查范围:认识化学科学、化学与STSE、有机化学基础、物质结构与性质、常见无机物及其应用、化学实验基础、化学反应原理
试卷题型(共 19题)
题型
数量
单选题
15
解答题
4
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.65 | 物理变化与化学变化 塑料 低碳经济 煤的综合利用 | |
| 2 | 0.65 | 有机物分离提纯操作的综合考查 苯的物理性质及其在实验中的体现 苯的溴代实验探究 | |
| 3 | 0.65 | 原子结构示意图、离子结构示意图 共价型分子结构式、电子式 同主族元素性质递变规律 | |
| 4 | 0.65 | 22.4L/mol适用条件 结合物质结构基础知识与NA相关推算 乙醇的组成、结构 | |
| 5 | 0.65 | 硅酸钠的俗名和用途 蒸馏与分馏 萃取和分液 | |
| 6 | 0.65 | 有机官能团的性质及结构 同分异构体的数目的确定 含有酚羟基的物质性质的推断 羧酸酯化反应 | |
| 7 | 0.85 | 氧化还原反应基本概念 氧化还原反应定义、本质及特征 | |
| 8 | 0.85 | 元素金属性与非金属性递变规律的理解及应用 元素非金属性强弱的比较方法 微粒半径大小的比较方法 “位构性”关系理解及应用 | |
| 9 | 0.65 | 有关铁及其化合物转化的流程题型 物质分离、提纯综合应用 常见无机物的制备 | |
| 10 | 0.65 | 离子方程式的正误判断 次氯酸及其性质 氯气与水的反应 电解池电极反应式及化学方程式的书写与判断 | |
| 11 | 0.65 | 常见能量转化形式 原电池电极反应式书写 原电池有关计算 | |
| 12 | 0.65 | 离子方程式的书写 氧化还原反应的几组概念 与氧化剂、还原剂有关的计算 | |
| 13 | 0.65 | 温度对化学反应速率的影响 化学平衡的移动及其影响因素 化学平衡的有关计算 化学平衡图像分析 | |
| 14 | 0.65 | 铁盐的检验 沉淀转化 常见阴离子的检验 物质性质实验方案的设计 | |
| 15 | 0.65 | 水溶液中水的电离程度及的计算 酸碱混合时的定性判断及计算 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 16 | 0.4 | 离子方程式的书写 溶度积常数相关计算 物质分离、提纯综合应用 常见无机物的制备 | 工业流程题 |
| 17 | 0.65 | 配制一定物质的量浓度的溶液实验的仪器 物质含量的测定 | 实验探究题 |
| 18 | 0.65 | 常见官能团名称、组成及结构 同分异构体的数目的确定 有机物的推断 有机推断综合考查 | 有机推断题 |
| 19 | 0.65 | 化学反应原理综合考查 | 原理综合题 |

 溶液
溶液

