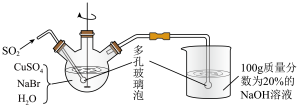
28. CuBr(溴化亚铜)是一种白色固体,不溶于水,在空气中会慢慢被氧化成绿色粉末,常用作催化剂,可用下图所示实验制得。
三颈烧瓶中的反应为 2Cu
2++SO
2+2Br
-+2H
2O=2CuBr↓+SO
42-+4H
+。
(1)实验所用蒸馏水需煮沸,目的是
_______________。装置中使用多孔玻璃泡的目的是
___________。
(2)将反应后得到的 CuBr 过滤并洗涤,检验 CuBr 是否洗净的方法是
______。
(3)烧杯中若 NaOH 的量不足,则烧杯中最终所得溶液中的溶质是
__________。
(4)CuBr 在空气中氧化所得绿色粉末为 xCuBr
2·yCu(OH)
2,为探究该粉末的化学式, 现进行如下实验:准确称取一定质量的绿色粉末,溶于足量乙酸中,用蒸馏水配制成 100 mL 溶液。
①取 25 mL 溶液,向其中加入足量的 AgNO
3 溶液,充分反应后过滤、洗涤、干燥, 所得淡黄色固体质量为 0.94 g。
②另取 25 mL 溶液,向其中加入过量的 KI 溶液,再用 0.400mol·L
-1Na
2S
2O
3 标准溶液滴定至终点,消耗 25.00 mL。已知反应过程中的方程式如下:2Cu
2++4I
﹣=2CuI↓+I
2、2S
2O
32-+I
2=2I
﹣+S
4O
62﹣。请确定该绿色粉末的化学式
_________(需要计算过程)。