22. 某同学利用如图装置模拟工业生产制备了少量硝酸,请结合所学知识完成下列问题。
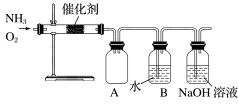
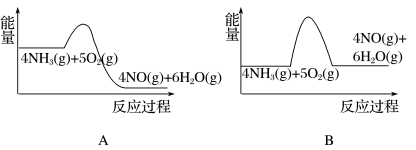
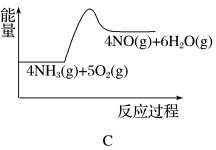
(1)实验时先用酒精喷灯加热催化剂,然后通入反应气体,当催化剂红热后撤离酒精喷灯,催化剂始终保持红热,温度可达到 700℃以上。下列图示中,能够正确表示该反应过程能量变化的是
_____(填字母)。
(2)高温时,2NO
2(g)
⇌ 2NO(g)+O
2(g),因此氨气与氧气反应难以生成 NO
2 。根据下列数据计算,当 4molNO
2 分解时,反应会
________________(填“吸收”或 “放出”)
_____________________kJ 能量。
NO
2(g)
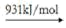
N(g)+2O(g)
NO(g)
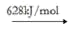
N(g)+O(g)
O
2(g)
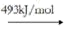
2O(g)
(3)在 2L 的恒温密闭容器中,通入等物质的量的 NO 和 O
2 气体,n(NO)随时间的变化如下表:
| t/s | 0 | 1 | 2 | 3 | 4 | 5 |
| n(NO)/mol | 0.020 | 0 014 | 0.010 | 0.007 | 0.006 | 0.006 |
①反应开始至第 1s 时,NO 的平均反应速率为
_____。
②在第 5s 时,O
2的转化率为
_____。
③容器中混合气体压强与反应开始时的压强比值为
_____。
④下列能说明反应已达平衡的是
_____。
a.单位时间内,每生成一定物质的量浓度的 NO,同时有相同物质的量浓度的O
2生成
b.气体混合物物质的量不再改变
c.气体混合物平均相对分子质量不再改变
d.容器内温度不再发生变化
e.密闭容器内气体颜色不再改变
f.混合气的密度不再改变