宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题
宁夏
高三
模拟预测
2020-06-06
447次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础
宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题
宁夏
高三
模拟预测
2020-06-06
447次
整体难度:
适中
考查范围:
有机化学基础、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础
一、单选题 添加题型下试题
单选题
|
容易(0.94)
解题方法
1. 运用化学知识对下列说法进行分析,不合理的是
| A.从健康的角度考虑臭氧比氯气更适合作自来水的消毒剂 |
| B.在“新冠肺炎战疫”发挥了重要作用的熔喷布口罩,其主要生产原料聚丙烯是混合物 |
| C.“一带一路”是现代丝绸之路。丝绸的主要成分是蛋白质,属于天然高分子化合物 |
| D.水墨山水画不易褪色的原因是墨汁中的炭黑具有吸附性 |
您最近一年使用:0次
2020-05-03更新
|
494次组卷
|
2卷引用:河南省顶尖名校2020届高三4月联考理科综合化学
单选题
|
适中(0.65)
名校
解题方法
2. NA是阿伏加 德罗常数的值。下列说法正确的是( )
| A.20gH218O和D2O的混合物中含有中子10NA |
| B.密闭容器中2molNO与1molO2充分反应,产物的分子数为2NA |
| C.1L0.1mol·L-1的Na2CO3溶液中HCO3-和CO32-离子数之和为0.1NA |
| D.pH=1的硫酸溶液,含有氢离子数目为2NA |
您最近一年使用:0次
2020-06-04更新
|
287次组卷
|
3卷引用:宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题
宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题(已下线)专题02 化学计量与化学计算-2020年高考真题和模拟题化学分项汇编甘肃省平凉市庄浪县第一中学2021届高三第四次模拟化学试题
单选题
|
适中(0.65)
解题方法
3. 主族元素Q、X、Y、Z、W的原子序数依次增大,且均不大于20。Q的简单氢化物和其最高价含氧酸可以化合成盐,X与Q同周期且是该周期主族元素中原子半径最小的元素;Z-具有与氩原子相同的电子层结构;Q、Y、W原子的最外层电子数之和为9。下列说法一定正确的是( )
| A.X与Z的简单氢化物的水溶液均呈强酸性 |
| B.Z和W形成的化合物的水溶液呈中性 |
| C.Y与Z形成的化合物只含离子键 |
| D.简单氢化物的沸点:Q>X |
您最近一年使用:0次
单选题
|
适中(0.65)
名校
解题方法
4. 某有机物的结构简式如图所示,下列有关该有机物的说法不正确的是( )


| A.苯环上的一氯代物有3种 |
| B.含有2种官能团 |
| C.分子中的所有碳原子一定共面 |
| D.能发生氧化反应、取代反应、还原反应 |
您最近一年使用:0次
2020-06-04更新
|
399次组卷
|
3卷引用:宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题
宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题(已下线)专题12 有机化合物-2020年高考真题和模拟题化学分项汇编甘肃省兰州市第一中学2020届高三冲刺模拟考试(二)理科综合化学试题
单选题
|
适中(0.65)
名校
解题方法
5. 海洋动物海鞘中含有种类丰富、结构新颖的次生代谢物,是海洋抗肿瘤活性物质的重要来源之一。一种从海鞘中提取具有抗肿瘤活性的天然产物的流程如下:

下列关于该流程中各步骤的说法中,错误的是( )

下列关于该流程中各步骤的说法中,错误的是( )
选项 | 步骤 | 采用装置 | 主要仪器 |
A | ① | 过滤装置 | 漏斗 |
B | ② | 分液装置 | 分液漏斗 |
C | ③ | 蒸发装置 | 坩埚 |
D | ④ | 蒸馏装置 | 蒸馏烧瓶 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2017-12-27更新
|
757次组卷
|
11卷引用:河南省洛阳市2018届高三上学期第一次统一考试(12月)化学试题1
河南省洛阳市2018届高三上学期第一次统一考试(12月)化学试题1河南省洛阳市2018届高三上学期第一次统一考试(12月)化学试题2山西省朔州市怀仁县第一中学2018-2019学年高二下学期第二次月考化学试题湖南省示范性高中江华一中2020年高考理科综测试化学试题(14)吉林省吉林市2020届高三第三次调研测试(4月) 理综化学试题宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题新疆吾尔自治区石河子第二中学2020-2021学年高一上学期第一次月考化学试题甘肃省武威市民勤县第一中学2019-2020学年高二下学期期中考试化学(理) 试题江苏省常州市戚墅堰高级中学2020-2021学年高一上学期期中质量调研考试化学试题新疆昌吉州第二中学2020-2021学年高二下学期第一次月考化学(A)试题福建省漳州市东山第二中学2021-2022学年高二下学期期中考试化学试题
单选题
|
适中(0.65)
名校
解题方法
6. 我国某科研团队设计了一种新型能量存储/转化装置(如图所示)。闭合K2、断开K1时,制氢并储能;断开K2、闭合K1时,供电。下列说法错误的是( )


| A.制氢时,溶液中K+向Pt电极移动 |
| B.供电时,Zn电极附近溶液的pH不变 |
| C.供电时,X电极发生还原反应 |
| D.制氢时,X电极反应式为Ni(OH)2-e-+OH-=NiOOH+H2O |
您最近一年使用:0次
2020-06-04更新
|
709次组卷
|
7卷引用:宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题
宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题(已下线)专题08 电化学及其应用-2020年高考真题和模拟题化学分项汇编(已下线)易错09 电化学基础-备战2021年高考化学一轮复习易错题山东师范大学附属中学2020-2021学年高二上学期期中考试化学试题、河北省祖冲之中学2020-2021学年高二上学期阶段性测试化学试题陕西省西安中学2021届高三第七次模拟考试化学试题第四章 本章复习提升2
单选题
|
较难(0.4)
解题方法
7. 常温下,在体积均为20mL、浓度均为0.1mol·L-1的HX溶液、HY溶液中分别滴加同浓度的NaOH溶液,反应后溶液中水电离的c(H+)表示为pH水=-lgc(H+)水。pH水与滴加氢氧化钠溶液体积的关系如图所示。下列推断正确的是
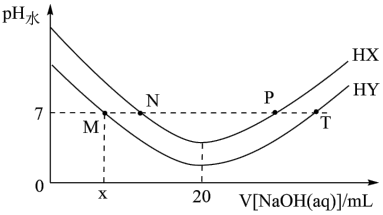

| A.HX的电离方程式为HX=H++X- |
| B.T点时c(Na+)=c(Y-)>c(H+)=c(OH-) |
| C.常温下用蒸馏水分别稀释N、P点溶液,pH都降低 |
D.常温下,HY的电离常数Ka=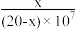 |
您最近一年使用:0次
二、解答题 添加题型下试题
解答题-实验探究题
|
适中(0.65)
8. 以硅藻土为载体的五氧化二钒(V2O5)是接触法生成硫酸的催化剂。从废钒催化剂中回收V2O5既避免污染环境又有利于资源综合利用。废钒催化剂的主要成分为:
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为___________ ,同时V2O4转成VO2+。“废渣1”的主要成分是__________________ 。
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为______ mol。
(3)“中和”作用之一是使钒以V4O124−形式存在于溶液中。“废渣2”中含有_______ 。
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124− R4V4O12+4OH−(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
R4V4O12+4OH−(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈_____ 性(填“酸”“碱”“中”)。
(5)“流出液”中阳离子最多的是________ 。
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式____________ 。
| 物质 | V2O5 | V2O4 | K2SO4 | SiO2 | Fe2O3 | Al2O3 |
| 质量分数/% | 2.2~2.9 | 2.8~3.1 | 22~28 | 60~65 | 1~2 | <1 |
以下是一种废钒催化剂回收工艺路线:

回答下列问题:
(1)“酸浸”时V2O5转化为VO2+,反应的离子方程式为
(2)“氧化”中欲使3 mol的VO2+变为VO2+,则需要氧化剂KClO3至少为
(3)“中和”作用之一是使钒以V4O124−形式存在于溶液中。“废渣2”中含有
(4)“离子交换”和“洗脱”可简单表示为:4ROH+ V4O124−
 R4V4O12+4OH−(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈
R4V4O12+4OH−(以ROH为强碱性阴离子交换树脂)。为了提高洗脱效率,淋洗液应该呈(5)“流出液”中阳离子最多的是
(6)“沉钒”得到偏钒酸铵(NH4VO3)沉淀,写出“煅烧”中发生反应的化学方程式
【知识点】 物质分离、提纯综合应用解读 常见无机物的制备解读
您最近一年使用:0次
2019-01-30更新
|
3386次组卷
|
12卷引用:2016年全国普通高等学校招生统一考试化学(新课标3卷精编版)
2016年全国普通高等学校招生统一考试化学(新课标3卷精编版)2017届湖南省衡阳八中高三上学期第二次月考化学试卷2017届贵州省凯里一中高三上第四次模拟化学试卷2016年全国普通高等学校招生统一考试化学(全国3卷参考版)黑龙江省哈尔滨市第三十二中学2020届高三上学期期末考试化学试题(已下线)专题七 工艺流程题(真题汇编)-2020年高考二轮模块化复习之《元素化合物》名师讲案与提分特训安徽省合肥市第一中学2020年高中毕业班教学质量监测卷理科综合化学试题宁夏银川九中、石嘴山三中、平罗中学三校2020届高三下学期联考理综化学试题陕西省西安市高新第一中学2020届高三教学质量监测理综化学试题山西省长治市第二中学校2022-2023学年高三上学期第四次月考化学试题河北省唐山市第一中学2022-2023学年高三上学期11月期中考试化学试题四川省内江市威远中学2023-2024学年高二上学期第一次月考化学试题
9. CO2是目前大气中含量最高的一种温室气体,CO2的综合利用是解决温室问题的有效途径。
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH。已知部分反应的热化学方程式如下:
CH3OH(g)+ O2(g)=CO2(g)+2H2O(1)△H1=-726.5kJ•mol-1
O2(g)=CO2(g)+2H2O(1)△H1=-726.5kJ•mol-1
H2(g)+ O2(g)=H2O(1)△H2=-285.8kJ•mol-1
O2(g)=H2O(1)△H2=-285.8kJ•mol-1
H2O(g)=H2O(l) △H3=-44kJ•mol-1
则CO2与H2反应生成气态CH3OH和水蒸气的热化学方程式为__ 。
(2)为研究CO2与CO之间的转化,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g) 2CO(g) △H,反应达平衡后,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示。回答下列问题:
2CO(g) △H,反应达平衡后,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示。回答下列问题:
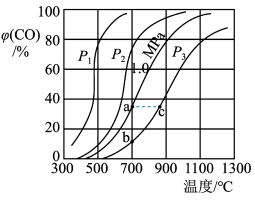
①压强p1__ 1.0MPa(填>、=或<)。
②900℃、1.0MPa时,足量碳与amolCO2反应达平衡后,CO2的转化率为__ ,该反应的平衡常数Kp=__ (保留小数点后一位数字)(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)①以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g) CH3COOH(g)。为了提高该反应中CO2的转化率,可以采取的措施是
CH3COOH(g)。为了提高该反应中CO2的转化率,可以采取的措施是___ (写一条即可)。
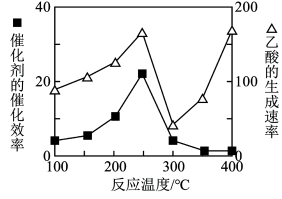
②在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,乙酸的生成速率降低的主要原因是__ ;300~400℃时,乙酸的生成速率升高的主要原因是__ 。
(4)将1.0×10-3mol/LCoSO4与1.2×10-3mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为___ mol/L。(已知:CoCO3的溶度积为:Ksp=1.0×10-13)
(1)研究表明CO2和H2在催化剂存在下可发生反应生成CH3OH。已知部分反应的热化学方程式如下:
CH3OH(g)+
 O2(g)=CO2(g)+2H2O(1)△H1=-726.5kJ•mol-1
O2(g)=CO2(g)+2H2O(1)△H1=-726.5kJ•mol-1H2(g)+
 O2(g)=H2O(1)△H2=-285.8kJ•mol-1
O2(g)=H2O(1)△H2=-285.8kJ•mol-1H2O(g)=H2O(l) △H3=-44kJ•mol-1
则CO2与H2反应生成气态CH3OH和水蒸气的热化学方程式为
(2)为研究CO2与CO之间的转化,让一定量的CO2与足量碳在体积可变的密闭容器中反应:C(s)+CO2(g)
 2CO(g) △H,反应达平衡后,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示。回答下列问题:
2CO(g) △H,反应达平衡后,测得压强、温度对CO的体积分数(φ(CO)%)的影响如图所示。回答下列问题:
①压强p1
②900℃、1.0MPa时,足量碳与amolCO2反应达平衡后,CO2的转化率为
(3)①以二氧化钛表面覆盖Cu2Al2O4为催化剂,可以将CO2和CH4直接转化成乙酸,CO2(g)+CH4(g)
 CH3COOH(g)。为了提高该反应中CO2的转化率,可以采取的措施是
CH3COOH(g)。为了提高该反应中CO2的转化率,可以采取的措施是②在不同温度下催化剂的催化效率与乙酸的生成速率如图所示。250~300℃时,乙酸的生成速率降低的主要原因是

(4)将1.0×10-3mol/LCoSO4与1.2×10-3mol/L的Na2CO3等体积混合,此时溶液中的Co2+的浓度为
您最近一年使用:0次
解答题-实验探究题
|
较难(0.4)
解题方法
10. 亚硝酰硫酸[M(NOSO4H)=127g·mol-1]主要用于分散染料重氮反应中取代亚硝酸钠,从而降低成本,提高产品质量。实验室用如图装置(夹持装置略)制备少量NOSO4H,并测定产品的纯度。已知:NOSO4H遇水分解,但溶于浓硫酸而不分解。

(1)装置A制取SO2,则A中反应的化学方程式为___ ,导管b的作用是___ 。
(2)SO2与装置B中盛有的浓硫酸和浓硝酸的混合液在维持体系温度不得高于20℃的条件下,反应制得NOSO4H。反应过程中,亚硝酰硫酸和硝酸的物质的量随时间的变化如图所示。反应进行到10min后,反应速度明显加快,其可能的原因是___ 。

(3)装置C的主要作用是__ 。
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是__ 。
(5)测定亚硝酰硫酸NOSO4H的纯度
准确称取1.500g产品放入250mL的碘量瓶中,加入0.1000mol·L-1、60.00mL的KMnO4标准溶液和10mL25%H2SO4溶液,然后摇匀。用0.2500mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
达到滴定终点时的现象为__ ,亚硝酰硫酸的纯度为__ 。

(1)装置A制取SO2,则A中反应的化学方程式为
(2)SO2与装置B中盛有的浓硫酸和浓硝酸的混合液在维持体系温度不得高于20℃的条件下,反应制得NOSO4H。反应过程中,亚硝酰硫酸和硝酸的物质的量随时间的变化如图所示。反应进行到10min后,反应速度明显加快,其可能的原因是

(3)装置C的主要作用是
(4)该实验装置存在可能导致NOSO4H产量降低的缺陷是
(5)测定亚硝酰硫酸NOSO4H的纯度
准确称取1.500g产品放入250mL的碘量瓶中,加入0.1000mol·L-1、60.00mL的KMnO4标准溶液和10mL25%H2SO4溶液,然后摇匀。用0.2500mol·L-1草酸钠标准溶液滴定,消耗草酸钠溶液的体积为20.00mL。
已知:2KMnO4+5NOSO4H+2H2O=K2SO4+2MnSO4+5HNO3+2H2SO4
2MnO4-+5C2O42-+16H+=2Mn2++10CO2↑+8H2O
达到滴定终点时的现象为
您最近一年使用:0次
解答题-结构与性质
|
适中(0.65)
解题方法
11. 工业上合成氨,CO易与铁触媒作用导致铁触媒失去催化活性:Fe+5CO═Fe(CO)5。为了防止催化剂铁触媒中毒,要除去CO,发生的反应为Cu(NH3)2OOCCH3+CO+NH3═Cu(NH3)3(CO)OOCCH3。回答下列问题:
(1)下列氮原子的电子排布图表示的状态中,能量最低的是__ (填字母序号)。
a. b.
b.
c. d.
d.
(2)写出CO的一种常见等电子体的结构式:___ ;C、N、O的第一电离能由大到小的顺序为__ (用元素符号表示)。
(3)与O同族的元素还有S、Se、Te,它们氢化物的沸点大小为H2O>H2Te>H2Se>H2S,其原因是___ 。
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价,1mol[Cu(NH3)2]+中含有σ键的数目___ 。则其中碳原子的杂化轨道类型是__ ,NH3分子的价电子对互斥理论模型是___ 。
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:

①若坐标参数A为(0,0,0),B为( ,
, ,
, ),则C的坐标参数为
),则C的坐标参数为__ ;
②若阿伏加 德罗常数为NA,该晶胞的边长为apm,则晶体的密度为___ g•cm-3。
(1)下列氮原子的电子排布图表示的状态中,能量最低的是
a.
 b.
b.
c.
 d.
d.
(2)写出CO的一种常见等电子体的结构式:
(3)与O同族的元素还有S、Se、Te,它们氢化物的沸点大小为H2O>H2Te>H2Se>H2S,其原因是
(4)配合物[Cu(NH3)2]OOCCH3中,铜显+1价,1mol[Cu(NH3)2]+中含有σ键的数目
(5)已知铜的一种氧化物Cu2O晶体的晶胞结构如图所示:

①若坐标参数A为(0,0,0),B为(
 ,
, ,
, ),则C的坐标参数为
),则C的坐标参数为②若阿伏加 德罗常数为NA,该晶胞的边长为apm,则晶体的密度为
您最近一年使用:0次
解答题-有机推断题
|
较难(0.4)
名校
解题方法
12. 聚合物H(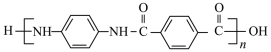 )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
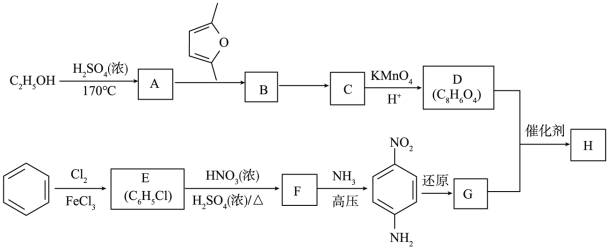
已知:①C、D、G均为芳香族化合物,分子中均只含两种不同化学环境的氢原子。
②Diels-Alder反应: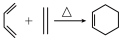
(1)生成A的反应类型是___________ ,F中所含官能团的结构简式为______________ 。
(2)B的结构简式是___________ ;“B→C”的反应中,除C外,另外一种产物名称是______ 。
(3)D+G→H的化学方程式是_____________________________________________ 。
(4)Q是D的同系物,相对分子质量比D大14,则Q可能的结构有______ 种,其中核磁共振氢谱有5组峰,且峰面积比为1:2:2:2:1的结构简式为_____________________ 。
(5)已知:乙炔与1,3-丁二烯也能发生Diels-Alder反应。请以1,3-丁二烯和乙炔为原料,选用必要的无机试剂合成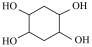 ,写出合成路线
,写出合成路线______________ 。(合成路线流程图示例:H2C=CH2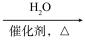 CH3CH2OH
CH3CH2OH CH3COOC2H5)。
CH3COOC2H5)。
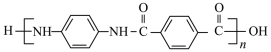 )是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下:
)是一种聚酰胺纤维,广泛用于各种刹车片,其合成路线如下: 
已知:①C、D、G均为芳香族化合物,分子中均只含两种不同化学环境的氢原子。
②Diels-Alder反应:
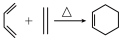
(1)生成A的反应类型是
(2)B的结构简式是
(3)D+G→H的化学方程式是
(4)Q是D的同系物,相对分子质量比D大14,则Q可能的结构有
(5)已知:乙炔与1,3-丁二烯也能发生Diels-Alder反应。请以1,3-丁二烯和乙炔为原料,选用必要的无机试剂合成
 ,写出合成路线
,写出合成路线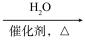 CH3CH2OH
CH3CH2OH CH3COOC2H5)。
CH3COOC2H5)。
【知识点】 根据要求书写同分异构体解读 氨基酸的成肽反应 有机物的合成 有机物的推断
您最近一年使用:0次
2020-04-27更新
|
781次组卷
|
7卷引用:湖北省荆州市2019届高三下学期4月质量检查(Ⅲ)理综试题
试卷分析
整体难度:适中
考查范围:有机化学基础、化学与STSE、认识化学科学、化学反应原理、物质结构与性质、化学实验基础
试卷题型(共 12题)
题型
数量
单选题
7
解答题
5
试卷难度
知识点分析
细目表分析 导出
| 题号 | 难度系数 | 详细知识点 | 备注 |
| 一、单选题 | |||
| 1 | 0.94 | 蛋白质的物理性质 化学科学对人类文明发展的意义 食品添加剂 合成纤维 | |
| 2 | 0.65 | 结合物质结构基础知识与NA相关推算 可逆反应及反应限度 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 | |
| 3 | 0.65 | 元素周期律、元素周期表的推断 根据原子结构进行元素种类推断 根据物质性质进行元素种类推断 | |
| 4 | 0.65 | 有机官能团的性质及结构 含碳碳双键物质的性质的推断 有机分子中原子共面的判断 | |
| 5 | 0.65 | 有机物分离提纯的几种常见操作 化学实验基础操作 蒸馏与分馏 萃取和分液 | |
| 6 | 0.65 | 原电池电极反应式书写 新型电池 原电池、电解池综合考查 电解池电极反应式及化学方程式的书写与判断 | |
| 7 | 0.4 | 水溶液中水的电离程度及的计算 弱电解质在水溶液中的电离平衡 盐溶液中微粒间的电荷守恒、物料守恒、质子守恒原理 盐溶液中离子浓度大小的比较 | |
| 二、解答题 | |||
| 8 | 0.65 | 物质分离、提纯综合应用 常见无机物的制备 | 实验探究题 |
| 9 | 0.65 | 盖斯定律及其有关计算 化学平衡常数的有关计算 转化率的相关计算及判断 溶度积常数相关计算 | 原理综合题 |
| 10 | 0.4 | 物质含量的测定 探究物质组成或测量物质的含量 物质制备的探究 综合实验设计与评价 | 实验探究题 |
| 11 | 0.65 | 物质结构与性质综合考查 电子排布式 等电子原理的应用 晶胞的有关计算 | 结构与性质 |
| 12 | 0.4 | 根据要求书写同分异构体 氨基酸的成肽反应 有机物的合成 有机物的推断 | 有机推断题 |



