回答下列问题:
(1)某工业废水中含有一定量的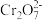 和
和 ,二者存在平衡:2
,二者存在平衡:2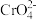 (黄色)+2H+
(黄色)+2H+
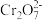 (橙色)+2H2O
(橙色)+2H2O
①若平衡体系滴加少量浓H2SO4(不考虑温度的影响),溶液显_______ 色。
②能说明该反应达平衡状态的是_____________ 。
a.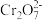 和
和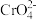 的浓度相同b.2v(
的浓度相同b.2v(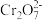 )=v(
)=v(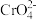 ) c.溶液的颜色不变
) c.溶液的颜色不变
(2)H2O2稀溶液易被催化分解,可使用的催化剂为(填序号)_______ 。
a.MnO2b.FeCl3c.Na2S2O3d.KMnO4
(3)密闭容器中发生如下反应:A(g)+3B(g) 2C(g) ΔH<0,根据下列速率—时间图象,回答下列问题。
2C(g) ΔH<0,根据下列速率—时间图象,回答下列问题。
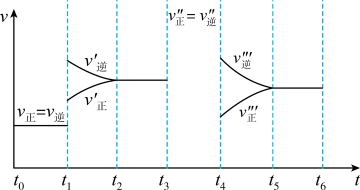
①下列时刻所改变的外界条件是:
t1________ ;t3________ ;t4________ ;
②产物C的体积分数最大的时间段是________ ;
③反应速率最大的时间段是________ 。
(1)某工业废水中含有一定量的
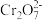 和
和 ,二者存在平衡:2
,二者存在平衡:2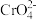 (黄色)+2H+
(黄色)+2H+
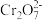 (橙色)+2H2O
(橙色)+2H2O①若平衡体系滴加少量浓H2SO4(不考虑温度的影响),溶液显
②能说明该反应达平衡状态的是
a.
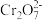 和
和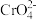 的浓度相同b.2v(
的浓度相同b.2v(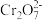 )=v(
)=v(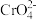 ) c.溶液的颜色不变
) c.溶液的颜色不变(2)H2O2稀溶液易被催化分解,可使用的催化剂为(填序号)
a.MnO2b.FeCl3c.Na2S2O3d.KMnO4
(3)密闭容器中发生如下反应:A(g)+3B(g)
 2C(g) ΔH<0,根据下列速率—时间图象,回答下列问题。
2C(g) ΔH<0,根据下列速率—时间图象,回答下列问题。
①下列时刻所改变的外界条件是:
t1
②产物C的体积分数最大的时间段是
③反应速率最大的时间段是
20-21高二·天津蓟州·阶段练习 查看更多[3]
天津市蓟县擂鼓台中学2020-2021学年高二上学期第一次月考化学试题(已下线)第10单元 化学反应速率与化学平衡(A卷 基础过关检测)-2021年高考化学一轮复习单元滚动双测卷湖南省长郡中学2020-2021学年高二上学期期中考试化学试题
更新时间:2020-10-19 20:46:58
|
相似题推荐
填空题
|
适中
(0.65)
名校
【推荐1】氮化硅(Si3N4)是一种新型陶瓷材料,它可由石英与焦炭在高温的氮气流中,通过以下反应制得:
3SiO2(s)+6C(s)+2N2(g) Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)
(1)该反应的还原产物是______ ;
(2)该反应的平衡常数表达式为K=____________ ;
(3)若知上述反应为放热反应,则其反应热△H______ 0(填“>”、“<”或“=”);升高温度,其平衡常数值______ (填“增大”、“减小”或“不变”);若已知CO生成速率为 (CO)=18mol•L﹣1•min﹣1,则N2消耗速率为
(CO)=18mol•L﹣1•min﹣1,则N2消耗速率为 (N2)=
(N2)=_________ ;
(4)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率 与时间t的关系如图,图中t4时引起平衡移动的条件可能是
与时间t的关系如图,图中t4时引起平衡移动的条件可能是__________ ;图中表示平衡混合物中CO的含量最高的一段时间是__________ 。

3SiO2(s)+6C(s)+2N2(g)
 Si3N4(s)+6CO(g)
Si3N4(s)+6CO(g)(1)该反应的还原产物是
(2)该反应的平衡常数表达式为K=
(3)若知上述反应为放热反应,则其反应热△H
 (CO)=18mol•L﹣1•min﹣1,则N2消耗速率为
(CO)=18mol•L﹣1•min﹣1,则N2消耗速率为 (N2)=
(N2)=(4)达到平衡后,改变某一外界条件(不改变N2、CO的量),反应速率
 与时间t的关系如图,图中t4时引起平衡移动的条件可能是
与时间t的关系如图,图中t4时引起平衡移动的条件可能是
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】回答下列问题:
(1)下图表示在密闭容器中反应:2SO2+O2 2SO3△H =-Q kJ/mol 到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b 过程中改变的条件可能是
2SO3△H =-Q kJ/mol 到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b 过程中改变的条件可能是_____ ;b→c过程中改变的条件可能是_____ ; 若增大压强时,将反应速度变化情况画在 c~d处____________ 。

(2)可逆反应mA(g)+nB(g) pC(g)达到平衡后,升高温度,B 的转化率变大;当减小压强,C 的体积分数减小。
pC(g)达到平衡后,升高温度,B 的转化率变大;当减小压强,C 的体积分数减小。
①用“>”、“=”或“<”填空:该反应的Δ H_____ 0,m+n_____ p。
②用“增大”“减小”或“不变”填空(其他条件不变):恒容下加入 B,则 A 的转化率_____ ;升高温度,则平衡时 B、C 的浓度之比 c(B)/c(C)将_____ ;加入催化剂,平衡时气体混合物的总物质的量_____ 。
③若 A、C 均为无色气体,B 为红色气体,用“变深”、“变浅”或“不变”填空:恒容下加入 C,平衡混合物的颜色_____ ;而恒压充入氖气,平衡混合物颜色_____ 。
(1)下图表示在密闭容器中反应:2SO2+O2
 2SO3△H =-Q kJ/mol 到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b 过程中改变的条件可能是
2SO3△H =-Q kJ/mol 到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,a→b 过程中改变的条件可能是
(2)可逆反应mA(g)+nB(g)
 pC(g)达到平衡后,升高温度,B 的转化率变大;当减小压强,C 的体积分数减小。
pC(g)达到平衡后,升高温度,B 的转化率变大;当减小压强,C 的体积分数减小。①用“>”、“=”或“<”填空:该反应的Δ H
②用“增大”“减小”或“不变”填空(其他条件不变):恒容下加入 B,则 A 的转化率
③若 A、C 均为无色气体,B 为红色气体,用“变深”、“变浅”或“不变”填空:恒容下加入 C,平衡混合物的颜色
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】一定温度下10L密闭容器中发生某可逆反应,其平衡常数表达为:K= 。
。
根据题意完成下列填空:
(1)写出该反应的化学方程式___ ;若温度升高,K增大,该反应是___ 反应(填“吸热”或“放热”)。
(2)能判断该反应一定达到平衡状态的是___ (选填编号)。
a.v正(H2O)=v逆(H2) b.容器中气体的相对分子质量不随时间改变
c.消耗nmol H2同时消耗nmolCO d.容器中物质的总物质的量不随时间改变
(3)该反应的v正 随时间变化的关系如图。t2时改变了某种条件,改变的条件可能是___ 、___ 。(填写2项)

(4)实验测得t2时刻容器内有1molH2O,5min后H2O的物质的量是0.8mol,这5min内H2O的平均反应速率为___ 。
 。
。根据题意完成下列填空:
(1)写出该反应的化学方程式
(2)能判断该反应一定达到平衡状态的是
a.v正(H2O)=v逆(H2) b.容器中气体的相对分子质量不随时间改变
c.消耗nmol H2同时消耗nmolCO d.容器中物质的总物质的量不随时间改变
(3)该反应的v正 随时间变化的关系如图。t2时改变了某种条件,改变的条件可能是

(4)实验测得t2时刻容器内有1molH2O,5min后H2O的物质的量是0.8mol,这5min内H2O的平均反应速率为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】有两个密闭容器A和B,A容器内有一个移动的活塞能使容器内保持恒压,B容器能保持恒容。起始时向这两个容器中分别充入等量的体积比为2:1的SO2和O2的混合气体,并使A和B的容积相等。在保持400℃的条件下使之发生如下反应:2 SO2+O2⇌2SO3。

(1)达到平衡时所需要的时间A容器比B容器_______ ,A容器中SO2的转化率比B容器_______ 。
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量氩气,A容器化学平衡_______ 移动,B容器化学平衡_______ 移动。
(3)达到(1)所述平衡后,若向两容器中通入等量的原反应气体,达到平衡时,A容器SO3物质的量分数_______ ;B容器中SO3的物质的量分数_______ 。(填增大、减小、不变)

(1)达到平衡时所需要的时间A容器比B容器
(2)达到(1)所述平衡后,若向两容器中通入数量不多的等量氩气,A容器化学平衡
(3)达到(1)所述平衡后,若向两容器中通入等量的原反应气体,达到平衡时,A容器SO3物质的量分数
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】汽车尾气是城市的主要空气污染物,研究控制汽车尾气成为保护环境的首要任务。
(1)汽车内燃机工作时发生反应:N2(g) + O2(g) 2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向5L密闭容器中充入6.5 molN2和7.5 molO2,在5 min时反应达到平衡状态,此时容器中NO的物质的量是5 mol。
2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向5L密闭容器中充入6.5 molN2和7.5 molO2,在5 min时反应达到平衡状态,此时容器中NO的物质的量是5 mol。
①5 min内该反应的平均速率υ (NO) =_______________ ;在T ℃时,该反应的平衡常数K = _____________ 。
②反应开始至达到平衡的过程中,容器中下列各项发生变化的是_______ (填序号)。
a.混合气体的密度
b.混合气体的压强
c.正反应速率
d.单位时间内,N2和NO的消耗量之比
(2)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。下图表示在其他条件不变时,反应:2NO(g)+2CO(g) 2CO2 (g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2 (g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。

①该反应的ΔH_____ 0 (选填“>”或“<”)。
②若催化剂的表面积S1>S2 ,在下图中画出c(NO) 在T1、S2 条件下达到平衡过程中的变化曲线_______________ 。
(1)汽车内燃机工作时发生反应:N2(g) + O2(g)
 2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向5L密闭容器中充入6.5 molN2和7.5 molO2,在5 min时反应达到平衡状态,此时容器中NO的物质的量是5 mol。
2NO(g),是导致汽车尾气中含有NO的原因之一。T ℃时,向5L密闭容器中充入6.5 molN2和7.5 molO2,在5 min时反应达到平衡状态,此时容器中NO的物质的量是5 mol。①5 min内该反应的平均速率υ (NO) =
②反应开始至达到平衡的过程中,容器中下列各项发生变化的是
a.混合气体的密度
b.混合气体的压强
c.正反应速率
d.单位时间内,N2和NO的消耗量之比
(2)当质量一定时,增大固体催化剂的表面积可提高化学反应速率。下图表示在其他条件不变时,反应:2NO(g)+2CO(g)
 2CO2 (g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
2CO2 (g)+N2(g) 中NO的浓度[c(NO)]随温度(T)、催化剂表面积(S)和时间(t)的变化曲线。
①该反应的ΔH
②若催化剂的表面积S1>S2 ,在下图中画出c(NO) 在T1、S2 条件下达到平衡过程中的变化曲线
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】甲烷自热重整是先进的制氢方法,包含甲烷氧化和水蒸气重整两个过程。
(1)甲烷自热重整时向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应如下:
①请用有关理论分析以上四个反应中反应Ⅰ速率最快的原因___ 。
②以上四个反应中,正向反应限度最大的是__ 。
a.反应Ⅰ b.反应Ⅱ c.反应Ⅲ d.反应Ⅳ
(2)甲烷水蒸气催化重整分为两阶段制备甲醇:
(ⅰ)制备合成气:CH4(g)+H2O(g) CO(g)+3H2(g)△H1=206.2kJ·mol-1
CO(g)+3H2(g)△H1=206.2kJ·mol-1
(ii)合成甲醇:CO(g)+2H2(g) CH3OH(g)△H2
CH3OH(g)△H2
制备合成气:将1.0molCH4和2.0molH2O(g)通入反应室(容积为100L),在一定条件下发生反应(ⅰ);CH4的平衡转化率与温度、压强的关系如图所示。
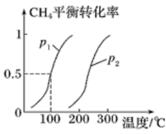
①已知100℃时达到平衡的时间为5min,则从反应开始到平衡,用氢气表示的平均反应速率为:v(H2)=___ mol·L-1·min-1。
②图中p1___ p2(填“<”、“>”或“=”)。
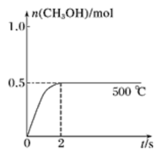
合成甲醇:在Cu2O/ZnO作催化剂的条件下,向2L的密闭容器中通入1molCO(g)和2molH2(g),发生反应(ⅱ),反应过程中CH3OH(g)的物质的量(n)与时间(t)及温度的关系如图所示。
③据研究,反应过程中起催化作用的为Cu2O。实际生产中随反应进行,Cu2O的量会减少,导致催化效率降低。若在反应体系中充入少量CO2,有利于保持Cu2O的催化效率不降低,原因是___ 。
④在500℃恒压条件下,请在图中画出反应体系中n(CH3OH)随时间t变化的总趋势图___ 。
(1)甲烷自热重整时向反应系统同时通入甲烷、氧气和水蒸气,发生的主要化学反应如下:
| 反应过程 | 反应序号 | 化学方程式 | △H/kJ·mol-1 | 活化能Ea/kJ·mol-1 |
| 甲烷氧化 | Ⅰ | CH4(g)+2O2(g)→CO2(g)+2H2O(g) | -802.6 | 125.6 |
| Ⅱ | CH4(g)+O2(g)→CO2(g)+2H2(g) | -322.0 | 172.5 | |
| 水蒸气重整 | Ⅲ | CH4(g)+H2O(g)→CO(g)+3H2(g) | +206.2 | 240.1 |
| Ⅳ | CH4(g)+2H2O(g)→CO2(g)+4H2(g) | +158.6 | 243.9 |
①请用有关理论分析以上四个反应中反应Ⅰ速率最快的原因
②以上四个反应中,正向反应限度最大的是
a.反应Ⅰ b.反应Ⅱ c.反应Ⅲ d.反应Ⅳ
(2)甲烷水蒸气催化重整分为两阶段制备甲醇:
(ⅰ)制备合成气:CH4(g)+H2O(g)
 CO(g)+3H2(g)△H1=206.2kJ·mol-1
CO(g)+3H2(g)△H1=206.2kJ·mol-1(ii)合成甲醇:CO(g)+2H2(g)
 CH3OH(g)△H2
CH3OH(g)△H2制备合成气:将1.0molCH4和2.0molH2O(g)通入反应室(容积为100L),在一定条件下发生反应(ⅰ);CH4的平衡转化率与温度、压强的关系如图所示。

①已知100℃时达到平衡的时间为5min,则从反应开始到平衡,用氢气表示的平均反应速率为:v(H2)=
②图中p1
合成甲醇:在Cu2O/ZnO作催化剂的条件下,向2L的密闭容器中通入1molCO(g)和2molH2(g),发生反应(ⅱ),反应过程中CH3OH(g)的物质的量(n)与时间(t)及温度的关系如图所示。
③据研究,反应过程中起催化作用的为Cu2O。实际生产中随反应进行,Cu2O的量会减少,导致催化效率降低。若在反应体系中充入少量CO2,有利于保持Cu2O的催化效率不降低,原因是
④在500℃恒压条件下,请在图中画出反应体系中n(CH3OH)随时间t变化的总趋势图

您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】氯化钙不能干燥NH3,因为CaCl2(s)+8NH3(g) CaCl2·8NH3(s) ΔH<0,该反应的平衡常数K=
CaCl2·8NH3(s) ΔH<0,该反应的平衡常数K=___________ ;向2L装有CaCl2的密闭容器中,通入2molNH3,反应10分钟,固体增重17g,则0~10分钟内,NH3的平均反应速率 =
=___________ ;若要将已吸收NH3的CaCl2重新恢复吸收NH3的能力,写出一种可采取的措施___________ 。
 CaCl2·8NH3(s) ΔH<0,该反应的平衡常数K=
CaCl2·8NH3(s) ΔH<0,该反应的平衡常数K= =
=
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】完成下列问题
(1)密闭容器中发生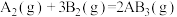 反应,若
反应,若 ,则正反应一定是
,则正反应一定是__________ 反应(填“放热”或“吸热”)。在其他条件不变的情况下,只改变起始 的物质的量,在a、b、c三点达到平衡时,
的物质的量,在a、b、c三点达到平衡时, 的物质的量由大到小的顺序为
的物质的量由大到小的顺序为_____ 。

(2)已知反应
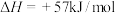 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化曲线如图所示。A、C两点气体的颜色
的体积分数随压强变化曲线如图所示。A、C两点气体的颜色_____ 点深。(填“A”或“C”)A、B两点的平均相对分子质量:A_____ B(填“>”“=”或“<”)。
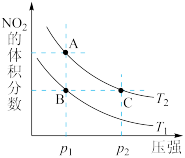
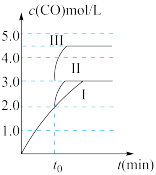
(3)在容积可变的密闭容器中发生反应 ,
, 随反应时间的变化如图中曲线Ⅰ所示,此时平衡时体积为1L,若在
随反应时间的变化如图中曲线Ⅰ所示,此时平衡时体积为1L,若在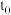 时刻改变一个条件,使曲线Ⅰ变为曲线Ⅲ时,可通过将容器的体积变为
时刻改变一个条件,使曲线Ⅰ变为曲线Ⅲ时,可通过将容器的体积变为__________ L实现。
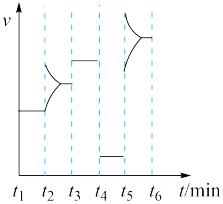
(4)某密闭容器中发生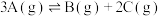 ,
,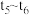 阶段,容器内A的物质的量减少了
阶段,容器内A的物质的量减少了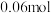 ,而此过程中容器与外界的热交换总量为akJ,书写反应的热化学方程式
,而此过程中容器与外界的热交换总量为akJ,书写反应的热化学方程式__________ 。
(1)密闭容器中发生
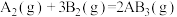 反应,若
反应,若 ,则正反应一定是
,则正反应一定是 的物质的量,在a、b、c三点达到平衡时,
的物质的量,在a、b、c三点达到平衡时, 的物质的量由大到小的顺序为
的物质的量由大到小的顺序为
(2)已知反应

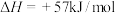 ,在温度为
,在温度为 、
、 时,平衡体系中
时,平衡体系中 的体积分数随压强变化曲线如图所示。A、C两点气体的颜色
的体积分数随压强变化曲线如图所示。A、C两点气体的颜色
(3)在容积可变的密闭容器中发生反应
 ,
, 随反应时间的变化如图中曲线Ⅰ所示,此时平衡时体积为1L,若在
随反应时间的变化如图中曲线Ⅰ所示,此时平衡时体积为1L,若在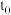 时刻改变一个条件,使曲线Ⅰ变为曲线Ⅲ时,可通过将容器的体积变为
时刻改变一个条件,使曲线Ⅰ变为曲线Ⅲ时,可通过将容器的体积变为
(4)某密闭容器中发生
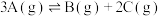 ,
,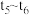 阶段,容器内A的物质的量减少了
阶段,容器内A的物质的量减少了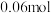 ,而此过程中容器与外界的热交换总量为akJ,书写反应的热化学方程式
,而此过程中容器与外界的热交换总量为akJ,书写反应的热化学方程式
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】偏二甲肼与N2O4是常用的火箭推进剂,二者发生如下化学反应:(CH3)2NNH2(l)+2N2O4(l)=2CO2(g)+3N2(g)+4H2O(g)(Ⅰ)
(1)反应(Ⅰ)中氧化剂是___ 。
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g) 2NO2(g) ΔH(Ⅱ)
2NO2(g) ΔH(Ⅱ)
当温度升高时,气体颜色变深,则反应(Ⅱ)中ΔH___ 0(填“>”或“<”),保持温度和体积不变向上述平衡体系中再充入一定量的N2O4,混合气体的颜色__ (填“变深”或“变浅”)。

(1)反应(Ⅰ)中氧化剂是
(2)火箭残骸中常现红棕色气体,原因为:N2O4(g)
 2NO2(g) ΔH(Ⅱ)
2NO2(g) ΔH(Ⅱ)当温度升高时,气体颜色变深,则反应(Ⅱ)中ΔH
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】在一定容积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)  CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=_______ 。
(2)该反应的正反应为_______ 反应(填“吸热”或“放热”)。
(3)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K_______ 1.0(填“大于”“小于”或“等于”)。
(4)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡_______ 移动(填“向正反应方向”“向逆反应方向”或“不”)。
 CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:
CO(g)+H2O(g),其化学平衡常数K和温度t的关系如表:| t/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)该反应的正反应为
(3)若830 ℃时,向容器中充入1 mol CO、5 mol H2O,反应达到平衡后,其化学平衡常数K
(4)830 ℃时,容器中的反应已达到平衡。在其他条件不变的情况下,扩大容器的容积,平衡
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】研究 之间的转化具有重要意义。
之间的转化具有重要意义。
已知:

将一定量 气体充入恒容的密闭容器中,控制反应温度为
气体充入恒容的密闭容器中,控制反应温度为 。
。
(1)下列可以作为反应达到平衡的判据是___________(填编号)。
(2)反应温度 时,体系中
时,体系中 、
、 随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为
随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为 ,
, 随t(时间)变化曲线如图虚线所示。
随t(时间)变化曲线如图虚线所示。
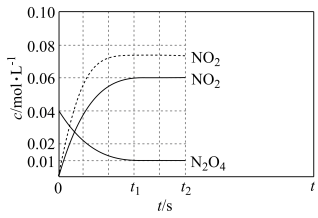
①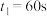 ,在0~60s时段,反应速率
,在0~60s时段,反应速率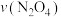 为
为___________ 
②反应温度为
___________ (填“大于”或“小于”) 。
。
③温度 时反应达平衡后,将反应容器的容积减少一半,平衡向
时反应达平衡后,将反应容器的容积减少一半,平衡向___________ (填“正反应”或“逆反应”)方向移动。
④ 时刻反应达到平衡,混合气体平衡总压强为p,
时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为75%,则反应
气体的平衡转化率为75%,则反应 的平衡常数
的平衡常数
___________ 。(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(3)NO氧化反应: 分两步进行,其反应过程能量变化示意图如图。
分两步进行,其反应过程能量变化示意图如图。
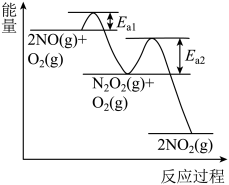
Ⅰ.

Ⅱ.

决定NO氧化反应速率的步骤是___________ (填“Ⅰ”或“Ⅱ”)。
 之间的转化具有重要意义。
之间的转化具有重要意义。已知:


将一定量
 气体充入恒容的密闭容器中,控制反应温度为
气体充入恒容的密闭容器中,控制反应温度为 。
。(1)下列可以作为反应达到平衡的判据是___________(填编号)。
| A.气体的压强不变 | B. |
| C.K不变 | D.容器内颜色不变 |
(2)反应温度
 时,体系中
时,体系中 、
、 随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为
随t(时间)变化曲线如图实线所示。保持其它条件不变,改变反应温度为 ,
, 随t(时间)变化曲线如图虚线所示。
随t(时间)变化曲线如图虚线所示。
①
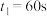 ,在0~60s时段,反应速率
,在0~60s时段,反应速率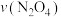 为
为
②反应温度为

 。
。③温度
 时反应达平衡后,将反应容器的容积减少一半,平衡向
时反应达平衡后,将反应容器的容积减少一半,平衡向④
 时刻反应达到平衡,混合气体平衡总压强为p,
时刻反应达到平衡,混合气体平衡总压强为p, 气体的平衡转化率为75%,则反应
气体的平衡转化率为75%,则反应 的平衡常数
的平衡常数
(3)NO氧化反应:
 分两步进行,其反应过程能量变化示意图如图。
分两步进行,其反应过程能量变化示意图如图。
Ⅰ.


Ⅱ.


决定NO氧化反应速率的步骤是
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】如图所示,甲、乙、丙分别表示在不同条件下,可逆反应A(g)+B(g)  xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
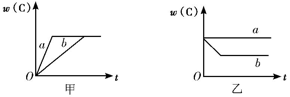
(1)若甲中两条曲线分别代表有催化剂和无催化剂的情况,则____ 曲线代表无催化剂时的情况。
(2)若乙表示反应达到平衡状态后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He后的情况,则___ 曲线表示恒温恒容的情况,且此时混合气体中w(C)___ (填“变大”“变小”或“不变”)。
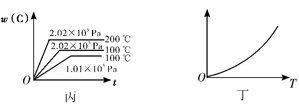
(3)根据丙可以判断该可逆反应的正反应是___ (填“放热”或“吸热”)反应,x的值为___ 。
(4)丁表示在某固定容积的密闭容器中,上述可逆反应达到平衡后,某物理量随温度(T)的变化情况,根据你的理解,丁的纵坐标可以是____ (填序号)。
①w(C) ②A的转化率 ③B的转化率 ④压强 ⑤c(A) ⑥c(B)
升高温度,平衡向____ (填“正反应”或“逆反应”)方向移动。
 xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。
xC(g)的生成物C的百分含量w(C)和反应时间(t)的关系。

(1)若甲中两条曲线分别代表有催化剂和无催化剂的情况,则
(2)若乙表示反应达到平衡状态后,分别在恒温恒压条件下和恒温恒容条件下向平衡混合气体中充入He后的情况,则
(3)根据丙可以判断该可逆反应的正反应是
(4)丁表示在某固定容积的密闭容器中,上述可逆反应达到平衡后,某物理量随温度(T)的变化情况,根据你的理解,丁的纵坐标可以是
①w(C) ②A的转化率 ③B的转化率 ④压强 ⑤c(A) ⑥c(B)
升高温度,平衡向
您最近一年使用:0次



