已知联氨(N2H4)为二元弱碱,常温下将盐酸滴加到联氨(N2H4)的水溶液中,混合溶液中微粒的物质的量分数δ(X)随-lg c(OH-)变化的关系如图所示。下列叙述错误的是
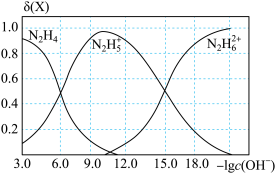
| A.Kb1(N2H4)=10-6.0 |
B.N2H6Cl2溶液中存在:c(Cl-)+c(OH-)=c(N2H )+2c(N2H )+2c(N2H )+c(H+) )+c(H+) |
| C.N2H5Cl溶液中:c(H+)>c(OH-) |
D.N2H5Cl在溶液中水解的离子方程式为:N2H +H2O⇌N2H +H2O⇌N2H +OH- +OH- |
20-21高二上·河南郑州·期中 查看更多[5]
河南省南阳市第一中学校2022届高三上学期第一次月考化学试题(已下线)2021年高考化学押题预测卷(湖北卷)03(含考试版、答题卡、参考答案、全解全析)江西省高安中学2021届高三第三次月考理综化学试题河南省鹤壁市高级中学2020-2021学年高二上学期尖子生联赛调研化学试题河南省郑州市郑州中学2020-2021学年高二上学期期中考试化学试题
更新时间:2020-11-29 18:02:48
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】向仅含SO 、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
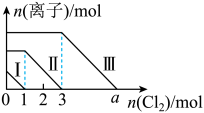
 、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
、I-、Br-且物质的量分别为m、n、6 mol 的钠盐溶液中通入适量氯气,溶液中这三种离子的物质的量的变化如图所示。下列说法中正确的是( )
| A.曲线Ⅱ代表Br-的变化情况 |
B.曲线Ⅰ对应的反应:SO +Cl2+H2O===2H++SO +Cl2+H2O===2H++SO +2Cl- +2Cl- |
C.通入的氯气为5 mol时,溶液中的主要阴离子为Cl-、SO |
D.溶液中n(Na+)=n(SO )+n(I-)+n(Br-) )+n(I-)+n(Br-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】KHC2O4•H2C2O4•2H2O(草酸三氢钾)主要用于缓冲溶液的配制。室温时,H2C2O4的Ka1=5.9×10-2,Ka2=6.4×10-5。下列有关0.1mol·L-1草酸三氢钾溶液的说法正确的是
A.c(H2C2O4)>c(K+)>c(HC2O ) ) |
B.c(K+)=c(C2O )+c(HC2O )+c(HC2O )+c(H2C2O4) )+c(H2C2O4) |
C.向其中滴加NaOH溶液至溶液呈中性:c(K+)>c(Na+)>c(HC2O )>c(C2O )>c(C2O ) ) |
D.与0.3mol·L-1NaOH溶液等体积混合:c(K+)+c(Na+)>2c(C2O )+c(HC2O )+c(HC2O ) ) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐1】常温下,下列有关醋酸溶液的叙述中不正确的是
| A.pH =4.3的CH3COOH与CH3COONa混合溶液中:c(Na+) < c(CH3COO-) |
| B.浓度为0.2 mol/L的CH3COOH溶液和浓度为0.1 mol/L的NaOH溶液等体积混合后:c(CH3COO -) - c(CH3COOH) = 2[c(H+) - c(OH-)] |
C.醋酸浓溶液加少量水稀释,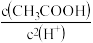 几乎不变 几乎不变 |
| D.含等物质的量的NaHC2O4和Na2C2O4的溶液:3c(Na+) = 2[c(HC2O4-) + c(C2O42-) + c(H2C2O4)] |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】常温下,下列说法正确的是
A.pH值都为4的稀盐酸和 溶液中,水的电离程度相同 溶液中,水的电离程度相同 |
B.浓度均为 的醋酸和NaOH溶液等体积混合后: 的醋酸和NaOH溶液等体积混合后: |
C.在含浓度都为 的 的 、 、 的混合溶液中滴加 的混合溶液中滴加 溶液,先出现沉淀的是 溶液,先出现沉淀的是 已知: 已知: , ,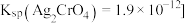 |
D.浓度均为 的 的 和 和 溶液中, 溶液中, 相同 相同 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】室温下,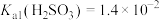 ,通过下列实验探究
,通过下列实验探究 、
、 溶液的性质:
溶液的性质:
实验1:用pH试纸测定0.1mol⋅L
 溶液的pH,测得pH约为10。
溶液的pH,测得pH约为10。
实验2:向0.1mol⋅L
 溶液中通入过量的
溶液中通入过量的 ,再滴入2滴紫色石蕊试剂,溶液呈红色。
,再滴入2滴紫色石蕊试剂,溶液呈红色。
实验3:向实验2溶液中逐滴滴加一定体积的盐酸,测得溶液pH为3。
实验4:向0.1mol⋅L
 溶液中加入等体积、等浓度的
溶液中加入等体积、等浓度的 溶液,产生白色沉淀。
溶液,产生白色沉淀。
下列说法正确的是
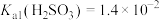 ,通过下列实验探究
,通过下列实验探究 、
、 溶液的性质:
溶液的性质:实验1:用pH试纸测定0.1mol⋅L

 溶液的pH,测得pH约为10。
溶液的pH,测得pH约为10。实验2:向0.1mol⋅L

 溶液中通入过量的
溶液中通入过量的 ,再滴入2滴紫色石蕊试剂,溶液呈红色。
,再滴入2滴紫色石蕊试剂,溶液呈红色。实验3:向实验2溶液中逐滴滴加一定体积的盐酸,测得溶液pH为3。
实验4:向0.1mol⋅L

 溶液中加入等体积、等浓度的
溶液中加入等体积、等浓度的 溶液,产生白色沉淀。
溶液,产生白色沉淀。下列说法正确的是
A.0.1mol⋅L 的 的 溶液中存在: 溶液中存在: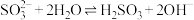 |
B.实验2可以得出: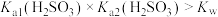 |
C.实验3得到的溶液中存在: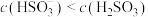 |
D.实验4中可推测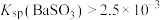 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,向1mol•L-1NH4Cl溶液中加入足量的镁条,该体系pH随时间变化的曲线如图所示。验观察到b点开始溶液中有白色沉淀生成,已知Ksp[Mg(OH)2]=1.8×10-11。下列说法错误的是


| A.常温下,NH4Cl的水解平衡常数数量级为10-10 |
| B.体系中,水的电离程度大小关系为a>c>b |
| C.b点时,溶液中c(Mg2+)=0.18mol∙L-1 |
D.a点溶液中,c( )+c(H+)<c(Cl-)+c(OH-) )+c(H+)<c(Cl-)+c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐3】常温下将KOH溶液滴加到二元弱酸( )溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是

 )溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
)溶液中,混合溶液的pH与离子浓度变化的关系如图所示。下列叙述错误的是
A. 的数量级为 的数量级为 |
B.曲线N表示pH与 的变化关系 的变化关系 |
C.KHX溶液中,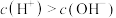 |
D.当混合溶液呈中性时, |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】下列实验操作、现象和结论或解释均正确的是
| 选项 | 实验操作 | 现象 | 结论或解释 |
| A | 取5mL0.1mol/LFeCl3溶液,滴加5~6滴0.1mol/LKI溶液,充分反应后,再滴加KSCN溶液 | 溶液变红 | FeCl3和KI的反应是可逆反应 |
| B | 将足量SO2通入Na2CO3溶液中逸出的气体通入足量的酸性KMnO4溶液,再通入澄清石灰水中 | 酸性KMnO4溶液颜色变浅,澄清石灰水变浑浊 | Ka1(H2SO3)>Ka1(H2CO3) |
| C | 将脱脂棉放入试管中,加入浓硫酸后搅成糊状,微热得到亮棕色溶液,加入新制Cu(OH)2悬浊液,加热 | 有砖红色沉淀生成 | 说明水解产物含有葡萄糖 |
| D | 将硫酸酸化的H2O2溶液滴入Fe(NO3)2溶液中 | 溶液变黄色 | 氧化性:H2O2>Fe3+ |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】25℃时,醋酸的 ,磷酸的
,磷酸的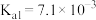 、
、 、
、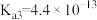 。下列说法不正确的是
。下列说法不正确的是
 ,磷酸的
,磷酸的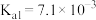 、
、 、
、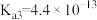 。下列说法不正确的是
。下列说法不正确的是A. 溶液: 溶液: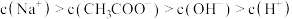 |
B.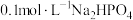 溶液: 溶液: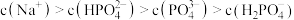 |
C.浓度均为 和 和 混合溶液: 混合溶液: |
D.浓度均为 醋酸和 醋酸和 溶液等体积混合: 溶液等体积混合: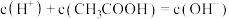 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】H2A为二元酸,其电离过程为:H2A H++HA-,HA-
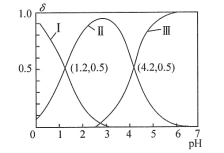
H++HA-,HA- H++A2-。常温时,向10mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向10mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
 H++HA-,HA-
H++HA-,HA- H++A2-。常温时,向10mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
H++A2-。常温时,向10mL0.1mol/LH2A水溶液中逐滴滴加0.1mol/LNaOH溶液,混合溶液中H2A、HA-和A2-的物质的量分数(δ)随pH变化的关系如图所示。下列说法正确的是
| A.H2A的Kal的数量级为10-1 |
| B.当溶液中c(H2A)=c(A2-)时,pH=2.9 |
| C.当溶液中c(Na+)=2c(A2-)+c(HA-)时,加入V(NaOH溶液)>10mL |
| D.常温下NaHA能促进水的电离 |
您最近一年使用:0次

 ,向20mL浓度均为
,向20mL浓度均为 的盐酸和醋酸的混合溶液中逐滴加入
的盐酸和醋酸的混合溶液中逐滴加入
 )>c(CH3COOH)>c(H+)>c(OH-)
)>c(CH3COOH)>c(H+)>c(OH-)
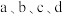 点溶液中,d点水的电离程度最大
点溶液中,d点水的电离程度最大 溶液与
溶液与 溶液等体积混合,测得
溶液等体积混合,测得 和铜氨各级配合物的物质的量分数
和铜氨各级配合物的物质的量分数 与平衡体系的
与平衡体系的 [平衡体系中
[平衡体系中 ]的关系如图所示。
]的关系如图所示。
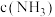 越大越有利于配位数多的铜氨配合物的形成
越大越有利于配位数多的铜氨配合物的形成 的平衡常数为
的平衡常数为



