I.甲醇水蒸气重整制氢(SRM)系统简单,产物中H2含量高、CO含量低(CO会损坏燃料电池的交换膜),是电动汽车氢氧燃料电池理想的氢源。其反应如下:
反应1(主):
反应2(副):
温度高于300C则会同时发生反应3: ,回答下列问题:
,回答下列问题:
(1)反应1能够自发进行的原因是_______ 。
(2)升温有利于提高CH3OH转化率,但也存在一个明显的缺点是_______ 。
II.甲制取低碳烯烃技术(DMTO)项目曾摘取了2014年度国家技术发明奖一等奖。DMTO主要包括煤的气化、液化、烯烃化三个阶段。回答下列问题:
(1)煤的气化。用化学方程式表示煤的气化的主要反应_______ 。
(2)煤的液化。下表中某些反应是煤的液化过程中的反应:
①反应I的平衡常数表达式K1=_______ ;
②b_______ 0(填“>”“<”或“=”),c与a、b之间的定量关系为_______ 。
③K3=_______ ,若反应Ⅲ是在500℃、容积为2L的密闭容器中进行的,测得某一时刻体系内 的物质的量分别为6mol、2mol、10mol、10mol,则此时CH3OH的生成速率
的物质的量分别为6mol、2mol、10mol、10mol,则此时CH3OH的生成速率_______ (填“>”“<”或“=”)CH3OH的消耗速率。
④对于反应III,在一容积不变的密闭容器中,下列措施可增加甲醇产率的是_______
A.升高温度 B.将CH3OH(g)从体系中分离
C.使用合适的催化剂 D.充入He,使体系总压强增大
(3)烯烃化阶段。图1是某工厂烯烃化阶段产物中乙烯、丙烯的选择性与温度、压强之间的关系(选择性:指生成某物质的百分比。图中I、II表示乙烯,III表示丙烯)。
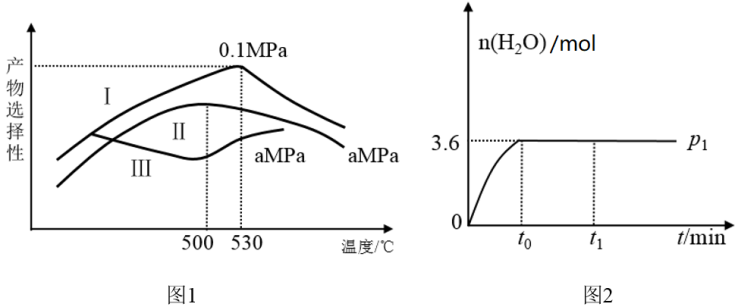
①为尽可能的获得乙烯,控制的生产条件为_______
②一定温度下某密闭容器中存在反应: 。在压强为P1时产物水的物质的量与时间的关系如图2所示,若t0时刻测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为
。在压强为P1时产物水的物质的量与时间的关系如图2所示,若t0时刻测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为_______ (保留三位有效数字)。
反应1(主):

反应2(副):

温度高于300C则会同时发生反应3:
 ,回答下列问题:
,回答下列问题:(1)反应1能够自发进行的原因是
(2)升温有利于提高CH3OH转化率,但也存在一个明显的缺点是
II.甲制取低碳烯烃技术(DMTO)项目曾摘取了2014年度国家技术发明奖一等奖。DMTO主要包括煤的气化、液化、烯烃化三个阶段。回答下列问题:
(1)煤的气化。用化学方程式表示煤的气化的主要反应
(2)煤的液化。下表中某些反应是煤的液化过程中的反应:
| 热化学方程式 | 平衡常数 | |
| 500℃ | 700℃ | |
I. | 2.0 | 0.2 |
II. | 1.0 | 2.3 |
III. | K3 | 4.6 |
①反应I的平衡常数表达式K1=
②b
③K3=
 的物质的量分别为6mol、2mol、10mol、10mol,则此时CH3OH的生成速率
的物质的量分别为6mol、2mol、10mol、10mol,则此时CH3OH的生成速率④对于反应III,在一容积不变的密闭容器中,下列措施可增加甲醇产率的是
A.升高温度 B.将CH3OH(g)从体系中分离
C.使用合适的催化剂 D.充入He,使体系总压强增大
(3)烯烃化阶段。图1是某工厂烯烃化阶段产物中乙烯、丙烯的选择性与温度、压强之间的关系(选择性:指生成某物质的百分比。图中I、II表示乙烯,III表示丙烯)。

①为尽可能的获得乙烯,控制的生产条件为
②一定温度下某密闭容器中存在反应:
 。在压强为P1时产物水的物质的量与时间的关系如图2所示,若t0时刻测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为
。在压强为P1时产物水的物质的量与时间的关系如图2所示,若t0时刻测得甲醇的体积分数为10%,此时甲醇乙烯化的转化率为
更新时间:2021-07-14 19:42:19
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】甲醇是重要的化工原料。
I.用二氧化碳和氢气合成甲醇:
(1)已知: (a、b均为正数),则表示
(a、b均为正数),则表示 燃烧热的热化学方程式为:
燃烧热的热化学方程式为:_______ 。
(2)若在体积为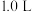 的恒容密闭容器中充入
的恒容密闭容器中充入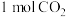 和
和 模拟工业合成甲醇的反应:
模拟工业合成甲醇的反应: ,二氧化碳的转化率和温度的关系如下图所示。
,二氧化碳的转化率和温度的关系如下图所示。
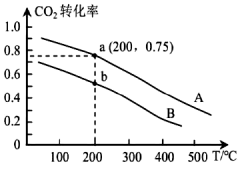
①下列能说明该反应达到平衡状态的是_______ 。
A.混合气体平均相对分子质量不变
B.混合气体密度不变
C.容器内压强恒定不变
D.反应速率满足以下关系:
②计算T=200℃时,该反应的化学平衡常数K=_______ (计算结果保留一位小数)。
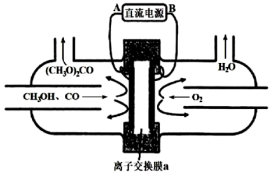
II.以甲醇为主要原料,电化学合成碳酸二甲酯【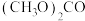 】的工作原理如下图所示。离子交换膜a为
】的工作原理如下图所示。离子交换膜a为_______ (填“阳膜”、“阴膜”),阴极的电极反应式为_______ 。
I.用二氧化碳和氢气合成甲醇:

(1)已知:
 (a、b均为正数),则表示
(a、b均为正数),则表示 燃烧热的热化学方程式为:
燃烧热的热化学方程式为:(2)若在体积为
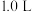 的恒容密闭容器中充入
的恒容密闭容器中充入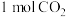 和
和 模拟工业合成甲醇的反应:
模拟工业合成甲醇的反应: ,二氧化碳的转化率和温度的关系如下图所示。
,二氧化碳的转化率和温度的关系如下图所示。
①下列能说明该反应达到平衡状态的是
A.混合气体平均相对分子质量不变
B.混合气体密度不变
C.容器内压强恒定不变
D.反应速率满足以下关系:

②计算T=200℃时,该反应的化学平衡常数K=
II.以甲醇为主要原料,电化学合成碳酸二甲酯【
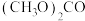 】的工作原理如下图所示。离子交换膜a为
】的工作原理如下图所示。离子交换膜a为
您最近一年使用:0次
【推荐2】甲醇来源丰富、价格低廉、运输贮存方便,是一种重要的化工原料。
工业生产甲醇的常用方法是:
 。
。
(1)已知:



 的反应热
的反应热
_______ 。
(2)不同的催化剂有着不同的催化活性,也有不同最佳反应温度。研究者向恒压密闭装置中通入混合气体[混合比例 ],生成甲醇时空收率随温度的变化曲线,如图所示:
],生成甲醇时空收率随温度的变化曲线,如图所示:
已知:时空收率表示单位物质的量催化剂表面甲醇的平均生成速率

①甲醇的时空收率为什么整体上出现“抛物线”形状_______ 。
②选择催化剂最佳配比_______ 、最佳反应温度_______ 。
③使用1 活性
活性 催化剂时,若反应温度由169℃升高到223℃,尝试计算反应速率之比
催化剂时,若反应温度由169℃升高到223℃,尝试计算反应速率之比
_______ 。223℃时氢气的平均反应速率_______ 
(3)①工业上利用甲醇蒸汽重整法制备氢气。该法中的一个主要反应为 ,此反应能自发进行的原因是
,此反应能自发进行的原因是_______ 。
②在稀硫酸介质中,甲醇燃料电池负极发生的电极反应式为_______ 。
工业生产甲醇的常用方法是:

 。
。(1)已知:




 的反应热
的反应热
(2)不同的催化剂有着不同的催化活性,也有不同最佳反应温度。研究者向恒压密闭装置中通入混合气体[混合比例
 ],生成甲醇时空收率随温度的变化曲线,如图所示:
],生成甲醇时空收率随温度的变化曲线,如图所示:已知:时空收率表示单位物质的量催化剂表面甲醇的平均生成速率

①甲醇的时空收率为什么整体上出现“抛物线”形状
②选择催化剂最佳配比
③使用1
 活性
活性 催化剂时,若反应温度由169℃升高到223℃,尝试计算反应速率之比
催化剂时,若反应温度由169℃升高到223℃,尝试计算反应速率之比

(3)①工业上利用甲醇蒸汽重整法制备氢气。该法中的一个主要反应为
 ,此反应能自发进行的原因是
,此反应能自发进行的原因是②在稀硫酸介质中,甲醇燃料电池负极发生的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】随着大气污染的日趋严重,国家拟于“十二五”期间,将二氧化硫(SO2)排放量减少8%,氮氧化物(NOx)排放量减少10%。目前,消除大气污染有多种方法。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为___________ 。
(2)全钒氧化还原液流电池,是目前发展势头强劲的优秀绿色环保储能电池。其电池总反应为:V3++VO2++H2O VO2++ 2H++V2+。
VO2++ 2H++V2+。
充电过程中,H+向_____ 迁移(填“阴极区”或“阳极区”)。充电时阴极反应式为_________ 。
(3)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g) N2(g)+2CO2(g);△H<0。
N2(g)+2CO2(g);△H<0。
该反应的化学平衡常数表达式为K=_______________ 。

若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如上图所示。若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将__________ 移动(填“向左”、 “向右”或“不”)。
20min时,若改变反应条件,导致N2浓度发生如上图所示的变化,则改变的条件可能是_____ (填序号)。
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42-而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O,则另一反应的离子方程式为________________ 。
(1)处理NOx的一种方法是利用甲烷催化还原NOx。已知:
CH4(g)+4NO2(g)=4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
CH4(g)+4NO(g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
则甲烷直接将NO2还原为N2的热化学方程式为
(2)全钒氧化还原液流电池,是目前发展势头强劲的优秀绿色环保储能电池。其电池总反应为:V3++VO2++H2O
 VO2++ 2H++V2+。
VO2++ 2H++V2+。充电过程中,H+向
(3)降低汽车尾气的方法之一是在排气管上安装催化转化器,发生如下反应:
2NO(g)+2CO(g)
 N2(g)+2CO2(g);△H<0。
N2(g)+2CO2(g);△H<0。该反应的化学平衡常数表达式为K=

若在一定温度下,将2molNO、1molCO充入1L固定容积的容器中,反应过程中各物质的浓度变化如上图所示。若保持温度不变,20min时再向容器中充入CO、N2各0.6mol,平衡将
20min时,若改变反应条件,导致N2浓度发生如上图所示的变化,则改变的条件可能是
①加入催化剂 ②降低温度 ③缩小容器体积 ④增加CO2的量
(4)利用Fe2+、Fe3+的催化作用,常温下将SO2转化为SO42-而实现SO2的处理(总反应为2SO2+O2+2H2O=2H2SO4)。已知,含SO2的废气通入含Fe2+、Fe3+的溶液时,其中一个反应的离子方程式为4Fe2+ + O2+ 4H+ = 4Fe3+ + 2H2O,则另一反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】课本里介绍的合成氨技术叫哈伯法,是德国诺贝尔化学奖获得者哈伯发明的。其合成原理为:N2(g)+3H2(g) 2NH3(g) ;△H <0
2NH3(g) ;△H <0
(1)下列关于工业合成氨的说法不正确的是______ 。
A.因为△H <0,所以该反应一定不需要加热
B.高压有利于氨气的生成
C.在高温下进行是为了提高反应物的转化率
D.使用催化剂加快反应速率是因为催化剂降低了反应的△H
(2)在恒温恒容密闭容器中进行合成氨的反应,下列能说明该反应已达到平衡状态的是_____ 。
a.容器内N2、H2、 NH3的浓度之比为1:3:2
b.v正(N2)=v逆(H2)
c.容器内压强保持不变
d.合气体的密度保持不变
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示H2物质的量)。

①图象中T2和T1的关系是: T2____ T1(填“>,<或=”,下同)
②a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是____ (填字母)。
(4)恒温下,往一个4 L的密闭容器中充入5.2 mol H2和 2 mol N2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
①此条件下该反应的氢气平衡浓度为______ 。
②若维持容器体积不变,温度不变,往原平衡体系中加入H2、 N2和NH3各 4mol,化学平衡将向__ 反应方向移动(填 “正”或“逆”)。
③N2(g)+3H2(g) 2NH3(g) ;△H =-92 kJ/mol。在恒温恒容的密闭容器中充入1 mol N2和一定量的H2发生反应。达到平衡后,测得反应放出的热量为18.4 kJ,混合气体的物质的量为3.6 mol,容器内的压强变为原来的90%,则起始时充入的H2的物质的量为
2NH3(g) ;△H =-92 kJ/mol。在恒温恒容的密闭容器中充入1 mol N2和一定量的H2发生反应。达到平衡后,测得反应放出的热量为18.4 kJ,混合气体的物质的量为3.6 mol,容器内的压强变为原来的90%,则起始时充入的H2的物质的量为_____ mol。
(5)已知:N2(g)+3H2(g) 2NH3(g) ;△H =-92 kJ/mol。
2NH3(g) ;△H =-92 kJ/mol。
N2(g) +O2(g) = 2NO(g) △H= +181 kJ/mol
2H2(g)+O2(g)= 2H2O(g) △H= -484 kJ/mol
写出氨气催化氧化生成NO和水蒸气的热化学方程式_____ 。
 2NH3(g) ;△H <0
2NH3(g) ;△H <0(1)下列关于工业合成氨的说法不正确的是
A.因为△H <0,所以该反应一定不需要加热
B.高压有利于氨气的生成
C.在高温下进行是为了提高反应物的转化率
D.使用催化剂加快反应速率是因为催化剂降低了反应的△H
(2)在恒温恒容密闭容器中进行合成氨的反应,下列能说明该反应已达到平衡状态的是
a.容器内N2、H2、 NH3的浓度之比为1:3:2
b.v正(N2)=v逆(H2)
c.容器内压强保持不变
d.合气体的密度保持不变
(3)某科研小组研究:在其他条件不变的情况下,改变起始物氢气的物质的量对工业合成氨反应的影响。实验结果如图所示(图中T表示温度,n表示H2物质的量)。

①图象中T2和T1的关系是: T2
②a、b、c、d四点所处的平衡状态中,反应物N2的转化率最高的是
(4)恒温下,往一个4 L的密闭容器中充入5.2 mol H2和 2 mol N2,反应过程中对NH3的浓度进行检测,得到的数据如下表所示:
| 时间/min | 5 | 10 | 15 | 20 | 25 | 30 |
| c(NH3)/mol·L-1 | 0.08 | 0.14 | 0.18 | 0.20 | 0.20 | 0.20 |
①此条件下该反应的氢气平衡浓度为
②若维持容器体积不变,温度不变,往原平衡体系中加入H2、 N2和NH3各 4mol,化学平衡将向
③N2(g)+3H2(g)
 2NH3(g) ;△H =-92 kJ/mol。在恒温恒容的密闭容器中充入1 mol N2和一定量的H2发生反应。达到平衡后,测得反应放出的热量为18.4 kJ,混合气体的物质的量为3.6 mol,容器内的压强变为原来的90%,则起始时充入的H2的物质的量为
2NH3(g) ;△H =-92 kJ/mol。在恒温恒容的密闭容器中充入1 mol N2和一定量的H2发生反应。达到平衡后,测得反应放出的热量为18.4 kJ,混合气体的物质的量为3.6 mol,容器内的压强变为原来的90%,则起始时充入的H2的物质的量为(5)已知:N2(g)+3H2(g)
 2NH3(g) ;△H =-92 kJ/mol。
2NH3(g) ;△H =-92 kJ/mol。N2(g) +O2(g) = 2NO(g) △H= +181 kJ/mol
2H2(g)+O2(g)= 2H2O(g) △H= -484 kJ/mol
写出氨气催化氧化生成NO和水蒸气的热化学方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】近年来全国各地长期被雾霾笼罩,雾霾颗粒中汽车尾气占20%以上。已知汽车尾气中的主要污染物为NOx、CO、超细颗粒(PM2.5)等有害物质。目前,已研究出了多种消除汽车尾气污染的方法。
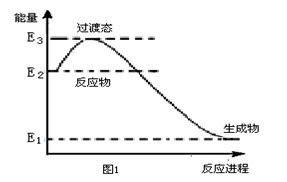
(1)催化剂存在时用H2将NO还原为N2。 图1是一定条件下H2还原NO生成N2和1 mol水蒸气的能量变化示意图, 写出该反应的热化学方程式__________ 。(ΔH 用E1、E2、E3表示)
(2)工业上可采用CO和H2合成甲醇,发生反应为(I)CO(g)+2H2(g) CH3OH(g) △H<0
CH3OH(g) △H<0
在恒容密闭容器里按体积比为1∶2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是__________ 。
A.正反应速率先增大后减小
B.逆反应速率先增大后减小
C.化学平衡常数K值增大
D.反应物的体积百分含量增大
E.混合气体的密度减小
F.氢气的转化率减小
(3)在汽车上安装三元催化转化器可实现反应:(Ⅱ)2NO(g)+2CO(g) N2(g)+2CO2(g) △H<0 。则该反应在
N2(g)+2CO2(g) △H<0 。则该反应在_______ (填“高温”、“低温”或“任何温度”)下能自发进行。
(4)将NO和CO以一定的流速通过两种不同的催化剂进行反应(Ⅱ),经过相同时间内测量逸出气体中NO的含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图2所示。
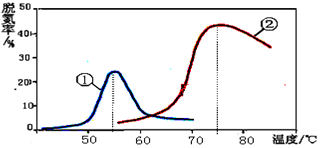
以下说法正确的是_______
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.曲线①、②最高点表示此时平衡转化率最高
D.两种催化剂分别适宜于55℃和75℃左右脱氮
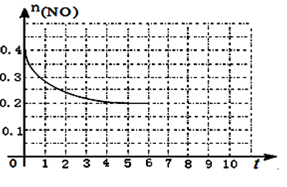
(5)在某温度下,2 L密闭容器中充入NO、CO各0.4 mol进行反应(Ⅱ),测得NO物质的量变化如图3所示,5分钟末反应达到平衡,该反应的平衡常数K=__________ ,第6分钟向容器中继续加入0.2 mol NO、0.2 mol CO、0.2 mol CO2和0.3 mol N2,请在图3中画出到9分钟末反应达到平衡NO的物质的量随时间的变化曲线。 ______________
(6)NOx是大气污染物之一,科学家们在尝试用更科学的方法将NOx脱氮转化成无毒的N2,减少对大气的污染。下列物质可能作为脱氮剂的是_______
A.NH3 B.CH4 C.KMnO4 D.尿素

(1)催化剂存在时用H2将NO还原为N2。 图1是一定条件下H2还原NO生成N2和1 mol水蒸气的能量变化示意图, 写出该反应的热化学方程式
(2)工业上可采用CO和H2合成甲醇,发生反应为(I)CO(g)+2H2(g)
 CH3OH(g) △H<0
CH3OH(g) △H<0在恒容密闭容器里按体积比为1∶2充入一氧化碳和氢气,一定条件下反应达到平衡状态。当改变反应的某一个条件后,下列变化能说明平衡一定向正反应方向移动的是
A.正反应速率先增大后减小
B.逆反应速率先增大后减小
C.化学平衡常数K值增大
D.反应物的体积百分含量增大
E.混合气体的密度减小
F.氢气的转化率减小
(3)在汽车上安装三元催化转化器可实现反应:(Ⅱ)2NO(g)+2CO(g)
 N2(g)+2CO2(g) △H<0 。则该反应在
N2(g)+2CO2(g) △H<0 。则该反应在(4)将NO和CO以一定的流速通过两种不同的催化剂进行反应(Ⅱ),经过相同时间内测量逸出气体中NO的含量,从而确定尾气脱氮率(脱氮率即NO的转化率),结果如图2所示。

图2
以下说法正确的是
A.第②种催化剂比第①种催化剂脱氮率高
B.相同条件下,改变压强对脱氮率没有影响
C.曲线①、②最高点表示此时平衡转化率最高
D.两种催化剂分别适宜于55℃和75℃左右脱氮
(5)在某温度下,2 L密闭容器中充入NO、CO各0.4 mol进行反应(Ⅱ),测得NO物质的量变化如图3所示,5分钟末反应达到平衡,该反应的平衡常数K=

图3
(6)NOx是大气污染物之一,科学家们在尝试用更科学的方法将NOx脱氮转化成无毒的N2,减少对大气的污染。下列物质可能作为脱氮剂的是
A.NH3 B.CH4 C.KMnO4 D.尿素
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】最近几年我国已加大对氮氧化物排放的控制力度。消除氮氧化物污染有多种方法。
(l)用CH4还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
②CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
③H2O(g)= H2O(l) △H=-44.0kJ·mol-1
CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式为_________________ 。
(2)用活性炭还原法也可处理氮氧化物。有关反应为:2C(s)+2NO2(g)=N2(g)+2CO2(g) △H<0,起始时向密闭容器中充入一定量的C(s)和NO2(g),在不同条件下,测得各物质的浓度变化状况如下图所示。

①0〜10min内,以CO2表示的平均反应速率v(CO2)=_______________ 。
②0~10min,10〜20 min,30〜40 min三个阶段NO2的转化率分别为α1、α2、α3,其中最小的为_________ ,其值是___________________ 。
③计算反应达到第一次平衡时的平衡常数K=____________ 。
④第10min时,若只改变了影响反应的一个条件,则改变的条件为______ (填选项字母)。
A.增加C(s)的量 B.减小容器体积 C.加入催化剂
⑤20~30min、40〜50 min时体系的温度分别为T1和T2,则T1_____ T2(填“> “<”或“=”), 判断的理由是_________________________ 。
(l)用CH4还原氮氧化物可以消除氮氧化物的污染。已知:
①CH4(g)+4NO2(g)= 4NO(g)+CO2(g)+2H2O(g) △H=-574kJ·mol-1
②CH4(g)+4NO (g)=2N2(g)+CO2(g)+2H2O(g) △H=-1160kJ·mol-1
③H2O(g)= H2O(l) △H=-44.0kJ·mol-1
CH4(g)与NO2(g)反应生成N2(g)、CO2(g)和H2O(1)的热化学方程式为
(2)用活性炭还原法也可处理氮氧化物。有关反应为:2C(s)+2NO2(g)=N2(g)+2CO2(g) △H<0,起始时向密闭容器中充入一定量的C(s)和NO2(g),在不同条件下,测得各物质的浓度变化状况如下图所示。

①0〜10min内,以CO2表示的平均反应速率v(CO2)=
②0~10min,10〜20 min,30〜40 min三个阶段NO2的转化率分别为α1、α2、α3,其中最小的为
③计算反应达到第一次平衡时的平衡常数K=
④第10min时,若只改变了影响反应的一个条件,则改变的条件为
A.增加C(s)的量 B.减小容器体积 C.加入催化剂
⑤20~30min、40〜50 min时体系的温度分别为T1和T2,则T1
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】甲醇是重要的化工原料,研究甲醇的制备及用途在工业上有重要的意义
(1)一种重要的工业制备甲醇的反应为
①

②
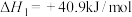
③

试计算 =
=_____  。
。
(2)对于反应 ,
, ,
, 。其中
。其中 、
、 分别为正、逆反应速率常数,
分别为正、逆反应速率常数, 为气体分压(分压
为气体分压(分压 物质的量分数
物质的量分数 总压)。在
总压)。在 下,分别按初始投料比
下,分别按初始投料比 ,
,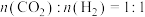 、
、 进行反应,测得
进行反应,测得 的平衡转化率随压强变化的关系如图所示:
的平衡转化率随压强变化的关系如图所示:

①投料比 的曲线是
的曲线是_____ 。(填“ ”、“
”、“ ”或“
”或“ ”)
”)
②已知点 在曲线
在曲线 上,计算该温度下压强平衡常数
上,计算该温度下压强平衡常数
_____ 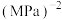 。(用平衡分压代替平衡浓度计算)
。(用平衡分压代替平衡浓度计算)
(3)甲醇催化制取丙烯的反应为: 。已知Arrhenius经验公式为
。已知Arrhenius经验公式为 (其中
(其中 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 为常数)。该反应的Arrhenius经验公式的实验数据如图所示:
为常数)。该反应的Arrhenius经验公式的实验数据如图所示:

①该反应的活化能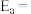
_____  。
。
②当用更高效催化剂时,请在图中画出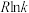 与
与 关系的曲线
关系的曲线_____ 。
(4)目前世界上一半以上的乙酸都采用甲醇与 反应来制备:
反应来制备: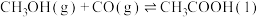
 。在恒压密闭容器中通入一定量的
。在恒压密闭容器中通入一定量的 和
和 气体,测得甲醇的转化率随温度变化关系如图所示:
气体,测得甲醇的转化率随温度变化关系如图所示:

①温度为 时,该反应的正反应速率
时,该反应的正反应速率
_____  (填“>”,“=”或“<”)。
(填“>”,“=”或“<”)。
② 、
、 、
、 三点逆反应速率由大到小的顺序为
三点逆反应速率由大到小的顺序为_____ 。[用“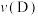 ”、“
”、“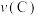 ”、“
”、“ ”表示]
”表示]
(1)一种重要的工业制备甲醇的反应为
①


②

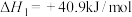
③


试计算
 =
= 。
。(2)对于反应
 ,
, ,
, 。其中
。其中 、
、 分别为正、逆反应速率常数,
分别为正、逆反应速率常数, 为气体分压(分压
为气体分压(分压 物质的量分数
物质的量分数 总压)。在
总压)。在 下,分别按初始投料比
下,分别按初始投料比 ,
,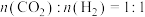 、
、 进行反应,测得
进行反应,测得 的平衡转化率随压强变化的关系如图所示:
的平衡转化率随压强变化的关系如图所示:
①投料比
 的曲线是
的曲线是 ”、“
”、“ ”或“
”或“ ”)
”)②已知点
 在曲线
在曲线 上,计算该温度下压强平衡常数
上,计算该温度下压强平衡常数
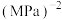 。(用平衡分压代替平衡浓度计算)
。(用平衡分压代替平衡浓度计算)(3)甲醇催化制取丙烯的反应为:
 。已知Arrhenius经验公式为
。已知Arrhenius经验公式为 (其中
(其中 为活化能,
为活化能, 为速率常数,
为速率常数, 和
和 为常数)。该反应的Arrhenius经验公式的实验数据如图所示:
为常数)。该反应的Arrhenius经验公式的实验数据如图所示:
①该反应的活化能
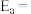
 。
。②当用更高效催化剂时,请在图中画出
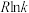 与
与 关系的曲线
关系的曲线(4)目前世界上一半以上的乙酸都采用甲醇与
 反应来制备:
反应来制备: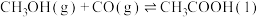
 。在恒压密闭容器中通入一定量的
。在恒压密闭容器中通入一定量的 和
和 气体,测得甲醇的转化率随温度变化关系如图所示:
气体,测得甲醇的转化率随温度变化关系如图所示:
①温度为
 时,该反应的正反应速率
时,该反应的正反应速率
 (填“>”,“=”或“<”)。
(填“>”,“=”或“<”)。②
 、
、 、
、 三点逆反应速率由大到小的顺序为
三点逆反应速率由大到小的顺序为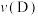 ”、“
”、“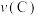 ”、“
”、“ ”表示]
”表示]
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】碳的化合物在工业上应用广泛,下面有几种碳的化合物的具体应用:
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+Cl2(g)=CH2ClCHClCH3(g) △H1=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2=CHCH2C1(g)+HCl(g) △H2=-100kJ·mol-1
在相同条件下,CH2=CHCH2Cl(g)+HCl(g)=CH2ClCHClCH3(g)的正反应活化能Ea(正)为132kJ·mol-1,则逆反应的活化能Ea(逆)为_______ kJ·mol-1
(2)在一定条件下可发生分解反应:CH3CHO(g)=CH4(g)+CO(g)某温度下向恒容密闭容器中加入一定量CH3CHO,测得CH3CHO浓度随时间的变化如表所示:
①2~5min内用CH3CHO表示的该反应的平均反应速率为_______ 。
②一定温度下,在恒容密闭容器中充入一定量CH3CHO进行该反应,能判断反应已达到化学平衡状态的是_______ 。
A.CH4和CO的浓度比保持不变
B.容器中压强不再变化
C.4molC-H断裂同时1molC≡O生成
D.气体的密度保持不变
(3)在一密闭容器中,起始时向该容器中充入6molH2S和3molCH4,发生反应:CH4(g)+2H2S(g) CS2(g)+4H2(g)。在压强为0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如下图所示:
CS2(g)+4H2(g)。在压强为0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如下图所示:
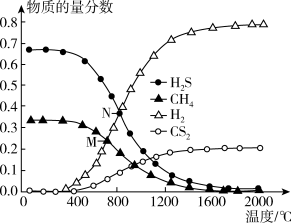
①该反应的△H_______ 0(填“>”或“<”)
②为提高H2S的平衡转化率,除改变温度外,还可采取的措施是_______ (列举一条)。N点对应温度下,该反应的Kp=_______ (MPa)2(Kp为以分压表示的平衡常数)。
(1)已知下列热化学方程式:
i.CH2=CHCH3(g)+Cl2(g)=CH2ClCHClCH3(g) △H1=-133kJ·mol-1
ii.CH2=CHCH3(g)+Cl2(g)=CH2=CHCH2C1(g)+HCl(g) △H2=-100kJ·mol-1
在相同条件下,CH2=CHCH2Cl(g)+HCl(g)=CH2ClCHClCH3(g)的正反应活化能Ea(正)为132kJ·mol-1,则逆反应的活化能Ea(逆)为
(2)在一定条件下可发生分解反应:CH3CHO(g)=CH4(g)+CO(g)某温度下向恒容密闭容器中加入一定量CH3CHO,测得CH3CHO浓度随时间的变化如表所示:
| t/min | 0 | 1 | 2 | 3 | 4 | 5 |
| c/(mol·L-1) | 1.00 | 0.71 | 0.50 | 0.35 | 0.25 | 0.17 |
②一定温度下,在恒容密闭容器中充入一定量CH3CHO进行该反应,能判断反应已达到化学平衡状态的是
A.CH4和CO的浓度比保持不变
B.容器中压强不再变化
C.4molC-H断裂同时1molC≡O生成
D.气体的密度保持不变
(3)在一密闭容器中,起始时向该容器中充入6molH2S和3molCH4,发生反应:CH4(g)+2H2S(g)
 CS2(g)+4H2(g)。在压强为0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如下图所示:
CS2(g)+4H2(g)。在压强为0.11MPa时,温度变化对平衡时产物的物质的量分数的影响如下图所示:
①该反应的△H
②为提高H2S的平衡转化率,除改变温度外,还可采取的措施是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】乙烷氧化脱氢制乙烯是石油化工的研究热点。羟基化氮化硼可高效催化乙烷氧化脱氢制乙烯,发生反应2C2H6(g)+O2(g)⇌2C2H4(g)+2H2O(g)△H。回答下列问题:
(1)已知:C2H6的燃烧热△H1=﹣1560 kJ/mol,C2H4的燃烧热△H2=﹣1411 kJ/mol,H2O(g) H2O(1)△H3=﹣44 kJ/mol,则△H=
H2O(1)△H3=﹣44 kJ/mol,则△H=___________ 。
(2)该反应分多步进行,其中的部分反应历程如图1所示(图中IS表示起始态,TS表示过渡态,FS表示终态)。这一部分反应中慢反应的能垒(活化能)E正=____ eV。


(3)向反应装置中按体积比1:1:4通入C2H6、O2和N2的混合气体,维持压强为0.1 MPa,反应t1min,测得乙烷转化率和乙烯选择性(乙烯选择性=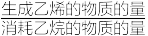 ×100%)随温度的变化如图2所示。
×100%)随温度的变化如图2所示。
①若想使乙烯的产率较高,应选择的反应温度是____ (填选项字母)。
A.570℃ B.585℃ C.600℃
②图2中,乙烷转化率____ (填“是”或“不是”)平衡转化率,判断依据是____ 。
③在580℃的条件下,进一步提高上述反应中C2H6的转化率的措施是____ (填选项字母)。
A.延长反应时间 B.增大O2的浓度 C.使用更高效的催化剂
④维持压强和投料比不变,在T℃(T>100)下反应t2min使反应达到平衡,若此时乙烷转化率为2a,乙烯选择性为100%,则该温度下反应2C2 H6(g)+O2(g)⇌2C2H4(g)+2H2O(g)的平衡常数Kp=____ MPa(Kp为以分压表示的平衡常数,分压=总压×物质的量分数。用含a的代数式表示,列出计算式即可)。
(1)已知:C2H6的燃烧热△H1=﹣1560 kJ/mol,C2H4的燃烧热△H2=﹣1411 kJ/mol,H2O(g)
 H2O(1)△H3=﹣44 kJ/mol,则△H=
H2O(1)△H3=﹣44 kJ/mol,则△H=(2)该反应分多步进行,其中的部分反应历程如图1所示(图中IS表示起始态,TS表示过渡态,FS表示终态)。这一部分反应中慢反应的能垒(活化能)E正=


(3)向反应装置中按体积比1:1:4通入C2H6、O2和N2的混合气体,维持压强为0.1 MPa,反应t1min,测得乙烷转化率和乙烯选择性(乙烯选择性=
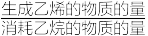 ×100%)随温度的变化如图2所示。
×100%)随温度的变化如图2所示。①若想使乙烯的产率较高,应选择的反应温度是
A.570℃ B.585℃ C.600℃
②图2中,乙烷转化率
③在580℃的条件下,进一步提高上述反应中C2H6的转化率的措施是
A.延长反应时间 B.增大O2的浓度 C.使用更高效的催化剂
④维持压强和投料比不变,在T℃(T>100)下反应t2min使反应达到平衡,若此时乙烷转化率为2a,乙烯选择性为100%,则该温度下反应2C2 H6(g)+O2(g)⇌2C2H4(g)+2H2O(g)的平衡常数Kp=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】有科学家正在研究用碳与一氧化氮反应处理环境问题。
C(s)+2NO(g) CO2(g)+N2(g)
CO2(g)+N2(g)
(1)在其它条件不变时,有下列措施:①加入固体C②使用催化剂③压缩容器容积增大压强④使CO2转化成干冰从体系中脱离,要提高NO的转化率,你认为可行的是____ 。
(2)这个反应的平衡常数表达式是____ ;
(3)在恒容恒温密闭容器中,科学家得到下列实验数据:
反应在该温度下的平衡常数K=____ ;
(4)若在(3)的实验中30min时开始升温,36min时达平衡,测得NO的转化率变为50%,则该反应的△H___ 0(填“>”、“<”、“=”),判断的理由是___ ;
(5)若科学家在30min后改变了某一条件,反应进行到40min时达平衡浓度分别为c(NO)=0.032mol/L,c(N2)=0.034mol/L,c(CO2)=0.017mol/L,则改变的条件可能是____ ,判断的依据是___ 。
C(s)+2NO(g)
 CO2(g)+N2(g)
CO2(g)+N2(g)(1)在其它条件不变时,有下列措施:①加入固体C②使用催化剂③压缩容器容积增大压强④使CO2转化成干冰从体系中脱离,要提高NO的转化率,你认为可行的是
(2)这个反应的平衡常数表达式是
(3)在恒容恒温密闭容器中,科学家得到下列实验数据:
| 时间(min) | 浓度(mol/L) | ||
| NO | N2 | CO2 | |
| 0 | 0.100 | 0 | 0 |
| 10 | 0.058 | 0.021 | 0.021 |
| 20 | 0.040 | 0.030 | 0.030 |
| 30 | 0.040 | 0.030 | 0.030 |
反应在该温度下的平衡常数K=
(4)若在(3)的实验中30min时开始升温,36min时达平衡,测得NO的转化率变为50%,则该反应的△H
(5)若科学家在30min后改变了某一条件,反应进行到40min时达平衡浓度分别为c(NO)=0.032mol/L,c(N2)=0.034mol/L,c(CO2)=0.017mol/L,则改变的条件可能是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】碳及其化合物广泛存在于自然界。请回答下列问题:
(1)反应Ⅰ:Fe(s)+CO2(g) FeO(s)+CO(g) ΔH1平衡常数为K1
FeO(s)+CO(g) ΔH1平衡常数为K1
反应Ⅱ:Fe(s)+H2O(g) FeO(s)+H2(g) ΔH1平衡常数为K2
FeO(s)+H2(g) ΔH1平衡常数为K2
不同温度下,K1、K2的值如下表:
现有反应Ⅲ:H2(g)+CO2(g) CO(g)+H2O(g),结合上表数据,反应Ⅲ是
CO(g)+H2O(g),结合上表数据,反应Ⅲ是___ (填“放热”或“吸热”)反应,为提高CO2的转化率可采用措施有___ (写出任意两条)。
(2)已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g) C2H5OH(g)+3H2O(g) ∆H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。
C2H5OH(g)+3H2O(g) ∆H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。

①图1中投料比相同,温度从高到低的顺序为______ 。
②图2中m1、m2、m3从大到小的顺序为____ 。
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质化学名称为____ ,T4温度时,该反应平衡常数KP的计算式为____ 。
(3)工业上常用高浓度的 K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图:
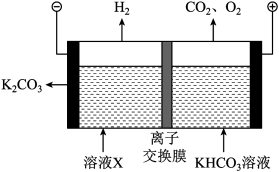
①在阳极区发生的反应包括____ 和H++HCO3- ==CO2↑+H2O
②简述CO32-在阴极区再生的原理:____ 。
(1)反应Ⅰ:Fe(s)+CO2(g)
 FeO(s)+CO(g) ΔH1平衡常数为K1
FeO(s)+CO(g) ΔH1平衡常数为K1反应Ⅱ:Fe(s)+H2O(g)
 FeO(s)+H2(g) ΔH1平衡常数为K2
FeO(s)+H2(g) ΔH1平衡常数为K2不同温度下,K1、K2的值如下表:
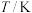 | 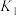 | 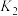 |
| 973 | 1.47 | 2.38 |
| 1173 | 2.15 | 1.67 |
现有反应Ⅲ:H2(g)+CO2(g)
 CO(g)+H2O(g),结合上表数据,反应Ⅲ是
CO(g)+H2O(g),结合上表数据,反应Ⅲ是(2)已知CO2催化加氢合成乙醇的反应原理为:2CO2(g)+6H2(g)
 C2H5OH(g)+3H2O(g) ∆H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。
C2H5OH(g)+3H2O(g) ∆H<0。设m为起始时的投料比,即m= n(H2)/ n(CO2)。
①图1中投料比相同,温度从高到低的顺序为
②图2中m1、m2、m3从大到小的顺序为
③图3表示在总压为5MPa的恒压条件下,且m=3时,平衡状态时各物质的物质的量分数与温度的关系。则曲线d代表的物质化学名称为
(3)工业上常用高浓度的 K2CO3溶液吸收CO2,得溶液X,再利用电解法使K2CO3溶液再生,其装置示意图如图:

①在阳极区发生的反应包括
②简述CO32-在阴极区再生的原理:
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】从低品位铜镍矿(含有Fe2O3、FeO、MgO、CuO等杂质)资源中提取镍和铜的一种工艺流程如下:
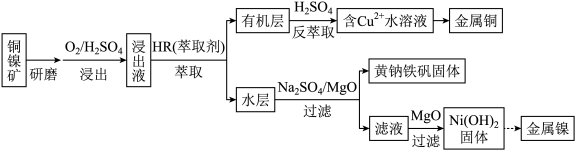
(1)上述流程中,加快反应速率的措施是_______ 。
(2)萃取时发生反应:Cu2+ + 2HR CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:
CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:_______ 。
(3)黄钠铁矾[NaFe3(OH)6(SO4)2]比Fe(OH)3更易形成沉淀。反应终点pH与Fe3+、Ni2+沉淀率的关系如下表。
① 生成黄钠铁矾的离子方程式是_______ 。
② 沉淀Fe3+时最适宜选用的反应终点pH是_______ 。
(4)第二次使用MgO调节pH使Ni2+沉淀完全,宜将pH调节至_______ (填序号)(已知Ksp[Ni(OH)2 ] = 2.1×10-15)。
a.6~7 b.9~10 c.11~12

(1)上述流程中,加快反应速率的措施是
(2)萃取时发生反应:Cu2+ + 2HR
 CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:
CuR2 + 2H+(HR、CuR2在有机层,Cu2+、H+等在水层)。解释反萃取时H2SO4的作用:(3)黄钠铁矾[NaFe3(OH)6(SO4)2]比Fe(OH)3更易形成沉淀。反应终点pH与Fe3+、Ni2+沉淀率的关系如下表。
| 反应终点pH | 沉淀率/% | |
| Fe3+ | Ni2+ | |
| 1.5 | 94.04 | 0.19 |
| 2.5 | 99.21 | 0.56 |
| 3.8 | 99.91 | 3.31 |
② 沉淀Fe3+时最适宜选用的反应终点pH是
(4)第二次使用MgO调节pH使Ni2+沉淀完全,宜将pH调节至
a.6~7 b.9~10 c.11~12
您最近一年使用:0次



