可乐中的食品添加剂有白砂糖、二氧化碳、焦糖色、磷酸、咖啡因等。可乐的辛辣味与磷酸(化学式为 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。
(1)室温下,测得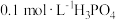 溶液的
溶液的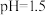 ,用电离方程式解释原因:
,用电离方程式解释原因:___________ 。
(2)羟基磷灰石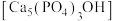 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: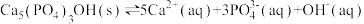 。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:___________ 。
(3)常温下,向磷酸溶液中滴加NaOH溶液,含磷微粒的分布比例与pH的关系如图所示。
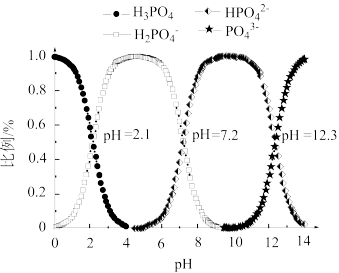
① 溶液显酸性。下列有关分析正确的是
溶液显酸性。下列有关分析正确的是___________ 。
a.溶液中
b. 的电离程度大于其水解程度
的电离程度大于其水解程度
c.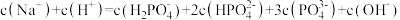
d.溶液中水的电离程度比纯水大
②当溶液的pH由4到10时,所发生反应的离子方程式是:___________ 。
(4)小组同学在实验室测定某可乐中磷酸的含量(不考虑白砂糖、咖啡因的影响)。
i.将可乐样品注入圆底烧瓶,加入活性炭,吸附色素。
ii.将可乐回流加热10 min,冷却至室温,过滤。
iii.取50.00 mL滤液,用百里香酚酞作指示剂,用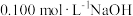 溶液滴定至终点时生成
溶液滴定至终点时生成 ,消耗NaOH溶液5.00 mL。
,消耗NaOH溶液5.00 mL。
①加热的目的是___________ 。
②该可乐样品中磷酸的含量为___________ g/L。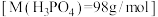
 ,沸点高难挥发)有一定关系。
,沸点高难挥发)有一定关系。(1)室温下,测得
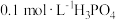 溶液的
溶液的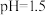 ,用电离方程式解释原因:
,用电离方程式解释原因:(2)羟基磷灰石
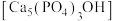 是牙釉质的主要成分,在唾液中存在平衡:
是牙釉质的主要成分,在唾液中存在平衡: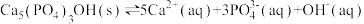 。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:
。 长期过量饮用可乐会破坏牙釉质,造成龋齿。结合平衡移动原理解释原因:(3)常温下,向磷酸溶液中滴加NaOH溶液,含磷微粒的分布比例与pH的关系如图所示。

①
 溶液显酸性。下列有关分析正确的是
溶液显酸性。下列有关分析正确的是a.溶液中

b.
 的电离程度大于其水解程度
的电离程度大于其水解程度c.
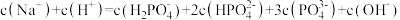
d.溶液中水的电离程度比纯水大
②当溶液的pH由4到10时,所发生反应的离子方程式是:
(4)小组同学在实验室测定某可乐中磷酸的含量(不考虑白砂糖、咖啡因的影响)。
i.将可乐样品注入圆底烧瓶,加入活性炭,吸附色素。
ii.将可乐回流加热10 min,冷却至室温,过滤。
iii.取50.00 mL滤液,用百里香酚酞作指示剂,用
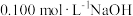 溶液滴定至终点时生成
溶液滴定至终点时生成 ,消耗NaOH溶液5.00 mL。
,消耗NaOH溶液5.00 mL。①加热的目的是
②该可乐样品中磷酸的含量为
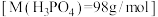
更新时间:2021-11-15 15:32:30
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
名校
解题方法
【推荐1】酸碱中和反应中溶液的 变化可用于各种研究
变化可用于各种研究
(1)用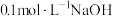 溶液分别滴定体积均为
溶液分别滴定体积均为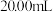 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。
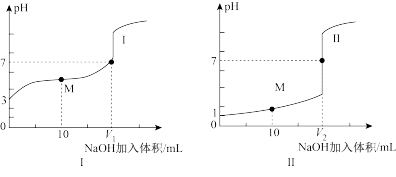
①滴定醋酸的曲线是①,判断理由是___________ 。
②滴定开始前,三种溶液中由水电离出的 最大的是
最大的是___________ (填化学式)。
③ 和
和 的关系:
的关系:
___________  (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。
(2)酸碱中和滴定可用于测定酸或碱的物质的量浓度,取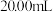 未知浓度的盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用
未知浓度的盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用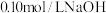 标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
①滴定达到终点的现象是___________ 。
②根据上述数据,可计算出该盐酸的浓度约为___________  (保留两位有效数字)。
(保留两位有效数字)。
③在上述实验中,下列操作会造成测定结果偏高的有___________ (填字母序号)。
A.滴定终点读数时俯视
B.锥形瓶水洗后未干燥
C.酸式滴定管使用前,水洗后未用待测盐酸润洗
D.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
E.碱式滴定管尖嘴部分有气泡,滴定后消失
 变化可用于各种研究
变化可用于各种研究(1)用
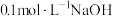 溶液分别滴定体积均为
溶液分别滴定体积均为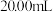 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。
①滴定醋酸的曲线是①,判断理由是
②滴定开始前,三种溶液中由水电离出的
 最大的是
最大的是③
 和
和 的关系:
的关系:
 (填“>”、“=”或“<”)。
(填“>”、“=”或“<”)。(2)酸碱中和滴定可用于测定酸或碱的物质的量浓度,取
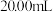 未知浓度的盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用
未知浓度的盐酸放入锥形瓶中,并滴加2~3滴酚酞作指示剂,用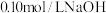 标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。| 实验编号 |  溶液的浓度( 溶液的浓度( ) ) | 滴定完成时, 溶液滴入的体积( 溶液滴入的体积( ) ) | 待测盐酸的体积( ) ) |
| 1 | 0.10 | 22.62 | 20.00 |
| 2 | 0.10 | 22.72 | 20.00 |
| 3 | 0.10 | 22.80 | 20.00 |
②根据上述数据,可计算出该盐酸的浓度约为
 (保留两位有效数字)。
(保留两位有效数字)。③在上述实验中,下列操作会造成测定结果偏高的有
A.滴定终点读数时俯视
B.锥形瓶水洗后未干燥
C.酸式滴定管使用前,水洗后未用待测盐酸润洗
D.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
E.碱式滴定管尖嘴部分有气泡,滴定后消失
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】成下列问题。
I.某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。
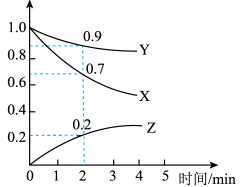
(1)由图中数据分析:该反应的化学方程式为___________ 。
(2)反应开始至2min,用Z表示的平均反应速率为___________ 。
II.回答下列有关水溶液的问题:
(3)写出下列物质的电离方程式:
NaHSO4___________
H2S___________
(4)下列两种溶液中,室温下由水电离生成的H+浓度之比(①:②)是___________ 。
①pH=1的盐酸 ②0.01mol·L-1的NaOH溶液
(5)已知在25℃和95℃时,水的电离平衡曲线如图所示:
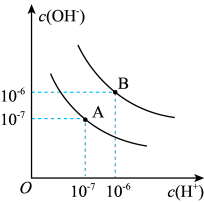
①在25℃时,水的电离平衡曲线应为________ (填“A”或“B”);95℃时水的离子积KW=______ 。
②25℃时,将pH=9的Ba(OH)2溶液与pH=4的H2SO4溶液混合,若冷却至25℃时所得混合溶液的pH=7,则Ba(OH)2溶液与H2SO4溶液的体积比为___________ 。
I.某温度时,在2L容器中,X、Y、Z三种物质的物质的量随时间变化的曲线如图所示。

(1)由图中数据分析:该反应的化学方程式为
(2)反应开始至2min,用Z表示的平均反应速率为
II.回答下列有关水溶液的问题:
(3)写出下列物质的电离方程式:
NaHSO4
H2S
(4)下列两种溶液中,室温下由水电离生成的H+浓度之比(①:②)是
①pH=1的盐酸 ②0.01mol·L-1的NaOH溶液
(5)已知在25℃和95℃时,水的电离平衡曲线如图所示:

①在25℃时,水的电离平衡曲线应为
②25℃时,将pH=9的Ba(OH)2溶液与pH=4的H2SO4溶液混合,若冷却至25℃时所得混合溶液的pH=7,则Ba(OH)2溶液与H2SO4溶液的体积比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】25℃时,测得溶液中微粒的 随
随 变化曲线如图(乙)所示,
变化曲线如图(乙)所示,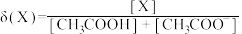 (X代表微粒为
(X代表微粒为 或者
或者 );用
);用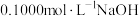 溶液滴定
溶液滴定 溶液,滴定曲线如图(甲);整个滴定过程中,忽略温度变化。
溶液,滴定曲线如图(甲);整个滴定过程中,忽略温度变化。

(1)图(乙)中曲线Ⅱ代表微粒为_______ ;醋酸电离平衡常数的数量级为_______ ,计算图(甲)A点溶液的
_______ (结果保留小数点后1位)。
(2)对图(甲)A点溶液加水稀释后,下列说法正确的是_________
(3)图(甲)A、B、C、D四点中,水的电离程度由小到大的顺序为_______ ,滴定过程中宜选用_______ 作酸碱指示剂。
(4)图(甲)C点溶液中离子浓度由大到小的顺序为_______ 。
(5)图(甲)D点溶液呈碱性的原因_______ (用离子方程式表示)。
 随
随 变化曲线如图(乙)所示,
变化曲线如图(乙)所示,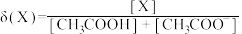 (X代表微粒为
(X代表微粒为 或者
或者 );用
);用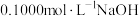 溶液滴定
溶液滴定 溶液,滴定曲线如图(甲);整个滴定过程中,忽略温度变化。
溶液,滴定曲线如图(甲);整个滴定过程中,忽略温度变化。
(1)图(乙)中曲线Ⅱ代表微粒为

(2)对图(甲)A点溶液加水稀释后,下列说法正确的是_________
A. 电离平衡常数增大 电离平衡常数增大 | B.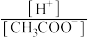 增大 增大 |
C.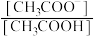 减小 减小 | D. 增大 增大 |
(4)图(甲)C点溶液中离子浓度由大到小的顺序为
(5)图(甲)D点溶液呈碱性的原因
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
【推荐1】含磷元素的化合物具有重要的性质和应用。
Ⅰ.亚磷酸( )是二元酸,与足量NaOH溶液反应生成
)是二元酸,与足量NaOH溶液反应生成 。
。
(1) 溶液中存在电离平衡:
溶液中存在电离平衡: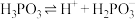 ,某温度下,
,某温度下, 的
的 溶液
溶液 ,即溶液中
,即溶液中 。求该温度下
。求该温度下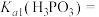
_______ 。( 的第二步电离忽略不计,结果保留两位有效数字。)
的第二步电离忽略不计,结果保留两位有效数字。)
Ⅱ.制备锂离子电池的正极材料的前体 的一种流程如下:
的一种流程如下:

资料:ⅰ.磷灰石的主要成分是
ⅱ. 可溶于水,
可溶于水, 微溶于水
微溶于水
ⅲ.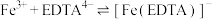
(2)制备
①用 溶液、
溶液、 溶液分步浸取磷灰石,生成HF、
溶液分步浸取磷灰石,生成HF、 和
和 ,主要反应是
,主要反应是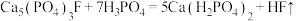 和
和_______ 。
②其他条件不变时,若仅用 溶液酸浸,浸取的速率低于用
溶液酸浸,浸取的速率低于用 、
、 分步浸取法,原因是
分步浸取法,原因是_______ 。
(3)制备
将 、
、 、
、 混合并调节溶液的pH制备
混合并调节溶液的pH制备 。
。
①酸性条件下,生成 的离子方程式是
的离子方程式是_______ 。
②各含磷微粒的物质的量分数与pH的关系如图。

 时,溶液中的
时,溶液中的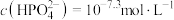 ,则
,则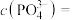
_______  。
。
③ 的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。研究表明,沉淀时可加入含
的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。研究表明,沉淀时可加入含 的溶液,可防止团聚,原因是
的溶液,可防止团聚,原因是_______ 。其他条件不变时,工业上选择 而不是更高的pH制备
而不是更高的pH制备 ,可能的原因是
,可能的原因是_______ (答出2点)。
Ⅰ.亚磷酸(
 )是二元酸,与足量NaOH溶液反应生成
)是二元酸,与足量NaOH溶液反应生成 。
。(1)
 溶液中存在电离平衡:
溶液中存在电离平衡: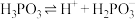 ,某温度下,
,某温度下, 的
的 溶液
溶液 ,即溶液中
,即溶液中 。求该温度下
。求该温度下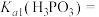
 的第二步电离忽略不计,结果保留两位有效数字。)
的第二步电离忽略不计,结果保留两位有效数字。) Ⅱ.制备锂离子电池的正极材料的前体
 的一种流程如下:
的一种流程如下:
资料:ⅰ.磷灰石的主要成分是

ⅱ.
 可溶于水,
可溶于水, 微溶于水
微溶于水ⅲ.
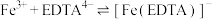
(2)制备

①用
 溶液、
溶液、 溶液分步浸取磷灰石,生成HF、
溶液分步浸取磷灰石,生成HF、 和
和 ,主要反应是
,主要反应是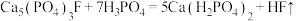 和
和②其他条件不变时,若仅用
 溶液酸浸,浸取的速率低于用
溶液酸浸,浸取的速率低于用 、
、 分步浸取法,原因是
分步浸取法,原因是(3)制备

将
 、
、 、
、 混合并调节溶液的pH制备
混合并调节溶液的pH制备 。
。①酸性条件下,生成
 的离子方程式是
的离子方程式是②各含磷微粒的物质的量分数与pH的关系如图。

 时,溶液中的
时,溶液中的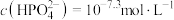 ,则
,则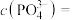
 。
。③
 的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。研究表明,沉淀时可加入含
的纯度及颗粒大小会影响其性能,沉淀速率过快容易团聚。研究表明,沉淀时可加入含 的溶液,可防止团聚,原因是
的溶液,可防止团聚,原因是 而不是更高的pH制备
而不是更高的pH制备 ,可能的原因是
,可能的原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】25℃时,部分物质的电离平衡常数如下表所示:
请回答下列问题。
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为___________ 。
(2)向0.1mol·L-1Na2CO3溶液中滴入酚酞溶液呈浅红色,其原因是___________ (用离子方程式表示),再将此溶液加热,溶液颜色___________ 。
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:___________ 。
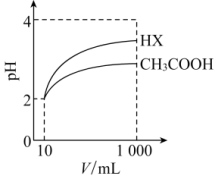
(4)10mLpH=2的醋酸与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数___________ (填“大于”“等于”或“小于”)醋酸的电离平衡常数,理由是___________ 。
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | Ka1=4.3×10-7 Ka2=5.6×10-11 | 4.7×10-8 |
(1)CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为
(2)向0.1mol·L-1Na2CO3溶液中滴入酚酞溶液呈浅红色,其原因是
(3)将少量CO2气体通入NaClO溶液中,写出反应的离子方程式:
(4)10mLpH=2的醋酸与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】请在标有序号的空白处填空:
(1)利用催化剂可使NO和CO发生反应:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)ΔH<0.已知增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面表中。
①请填全表中的各空格;
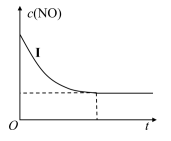
②实验Ⅰ中,NO的物质的量浓度(c)随时间(t)的变化如图所示。
请在给出的坐标图中画出实验Ⅱ、Ⅲ中NO的物质的量浓度(c)随时间(t)变化的曲线,并标明各曲线的实验编号_____ 。
(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=64.39kJ∙mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=196.46kJ∙mol-1
H2(g)+ O2(g)=H2O(l) ΔH=-285.84kJ∙mol-1
O2(g)=H2O(l) ΔH=-285.84kJ∙mol-1
在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为_____ .
(3)25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
①CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为_____ .
②体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数_____ (填“大于”、“等于”或“小于”)醋酸的电离平衡常数;理由是_____ .

(4)①求常温下pH=2的H2SO4溶液中由H2O电离的c(H+)和c(OH-).
c(H+)=_____ ,c(OH-)=_____ 。
②在某温度时,测得0.01mol∙L-1的NaOH溶液pH=11,在此温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合,若所得混合液为中性,且a+b=12,则Va:Vb=_____ 。
(1)利用催化剂可使NO和CO发生反应:2NO(g)+2CO(g)⇌2CO2(g)+N2(g)ΔH<0.已知增大催化剂的比表面积可提高化学反应速率.为了分别验证温度、催化剂的比表面积对化学反应速率的影响规律,某同学设计了三组实验,部分实验条件已经填在下面表中。
①请填全表中的各空格;
| 实验 编号 | T(℃) | NO初始浓度 (mol∙L-1) | CO初始浓度 (mol∙L-1) | 催化剂的比表 面积(m2∙g-1) |
| Ⅰ | 280 | 1.2×10-3 | 5.8×10-3 | 82 |
| Ⅱ | 1.2×10-3 | 124 | ||
| Ⅲ | 350 | 82 |
②实验Ⅰ中,NO的物质的量浓度(c)随时间(t)的变化如图所示。
请在给出的坐标图中画出实验Ⅱ、Ⅲ中NO的物质的量浓度(c)随时间(t)变化的曲线,并标明各曲线的实验编号

(2)用H2O2和H2SO4的混合溶液可溶出印刷电路板金属粉末中的铜.已知:
Cu(s)+2H+(aq)=Cu2+(aq)+H2(g) ΔH=64.39kJ∙mol-1
2H2O2(l)=2H2O(l)+O2(g) ΔH=196.46kJ∙mol-1
H2(g)+
 O2(g)=H2O(l) ΔH=-285.84kJ∙mol-1
O2(g)=H2O(l) ΔH=-285.84kJ∙mol-1在H2SO4溶液中Cu与H2O2反应生成Cu2+和H2O的热化学方程式为
(3)25℃时,部分物质的电离平衡常数如表所示:
| 化学式 | CH3COOH | H2CO3 | HClO |
| 电离平衡常数 | 1.7×10-5 | K1=4.3×10-7 K2=5.6×10-11 | 3.0×10-8 |
请回答下列问题:
①CH3COOH、H2CO3、HClO的酸性由强到弱的顺序为
②体积为10mLpH=2的醋酸溶液与一元酸HX分别加水稀释至1000mL,稀释过程中pH变化如图所示,则HX的电离平衡常数

(4)①求常温下pH=2的H2SO4溶液中由H2O电离的c(H+)和c(OH-).
c(H+)=
②在某温度时,测得0.01mol∙L-1的NaOH溶液pH=11,在此温度下,将pH=a的NaOH溶液VaL与pH=b的硫酸VbL混合,若所得混合液为中性,且a+b=12,则Va:Vb=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐1】电离平衡常数和电离度(电离度是指已电离的电解质分子数占原来总分子数的百分比)均可衡量弱电解质的电离,下表是常温下几种弱酸的电离平衡常数( )和弱碱的电离平衡常数(
)和弱碱的电离平衡常数( ),回答下列问题:
),回答下列问题:
(1) 的水溶液呈①
的水溶液呈①___________ (填“酸性”、“中性”或“碱性”),理由是(通过计算说明)②___________ ;溶液中各离子浓度大小关系是③___________ 。
(2) 的电离平衡常数表达式
的电离平衡常数表达式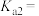
___________ ;
(3)常温下,浓度相同的四种溶液NaF、 、
、 、
、 ,pH由大到小的顺序是
,pH由大到小的顺序是___________ 。
(4)将过量 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为___________ 。
 )和弱碱的电离平衡常数(
)和弱碱的电离平衡常数( ),回答下列问题:
),回答下列问题:| 弱酸或弱碱 | HF |  |  |  |  |
| 电离平衡常数 | 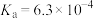 |  |   | 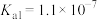 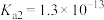 |  |
 的水溶液呈①
的水溶液呈①(2)
 的电离平衡常数表达式
的电离平衡常数表达式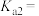
(3)常温下,浓度相同的四种溶液NaF、
 、
、 、
、 ,pH由大到小的顺序是
,pH由大到小的顺序是(4)将过量
 通入
通入 溶液中,反应的离子方程式为
溶液中,反应的离子方程式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】钠及其化合物具有广泛的用途。
(1)常温下,浓度均为0.1 mol/L的下列五种钠盐溶液的pH如表所示:
上述几种钠盐的阴离子,结合氢离子能力最强的是______ (填离子符号),根据表中数据,将浓度均为0.01mol/L的下列四种溶液分别稀释100倍,pH变化最大的是______ .(填字母)。
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)已知几种离子开始沉淀时溶液的pH如下表所示:
当向含有相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,________ (填离子符号)先沉淀;Ksp[Fe(OH)2]______ (填“>”“=”或“<”)Ksp[Mg(OH)2];要使0.2 mol/L的硫酸铜溶液中铜离子沉淀较为完全(使铜离子的浓度降至原来的千分之一),则应向溶液中加入氢氧化钠溶液使溶液pH=_______ 。{Cu(OH)2的Ksp=2×10-20。}
(1)常温下,浓度均为0.1 mol/L的下列五种钠盐溶液的pH如表所示:
| 溶质 | CH3COONa | NaHCO3 | Na2CO3 | NaClO | NaCN |
| pH | 8.8 | 9.7 | 11.6 | 10.3 | 11.1 |
上述几种钠盐的阴离子,结合氢离子能力最强的是
A.HCN B.HClO C.CH3COOH D.H2CO3
(2)已知几种离子开始沉淀时溶液的pH如下表所示:
| 离子 | Fe2+ | Cu2+ | Mg2+ |
| pH | 7.6 | 5.2 | 10.4 |
当向含有相同浓度的Cu2+、Mg2+、Fe2+的溶液中滴加氢氧化钠溶液时,
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐3】铜盐是五颜六色的。某学习小组发现固体 (白色)、固体
(白色)、固体 (棕黄色)、固体
(棕黄色)、固体 (深褐色)。
(深褐色)。 和
和 溶液呈蓝色,
溶液呈蓝色, 溶液时而呈绿色,时而呈蓝色,于是对颜色不同的原因展开了探究。
溶液时而呈绿色,时而呈蓝色,于是对颜色不同的原因展开了探究。
【查阅资料】
1.固体铜盐的颜色与阴离子极化能力有关,随化学键共价性增强,吸收光的能量下降,因此颜色加深。
2.在 溶液中存在如下平衡:
溶液中存在如下平衡:

【提出假设】
1.铜盐的颜色不同与离子种类有关。
2. 溶液呈绿色的原因是溶液中既有黄色的
溶液呈绿色的原因是溶液中既有黄色的 ,又有蓝色的
,又有蓝色的 ,根据光学原理蓝色和黄色的混合色为绿色。
,根据光学原理蓝色和黄色的混合色为绿色。
【设计方案】
回答下列问题:
(1)解释 的颜色深于
的颜色深于 的原因
的原因___________ 。
(2)配制 溶液的方法是
溶液的方法是___________ 。
(3)根据表中信息,补充试剂和数据:饱和___________ 、a=___________ 。
(4)实验4和5中溶液颜色差异的原因___________ (用平衡移动原理解释)。
(5)以上实验说明影响 溶液颜色的因素主要有
溶液颜色的因素主要有___________ 。(答两点即可)
【实验结论】假设1,2成立。
(6) 溶液呈现不同颜色的根本原因与
溶液呈现不同颜色的根本原因与 、
、 和
和___________ 微粒(写结构式)的浓度有关。
 (白色)、固体
(白色)、固体 (棕黄色)、固体
(棕黄色)、固体 (深褐色)。
(深褐色)。 和
和 溶液呈蓝色,
溶液呈蓝色, 溶液时而呈绿色,时而呈蓝色,于是对颜色不同的原因展开了探究。
溶液时而呈绿色,时而呈蓝色,于是对颜色不同的原因展开了探究。【查阅资料】
1.固体铜盐的颜色与阴离子极化能力有关,随化学键共价性增强,吸收光的能量下降,因此颜色加深。
2.在
 溶液中存在如下平衡:
溶液中存在如下平衡:
【提出假设】
1.铜盐的颜色不同与离子种类有关。
2.
 溶液呈绿色的原因是溶液中既有黄色的
溶液呈绿色的原因是溶液中既有黄色的 ,又有蓝色的
,又有蓝色的 ,根据光学原理蓝色和黄色的混合色为绿色。
,根据光学原理蓝色和黄色的混合色为绿色。【设计方案】
| 序号 | 温度/℃ | V( 氯化铜)/mL 氯化铜)/mL | V(饱和硫酸铜)/mL | V(饱和___________)/mL | V(饱和氯化钠)/mL | V(水)/mL | 溶液颜色 |
| 1 | 25 | 4.0 | 无色 | ||||
| 2 | 25 | 4.0 | 无色 | ||||
| 3 | 25 | 4.0 | 蓝色 | ||||
| 4 | 25 | 4.0 | 绿色 | ||||
| 5 | 25 | 2.0 | a | 蓝绿色 | |||
| 6 | 25 | 2.0 | 2.0 | 蓝绿色 | |||
| 7 | 25 | 2.0 | 2.0 | 黄绿色 | |||
| 8 | 50 | 4.0 | 黄绿色 |
(1)解释
 的颜色深于
的颜色深于 的原因
的原因(2)配制
 溶液的方法是
溶液的方法是(3)根据表中信息,补充试剂和数据:饱和
(4)实验4和5中溶液颜色差异的原因
(5)以上实验说明影响
 溶液颜色的因素主要有
溶液颜色的因素主要有【实验结论】假设1,2成立。
(6)
 溶液呈现不同颜色的根本原因与
溶液呈现不同颜色的根本原因与 、
、 和
和
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】捕集CO2的技术对解决全球温室效应意义重大。目前国际空间站处理CO2的一个重要方法是将CO2还原,涉及的化学反应如下:CO2(g)+4H2(g)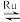 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)
完成下列填空:
(1)该反应的平衡常数表达式为________________________________ 。如果改变某种条件,平衡向正反应方向移动,则平衡常数________ (填写编号)。
a、一定增大 b、一定减小 c、可能增大 d、可能减小 e、可能不变
(2)为了提高CO2的捕获百分率,可采取的措施是____________________ 。(任写一条)
(3)向2L某密闭容器充入1mol CO2和4mol H2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为_______________ 。CO2还可应用于纯碱工业。工业生产纯碱的过程中,向饱和的氨化食盐水中通入足量CO2的生产环节又被称为“碳酸化”。
(4)碳酸化时产生的现象是____________________________ 。碳酸化过程中,溶液中c(CO32-)的变化情况为____________________ 。
(5)碳酸化后过滤,留在滤液中的阳离子主要有_______________ (填写化学式)。简述检验滤液中Cl- 离子的实验操作。________________________________
 CH4(g)+2H2O(g)+Q(Q>0)
CH4(g)+2H2O(g)+Q(Q>0)完成下列填空:
(1)该反应的平衡常数表达式为
a、一定增大 b、一定减小 c、可能增大 d、可能减小 e、可能不变
(2)为了提高CO2的捕获百分率,可采取的措施是
(3)向2L某密闭容器充入1mol CO2和4mol H2,一定条件下发生上述反应。5min末测得气体的物质的量减少了20%,则0~5min内CO2的平均反应速率为
(4)碳酸化时产生的现象是
(5)碳酸化后过滤,留在滤液中的阳离子主要有
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】以天然气为原料合成甲醇。有关热化学方程式如下:
①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②CO(g)+2H2(g) CH3OH(g) ΔH2
CH3OH(g) ΔH2
③2CH4(g)+O2(g) 2CH3OH(g) ΔH3=-251.0 kJ·mol-1
2CH3OH(g) ΔH3=-251.0 kJ·mol-1
(1)ΔH2=________ kJ·mol-1。
(2)在恒容密闭容器里,按物质的量比1:1加入一定量的碳和水蒸气反应生成水煤气。一定条件下达到平衡,当改变反应的某一条件时,下列变化能说明平衡一定向正反应方向移动的是_________ 。(填序号)
A.正反应速率先增大后减少 B.化学平衡常数K减少
B.化学平衡常数K减少
C.再加入一定量碳 D.反应物气体体积分数增大
D.反应物气体体积分数增大
(3)在体积可变的密闭容器中投入1molCO和2mol H2,在不同条件下发生反应:CO(g)+2H2(g) CH3OH(g)。实验测得CH3OH的物质的量随温度、压强的变化如下图所示。
CH3OH(g)。实验测得CH3OH的物质的量随温度、压强的变化如下图所示。

①该反应自发进行的条件是________ (填“低温”、“高温”或“任意温度”)
②506K时,反应平衡时H2的转化率为________ ;压强:p1________ (填“>”“<”或“=”)p2。
③反应速率:N点v正(CO)________ (填“>”“<”或“=”)M点v逆(CO)。
(4)已知常温下,H2A在水中存在以下平衡:H2A H++HA﹣,HA﹣
H++HA﹣,HA﹣ H++A2﹣,H2A的钙盐(CaA)饱和溶液中存在平衡:CaA(s)⇌Ca2+(aq)+A2﹣(aq)△H>0。
H++A2﹣,H2A的钙盐(CaA)饱和溶液中存在平衡:CaA(s)⇌Ca2+(aq)+A2﹣(aq)△H>0。
①温度升高时,Ksp________ (填“增大”、“减小”或“不变”下同)。
②滴加少量浓盐酸,c(Ca2+)________ 。
①2CH4(g)+O2(g)=2CO(g)+4H2(g) ΔH1=-70.8 kJ·mol-1
②CO(g)+2H2(g)
 CH3OH(g) ΔH2
CH3OH(g) ΔH2③2CH4(g)+O2(g)
 2CH3OH(g) ΔH3=-251.0 kJ·mol-1
2CH3OH(g) ΔH3=-251.0 kJ·mol-1(1)ΔH2=
(2)在恒容密闭容器里,按物质的量比1:1加入一定量的碳和水蒸气反应生成水煤气。一定条件下达到平衡,当改变反应的某一条件时,下列变化能说明平衡一定向正反应方向移动的是
A.正反应速率先增大后减少
 B.化学平衡常数K减少
B.化学平衡常数K减少C.再加入一定量碳
 D.反应物气体体积分数增大
D.反应物气体体积分数增大(3)在体积可变的密闭容器中投入1molCO和2mol H2,在不同条件下发生反应:CO(g)+2H2(g)
 CH3OH(g)。实验测得CH3OH的物质的量随温度、压强的变化如下图所示。
CH3OH(g)。实验测得CH3OH的物质的量随温度、压强的变化如下图所示。
①该反应自发进行的条件是
②506K时,反应平衡时H2的转化率为
③反应速率:N点v正(CO)
(4)已知常温下,H2A在水中存在以下平衡:H2A
 H++HA﹣,HA﹣
H++HA﹣,HA﹣ H++A2﹣,H2A的钙盐(CaA)饱和溶液中存在平衡:CaA(s)⇌Ca2+(aq)+A2﹣(aq)△H>0。
H++A2﹣,H2A的钙盐(CaA)饱和溶液中存在平衡:CaA(s)⇌Ca2+(aq)+A2﹣(aq)△H>0。①温度升高时,Ksp
②滴加少量浓盐酸,c(Ca2+)
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】工业上用含三价钒( )为主的某石煤为原料(含有
)为主的某石煤为原料(含有 、CaO等杂质),钙化法焙烧制备
、CaO等杂质),钙化法焙烧制备 ,其流程如下:
,其流程如下:

【资料】:+5价钒在溶液中的主要存在形式与溶液pH的关系:
(1)焙烧:向石煤中加生石灰焙烧,将 转化为
转化为 的化学方程式是
的化学方程式是_______ 。
(2)酸浸:
① 难溶于水,可溶于盐酸。若焙砂酸浸时溶液的
难溶于水,可溶于盐酸。若焙砂酸浸时溶液的 ,
, 溶于盐酸的离子方程式是
溶于盐酸的离子方程式是_______ 。
②酸度对钒和铝的溶解量的影响如图所示:
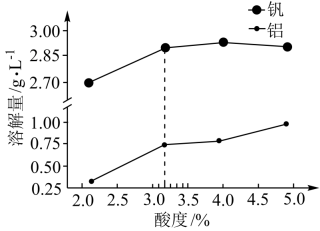
酸浸时溶液的酸度控制在大约3.2%,根据图推测,酸浸时不选择更高酸度的原因是_______ 。
(3)转沉:将浸出液中的钒转化为 固体,其流程如下:
固体,其流程如下:

①浸出液中加入石灰乳的作用是_______ 。
②已知 的溶解度小于
的溶解度小于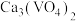 。向
。向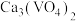 沉淀中加入
沉淀中加入 溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:
溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:_______ 。
③向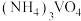 溶液中加入
溶液中加入 溶液,控制溶液的
溶液,控制溶液的 。当
。当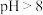 时,
时, 的产量明显降低,原因是
的产量明显降低,原因是_______ 。
(4)测定产品中 的纯度:称取ag产品,先用硫酸溶解,得到
的纯度:称取ag产品,先用硫酸溶解,得到 溶液。再加入
溶液。再加入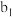 mL
mL 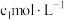
 溶液(
溶液(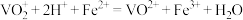 )。最后用
)。最后用 溶液滴定过量的
溶液滴定过量的 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 mL。已知
mL。已知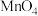 被还原为
被还原为 ,假设杂质不参与反应。则产品中
,假设杂质不参与反应。则产品中 的质量分数是
的质量分数是_______ 。( 的摩尔质量:
的摩尔质量: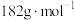 )
)
(5)全钒液流电池是具有发展前景的、用作储能系统的蓄电池,已知放电时 发生氧化反应,电池原理(电解液中含
发生氧化反应,电池原理(电解液中含 )如图:
)如图:
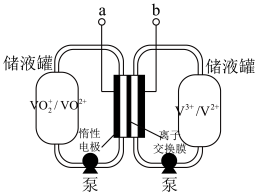
①a是_______ (填“正极”或“负极”)。
②该蓄电池反应方程式为_______ (标出“充电”“放电”方向)。
 )为主的某石煤为原料(含有
)为主的某石煤为原料(含有 、CaO等杂质),钙化法焙烧制备
、CaO等杂质),钙化法焙烧制备 ,其流程如下:
,其流程如下:
【资料】:+5价钒在溶液中的主要存在形式与溶液pH的关系:
| pH | 4~6 | 6~8 | 8~10 | 10~12 |
| 主要离子 |  |  |  |  |
 转化为
转化为 的化学方程式是
的化学方程式是(2)酸浸:
①
 难溶于水,可溶于盐酸。若焙砂酸浸时溶液的
难溶于水,可溶于盐酸。若焙砂酸浸时溶液的 ,
, 溶于盐酸的离子方程式是
溶于盐酸的离子方程式是②酸度对钒和铝的溶解量的影响如图所示:

酸浸时溶液的酸度控制在大约3.2%,根据图推测,酸浸时不选择更高酸度的原因是
(3)转沉:将浸出液中的钒转化为
 固体,其流程如下:
固体,其流程如下:
①浸出液中加入石灰乳的作用是
②已知
 的溶解度小于
的溶解度小于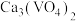 。向
。向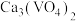 沉淀中加入
沉淀中加入 溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:
溶液,可使钒从沉淀中溶出。结合化学用语,用平衡移动原理解释其原因:③向
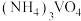 溶液中加入
溶液中加入 溶液,控制溶液的
溶液,控制溶液的 。当
。当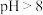 时,
时, 的产量明显降低,原因是
的产量明显降低,原因是(4)测定产品中
 的纯度:称取ag产品,先用硫酸溶解,得到
的纯度:称取ag产品,先用硫酸溶解,得到 溶液。再加入
溶液。再加入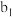 mL
mL 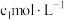
 溶液(
溶液(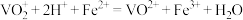 )。最后用
)。最后用 溶液滴定过量的
溶液滴定过量的 至终点,消耗
至终点,消耗 溶液的体积为
溶液的体积为 mL。已知
mL。已知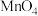 被还原为
被还原为 ,假设杂质不参与反应。则产品中
,假设杂质不参与反应。则产品中 的质量分数是
的质量分数是 的摩尔质量:
的摩尔质量: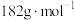 )
)(5)全钒液流电池是具有发展前景的、用作储能系统的蓄电池,已知放电时
 发生氧化反应,电池原理(电解液中含
发生氧化反应,电池原理(电解液中含 )如图:
)如图:
①a是
②该蓄电池反应方程式为
您最近一年使用:0次



