C、N、S的氧化物常会造成一些环境问题,科研工作者正在研究用各种化学方法来消除这些物质对环境的影响。
(1)已知:2C(s)+O2(g)=2CO(g) ΔH1=-221 kJ·mol-1
4Al(g)+3O2(g) =2Al2O3(s) ΔH2=-3351 kJ·mol-1
2Al(g)+N2(g)=2AlN(s) ΔH3=-318 kJ·mol-1
碳热还原Al2O3合成 AlN 的总热化学方程式是_______ ;
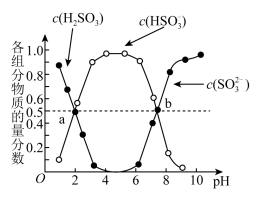
(2)“亚硫酸盐法”吸收烟气中的SO2,室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示。请写出a点时n(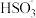 ):n(H2SO3)=
):n(H2SO3)=_______ ,b点时溶液pH=7,则n( ):n(
):n(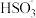 )=
)=_______ ;
(3)催化氧化法去除NO,一定条件下,用NH3消除NO污染,其反应原理为:4NH3+6NO 5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4∶l、3∶l、1∶3时,得到NO脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4∶l、3∶l、1∶3时,得到NO脱除率曲线如图所示:
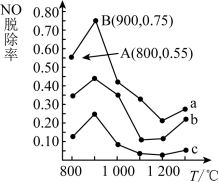
①曲线c对应NH3与NO的物质的量之比是_______ ,
②曲线a中NO的起始浓度为6×10-4 mg·m-3,从A点到B点经过0.8 s,该时间段内NO的脱除速率为_______ mg·m-3·s-1;
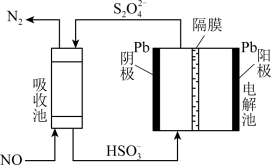
(4)间接电化学法可除NO。其原理如图所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性)_______ 。
(1)已知:2C(s)+O2(g)=2CO(g) ΔH1=-221 kJ·mol-1
4Al(g)+3O2(g) =2Al2O3(s) ΔH2=-3351 kJ·mol-1
2Al(g)+N2(g)=2AlN(s) ΔH3=-318 kJ·mol-1
碳热还原Al2O3合成 AlN 的总热化学方程式是
(2)“亚硫酸盐法”吸收烟气中的SO2,室温条件下,将烟气通入(NH4)2SO3溶液中,测得溶液pH与含硫组分物质的量分数的变化关系如图所示。请写出a点时n(
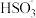 ):n(H2SO3)=
):n(H2SO3)= ):n(
):n(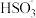 )=
)=
(3)催化氧化法去除NO,一定条件下,用NH3消除NO污染,其反应原理为:4NH3+6NO
 5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4∶l、3∶l、1∶3时,得到NO脱除率曲线如图所示:
5N2+6H2O。不同温度条件下,n(NH3):n(NO)的物质的量之比分别为4∶l、3∶l、1∶3时,得到NO脱除率曲线如图所示:
①曲线c对应NH3与NO的物质的量之比是
②曲线a中NO的起始浓度为6×10-4 mg·m-3,从A点到B点经过0.8 s,该时间段内NO的脱除速率为
(4)间接电化学法可除NO。其原理如图所示,写出电解池阴极的电极反应式(阴极室溶液呈酸性)

更新时间:2022-02-12 17:03:46
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
【推荐1】 是大气污染物,同时也是重要的化工原料,可用于制备硫酸。回答下列问题:
是大气污染物,同时也是重要的化工原料,可用于制备硫酸。回答下列问题:
(1) 在
在 作用下的催化氧化是工业上生产硫酸的主要反应,催化反应的机理如下。
作用下的催化氧化是工业上生产硫酸的主要反应,催化反应的机理如下。
第一步: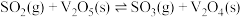
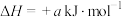
第二步: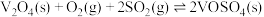
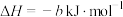
第三步: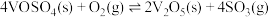
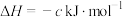
①写出 催化氧化的热化学方程式
催化氧化的热化学方程式___________ 。
②为研究①中 催化氧化的反应(
催化氧化的反应( ),某同学设计了如图三种已装固体
),某同学设计了如图三种已装固体 催化剂的密闭容器。
催化剂的密闭容器。
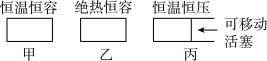
在初始体积与温度相同的条件下,甲、乙、丙中均按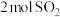 、
、 投料,达到平衡时,三个容器中
投料,达到平衡时,三个容器中 的转化率从大到小的顺序为
的转化率从大到小的顺序为___________ (用“甲、乙、丙”表示)。
(2)硝化法既能生产硫酸,也能处理 ,主要反应为
,主要反应为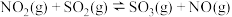
 。
。 时,向恒容密闭容器中加入等物质的量的
时,向恒容密闭容器中加入等物质的量的 和
和 ,达到平衡时NO和
,达到平衡时NO和 的物质的量浓度之比为
的物质的量浓度之比为 。
。 时,该反应的化学平衡常数为
时,该反应的化学平衡常数为___________ 。 时,向某容器中同时充入
时,向某容器中同时充入 、
、 、
、 、NO各1 mol,则此时
、NO各1 mol,则此时
___________  (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3) 可用NaOH溶液吸收。已知:常温下,
可用NaOH溶液吸收。已知:常温下, 的电离常数
的电离常数 ,
, 。常温下,
。常温下, 溶液显
溶液显___________ (填“酸”“碱”或“中”)性,结合方程式和计算说明原因___________ 。
(4)利用电化学方法将 转化为
转化为 的原理如图所示。
的原理如图所示。

①催化剂a表面的反应是___________ 。
②加入一定量水后停止进水,若左右两边得到的硫酸混合后质量分数仍为49%,则理论上参加反应的 与加入的
与加入的 的质量之比为
的质量之比为___________ 。
 是大气污染物,同时也是重要的化工原料,可用于制备硫酸。回答下列问题:
是大气污染物,同时也是重要的化工原料,可用于制备硫酸。回答下列问题:(1)
 在
在 作用下的催化氧化是工业上生产硫酸的主要反应,催化反应的机理如下。
作用下的催化氧化是工业上生产硫酸的主要反应,催化反应的机理如下。第一步:
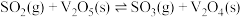
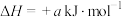
第二步:
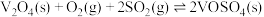
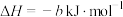
第三步:
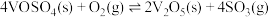
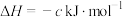
①写出
 催化氧化的热化学方程式
催化氧化的热化学方程式②为研究①中
 催化氧化的反应(
催化氧化的反应( ),某同学设计了如图三种已装固体
),某同学设计了如图三种已装固体 催化剂的密闭容器。
催化剂的密闭容器。
在初始体积与温度相同的条件下,甲、乙、丙中均按
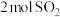 、
、 投料,达到平衡时,三个容器中
投料,达到平衡时,三个容器中 的转化率从大到小的顺序为
的转化率从大到小的顺序为(2)硝化法既能生产硫酸,也能处理
 ,主要反应为
,主要反应为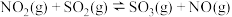
 。
。 时,向恒容密闭容器中加入等物质的量的
时,向恒容密闭容器中加入等物质的量的 和
和 ,达到平衡时NO和
,达到平衡时NO和 的物质的量浓度之比为
的物质的量浓度之比为 。
。 时,该反应的化学平衡常数为
时,该反应的化学平衡常数为 时,向某容器中同时充入
时,向某容器中同时充入 、
、 、
、 、NO各1 mol,则此时
、NO各1 mol,则此时
 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)
 可用NaOH溶液吸收。已知:常温下,
可用NaOH溶液吸收。已知:常温下, 的电离常数
的电离常数 ,
, 。常温下,
。常温下, 溶液显
溶液显(4)利用电化学方法将
 转化为
转化为 的原理如图所示。
的原理如图所示。
①催化剂a表面的反应是
②加入一定量水后停止进水,若左右两边得到的硫酸混合后质量分数仍为49%,则理论上参加反应的
 与加入的
与加入的 的质量之比为
的质量之比为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】醇类的制取是近年来研究的热点。通过CH3COOCH3为原料在催化剂作用下加氢可同时制取乙醇和甲醇,包括以下主要反应:
反应I:CH3COOCH3(g)+2H2(g)⇌C2H5OH(g)+CH3OH(g) △H1=-71kJ·mol-1
反应II:CH3COOCH3(g)+H2(g)⇌CH3CHO(g)+CH3OH(g) △H2
(1)查阅资料知:标准摩尔生成焓是指在25℃和101kPa时,由元素最稳定的单质生成lmol纯化合物时的焓变,符号为 。已知以下物质的标准摩尔生成焓如下表所示:
。已知以下物质的标准摩尔生成焓如下表所示:
则C2H5OH(g)的标准摩尔生成焓 =
=_______ kJ∙mol-1。
(2)将一定量的CH3OH与CH3CHO混合气体置于绝热恒容密闭容器中,只发生反应II,逆反应速率随时间变化的趋势如图所示(不考虑催化剂的影响),则反应II的△H2_______ 0(填“>”“<”或“=”);下列选项中一定能说明反应II达到平衡状态的是_______ (填序号)。
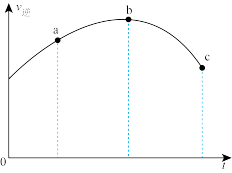
A.密闭体系的压强保持不变 B.甲醇与乙醛的分压之比不变
C.乙酸甲酯的体积分数保持不变 D.气体的平均摩尔质量保持不变
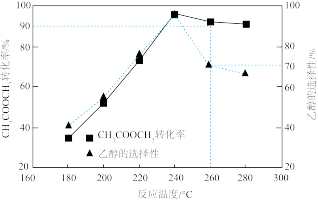
(3)一定条件下在1L密闭容器内通入一定量的CH3COOCH3和H2发生反应I和II,测得不同温度下达平衡时CH3COOCH3转化率和乙醇的选择性如图所示。温度高于240℃时,随温度升高乙醇的选择性降低的原因是_______ 。
(4)将物质的量均为amol的CH3COOCH3(g)和H2(g)分别加入恒温恒压的两个密闭容器甲(25℃、p1)、乙(25℃、p2)中,若只发生反应II,其正反应速率v正=k正·p(CH3COOCH3)·p(H2),p为物质分压,若容器甲与乙中平衡时正反应速率之比v甲:v乙=16:25,则甲、乙容器的体积之比为_______ 。
(5)一种以甲醇为原料,利用SnO2(mSnO2/CC)和CuO纳米片(CuONS/CF)作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示:
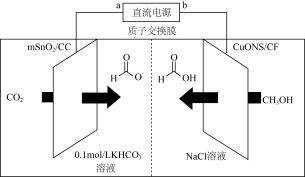
①若以Fe-Cu-浓硝酸构成的原电池为直流电源,则电极a应为_______ (填“Fe”或“Cu”)。电解过程中阳极上发生反应的电极反应式为_______ 。
②若有lmolH+通过质子交换膜时,则该装置生成HCOO-和HCOOH共计_______ mol。
反应I:CH3COOCH3(g)+2H2(g)⇌C2H5OH(g)+CH3OH(g) △H1=-71kJ·mol-1
反应II:CH3COOCH3(g)+H2(g)⇌CH3CHO(g)+CH3OH(g) △H2
(1)查阅资料知:标准摩尔生成焓是指在25℃和101kPa时,由元素最稳定的单质生成lmol纯化合物时的焓变,符号为
 。已知以下物质的标准摩尔生成焓如下表所示:
。已知以下物质的标准摩尔生成焓如下表所示:| 物质 | CH3COOCH3(g) | CH3CHO(g) |
 /kJ·mol-1 /kJ·mol-1 | -413 | -201 |
 =
=(2)将一定量的CH3OH与CH3CHO混合气体置于绝热恒容密闭容器中,只发生反应II,逆反应速率随时间变化的趋势如图所示(不考虑催化剂的影响),则反应II的△H2

A.密闭体系的压强保持不变 B.甲醇与乙醛的分压之比不变
C.乙酸甲酯的体积分数保持不变 D.气体的平均摩尔质量保持不变
(3)一定条件下在1L密闭容器内通入一定量的CH3COOCH3和H2发生反应I和II,测得不同温度下达平衡时CH3COOCH3转化率和乙醇的选择性如图所示。温度高于240℃时,随温度升高乙醇的选择性降低的原因是

(4)将物质的量均为amol的CH3COOCH3(g)和H2(g)分别加入恒温恒压的两个密闭容器甲(25℃、p1)、乙(25℃、p2)中,若只发生反应II,其正反应速率v正=k正·p(CH3COOCH3)·p(H2),p为物质分压,若容器甲与乙中平衡时正反应速率之比v甲:v乙=16:25,则甲、乙容器的体积之比为
(5)一种以甲醇为原料,利用SnO2(mSnO2/CC)和CuO纳米片(CuONS/CF)作催化电极,制备甲酸(甲酸盐)的电化学装置的工作原理如图所示:

①若以Fe-Cu-浓硝酸构成的原电池为直流电源,则电极a应为
②若有lmolH+通过质子交换膜时,则该装置生成HCOO-和HCOOH共计
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐3】碳和氮的氧化物的综合处理可以缓解环境压力,有利于加快实现“绿水青山”的目标。回答下列问题:
(1)一种利用一氧化碳脱硝的方法涉及如下反应:
ⅰ.2NO(g) N2(g)+O2(g) △H=-180kJ·mol-1
N2(g)+O2(g) △H=-180kJ·mol-1
ⅱ.2NO(g)+O2(g) 2NO2(g) △H=-98kJ·mol-1
2NO2(g) △H=-98kJ·mol-1
ⅲ.CO(g)+NO2(g) NO(g)+CO2(g) △H=-234kJ·mol-1
NO(g)+CO2(g) △H=-234kJ·mol-1
①一氧化碳与一氧化氮反应生成无污染气体的热化学方程式为___________ 。
②反应ⅲ的速率方程为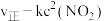 (k为只受温度影响的速率常数),则既能加快反应ⅲ的速率,又能增大
(k为只受温度影响的速率常数),则既能加快反应ⅲ的速率,又能增大 产量的措施是
产量的措施是___________ 。
③一定温度下,向 恒容密闭容器中充入
恒容密闭容器中充入 和
和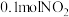 ,
, 末达到平衡。实验测得反应前容器内气体压强为
末达到平衡。实验测得反应前容器内气体压强为 ,平衡时容器内气体压强为
,平衡时容器内气体压强为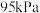 ,
, 的分压均为
的分压均为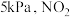 分压为
分压为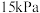 。则
。则 内平均反应速率
内平均反应速率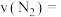
___________  ;反应ⅱ的平衡常数
;反应ⅱ的平衡常数
___________  (
( 是用分压表示的平衡常数)。
是用分压表示的平衡常数)。
④平衡体系中 的体积分数随温度的变化关系如图1所示。下列说法正确的是
的体积分数随温度的变化关系如图1所示。下列说法正确的是___________ (填选项字母)。
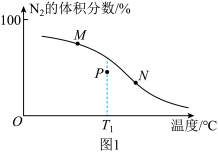
A.反应物的有效碰撞几率:
B.改变催化剂,可以提高 的平衡体积分数
的平衡体积分数
C.若在起始温度为 的绝热容器中重复实验,
的绝热容器中重复实验, 的平衡体积分数可能达到P点数值
的平衡体积分数可能达到P点数值
(2)实验证明:亚铁的氨酸鳌合物因对 有很强的络合活性前用于湿法脱硝,其原理为Fe(II)-EDTA+NO
有很强的络合活性前用于湿法脱硝,其原理为Fe(II)-EDTA+NO Fe(II)-EDTA(NO)。若体系中存在
Fe(II)-EDTA(NO)。若体系中存在 ,脱硝效率明显降低的原因为
,脱硝效率明显降低的原因为___________ ;避免脱硝效率降低的措施为___________ 。
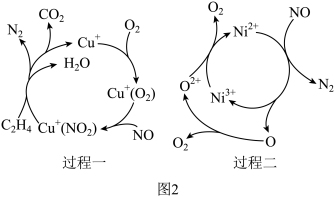
(3)我国科研工作者提出 脱除可通过如图2所示两种过程完成。实际生产中更适宜选择过程二的原因为
脱除可通过如图2所示两种过程完成。实际生产中更适宜选择过程二的原因为___________ 。
(1)一种利用一氧化碳脱硝的方法涉及如下反应:
ⅰ.2NO(g)
 N2(g)+O2(g) △H=-180kJ·mol-1
N2(g)+O2(g) △H=-180kJ·mol-1ⅱ.2NO(g)+O2(g)
 2NO2(g) △H=-98kJ·mol-1
2NO2(g) △H=-98kJ·mol-1ⅲ.CO(g)+NO2(g)
 NO(g)+CO2(g) △H=-234kJ·mol-1
NO(g)+CO2(g) △H=-234kJ·mol-1①一氧化碳与一氧化氮反应生成无污染气体的热化学方程式为
②反应ⅲ的速率方程为
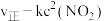 (k为只受温度影响的速率常数),则既能加快反应ⅲ的速率,又能增大
(k为只受温度影响的速率常数),则既能加快反应ⅲ的速率,又能增大 产量的措施是
产量的措施是③一定温度下,向
 恒容密闭容器中充入
恒容密闭容器中充入 和
和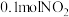 ,
, 末达到平衡。实验测得反应前容器内气体压强为
末达到平衡。实验测得反应前容器内气体压强为 ,平衡时容器内气体压强为
,平衡时容器内气体压强为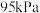 ,
, 的分压均为
的分压均为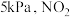 分压为
分压为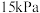 。则
。则 内平均反应速率
内平均反应速率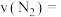
 ;反应ⅱ的平衡常数
;反应ⅱ的平衡常数
 (
( 是用分压表示的平衡常数)。
是用分压表示的平衡常数)。④平衡体系中
 的体积分数随温度的变化关系如图1所示。下列说法正确的是
的体积分数随温度的变化关系如图1所示。下列说法正确的是
A.反应物的有效碰撞几率:

B.改变催化剂,可以提高
 的平衡体积分数
的平衡体积分数C.若在起始温度为
 的绝热容器中重复实验,
的绝热容器中重复实验, 的平衡体积分数可能达到P点数值
的平衡体积分数可能达到P点数值(2)实验证明:亚铁的氨酸鳌合物因对
 有很强的络合活性前用于湿法脱硝,其原理为Fe(II)-EDTA+NO
有很强的络合活性前用于湿法脱硝,其原理为Fe(II)-EDTA+NO Fe(II)-EDTA(NO)。若体系中存在
Fe(II)-EDTA(NO)。若体系中存在 ,脱硝效率明显降低的原因为
,脱硝效率明显降低的原因为(3)我国科研工作者提出
 脱除可通过如图2所示两种过程完成。实际生产中更适宜选择过程二的原因为
脱除可通过如图2所示两种过程完成。实际生产中更适宜选择过程二的原因为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】Ⅰ.某温度时,在一个容积为2 L的密闭容器中,X、Y、Z三种物质的物质的量随时间的变化曲线如图1所示。根据图中数据,填写下列空白。

(1)该反应的化学方程式为________________________________________ 。
(2)反应开始至2 min,气体Z的平均反应速率v(Z)=________ 。
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的________ 倍。
②若此时将容器的体积缩小为原来的 ,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为________ (填“放热”或“吸热”)反应。
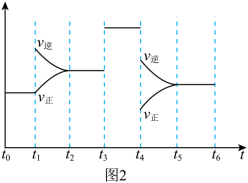
(4)上述反应在t1~t6内反应速率与时间图象如图2所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是 (填字母)。
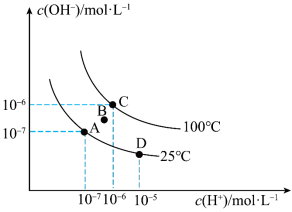
Ⅱ.已知水溶液中c(H+)和c(OH-)的关系如图所示:
(5)图中B点水的离子积常数___________ 10-12(填“>”、“=”或“<”)。
(6)从A点到D点,可采取的措施是___________ 。
a.升温 b.加入少量盐酸 c.降温 d.加入少量NaOH
(7)100℃时,pH=2的盐酸中水电离产生的H+浓度为___________ mol/L。
(8)25℃时,将pH=12的NaOH溶液与pH=3的H2SO4溶液混合,若所得混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为___________ 。

(1)该反应的化学方程式为
(2)反应开始至2 min,气体Z的平均反应速率v(Z)=
(3)若X、Y、Z均为气体,反应达到平衡时:
①压强是开始时的
②若此时将容器的体积缩小为原来的
 ,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为
,达到平衡时,容器内温度将升高(容器不与外界进行热交换),则该反应的正反应为(4)上述反应在t1~t6内反应速率与时间图象如图2所示,在每一时刻均改变一个影响反应速率的因素,则下列说法正确的是 (填字母)。

| A.在t1时增大了压强 | B.B.在t3时加入催化剂 |
| C.在t4时降低了温度 | D.t2~t3时X的转化率最高 |
Ⅱ.已知水溶液中c(H+)和c(OH-)的关系如图所示:

(5)图中B点水的离子积常数
(6)从A点到D点,可采取的措施是
a.升温 b.加入少量盐酸 c.降温 d.加入少量NaOH
(7)100℃时,pH=2的盐酸中水电离产生的H+浓度为
(8)25℃时,将pH=12的NaOH溶液与pH=3的H2SO4溶液混合,若所得混合溶液pH=7,则NaOH溶液与H2SO4溶液的体积比为
您最近一年使用:0次
【推荐2】一定温度下,在10L密闭容器中加入5molSO2和3molO2,发生反应2SO2(g)+O2(g)  2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。
2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。
(1)10分钟内v(SO2)=_______ 。
(2)平衡时SO3的浓度是_______ ,SO2的转化率是_______ 。
(3)平衡时容器内气体的总物质的量为_______ mol。
(4)物质的浓度不再改变标志着该反应已达平衡。下列还可以说明该反应已达平衡的是_______ (填序号)。
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3):n(O2):n(SO2)=2:1:2
(5)该温度下,SO3(g) SO3(g)+
SO3(g)+ O2(g)的平衡常数K=
O2(g)的平衡常数K=_______ 。
 2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。
2SO3(g),10min时,反应达到平衡状态,此时有3molSO2发生了反应。(1)10分钟内v(SO2)=
(2)平衡时SO3的浓度是
(3)平衡时容器内气体的总物质的量为
(4)物质的浓度不再改变标志着该反应已达平衡。下列还可以说明该反应已达平衡的是
①体系内压强不再改变
②容器内气体的密度不再改变
③混合气体的平均相对分子质量不再改变
④v正(SO3)=2v逆(O2)
⑤n(SO3):n(O2):n(SO2)=2:1:2
(5)该温度下,SO3(g)
 SO3(g)+
SO3(g)+ O2(g)的平衡常数K=
O2(g)的平衡常数K=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】为了探究反应速率的影响因素和反应限度,依据科学研究,对于多因素(变量)问题,常采用只改变某一个因素,控制其他因素不变的研究方法,某实验小组进行如下实验:
I.用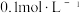 的硫代硫酸钠与
的硫代硫酸钠与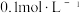 硫酸反应,实验数据如表1:
硫酸反应,实验数据如表1:
表1
(1)表1中V1=_______ ,V3=_______ ,t的取值范围是_______ (填标号)。
a.<15 b.1 5~20 c.>20
Ⅱ.取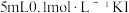 溶液于试管中,并加入5~6滴
溶液于试管中,并加入5~6滴 溶液,充分反应,将反应后的溶液分成两等份。一份继续滴加5~6滴淀粉溶液,溶液变蓝;另一份继续滴加2mL CCl4充分振荡,取出上层清液,滴入2 滴KSCN溶液,观察到溶液变红。
溶液,充分反应,将反应后的溶液分成两等份。一份继续滴加5~6滴淀粉溶液,溶液变蓝;另一份继续滴加2mL CCl4充分振荡,取出上层清液,滴入2 滴KSCN溶液,观察到溶液变红。
(2)根据上述实验现象,写出KI溶液与FeCl3溶液反应的离子方程式:_______ ;“取出上层清液,滴入2滴KSCN溶液,观察到溶液变红[产生了Fe(SCN)3]”描述中发生反应的离子方程式为_______ 。
Ⅲ.在500℃和101kPa条件下,将一定量的SO2和O2充入含有催化剂的密闭容器中,传感器测得各组分浓度随时间变化如表2:
表2
(3)c1=_______ ,0~40s内, 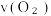 =
= _____ mol·L-1·min-1
(4)反应达到平衡时,SO3的体积分数为_____ (保留3位有效数字)。
I.用
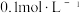 的硫代硫酸钠与
的硫代硫酸钠与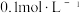 硫酸反应,实验数据如表1:
硫酸反应,实验数据如表1:表1
| 编号 | Na2S2O3体积/mL | 加水的体积/mL | 硫酸体积/mL | 水浴温度/℃ | 出现浑浊用时/s |
| 1 | 2 | 1 | 2 | 25 | 15 |
| 2 | 1 | V1 | 2 | 25 | 20 |
| 3 | 2 | V2 | V3 | 35 | t |
a.<15 b.1 5~20 c.>20
Ⅱ.取
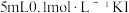 溶液于试管中,并加入5~6滴
溶液于试管中,并加入5~6滴 溶液,充分反应,将反应后的溶液分成两等份。一份继续滴加5~6滴淀粉溶液,溶液变蓝;另一份继续滴加2mL CCl4充分振荡,取出上层清液,滴入2 滴KSCN溶液,观察到溶液变红。
溶液,充分反应,将反应后的溶液分成两等份。一份继续滴加5~6滴淀粉溶液,溶液变蓝;另一份继续滴加2mL CCl4充分振荡,取出上层清液,滴入2 滴KSCN溶液,观察到溶液变红。(2)根据上述实验现象,写出KI溶液与FeCl3溶液反应的离子方程式:
Ⅲ.在500℃和101kPa条件下,将一定量的SO2和O2充入含有催化剂的密闭容器中,传感器测得各组分浓度随时间变化如表2:
表2
| 反应时间/s | 0 | 10 | 20 | 30 | 40 | 50 | 60 |
| c(SO2)/(mol·L-1) | 10 | c1 | 5 | 3.5 | 2.5 | c2 | c2 |
| c(O2)/(mol·L-1) | 5 | 3.5 | 2.5 | 1.75 | c3 | 1 | 1 |
| c(SO3)/(mol·L-1) | 0 | 3 | 5 | 6.5 | 7.5 | 8 | 8 |
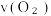 =
= (4)反应达到平衡时,SO3的体积分数为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】硒(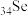 )与人类的健康密切相关。硒元素的发现已有200多年,人们对硒的认识已经进入全新阶段。
)与人类的健康密切相关。硒元素的发现已有200多年,人们对硒的认识已经进入全新阶段。
(1) 元素原子结构示意图为:
元素原子结构示意图为:_______ 。
(2) 、
、 、
、 三种氢化物的稳定性大小顺序是
三种氢化物的稳定性大小顺序是_______ ,其中还原性最强的是_______ 。
下表是O、S、 、
、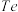 四种元素单质分别与
四种元素单质分别与 反应生成1mol气态氢化物的反应热,其中表示生成1mol硒化氢反应热的是
反应生成1mol气态氢化物的反应热,其中表示生成1mol硒化氢反应热的是_______ (填字母代号)。
(3)工业上用浓 焙烧
焙烧 的方法提取硒,反应产生
的方法提取硒,反应产生 、
、 的混合气体,写出反应的化学方程式
的混合气体,写出反应的化学方程式_______ 。理论上该反应每转移1mol电子,可得到 的质量为
的质量为_______ g。(保留一位小数)
(4)已知硒酸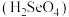 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: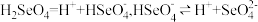 。
。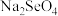 溶液的离子浓度由大到小的顺序为
溶液的离子浓度由大到小的顺序为_______ , 与
与 两种元素的守恒关系为:
两种元素的守恒关系为: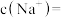
_______ 。
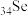 )与人类的健康密切相关。硒元素的发现已有200多年,人们对硒的认识已经进入全新阶段。
)与人类的健康密切相关。硒元素的发现已有200多年,人们对硒的认识已经进入全新阶段。(1)
 元素原子结构示意图为:
元素原子结构示意图为:(2)
 、
、 、
、 三种氢化物的稳定性大小顺序是
三种氢化物的稳定性大小顺序是下表是O、S、
 、
、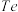 四种元素单质分别与
四种元素单质分别与 反应生成1mol气态氢化物的反应热,其中表示生成1mol硒化氢反应热的是
反应生成1mol气态氢化物的反应热,其中表示生成1mol硒化氢反应热的是| A | B | C | D |
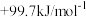 | 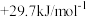 |  | 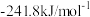 |
 焙烧
焙烧 的方法提取硒,反应产生
的方法提取硒,反应产生 、
、 的混合气体,写出反应的化学方程式
的混合气体,写出反应的化学方程式 的质量为
的质量为(4)已知硒酸
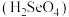 在水溶液中的电离方程式为:
在水溶液中的电离方程式为: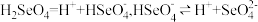 。
。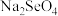 溶液的离子浓度由大到小的顺序为
溶液的离子浓度由大到小的顺序为 与
与 两种元素的守恒关系为:
两种元素的守恒关系为: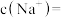
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐2】铁及其化合物在日常生活、生产中应用广泛,研究铁及其化合物的应用意义重大。回答下列问题:
(1)已知高炉炼铁过程中会发生如下反应:
Fe2O3(s)+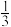 CO(g)=
CO(g)= Fe3O4(s)+
Fe3O4(s)+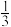 CO2(g) ∆H1
CO2(g) ∆H1
Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) ∆H2
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ∆H3
则∆H3的表达式为___________ (用含∆H1、∆H2的代数式表示)。
(2)铁等金属可用作CO与氢气反应的催化剂。已知某种催化剂可用来催化反应CO(g)+3H2(g) CH4(g)+H2O(g) ∆H<0。在T℃、106Pa时将1molCO和3molH2加入容积可变的密闭容器中,实验测得CO的体积分数φ(CO)如下表所示:
CH4(g)+H2O(g) ∆H<0。在T℃、106Pa时将1molCO和3molH2加入容积可变的密闭容器中,实验测得CO的体积分数φ(CO)如下表所示:
①下列能判断反应CO(g)+3H2(g) CH4(g)+H2O(g)达到平衡的是
CH4(g)+H2O(g)达到平衡的是___________ (填序号)。
a.容器内压强不再发生变化
b.v正(CO)=3v逆(H2)
c.混合气体的密度不再发生变化
d.混合气体的平均相对分子质量不再发生变化
②达到平衡时H2的转化率为___________ (保留一位小数);在T℃、P0时该反应的压强平衡常数Kp=___________ (用简单分数表示,分压=总压×物质的量分数);第50min后,保持温度不变,向该密闭容器中再充入1molCO和3molH2,则H2的转化率___________ (填“增大”“减小”或“不变”)。
(3)某种含铁催化剂可以催化合成乙烯:6H2(g)+2CO2(g) CH2=CH2(g)+4H2O(g)。已知温度对CO2的平衡转化率、t时刻的实际转化率和催化剂催化效率的影响如图甲所示,结合图象分析温度低于250°C时CO2实际转化率变大的原因:
CH2=CH2(g)+4H2O(g)。已知温度对CO2的平衡转化率、t时刻的实际转化率和催化剂催化效率的影响如图甲所示,结合图象分析温度低于250°C时CO2实际转化率变大的原因:___________ 。
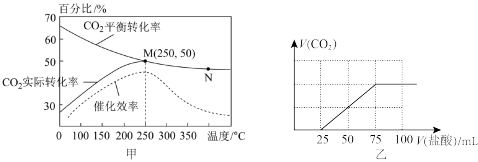
(4)把高炉出来的CO2气体经过处理后通入NaOH溶液中完全吸收。再用0.01mol·L-1的盐酸溶液进行滴定,所得气体与滴入的盐酸体积的关系如图乙,则该溶液中所有离子浓度由大到小的顺序为___________ 。
(1)已知高炉炼铁过程中会发生如下反应:
Fe2O3(s)+
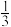 CO(g)=
CO(g)= Fe3O4(s)+
Fe3O4(s)+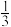 CO2(g) ∆H1
CO2(g) ∆H1Fe3O4(s)+4CO(g)=3Fe(s)+4CO2(g) ∆H2
Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g) ∆H3
则∆H3的表达式为
(2)铁等金属可用作CO与氢气反应的催化剂。已知某种催化剂可用来催化反应CO(g)+3H2(g)
 CH4(g)+H2O(g) ∆H<0。在T℃、106Pa时将1molCO和3molH2加入容积可变的密闭容器中,实验测得CO的体积分数φ(CO)如下表所示:
CH4(g)+H2O(g) ∆H<0。在T℃、106Pa时将1molCO和3molH2加入容积可变的密闭容器中,实验测得CO的体积分数φ(CO)如下表所示:| t/min | 0 | 10 | 20 | 30 | 40 | 50 |
| φ(CO) | 0.250 | 0.230 | 0.214 | 0.202 | 0.200 | 0.200 |
①下列能判断反应CO(g)+3H2(g)
 CH4(g)+H2O(g)达到平衡的是
CH4(g)+H2O(g)达到平衡的是a.容器内压强不再发生变化
b.v正(CO)=3v逆(H2)
c.混合气体的密度不再发生变化
d.混合气体的平均相对分子质量不再发生变化
②达到平衡时H2的转化率为
(3)某种含铁催化剂可以催化合成乙烯:6H2(g)+2CO2(g)
 CH2=CH2(g)+4H2O(g)。已知温度对CO2的平衡转化率、t时刻的实际转化率和催化剂催化效率的影响如图甲所示,结合图象分析温度低于250°C时CO2实际转化率变大的原因:
CH2=CH2(g)+4H2O(g)。已知温度对CO2的平衡转化率、t时刻的实际转化率和催化剂催化效率的影响如图甲所示,结合图象分析温度低于250°C时CO2实际转化率变大的原因:
(4)把高炉出来的CO2气体经过处理后通入NaOH溶液中完全吸收。再用0.01mol·L-1的盐酸溶液进行滴定,所得气体与滴入的盐酸体积的关系如图乙,则该溶液中所有离子浓度由大到小的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】研究电解质在水溶液中的平衡能了解它的存在形式,有重要的实际意义。
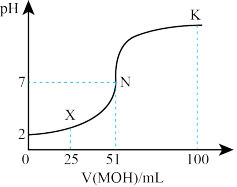
常温下,向100 mL0.01 mol·L-1HA的溶液中逐滴加入0.02 mol·L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。
(1)常温下,0.01 mol·L-1HA溶液中由水电离出的c(H+)=__________ mol·L-1。
(2)常温下一定浓度的MA稀溶液的pH=a,则a________ 7(填“>”、“<”或“=”),用离子方程式表示其原因为____________________________ 。
(3)X点时,溶液中c(H+)、c(M+)、c(A-)由大到小的顺序是__________________ 。
(4)K点时,溶液中c(H+)+c(M+)-c(OH-)=_____________ mol•L-1。

常温下,向100 mL0.01 mol·L-1HA的溶液中逐滴加入0.02 mol·L-1MOH溶液,所得溶液的pH随MOH溶液的体积变化如图所示(溶液体积变化忽略不计)。
(1)常温下,0.01 mol·L-1HA溶液中由水电离出的c(H+)=
(2)常温下一定浓度的MA稀溶液的pH=a,则a
(3)X点时,溶液中c(H+)、c(M+)、c(A-)由大到小的顺序是
(4)K点时,溶液中c(H+)+c(M+)-c(OH-)=
您最近一年使用:0次
【推荐1】NO、SO2是大气污染物但又有着重要用途。
I.已知:N2(g)+O2(g) = 2NO(g) ∆H1=+180.5kJ/mol
C(s)+ O2(g) = CO2(g) ∆H2=-393.5kJ/mol
2C(s)+ O2(g) = 2CO(g) ∆H3=-221.0kJ/mol
(1)某反应的平衡常数表达式K=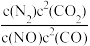 ,此反应的热化学方程式为:
,此反应的热化学方程式为:_____
(2)向绝热恒容密闭容器中充入等量的NO和CO进行反应,能判断反应已达到化学平衡状态的是_____ (填序号)
a.NO和N2浓度比为2:1 b.v正(CO)=2v逆(N2)
c.混合气体的密度保持不变 d.该反应平衡常数保持不变
II.(3)SO2可用于制Na2S2O3。为探究某浓度的Na2S2O3的化学性质,某同学设计如图实验流程:

用离子方程式表示Na2S2O3溶液具有碱性的原因_____ ,Na2S2O3与足量氯水反应的离子方程式是____
(4)含SO2的烟气可用Na2SO3溶液吸收。
可将吸收液送至电解槽再生后循环使用。再生电解槽如图1所示。a电极上含硫微粒放电的反应式为___ (任写一个)
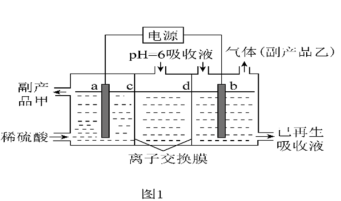
(5)2SO3(g)⇌2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图2所示。
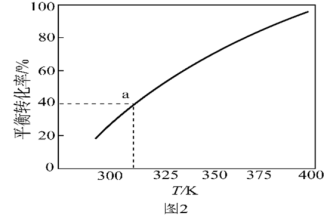
图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp=_____  用平衡分压代替平衡浓度计算,分压=
用平衡分压代替平衡浓度计算,分压= 总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将
总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将_______ (填“向正反应方向”或“向逆反应方向”“不”)移动。
I.已知:N2(g)+O2(g) = 2NO(g) ∆H1=+180.5kJ/mol
C(s)+ O2(g) = CO2(g) ∆H2=-393.5kJ/mol
2C(s)+ O2(g) = 2CO(g) ∆H3=-221.0kJ/mol
(1)某反应的平衡常数表达式K=
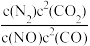 ,此反应的热化学方程式为:
,此反应的热化学方程式为:(2)向绝热恒容密闭容器中充入等量的NO和CO进行反应,能判断反应已达到化学平衡状态的是
a.NO和N2浓度比为2:1 b.v正(CO)=2v逆(N2)
c.混合气体的密度保持不变 d.该反应平衡常数保持不变
II.(3)SO2可用于制Na2S2O3。为探究某浓度的Na2S2O3的化学性质,某同学设计如图实验流程:

用离子方程式表示Na2S2O3溶液具有碱性的原因
(4)含SO2的烟气可用Na2SO3溶液吸收。
可将吸收液送至电解槽再生后循环使用。再生电解槽如图1所示。a电极上含硫微粒放电的反应式为

(5)2SO3(g)⇌2SO2(g)+O2(g),将一定量的SO3放入恒容的密闭容器中,测得其平衡转化率随温度变化如图2所示。

图中a点对应温度下,已知SO3的起始压强为P0,该温度下反应的平衡常数Kp=
 用平衡分压代替平衡浓度计算,分压=
用平衡分压代替平衡浓度计算,分压= 总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将
总压×物质的量分数)。在该温度下达到平衡,再向容器中加入等物质的量SO2和SO3,平衡将
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】NO是主要大气污染物,治理的办法之一是在一定条件下使NO与H2反应生成可参与大气生态循环的无毒气体,反应原理为:2NO(g)+2H2(g)=N2(g)+2H2O(g)。
(1)研究发现,NO与H2的反应过程可分为三步,每步均为基元反应:
①2NO=N2O2(快) ②N2O2+H2=N2O+H2O(慢) ③……(快)
i.第③步对应的基元反应是_______ 。
ii.整个反应过程中活化能最大的反应是第_______ 步。
(2)反应速率方程可表示反物浓度与反应速率的定量关系。NO与H2反应的速率方程为:V=k·[NO]m[H2]n,其中k为常数,指数m、n可以通过实验进行测定。已知在T℃时,不同浓度NO与H2对应的反应速率如下表所示:
可以推测,速率方程中的m=_______ ;n=_______ 。
用间接电化学法可对大气污染物NO进行无害化处理,其工作原理如图所示。
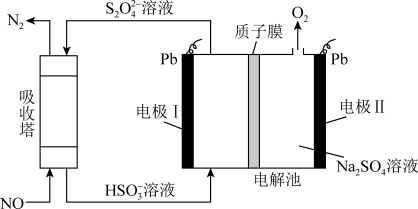
(3)电极Ⅰ为_______ 极(填“阴”或“阳”),其电极反应式为_______ 。
(4)电解时H+从电极_______ 向电极_______ 迁移(两空均选填“Ⅰ”或“Ⅱ”)。已知吸收塔中的反应为2NO+2S2O +2H2O=N2+4HSO
+2H2O=N2+4HSO ,利用该方法每处理1mol NO,可同时得到
,利用该方法每处理1mol NO,可同时得到_______ g O2。
(1)研究发现,NO与H2的反应过程可分为三步,每步均为基元反应:
①2NO=N2O2(快) ②N2O2+H2=N2O+H2O(慢) ③……(快)
i.第③步对应的基元反应是
ii.整个反应过程中活化能最大的反应是第
(2)反应速率方程可表示反物浓度与反应速率的定量关系。NO与H2反应的速率方程为:V=k·[NO]m[H2]n,其中k为常数,指数m、n可以通过实验进行测定。已知在T℃时,不同浓度NO与H2对应的反应速率如下表所示:
| 序号 | [NO]/mol·L-1 | [H2]mol·L-1 | v/mol·L-1·min-1 |
| Ⅰ | 6.0×10-3 | 1.0×10-3 | 1.8×10-4 |
| Ⅱ | 6.0×10-3 | 2.0×10-3 | 3.6×10-4 |
| Ⅲ | 2.0×10-3 | 6.0×10-3 | 1.2×10-4 |
可以推测,速率方程中的m=
用间接电化学法可对大气污染物NO进行无害化处理,其工作原理如图所示。

(3)电极Ⅰ为
(4)电解时H+从电极
 +2H2O=N2+4HSO
+2H2O=N2+4HSO ,利用该方法每处理1mol NO,可同时得到
,利用该方法每处理1mol NO,可同时得到
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐3】四种短周期元素A、B、C、D的性质或结构信息如下。
信息① 原子半径大小:A>B>C>D
信息② 四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题。
(1)①C元素在周期表中的位置_________ , 请写出BC2分子的电子式____________ 。
②A元素的单质与物质甲发生反应的离子方程式___________________ 。
③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式。负极__________ ;正极__________ ;
(2)A所在周期中, E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,

X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中Y极上的电极反应式________________ 检验Y电极反应产物的方法是___________
②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为______ (假设电解液的体积保持不变,常温下)
信息① 原子半径大小:A>B>C>D
信息② 四种元素之间形成的某三种分子的比例模型及部分性质:

请根据上述信息回答下列问题。
(1)①C元素在周期表中的位置
②A元素的单质与物质甲发生反应的离子方程式
③以Pt为电极,KOH为电解质溶液,两极分别通入乙和C的单质可组成燃料电池,写出电池的电极反应式。负极
(2)A所在周期中, E元素的单质还原性最强,A、E单质反应得到的化合物M是一种重要的化工原料,如图是电解100ml饱和M溶液的装置,

X、Y都是惰性电极,实验开始时,同时在两边各滴入几滴酚酞试液,则
①电解池中Y极上的电极反应式
②电解一段时间后,若阴极收集到112ml标准状况下的气体,此时电解液的PH为
您最近一年使用:0次



