根据下列实验操作和现象所得到的结论正确的是
| 选项 | 实验操作和现象 | 实验结论 |
| A | 向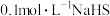 溶液中滴加几滴酚酞试剂,溶液变红 溶液中滴加几滴酚酞试剂,溶液变红 | 溶液中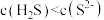 |
| B | 向 溶液中加水稀释,溶液的 溶液中加水稀释,溶液的 升高 升高 | 加水稀释抑制 的电离 的电离 |
| C | 向 溶液中通入少量氯气,有乳白色浑浊产生 溶液中通入少量氯气,有乳白色浑浊产生 | 氧化性: |
| D | 向KI溶液中滴加少量的 溶液,再滴加 溶液,再滴加 溶液,溶液变红 溶液,溶液变红 |  与 与 不反应 不反应 |
| A.A | B.B | C.C | D.D |
更新时间:2022-04-23 20:27:47
|
相似题推荐
单选题
|
较难
(0.4)
【推荐1】部分弱酸的电离平衡常数如下表:
下列选项错误的是
| 弱酸 | HCOOH | HCN | H2CO3 |
| 电离平衡常数(25 ℃) | Ki=1.77×10-4 | Ki=4.9×10-10 | Ki1=4.3×10-7 Ki2=5.6×10-11 |
A.2CN-+H2O+CO2=2HCN+CO |
B.2HCOOH+CO =2HCOO-+H2O+CO2↑ =2HCOO-+H2O+CO2↑ |
C.由数据可知酸性:HCOOH>H2CO3>HCN>HCO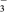 |
| D.25 ℃时,在等浓度的CH3COOH溶液和HCN溶液中,水的电离程度后者大 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】已知25℃时有关弱酸的电离平衡常数如下:
则下列有关说法正确的是
| 弱酸化学式 |  | HCN |  |
| 电离平衡常数 |  |  |  |
A.浓度均为 的上述三种溶液,加水稀释10倍后,三者物质的量浓度的关系为 的上述三种溶液,加水稀释10倍后,三者物质的量浓度的关系为 |
B.等体积等浓度的上述三种酸溶液中, 的物质的量分别为a mol、b mol、c mol,其关系为a>c>b 的物质的量分别为a mol、b mol、c mol,其关系为a>c>b |
C.NaCN溶液中通入少量 发生的化学反应为 发生的化学反应为 |
D.稀释HCN溶液过程中, 减小 减小 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】常温时,用NaOH固体调节0.1mol·L-1的H3AsO4溶液的pH,忽略溶液体积的变化,各含砷微粒的分布分数随pH的变化关系如图所示。下列说法错误的是


A.曲线②④分别代表H2AsO 和AsO 和AsO 的分布分数 的分布分数 |
| B.W、Q、R三点对应溶液中水的电离程度最大的是R点 |
C.R点对应溶液中c(Na+)<c(H2AsO )+5c(AsO )+5c(AsO ) ) |
| D.M点对应溶液的pH=9.22 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】Ga与Al同为第IIIA族元素,常温下,向NaGa(OH)4溶液中滴加醋酸溶液,溶液中Ga3+及其与OH-形成的微粒的浓度分数α随溶液pH变化的关系如图所示。已知CH3COOH的电离平衡常数Ka=1.8×10-5,关于该过程的说法正确的是
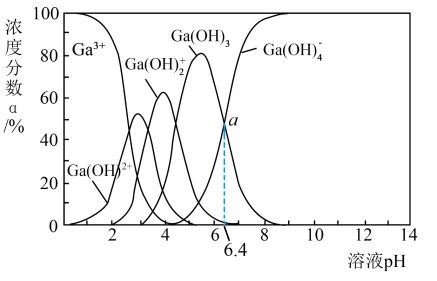

| A.Ga(OH)4的浓度分数先减小后增大 |
B.Ga3++H2O Ga(OH)2++H+,该平衡常数K的数量级为10-2 Ga(OH)2++H+,该平衡常数K的数量级为10-2 |
C.若a点时c[Ga(OH) ]=1mol/L,Ga(OH) ]=1mol/L,Ga(OH) (aq)+CH3COOH(aq) (aq)+CH3COOH(aq) Ga(OH)3(s)+H2O(l)+CH3COO-(aq)的平衡常数K=1.8×101.4 Ga(OH)3(s)+H2O(l)+CH3COO-(aq)的平衡常数K=1.8×101.4 |
D.pH=7时c(Na+)+3c(Ga3+)+2c(Ga(OH)2+)+c(Ga(OH) )=c[Ga(OH) )=c[Ga(OH) ] ] |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐3】常温下,向20mL 0.01mol/L CH3COOH溶液中逐滴加入0.01mol/L的NaOH溶液,溶液中由水电离出的c(H+)随加入NaOH溶液的体积变化示意图如下图,下列说法正确的是
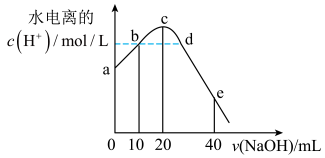

| A.从a到c,加入NaOH溶液对醋酸的电离既有促进作用也有抑制作用 |
| B.b、d两点溶液的pH相同 |
| C.e点所示溶液中,c(Na+)=2c(CH3COO-)+2c(CH3COOH)=0.01mol/L |
| D.c点所示溶液中,c(Na+)>c(CH3COO-)>c(OH-)>c(H+) |
您最近半年使用:0次

 的
的 、
、 溶液的pH
溶液的pH 的电离能力
的电离能力 溶液、澄清石灰水,观察现象
溶液、澄清石灰水,观察现象 和
和 气体
气体 溶于过量热浓盐酸中,再滴加几滴
溶于过量热浓盐酸中,再滴加几滴 溶液,观察溶液颜色变化
溶液,观察溶液颜色变化


