磷酸是生产磷肥和饲料营养剂的原料,同时还是常用的食品添加剂。常温下H3PO4在水中各级电离的过程如图所示。已知:pK=-1gK。
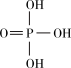






下列相关说法正确的是
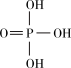






下列相关说法正确的是
A.反应H3PO4+2  3 3 pK=16 pK=16 |
B.Na2HPO4溶液中:c( )>2c(H3PO4)+ c( )>2c(H3PO4)+ c( ) ) |
| C.用NaOH溶液滴定NaH2PO4溶液时宜选用甲基橙做指示剂 |
D.H3PO4和Na3PO4组成的混合溶液pH=6时,溶液中:c( )>c( )>c( )>c(H3PO4) )>c(H3PO4) |
2022·湖北武汉·一模 查看更多[2]
更新时间:2022-05-15 15:46:46
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】分子结构修饰是指保持分子的基本结构不变,仅改变分子结构中的某些基团而得到的新分子。分子结构被修饰后,分子的性质发生了改变。已知部分羧酸的分子组成和结构、电离常数如表。下列说法正确的是
| 羧酸 | CH3CH2COOH | CH3COOH | CH2ClCOOH | CF3COOH |
| 电离常数(25℃) | a | b | c | d |
| A.a>b>c>d | B.b>a>c>d | C.c>b>a>d | D.d>c>b>a |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列叙述错误的是
A.向  溶液中加入少量NaOH固体, 溶液中加入少量NaOH固体, 的电离平衡向正反应方向移动 的电离平衡向正反应方向移动 |
B.将10 mL  的氨水加蒸馏水稀释到1 L后, 的氨水加蒸馏水稀释到1 L后, 的电离程度增大, 的电离程度增大, 增大 增大 |
C.室温下,将pH=11的氨水与pH=3的盐酸等体积混合,所得溶液中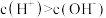 |
| D.某温度下,0.01 mol/L的盐酸稀释100倍后,盐酸溶液pH=4 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用NA表示阿伏加德罗常数的值。下列判断正确的是
| A.10g重水中含有电子数目为4NA |
| B.标准状况下22.4LCH3Cl分子中所含的C—H键总数为3NA |
| C.7.1gCl2与足量的水反应转移的电子总数为0.1NA |
| D.向1L0.1mol/LNaCN溶液中加入适量HCN使溶液呈酸性,则溶液中CN-的数目小于0.1NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列说法正确的是( )
| A.为确定某酸H2A是强酸还是弱酸,可测NaHA溶液的pH。若pH>7,则H2A是弱酸;若pH<7,则H2A是强酸 |
| B.用0.200 0 mol·L−1NaOH标准溶液滴定HCl与CH3COOH的混合液(混合液中两种酸的浓度均约为0.1 mol·L−1),至中性时,溶液中的酸未被完全中和 |
| C.0.1 mol·L−1氢氧化钠溶液与0.2 mol·L−1草酸氢钠溶液等体积混合:2c(OH-)+c(C2O42-)=c(HC2O4-)+2c(H+) |
| D.相同温度下,将足量氯化银固体分别放入相同体积的①蒸馏水、② 0.1 mol·L−1盐酸、③ 0.1 mol·L−1氯化镁溶液、④ 0.1 mol·L−1硝酸银溶液中,Ag+浓度:①<④=②<③ |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】室温下,通过下列1实验探究 K2CO3的性质。
实验1:配制100mL、 K2CO3溶液,测得溶液 pH 约为11.6;
K2CO3溶液,测得溶液 pH 约为11.6;
实验2: 取 10mL K2CO3溶液,向其中缓慢滴入等体积、等浓度的稀盐酸后测得混合溶液的pH约为8.0;
K2CO3溶液,向其中缓慢滴入等体积、等浓度的稀盐酸后测得混合溶液的pH约为8.0;
实验3: 取 10mL K2CO3溶液,将其缓慢滴加到等体积、等浓度的稀盐酸中;
K2CO3溶液,将其缓慢滴加到等体积、等浓度的稀盐酸中;
实验4: 取 10mL K2CO3溶液,向其中加入一定量
K2CO3溶液,向其中加入一定量 固体充分搅拌,一段时间后过滤, 向滤渣中加入足量稀盐酸,固体部分溶解。
固体充分搅拌,一段时间后过滤, 向滤渣中加入足量稀盐酸,固体部分溶解。
下列说法正确的是
实验1:配制100mL、
 K2CO3溶液,测得溶液 pH 约为11.6;
K2CO3溶液,测得溶液 pH 约为11.6;实验2: 取 10mL
 K2CO3溶液,向其中缓慢滴入等体积、等浓度的稀盐酸后测得混合溶液的pH约为8.0;
K2CO3溶液,向其中缓慢滴入等体积、等浓度的稀盐酸后测得混合溶液的pH约为8.0;实验3: 取 10mL
 K2CO3溶液,将其缓慢滴加到等体积、等浓度的稀盐酸中;
K2CO3溶液,将其缓慢滴加到等体积、等浓度的稀盐酸中;实验4: 取 10mL
 K2CO3溶液,向其中加入一定量
K2CO3溶液,向其中加入一定量 固体充分搅拌,一段时间后过滤, 向滤渣中加入足量稀盐酸,固体部分溶解。
固体充分搅拌,一段时间后过滤, 向滤渣中加入足量稀盐酸,固体部分溶解。下列说法正确的是
A.实验1 所得溶液中,  |
B.由实验2可得出:  |
C.实验3所得溶液中,  |
D.实验4,加入稀盐酸后的上层清液中,  |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列有关电解质溶液的叙述正确的是
| A.向Mg(OH)2悬浊液中加入NH4Cl固体,c(Mg2+)、c(OH−)均增大 |
| B.将pH=3的醋酸溶液稀释后,溶液中所有离子的浓度均减小 |
| C.0.1 mol·L−1 NaHCO3溶液中,c(Na+)>c(HCO3-)>c(CO32-)>c(H2CO3) |
| D.0.01 mol·L−1 Na2CO3溶液与0.01 mol·L−1 NaHCO3溶液等体积混合一定存在:3c(CO32-)+3c(HCO3-)+3c(H2CO3)=2c(Na+) |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】下列说法正确的是
| A.将FeCl3溶液加热蒸干,并灼烧最终得到Fe2O3 |
| B.25℃时CH3COONa溶液的Kw大于100℃时CH3COONa溶液的Kw |
| C.100℃时,将pH=2的盐酸与PH=12的NaOH溶液等体积混合,溶液呈中性 |
| D.一般而言,弱电解质的浓度越大,其电离度越小,电离常数也越小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列有关电解质溶液的说法正确的是
A.向盐酸中加入氨水至中性,溶液中 |
B.将CH3COONa溶液从20℃升温至30℃,溶液中 增大 增大 |
| C.常温下,pH为3的醋酸溶液中加入醋酸钠固体,溶液pH增大 |
D.0.1molAgCl和0.1molAgI混合后加入1L水中,所得溶液中 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐3】已知常温下CH3COOH和NH3·H2O的电离平衡常数分别为Ka =Kb =1.75x10-5mol/L。若在常温下向0.1mol/L的醋酸溶液中逐滴加入相同浓度的氨水直至完全过量,则下列说法正确的是( )
| A.加入氨水的过程中,溶液的导电性一直不断增强 |
| B.pH=3的醋酸与pH=11的氨水等体积混合,所得的溶液由水电离出的c(H+)=1x10-7mol/L |
| C.若Ka、Kb、Kw分别表示常温下CH3COOH的电离平衡常数、CH3COO-的水解平衡常数和水的离子积常数,则三者之间的关系为Ka•Kb=Kw |
| D.该等式在滴加过程中始终成立c(CH3COO-)+c(CH3COOH)=c(NH4+)+c(NH3·H2O) |
您最近一年使用:0次

 、
、 、
、 与pH的关系如图所示。25℃时,
与pH的关系如图所示。25℃时, 、
、 。下列说法正确的是
。下列说法正确的是
 。②
。② 。
。
 的水解常数
的水解常数
 与
与 溶液中,所加入溶液的体积(V)和混合液的pH的关系曲线如图所示。下列结论正确的是(
溶液中,所加入溶液的体积(V)和混合液的pH的关系曲线如图所示。下列结论正确的是(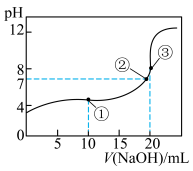


 恰好反应完,溶液中有:
恰好反应完,溶液中有: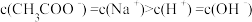


 溶液滴定10.00mL 0.0100
溶液滴定10.00mL 0.0100 、
、 、
、 的浓度c(X)随
的浓度c(X)随 的变化曲线如图所示(忽略滴定过程中
的变化曲线如图所示(忽略滴定过程中 的逸出)。下列说法错误的是
的逸出)。下列说法错误的是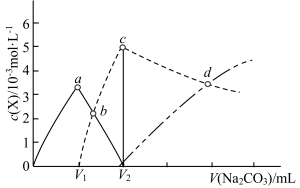
 ,
, ;
; 。
。





