下列选项中,为完成相应头验,进行的设计或相夹操作(部分夹持装置已略去)合理的是
| A | B | C | D |
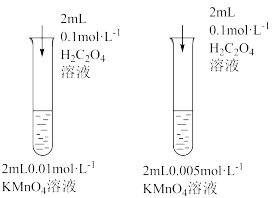
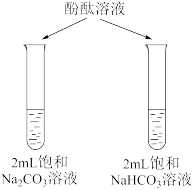
| 证明增加反应物浓度可以加快化学反应速率 | 证明碳酸钠水解能力比碳酸氢钠强 | 比较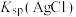 和 和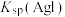 的大小 的大小 | 用 标准溶液滴定锥形瓶中的盐酸 标准溶液滴定锥形瓶中的盐酸 |
 |  |  |  |
| A.A | B.B | C.C | D.D |
更新时间:2023-02-12 20:59:16
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】反应2NO + 2CO N2 + 2CO2可应用于汽车尾气净化,下列关于该反应的说法正确的是
N2 + 2CO2可应用于汽车尾气净化,下列关于该反应的说法正确的是
 N2 + 2CO2可应用于汽车尾气净化,下列关于该反应的说法正确的是
N2 + 2CO2可应用于汽车尾气净化,下列关于该反应的说法正确的是| A.升高温度能加快反应速率 |
| B.减小NO浓度能加快反应速率 |
| C.使用恰当的催化剂不能加快反应速率 |
| D.CO可以100%转化为产物 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】下列对化学反应速率分析错误的是
| A.对于气体参加的化学反应,增大压强使容器容积减小,单位体积内活化分子数增多 |
B. 与水反应时,增加水的用量可以加快化学反应速率 与水反应时,增加水的用量可以加快化学反应速率 |
| C.升高温度,使反应物分子中活化分子百分数增大 |
| D.加入适宜的催化剂,使反应物分子中活化分子百分数增大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】用 的
的 标准溶液滴定某未知浓度的
标准溶液滴定某未知浓度的 溶液,下列说法错误的是
溶液,下列说法错误的是
 的
的 标准溶液滴定某未知浓度的
标准溶液滴定某未知浓度的 溶液,下列说法错误的是
溶液,下列说法错误的是| A.该滴定实验不需要指示剂 |
| B.该实验用到的玻璃仪器有酸式滴定管、碱式滴定管、锥形瓶 |
| C.滴定管使用前需检验是否漏液 |
D.若滴定终止时,仰视读数,所测 浓度偏高 浓度偏高 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】常用甲醛法测定铵盐中的氮: 与甲醛可迅速发生反应:
与甲醛可迅速发生反应: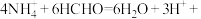
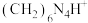 ,选用酚酞作指示剂,用标准NaOH溶液滴定生成物可确定铵盐中的含氮量[
,选用酚酞作指示剂,用标准NaOH溶液滴定生成物可确定铵盐中的含氮量[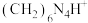 也能与NaOH溶液反应]。实验步骤如下:
也能与NaOH溶液反应]。实验步骤如下:
①配制500mL 标准溶液;
标准溶液;
②准确称取0.18g 样品置于250mL锥形瓶中,加入50mL蒸馏水使其溶解;
样品置于250mL锥形瓶中,加入50mL蒸馏水使其溶解;
③再加适量甲醛溶液和1滴酚酞指示剂,充分振荡后静置使 样品完全反应;
样品完全反应;
④最后用 标准液滴定至终点,起始和终点读数分别为
标准液滴定至终点,起始和终点读数分别为 、
、 。
。
对于上述实验,下列说法错误的是
 与甲醛可迅速发生反应:
与甲醛可迅速发生反应: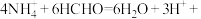
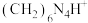 ,选用酚酞作指示剂,用标准NaOH溶液滴定生成物可确定铵盐中的含氮量[
,选用酚酞作指示剂,用标准NaOH溶液滴定生成物可确定铵盐中的含氮量[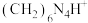 也能与NaOH溶液反应]。实验步骤如下:
也能与NaOH溶液反应]。实验步骤如下:①配制500mL
 标准溶液;
标准溶液;②准确称取0.18g
 样品置于250mL锥形瓶中,加入50mL蒸馏水使其溶解;
样品置于250mL锥形瓶中,加入50mL蒸馏水使其溶解;③再加适量甲醛溶液和1滴酚酞指示剂,充分振荡后静置使
 样品完全反应;
样品完全反应;④最后用
 标准液滴定至终点,起始和终点读数分别为
标准液滴定至终点,起始和终点读数分别为 、
、 。
。对于上述实验,下列说法错误的是
| A.容量瓶使用完毕,应洗净、晾干,玻璃磨口瓶塞应在瓶塞与瓶口处垫一张纸条 |
| B.当滴入半滴NaOH溶液,锥形瓶中溶液颜色由无色变为粉红色,且半分钟内不褪色即达到滴定终点 |
| C.步骤③中若选用甲基橙做指示剂,将导致测定结果偏大 |
| D.步骤②滴定终点时仰视读数,将导致测定结果偏大 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】室温下,下列实验探究方案能达到探究目的的是
| 选项 | 探究方案 | 探究目的 |
| A | 室温下,用pH计测定浓度均为 的 的 溶液和 溶液和 溶液的pH 溶液的pH | 比较 和 和 的酸性强弱 的酸性强弱 |
| B | 向滴有酚酞的氨水中加入 溶液红色变浅 溶液红色变浅 |  溶液呈酸性 溶液呈酸性 |
| C | 向盛有 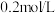  溶液的试管中滴加2滴 溶液的试管中滴加2滴  溶液,产生白色沉淀后,再滴加2滴 溶液,产生白色沉淀后,再滴加2滴  溶液,又产生红褐色沉淀 溶液,又产生红褐色沉淀 | 验证该温度下: |
| D | 以Zn、Fe为电极,以酸化的3% 溶液作电解质溶液,连接成原电池装置,过一段时间,用胶头滴管从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴 溶液作电解质溶液,连接成原电池装置,过一段时间,用胶头滴管从Fe电极区域取少量溶液于试管中,再向试管中滴入2滴 溶液,观察现象 溶液,观察现象 | 探究金属的电化学保护法 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】室温下,将1.000mol·L-1盐酸滴入20.00mL 1.000mol·L-1氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是
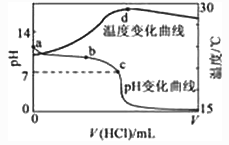

| A.a点由水电离出的c(H+)=1.0×10-14mol/L |
| B.b点:c(NH4+)+c(NH3·H2O) >c(Cl-) |
| C.b点时加入的盐酸体积小于20.00mL,而c点时加入的盐酸体积大于20.00mL |
| D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】NA是阿伏加德罗常数的值。下列说法正确的是
| A.2.24LCl2溶于水制成饱和氯水,转移电子数目为0.1NA |
| B.1L0.1mol·L−1H2C2O4溶液中含有的H+离子数为0.2NA |
C.1L1mol·L−1氯化铵水溶液中 与H+离子数之和大于NA 与H+离子数之和大于NA |
| D.0.5molN2和1.5molH2充分反应,生成NH3的数目为NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】用下列装置不能达到实验目的的是
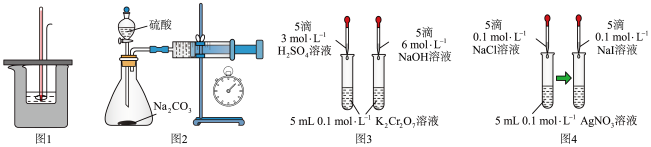

| A.图1:测量强酸强碱中和反应的反应热 |
B.图2:测定 和稀硫酸反应的速率 和稀硫酸反应的速率 |
| C.图3:验证浓度对化学平衡的影响 |
D.图4:证明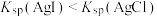 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,Ksp(MnS)=2.5×10-13,Ksp(FeS)=6.3×10-18。FeS和MnS在水中的沉淀溶解平衡曲线如图所示(X2+表示Fe2+或Mn2+),下列说法错误的是( )
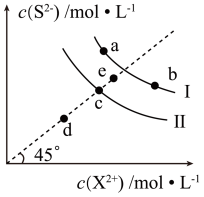

| A.曲线I表示MnS的沉淀溶解平衡曲线 |
| B.升高温度,曲线Ⅱ上的c点可沿虚线平移至d点 |
C.常温下,反应MnS(s)+Fe2+(aq) FeS(s)+Mn2+(aq)的平衡常数K≈4×104 FeS(s)+Mn2+(aq)的平衡常数K≈4×104 |
| D.向b点溶液中加入少量Na2S固体,溶液组成由b点沿工线向a点方向移动 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】下列实验操作、实验现象、解释或结论都正确且有因果关系的是
| 选项 | 实验操作 | 实验现象 | 解释或结论 |
| A | 向盛有   溶液的试管中滴加 溶液的试管中滴加   溶液,再向其中滴加一定量 溶液,再向其中滴加一定量 溶液 溶液 | 先有白色沉淀生成,后又产生黄色沉淀 | 常温下,溶度积: |
| B | 常温下,用 计分别测定 计分别测定  溶液和 溶液和  溶液的 溶液的 | 测得 都等于7 都等于7 | 同温下,不同浓度的 溶液中水的电离程度相同 溶液中水的电离程度相同 |
| C | 用铂( )电极电解等浓度的足量 )电极电解等浓度的足量 、 、 混合溶液 混合溶液 | 阴极有红色固体物质析出 | 金属活动性: |
| D | 向   溶液中滴加 溶液中滴加   溶液,充分反应后,取少量反应后溶液于试管中,再滴入几滴 溶液,充分反应后,取少量反应后溶液于试管中,再滴入几滴 溶液 溶液 | 溶液变红 |  与 与 的反应为可逆反应 的反应为可逆反应 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次



