25℃时,用 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 、pH及微粒分布分数
、pH及微粒分布分数 [
[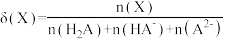 ,X表示
,X表示 、
、 或
或 ]的关系如图所示:
]的关系如图所示:
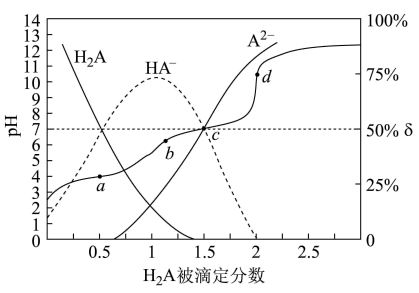
下列说法错误的是
 溶液滴定同浓度的
溶液滴定同浓度的 溶液,
溶液, 被滴定分数
被滴定分数 、pH及微粒分布分数
、pH及微粒分布分数 [
[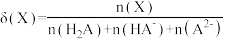 ,X表示
,X表示 、
、 或
或 ]的关系如图所示:
]的关系如图所示:
下列说法错误的是
A.25℃时, 第一步电离平衡常数 第一步电离平衡常数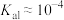 |
B.c点溶液中: |
C.a、b、c、d四点溶液中水的电离程度: |
D.用NaOH溶液滴定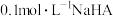 溶液可用甲基橙作指示剂 溶液可用甲基橙作指示剂 |
更新时间:2023-03-25 17:57:47
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】 为二元弱酸,在25℃时,溶液中
为二元弱酸,在25℃时,溶液中 及
及 浓度的负对数pc随溶液pH变化的关系如图所示[已知:溶液中始终保持
浓度的负对数pc随溶液pH变化的关系如图所示[已知:溶液中始终保持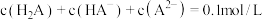 ]。下列有关叙述错误的是
]。下列有关叙述错误的是
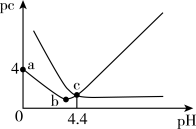
 为二元弱酸,在25℃时,溶液中
为二元弱酸,在25℃时,溶液中 及
及 浓度的负对数pc随溶液pH变化的关系如图所示[已知:溶液中始终保持
浓度的负对数pc随溶液pH变化的关系如图所示[已知:溶液中始终保持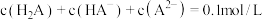 ]。下列有关叙述错误的是
]。下列有关叙述错误的是
A.b点: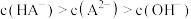 |
| B.由a点到c点的过程中,水的电离程度一直增大 |
C. 的 的 约为 约为 |
D.NaHA溶液中 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】下列说法正确的是
| A.饱和氯水中加水稀释,促进氯水中水的电离 |
| B.向氨水中加入氯化铵,由于氯化铵溶液呈酸性,所以溶液pH降低 |
C.碳酸钠溶液中存在CO32-+H2O HCO3-+OH-平衡,若通入CO2,则平衡逆向移动 HCO3-+OH-平衡,若通入CO2,则平衡逆向移动 |
| D.向氢氧化镁悬浊液中加水稀释,Mg(OH)2沉淀溶解平衡正向移动,但c(Mg2+)降低 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】某温度下,向体积均为20.00mL、浓度均为0.1mol•L-1的NaCl溶液、Na2CrO4溶液中分别滴加0.1mol•L-1的AgNO3溶液,滴定过程中的pX(PX=-lgX,X=Cl-、CrO )与滴加AgNO3溶液体积的关系如图所示。下列说法正确的是
)与滴加AgNO3溶液体积的关系如图所示。下列说法正确的是

 )与滴加AgNO3溶液体积的关系如图所示。下列说法正确的是
)与滴加AgNO3溶液体积的关系如图所示。下列说法正确的是
| A.曲线II表示AgNO3溶液滴定NaCl溶液的过程 |
| B.Ksp(Ag2CrO4)=10-2b |
| C.其他条件不变,如果NaCl溶液浓度改为0.05mol•L-1,则滴定终点向上移动 |
| D.若a=5 b=4,则用AgNO3标准液滴定NaCl时可用K2CrO4溶液做指示剂 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】用0.1 mol·L−1 NaOH标准溶液滴定20 mL等浓度的三元酸H3A,得到pH与V(NaOH)、lgX[X=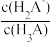 或
或 或
或 ]的关系分别如图1、图2所示。下列说法错误的是
]的关系分别如图1、图2所示。下列说法错误的是
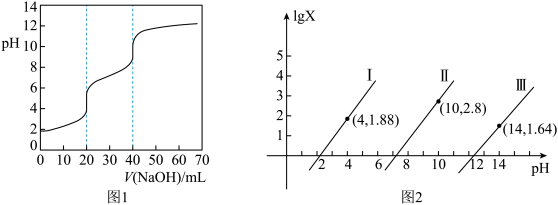
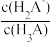 或
或 或
或 ]的关系分别如图1、图2所示。下列说法错误的是
]的关系分别如图1、图2所示。下列说法错误的是
A.曲线Ⅲ表示pH与lg 的变化关系 的变化关系 |
| B.由图1知中和Na2HA溶液时,未出现pH突跃 |
C.当体系中溶液的pH=9时, =1.8 =1.8 |
| D.当滴入20 mL NaOH溶液时,c(Na+)>c(H2A−)>c(H+)>c(HA2−)>c(OH−) |
您最近一年使用:0次
单选题
|
较难
(0.4)
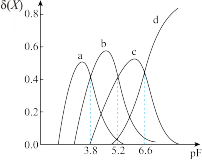
【推荐1】AlF3存在分步电离,常温下向某浓度的AlF3溶液中加入NaF,实验测定A13+、AlF2+、AlF 、AlF3在所有含铝元素微粒中的分布分数随pF[pF=-lgc(F-)]变化如图所示,[已知δ(X)为含铝微粒的分布分数,如δ(Al3+)=
、AlF3在所有含铝元素微粒中的分布分数随pF[pF=-lgc(F-)]变化如图所示,[已知δ(X)为含铝微粒的分布分数,如δ(Al3+)=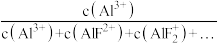 ],下列说法错误的是
],下列说法错误的是
 、AlF3在所有含铝元素微粒中的分布分数随pF[pF=-lgc(F-)]变化如图所示,[已知δ(X)为含铝微粒的分布分数,如δ(Al3+)=
、AlF3在所有含铝元素微粒中的分布分数随pF[pF=-lgc(F-)]变化如图所示,[已知δ(X)为含铝微粒的分布分数,如δ(Al3+)=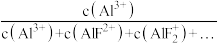 ],下列说法错误的是
],下列说法错误的是
A.曲线b表示AlF |
B.pF=4.6时,c(AlF )>c(AlF2+)>c(AlF3) )>c(AlF2+)>c(AlF3) |
| C.常温下,AlF3⇌Al3++3F-的化学平衡常数数量级为10-16 |
D.pF=6.6时,5c(AlF2+)+c(AlF )+c(H+)=c(F-)+c(OH-) )+c(H+)=c(F-)+c(OH-) |
您最近一年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐2】常温下已知两种一元弱酸HX和HY,如果向NaX溶液中通CO2气体,只能生成HX和NaHCO3;往NaY溶液中通入CO2则生成HY和Na2CO3。有关叙述正确的是
| A.三种酸的电离常数:Ki1(H2CO3) > Ki(HX) > Ki(HY) > Ki2(H2CO3) |
| B.NaX溶液中通入足量CO2后的离子浓度:c(HCO3-)>c(CO32-)>c(X-) |
| C.同浓度溶液的碱性:NaX > Na2CO3 > NaY > NaHCO3 |
| D.结合H+的能力:Y- > CO32- > X- > HCO3- |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐1】不能证明CH3COOH是弱电解质的实验事实是
| A.CH3COONa 溶液显碱性 |
| B.0.1mol/LCH3COOH溶液pH>1 |
| C.用CH3COOH溶液浸泡水壶中的水垢,可将其清除 |
| D.25 ℃时,0.1mo/LCH3COOH溶液比0.1mol/LHCl 溶液导电性弱 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】甘氨酸在水溶液中存在: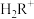 )=c(R-),此时溶液的pH称为等电点,用pI表示。向含1molHOOC-CH2-NH3Cl的溶液中不断滴加NaOH溶液,所加NaOH的物质的量与溶液的pH关系如图所示,下列说法不正确的是
)=c(R-),此时溶液的pH称为等电点,用pI表示。向含1molHOOC-CH2-NH3Cl的溶液中不断滴加NaOH溶液,所加NaOH的物质的量与溶液的pH关系如图所示,下列说法不正确的是
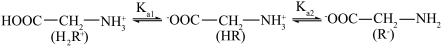
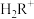 )=c(R-),此时溶液的pH称为等电点,用pI表示。向含1molHOOC-CH2-NH3Cl的溶液中不断滴加NaOH溶液,所加NaOH的物质的量与溶液的pH关系如图所示,下列说法不正确的是
)=c(R-),此时溶液的pH称为等电点,用pI表示。向含1molHOOC-CH2-NH3Cl的溶液中不断滴加NaOH溶液,所加NaOH的物质的量与溶液的pH关系如图所示,下列说法不正确的是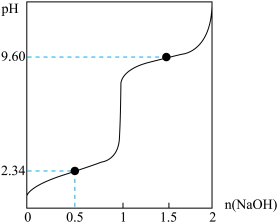
A.甘氨酸的水溶液中存在:c(HOOC-CH2-NH )+c(H+)=c(H2N-CH2-COO-)+c(OH-) )+c(H+)=c(H2N-CH2-COO-)+c(OH-) |
| B.Ka2=10-9.60 |
| C.甘氨酸的水溶液显碱性 |
| D.甘氨酸的pI为5.97 |
您最近一年使用:0次


 、Cl-
、Cl- 、ClO-
、ClO- 、
、
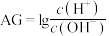 ,室温下用0.1
,室温下用0.1 的HCl溶液滴定10.00mL 0.1
的HCl溶液滴定10.00mL 0.1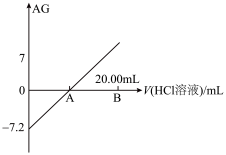

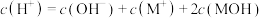
 时,向
时,向 邻苯二甲酸
邻苯二甲酸 溶液中加入
溶液中加入 固体,混合溶液的pH随
固体,混合溶液的pH随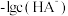 以及
以及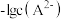 的关系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发).下列有关叙述错误的是
的关系如图所示(忽略溶液体积变化和邻苯二甲酸的挥发).下列有关叙述错误的是
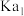 约为
约为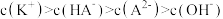
 先增大后减小
先增大后减小 时,
时,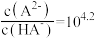
 溶液中滴加几滴溴水,振荡,再滴加
溶液中滴加几滴溴水,振荡,再滴加 淀粉溶液,溶液显蓝色
淀粉溶液,溶液显蓝色 的氧化性比
的氧化性比 的强
的强 的
的 、
、 混合溶液中滴加少量
混合溶液中滴加少量 溶液,有黄色沉淀生成
溶液,有黄色沉淀生成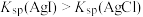
 试纸测得:
试纸测得: 溶液的
溶液的 溶液的
溶液的 电离出
电离出 的能力比
的能力比 的强
的强 溶液,溶液变为血红色
溶液,溶液变为血红色


