同温同压下,研究Cl2分别在不同浓度的盐酸和NaCl溶液中的溶解度(用溶解Cl2的物质的量浓度表示)变化如图所示。已知氯气在溶解时存在以下

①Cl2(aq)+H2O HClO+H++Cl- K1=4.2×10-4
HClO+H++Cl- K1=4.2×10-4
②Cl2(aq)+Cl- Cl3(aq) K2=0.19
Cl3(aq) K2=0.19
③HClO H++C1O- Ka=3.2×10-8
H++C1O- Ka=3.2×10-8
下列说法错误的是

①Cl2(aq)+H2O
 HClO+H++Cl- K1=4.2×10-4
HClO+H++Cl- K1=4.2×10-4②Cl2(aq)+Cl-
 Cl3(aq) K2=0.19
Cl3(aq) K2=0.19③HClO
 H++C1O- Ka=3.2×10-8
H++C1O- Ka=3.2×10-8下列说法错误的是
A.随着NaCl浓度的增大,Cl2溶解度减小,溶液中 减小 减小 |
| B.随着盐酸浓度的增大,反应①被抑制,反应②为主要反应从而促进Cl2溶解 |
| C.a点时,c(H+)>c(Cl-)>c(Cl3-)>c(ClO-) |
| D.b点时,c(Na+)<c(Cl-)+c(Cl3-)+c(ClO-) |
2023·山东济南·模拟预测 查看更多[3]
(已下线)专题09 水溶液中的离子平衡-2023年高考化学真题题源解密(新高考专用)(已下线)【知识图鉴】单元讲练测选择性必修1第3单元02基础练山东省实验中学2023届高三下学期5月第一次模拟考试化学试题
更新时间:2023/05/06 07:08:50
|
相似题推荐
单选题
|
较难
(0.4)
解题方法
【推荐1】某溶液中含有大量的Cl一、Br一、I一,若向l L该混合溶液中通入一定量的Cl2,溶液中Cl-、Br一、I一的物质的量与通入Cl2的体积(标准状况)的关系如下表所示,原溶液中Cl一、Br一、I一的物质的量浓度之比为
| Cl2的体积(标准状况) | 5.6L | 11.2L | 22.4L |
| n(Cl-) | 1.5mol | 2.0mol | 3.0mol |
| n(Br-) | 3.0mol | 2.8mol | 1.8mol |
| n(I-) | xmol | 0 | 0 |
| A.5:15:4 | B.5:12:4 | C.15 : 30 : 8 | D.条件不足,无法计算 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐2】向FeI2、FeBr2的混合溶液中通入适量氯气,溶液中某些离子的物质的量变化情况如图所示。则下列说法中正确的是


| A.还原性:I-<Fe2+<Br- |
| B.原混合溶液中Br-的物质的量为4mol |
| C.线段BC表示Cl-的物质的量变化 |
| D.原溶液中:n(Fe2+):n(I-):n(Br-)=2:1:3 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐3】用NA表示阿伏加 德罗常数的值,下列有关说法正确的是
| A.2.0gH218O与D2O的混合物中所含中子数为NA |
| B.5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
| C.1molH2与足量O2反应生成的H2O中含有的共价键总数为NA |
| D.在反应11P4+60CuSO4+96H2O===20Cu3P+24H3PO4+60H2SO4中,6molCuSO4能氧化白磷的分子数为1.1NA |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】 和
和 存在的水溶液中有如下平衡:
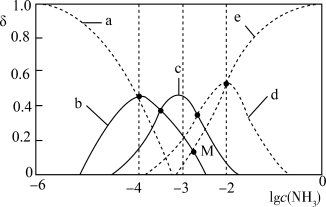
存在的水溶液中有如下平衡: 。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的
。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的 关系如图所示。下列说法正确的是
关系如图所示。下列说法正确的是
 和
和 存在的水溶液中有如下平衡:
存在的水溶液中有如下平衡: 。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的
。向某浓度的硫酸铜溶液中滴加浓氨水,实验测得含Cu微粒的物质的量分布分数(δ)与溶液中游离氨的 关系如图所示。下列说法正确的是
关系如图所示。下列说法正确的是
A.曲线d表示 |
B.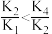 |
C. 时, 时, |
D.M点时,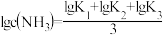 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】常温下,向 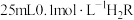 溶液中逐滴加入等浓度的 NaOH 溶液,所得溶液中含 R元素的微粒的物质的量分数与溶液 pH 的关系如图,下列说法错误的是
溶液中逐滴加入等浓度的 NaOH 溶液,所得溶液中含 R元素的微粒的物质的量分数与溶液 pH 的关系如图,下列说法错误的是
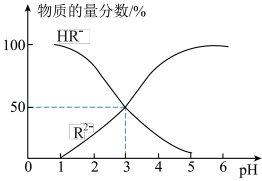
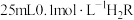 溶液中逐滴加入等浓度的 NaOH 溶液,所得溶液中含 R元素的微粒的物质的量分数与溶液 pH 的关系如图,下列说法错误的是
溶液中逐滴加入等浓度的 NaOH 溶液,所得溶液中含 R元素的微粒的物质的量分数与溶液 pH 的关系如图,下列说法错误的是
A.Na2R水解的离子方程式为 |
| B.常温下, Na2R水解常数Kh=10-11 |
C.0.1mol·L-1NaHR 溶液中存在  |
D.常温下,等物质的量浓度的 NaHR 与  溶液等体积混合后得到的溶液 溶液等体积混合后得到的溶液  |
您最近半年使用:0次
单选题
|
较难
(0.4)
解题方法
【推荐3】H2C2O4水溶液中部分微粒的分布分数δ与pH关系如图所示,下列说法正确的是
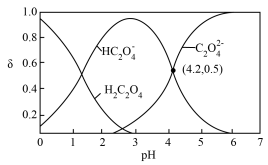

A.向H2C2O4溶液中滴加NaOH溶液至pH=2.5:c(H2C2O4)+c(C2O )>c(HC2O )>c(HC2O ) ) |
| B.由图可知:H2C2O4的Ka1=10-4.2 |
C.向H2C2O4溶液中滴加NaOH溶液至pH=7,则溶液中:2c(C2O )>c(Na+) )>c(Na+) |
D.将0.01 mol·L-1的H2C2O4溶液与0.02 mol·L-1 NaOH溶液等体积混合后的溶液中:c(OH-)=c(H+)+c(HC2O )+2c(H2C2O4) )+2c(H2C2O4) |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】设NA为阿伏加德罗常数的值,关于常温下 的
的 溶液(
溶液(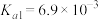 ) ,下列说法正确的是
) ,下列说法正确的是
 的
的 溶液(
溶液(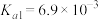 ) ,下列说法正确的是
) ,下列说法正确的是| A.每升溶液中的H+数目约为0.001NA |
B.溶液中c(H3PO4)=c(H2PO )+2c(HPO )+2c(HPO )+3c(PO )+3c(PO ) ) |
| C.加热后,电离平衡常数增大,溶液pH减小 |
| D.加入少量Na3PO4固体后,增大 |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,某水溶液中二元弱酸 的物质的量浓度为
的物质的量浓度为 ,该溶液中存在
,该溶液中存在 ,通过调节溶液
,通过调节溶液 可使
可使 转化为
转化为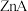 沉淀,体系中
沉淀,体系中 与
与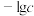 关系如图所示(
关系如图所示( 为
为 、
、 和
和 的浓度,单位为
的浓度,单位为 ),下列说法错误的是
),下列说法错误的是

 的物质的量浓度为
的物质的量浓度为 ,该溶液中存在
,该溶液中存在 ,通过调节溶液
,通过调节溶液 可使
可使 转化为
转化为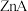 沉淀,体系中
沉淀,体系中 与
与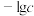 关系如图所示(
关系如图所示( 为
为 、
、 和
和 的浓度,单位为
的浓度,单位为 ),下列说法错误的是
),下列说法错误的是
A.线①表示 |
B.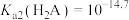 |
C. 的溶液中 的溶液中 |
D. 的溶液中 的溶液中 |
您最近半年使用:0次
单选题
|
较难
(0.4)
【推荐1】下列溶液中各微粒的浓度关系一定正确的是
| A.某酸性溶液中只含NH4+、Cl-、H+、OH-四种离子,则溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| B.在Na2CO3和NaHCO3的混合溶液中:c(Na+)+c(H+)=c(HCO3-)+c(OH-)+c(CO32-) |
| C.将0.1 mol CuSO4·(NH4)2SO4·6H2O溶于水配成的1 L溶液中:c(SO42-)>c(NH4+)>c(Cu2+)>c(H+)>c(OH-) |
| D.等体积、等浓度的NaX溶液和弱酸HX溶液的混合后的溶液中:c(Na+)>c(HX)>c(X-)>c(H+)>c(OH-) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】常温下,现有0.1 mol/L的NH4HCO3溶液,pH=7.8。已知含氮(或含碳)各微粒的分布分数(平衡时某种微粒的浓度占各种微粒浓度之和的分数)与pH的关系如下图所示。下列说法不正确的是( )
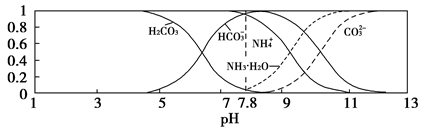

A.NH4HCO3溶液中存在下列守恒关系:c(NH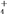 )+c(NH3·H2O)=c(HCO )+c(NH3·H2O)=c(HCO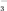 )+c(CO )+c(CO )+c(H2CO3) )+c(H2CO3) |
B.往该溶液中逐滴滴加氢氧化钠时NH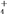 和HCO 和HCO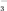 浓度逐渐减小 浓度逐渐减小 |
| C.通过分析可知常温下Kb(NH3·H2O)>Ka1(H2CO3) |
D.当溶液的pH=9时,溶液中存在下列关系:c(HCO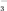 )>c(NH )>c(NH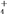 )>c(NH3·H2O)>c(CO )>c(NH3·H2O)>c(CO ) ) |
您最近半年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】室温下,通过下列实验探究0.0100 Na2C2O4溶液的性质。
Na2C2O4溶液的性质。
实验1:实验测得0.0100 Na2C2O4溶液pH为8.6。
Na2C2O4溶液pH为8.6。
实验2:向溶液中滴加等体积0.0100 HCl溶液,pH由8.6降为4.8。
HCl溶液,pH由8.6降为4.8。
实验3:向溶液中加入等体积0.0200 CaCl2溶液,出现白色沉淀。
CaCl2溶液,出现白色沉淀。
已知室温时 ,下列说法
,下列说法不正确 的是
 Na2C2O4溶液的性质。
Na2C2O4溶液的性质。实验1:实验测得0.0100
 Na2C2O4溶液pH为8.6。
Na2C2O4溶液pH为8.6。实验2:向溶液中滴加等体积0.0100
 HCl溶液,pH由8.6降为4.8。
HCl溶液,pH由8.6降为4.8。实验3:向溶液中加入等体积0.0200
 CaCl2溶液,出现白色沉淀。
CaCl2溶液,出现白色沉淀。已知室温时
 ,下列说法
,下列说法A.0.0100 Na2C2O4溶液中满足: Na2C2O4溶液中满足: |
B.实验2滴加盐酸过程中: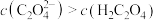 |
C.实验2所得的溶液中: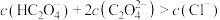 |
D.实验3所得上层清液中  |
您最近半年使用:0次



