水溶液广泛存在于生命体及其赖以生存的环境中。弱电解质的电离平衡、盐类的水解平衡和难溶电解质的沉淀溶解平衡都与日常生活、工农业生产等息息相关。回答下列问题:
(1)25℃时,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,反应后溶液中c( )=c(Cl-),则a
)=c(Cl-),则a___________ 0.01(填“>”、“<”或“=”)。
(2)25℃时,pH=12的NaOH溶液100 mL,要使它的pH降为11,如果加0.01 mol/L HCl溶液,应加___________ mL (结果保留三位有效数字,体积变化忽略不计)。
(3)25℃时,pH=3的盐酸和pH=10的Ba(OH)2溶液中由水电离出的c(H)之比为______ 。
(4)25℃时,已知NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.4×10-2,Ka2=1.4×10-8,则SO2被氨水捕获所得的(NH4)2SO3溶液呈___________ (填“酸”、“碱”或“中")性;SO2也可以被NaOH溶液捕获,所得溶液中c( )∶c(
)∶c( )=1时,该溶液的c(H+)=
)=1时,该溶液的c(H+)=___________ 。
(5)Mg(OH)2是水垢成分之一,室温下Mg(OH)2的Ksp=5.0×10-12,向0.05 mol/L的MgCl2溶液中通入NH3至刚好出现沉淀时,溶液的pH为___________ 。
(6)向0.1 mol/L CH3COOH溶液中加入少量水,溶液中
___________ (填“增大”、“减小”或“不变”)。
(1)25℃时,将a mol/L的氨水与0.01 mol/L的盐酸等体积混合,反应后溶液中c(
 )=c(Cl-),则a
)=c(Cl-),则a(2)25℃时,pH=12的NaOH溶液100 mL,要使它的pH降为11,如果加0.01 mol/L HCl溶液,应加
(3)25℃时,pH=3的盐酸和pH=10的Ba(OH)2溶液中由水电离出的c(H)之比为
(4)25℃时,已知NH3·H2O的Kb=1.8×10-5,H2SO3的Ka1=1.4×10-2,Ka2=1.4×10-8,则SO2被氨水捕获所得的(NH4)2SO3溶液呈
 )∶c(
)∶c( )=1时,该溶液的c(H+)=
)=1时,该溶液的c(H+)=(5)Mg(OH)2是水垢成分之一,室温下Mg(OH)2的Ksp=5.0×10-12,向0.05 mol/L的MgCl2溶液中通入NH3至刚好出现沉淀时,溶液的pH为
(6)向0.1 mol/L CH3COOH溶液中加入少量水,溶液中

更新时间:2023-12-07 22:54:06
|
相似题推荐
填空题
|
适中
(0.65)
名校
解题方法
【推荐1】C元素是组成化合物种类最多的元素,含C元素的酸有也多种,其中氢氰酸(HCN)和草酸( )是两种比较特殊的酸。
)是两种比较特殊的酸。
(1)氢氰酸有剧毒,25℃时,该酸的电离常数为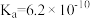 。
。
①HCN在水溶液中的电离方程式为_______ 。
②25℃时KCN溶液中 的水解常数
的水解常数
_______ (保留一位小数)。
③0.2 mol/L的KOH溶液与0.4 mol/L的HCN溶液等体积混合后,恢复到25℃,混合溶液中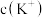 和
和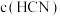 浓度大小关系是
浓度大小关系是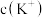
_______ 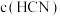 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。
④已知T℃时, ,
, ,则T℃下,
,则T℃下, ,该反应的平衡常数K=
,该反应的平衡常数K=_______ 。
(2)为测定某草酸晶体产品中( )的质量分数,称取14.0 g产品溶于水,配制成500 mL溶液,用浓度为0.10 mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00 mL,实验结果记录如表:(杂质不与高锰酸钾反应,
)的质量分数,称取14.0 g产品溶于水,配制成500 mL溶液,用浓度为0.10 mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00 mL,实验结果记录如表:(杂质不与高锰酸钾反应, 相对分子质量为126)
相对分子质量为126)
已知反应:
①滴定终点的现象是_______ 。
②通过实验数据,计算该产品中( )的质量分数为
)的质量分数为_______ 。
③下列操作会导致测定结果偏低的是_______ 。
A.锥形瓶用待测液润洗
B.装酸性高锰酸钾溶液的滴定管没有润洗
C.滴定前滴定管尖嘴处有气泡,滴定结束后气泡消失
D.滴定前平视,滴定结束时俯视
 )是两种比较特殊的酸。
)是两种比较特殊的酸。(1)氢氰酸有剧毒,25℃时,该酸的电离常数为
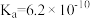 。
。①HCN在水溶液中的电离方程式为
②25℃时KCN溶液中
 的水解常数
的水解常数
③0.2 mol/L的KOH溶液与0.4 mol/L的HCN溶液等体积混合后,恢复到25℃,混合溶液中
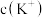 和
和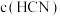 浓度大小关系是
浓度大小关系是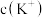
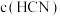 (填“>”、“<”或“=”)。
(填“>”、“<”或“=”)。④已知T℃时,
 ,
, ,则T℃下,
,则T℃下, ,该反应的平衡常数K=
,该反应的平衡常数K=(2)为测定某草酸晶体产品中(
 )的质量分数,称取14.0 g产品溶于水,配制成500 mL溶液,用浓度为0.10 mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00 mL,实验结果记录如表:(杂质不与高锰酸钾反应,
)的质量分数,称取14.0 g产品溶于水,配制成500 mL溶液,用浓度为0.10 mol/L的酸性高锰酸钾溶液滴定,每次所取待测液体积均为25.00 mL,实验结果记录如表:(杂质不与高锰酸钾反应, 相对分子质量为126)
相对分子质量为126)| 实验次数 | 第一次 | 第二次 | 第三次 |
消耗 溶液体积/mL 溶液体积/mL | 20.05 | 19.95 | 24.36 |

①滴定终点的现象是
②通过实验数据,计算该产品中(
 )的质量分数为
)的质量分数为③下列操作会导致测定结果偏低的是
A.锥形瓶用待测液润洗
B.装酸性高锰酸钾溶液的滴定管没有润洗
C.滴定前滴定管尖嘴处有气泡,滴定结束后气泡消失
D.滴定前平视,滴定结束时俯视
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
解题方法
【推荐2】现有浓度均为0.1mol/L的下列溶液:① ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦氨水,请回答下列问题:
⑦氨水,请回答下列问题:
(1)①②③④⑤⑥⑦七种溶液中 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号)___________ 。
(2)溶液②中各离子浓度由大到小的顺序是___________ 。
(3)室温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,混合溶液中
___________  (填“>”“=”或“<”)。
(填“>”“=”或“<”)。
(4)已知t℃, ,在t℃时将pH=11的NaOH溶液aL与pH=2的
,在t℃时将pH=11的NaOH溶液aL与pH=2的 的溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=
的溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=___________ 。
(5)硫酸肼(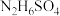 )是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与
)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与 类似,写出硫酸肼第一步水解反应的离子方程式:
类似,写出硫酸肼第一步水解反应的离子方程式:___________ 。
(6)常温下,将 的醋酸与
的醋酸与 溶液等体积混合,充分反应后,溶液中存在
溶液等体积混合,充分反应后,溶液中存在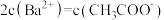 ,则该混合溶液中醋酸的电离常数Ka=
,则该混合溶液中醋酸的电离常数Ka=___________ (用含a和b的代数式表示)。
 ②
② ③
③ ④
④ ⑤
⑤ ⑥
⑥ ⑦氨水,请回答下列问题:
⑦氨水,请回答下列问题:(1)①②③④⑤⑥⑦七种溶液中
 浓度由大到小的顺序是(填序号)
浓度由大到小的顺序是(填序号)(2)溶液②中各离子浓度由大到小的顺序是
(3)室温下,pH=3的醋酸和pH=11的氢氧化钠溶液等体积混合后,混合溶液中

 (填“>”“=”或“<”)。
(填“>”“=”或“<”)。(4)已知t℃,
 ,在t℃时将pH=11的NaOH溶液aL与pH=2的
,在t℃时将pH=11的NaOH溶液aL与pH=2的 的溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=
的溶液bL混合(忽略混合后溶液体积的变化),若所得混合溶液的pH=10,则a∶b=(5)硫酸肼(
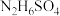 )是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与
)是一种重要的化工原料,属于离子化合物,易溶于水,溶液呈酸性,水解原理与 类似,写出硫酸肼第一步水解反应的离子方程式:
类似,写出硫酸肼第一步水解反应的离子方程式:(6)常温下,将
 的醋酸与
的醋酸与 溶液等体积混合,充分反应后,溶液中存在
溶液等体积混合,充分反应后,溶液中存在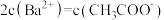 ,则该混合溶液中醋酸的电离常数Ka=
,则该混合溶液中醋酸的电离常数Ka=
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】25℃时,有关物质的电离平衡常数如下:
(1)以上三种电解质的酸性由强至弱顺序为__________________ (用化学式表示,下同)。
(2)常温下,0.02 mol·L-1的CH3COOH溶液的电离度约为______ ,体积为10mLpH=2的醋酸溶液与亚硫酸溶液分别加蒸馏水稀释至1000mL,稀释后溶液的pH,前者________ 后者(填“>、<或=”)。
(3)已知NaHSO3溶液显酸性,其原因是____________ (离子方程式配适当文字叙述)。
(4)H2SO3溶液和NaHCO3溶液反应的主要离子方程式为_______________________ 。
| 化学式 | CH3COOH | H2CO3 | H2SO3 |
| 电离平衡常数K | K=1.8×10-5 | K1=4.3×10-7 K2=5.6×10-11 | K1=1.5×10-2 K2=1.02×10-7 |
(1)以上三种电解质的酸性由强至弱顺序为
(2)常温下,0.02 mol·L-1的CH3COOH溶液的电离度约为
(3)已知NaHSO3溶液显酸性,其原因是
(4)H2SO3溶液和NaHCO3溶液反应的主要离子方程式为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐1】(1)常温下,0.1mol/L的醋酸和0.1mol/L的盐酸各100mL分别与足量的锌粒反应,产生的气体体积前者_______ 后者。(填“大于”“等于”“小于”)
(2)常温下0.1mol/L的醋酸和pH=1的醋酸各100mL分别与足量的锌粒反应,产生的气体前者比后者_____________ 。
(3)在25℃条件下将pH=5的氯化铵溶液稀释100倍,稀释后溶液的pH为(填选项字母,下同)______ 。
A.5 B.7 C.3 — 5之间 D.5 — 7之间
(4)25℃时,向0.1mol/L的醋酸溶液中加入少量醋酸钠晶体,当晶体溶解后测得溶液pH将______ 。
A.增大 B.减小 C.不变 D.无法确定
(5)室温下,向0.1mol/L的H2SO4中加入足量的锌粒,若想减慢制取H2的速率,但又不影响H2的体积,可以向硫酸溶液中加入__________ 试剂。
A.碳酸钠晶体 B.醋酸钠晶体 C.滴加少量的硫酸铜溶液 D.水
(2)常温下0.1mol/L的醋酸和pH=1的醋酸各100mL分别与足量的锌粒反应,产生的气体前者比后者
(3)在25℃条件下将pH=5的氯化铵溶液稀释100倍,稀释后溶液的pH为(填选项字母,下同)
A.5 B.7 C.3 — 5之间 D.5 — 7之间
(4)25℃时,向0.1mol/L的醋酸溶液中加入少量醋酸钠晶体,当晶体溶解后测得溶液pH将
A.增大 B.减小 C.不变 D.无法确定
(5)室温下,向0.1mol/L的H2SO4中加入足量的锌粒,若想减慢制取H2的速率,但又不影响H2的体积,可以向硫酸溶液中加入
A.碳酸钠晶体 B.醋酸钠晶体 C.滴加少量的硫酸铜溶液 D.水
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐2】在一定温度下,有a.盐酸 b.硫酸 c.醋酸三种酸:
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是___________ (用字母表示,下同)。
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是___________ 。
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是___________ 。
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是___________ 。
(5)当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为___________ ,反应所需时间的长短关系是___________ 。
(6)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是___________ 。
(7)将c(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为___________ 。
(1)当三种酸物质的量浓度相同时,c(H+)由大到小的顺序是
(2)同体积、同物质的量浓度的三种酸,中和NaOH的能力由大到小的顺序是
(3)若三者c(H+)相同时,物质的量浓度由大到小的顺序是
(4)当三者c(H+)相同且体积也相同时,分别放入足量的锌,相同状况下产生气体的体积由大到小的顺序是
(5)当三者c(H+)相同且体积相同时,同时加入形状、密度、质量完全相同的锌,若产生相同体积的H2(相同状况),则开始时反应速率的大小关系为
(6)将c(H+)相同的三种酸均加水稀释至原来的100倍后,c(H+)由大到小的顺序是
(7)将c(H+)相同且体积也相同的三种酸,分别与等浓度的NaOH稀溶液反应至pH=7,则消耗NaOH溶液的体积大小关系为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】根据所学知识回答问题
Ⅰ、常温下,用“酸性”“碱性”“中性”或“不确定”填空。
(1)相同浓度的HCl和NaOH溶液等体积混合。___________ 。
(2)pH=2的HCl和pH=12的NaOH溶液等体积混合。___________ 。
(3)pH=2的HCl和pH=12的NH3·H2O等体积混合。___________ 。
Ⅱ、25 ℃时,部分物质的电离平衡常数如表所示:
(4)上述五种酸的酸性由强到弱的顺序是___________ 。
(5)该温度下,0.10 mol·L-1 HNO2溶液中的c(H+)=___________ mol·L-1。
(6)25 ℃时,向NaClO溶液中通入少量的CO2,发生反应的离子方程式为___________ 。
(7)下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是___________ (填序号)。
A.升高温度 B.加水稀释 C.加少量CH3COONa固体
D.加入少量冰醋酸 E.加入少量NaOH固体(温度不变)
Ⅰ、常温下,用“酸性”“碱性”“中性”或“不确定”填空。
(1)相同浓度的HCl和NaOH溶液等体积混合。
(2)pH=2的HCl和pH=12的NaOH溶液等体积混合。
(3)pH=2的HCl和pH=12的NH3·H2O等体积混合。
Ⅱ、25 ℃时,部分物质的电离平衡常数如表所示:
化学式 | 电离平衡常数(Ka或Kb) |
CH3COOH | 1.8×10-5 |
HNO2 | 4.9×10-4 |
HCN | 5×10-10 |
HClO | 3×10-8 |
H2CO3 | Ka1=4.3×10-7 Ka2=5.6×10-11 |
NH3·H2O | 1.8×10-5 |
(5)该温度下,0.10 mol·L-1 HNO2溶液中的c(H+)=
(6)25 ℃时,向NaClO溶液中通入少量的CO2,发生反应的离子方程式为
(7)下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是
A.升高温度 B.加水稀释 C.加少量CH3COONa固体
D.加入少量冰醋酸 E.加入少量NaOH固体(温度不变)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】下表是几种常见弱酸的电离平衡常数:
(1)写出碳酸的电离方程式_______
(2)25℃时,向NaClO溶液中通入少量CO2,反应的离子方程式_______
(3)①常温下,用0.100mol/LNaOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图,c点所示溶液中:2c(C2O )+2c(HC2O
)+2c(HC2O )+2c(H2C2O4)=c(Na+),该草酸溶液的物质的量浓度为
)+2c(H2C2O4)=c(Na+),该草酸溶液的物质的量浓度为_______ mol·L-1
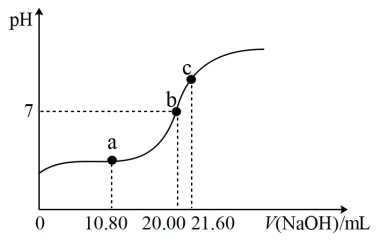
②a点所示溶液中,c(Na+)、c(H+)、c(OH-)、c(HC2O )、c(C2O
)、c(C2O )各离子的浓度由大到小的顺序为
)各离子的浓度由大到小的顺序为_______
(4)滴定过程中选择的指示剂为_______ ,滴定终点的颜色变化为_______ 。
(5)常温下,将SO2通入氨水中,当溶液中的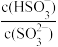 =
=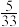 时,此时使溶液的pH为
时,此时使溶液的pH为_______ 。
| 化学式 | HClO | H2SO3 | HCN | H2CO3 | H2C2O4 |
| 电离平衡常数 | K=4.0×10-8 | K1=1.2×10-2 K2=6.6×10-8 | K=6.2×10-10 | K1=4.4×10-7 K2=4.7×10-11 | K1=5.4×10-2 K2=5.4×10-5 |
(1)写出碳酸的电离方程式
(2)25℃时,向NaClO溶液中通入少量CO2,反应的离子方程式
(3)①常温下,用0.100mol/LNaOH溶液滴定20.00mL某未知浓度的H2C2O4溶液,滴定曲线如图,c点所示溶液中:2c(C2O
 )+2c(HC2O
)+2c(HC2O )+2c(H2C2O4)=c(Na+),该草酸溶液的物质的量浓度为
)+2c(H2C2O4)=c(Na+),该草酸溶液的物质的量浓度为
②a点所示溶液中,c(Na+)、c(H+)、c(OH-)、c(HC2O
 )、c(C2O
)、c(C2O )各离子的浓度由大到小的顺序为
)各离子的浓度由大到小的顺序为(4)滴定过程中选择的指示剂为
(5)常温下,将SO2通入氨水中,当溶液中的
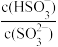 =
=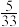 时,此时使溶液的pH为
时,此时使溶液的pH为
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】按要求填空:
(1)为了证明醋酸是弱电解质,某同学分别取pH=3醋酸和盐酸各1mL,分别用蒸馏水稀释到100mL,然后用pH试纸分别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是___ 。
(2)已知室温时,0.1mol∙L-1某一元酸HA在水中有0.1%发生电离,回答下列问题:
①该溶液中c(H+)=__ mol∙L-1。②HA的电离平衡常数K=___ 。
③由HA电离出的c(H+)约为水电离出的c(H+)的__ 倍。
(3)部分弱酸的电离平衡常数如表:
按要求回答下列问题:
①HCOOH、H2S、H2CO3、HClO的酸性由强到弱的顺序为__ 。
②同浓度的HCOO-、HS-、S2-、HCO 、CO
、CO 、ClO-结合H+的能力由强到弱的顺序为
、ClO-结合H+的能力由强到弱的顺序为__ 。
③运用上述电离常数及物质的特性写出下列反应的离子方程式
ⅰ.Na2CO3溶液中通入过量H2S___ 。
ⅱ.过量CO2通入NaClO溶液中__ 。
(4)已知0.1mol·L-1的氢氟酸溶液中存在电离平衡:HF F-+H+,要使溶液中
F-+H+,要使溶液中 增大,可以采取的措施是
增大,可以采取的措施是__ 。
①加少量烧碱 ②通入少量HCl气体 ③通入少量HF气体 ④加水
(1)为了证明醋酸是弱电解质,某同学分别取pH=3醋酸和盐酸各1mL,分别用蒸馏水稀释到100mL,然后用pH试纸分别测定两溶液的pH,则可认定醋酸是弱电解质,判断的依据是
(2)已知室温时,0.1mol∙L-1某一元酸HA在水中有0.1%发生电离,回答下列问题:
①该溶液中c(H+)=
③由HA电离出的c(H+)约为水电离出的c(H+)的
(3)部分弱酸的电离平衡常数如表:
| 弱酸 | HCOOH | H2S | H2CO3 | HClO |
| 电离平衡 常数(25℃) | K=1.77×10-4 | K1=1.3×10-7 K2=7.1×10-15 | K1=4.4×10-7 K2=4.7×10-11 | K=3.0×10-8 |
按要求回答下列问题:
①HCOOH、H2S、H2CO3、HClO的酸性由强到弱的顺序为
②同浓度的HCOO-、HS-、S2-、HCO
 、CO
、CO 、ClO-结合H+的能力由强到弱的顺序为
、ClO-结合H+的能力由强到弱的顺序为③运用上述电离常数及物质的特性写出下列反应的离子方程式
ⅰ.Na2CO3溶液中通入过量H2S
ⅱ.过量CO2通入NaClO溶液中
(4)已知0.1mol·L-1的氢氟酸溶液中存在电离平衡:HF
 F-+H+,要使溶液中
F-+H+,要使溶液中 增大,可以采取的措施是
增大,可以采取的措施是①加少量烧碱 ②通入少量HCl气体 ③通入少量HF气体 ④加水
| A.①② | B.①③ | C.②④ | D.③④ |
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】完成下列问题。
(1)写出下列物质在水溶液中的电离方程式:
CH3COOH的电离_______ 。
NH3·H2O的电离_______ 。
(2)明矾(KAl(SO4)2)可用于净水,原因是(用离子方程式表示):_______ 。
(3)NH4Cl溶液显_______ 性,CH3COONa溶液显_______ 性,NaCl溶液显_______ 性,100℃pH=6的纯水显_______ 性。
(4)pH=a的CH3COOH溶液稀释100倍后所得溶液pH_______ a+2(填”>”或“<”或“=”)。
(5)0.05mol·L-1H2SO4溶液的pH=_______ 。
(1)写出下列物质在水溶液中的电离方程式:
CH3COOH的电离
NH3·H2O的电离
(2)明矾(KAl(SO4)2)可用于净水,原因是(用离子方程式表示):
(3)NH4Cl溶液显
(4)pH=a的CH3COOH溶液稀释100倍后所得溶液pH
(5)0.05mol·L-1H2SO4溶液的pH=
您最近一年使用:0次
【推荐1】碱性锌锰电池是日常生活中消耗量最大的电池,其构造如图所示。
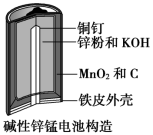
放电时总反应为Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH。从废旧碱性锌锰电池中回收Zn和MnO2的工艺如图所示:
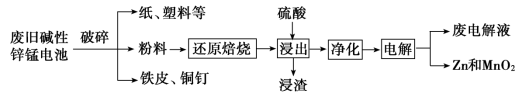
“净化”是为了除去浸出液中的Fe2+,方法是:加入___________ (填化学式)溶液将Fe2+氧化为Fe3+,再调节pH使Fe3+沉淀完全。已知浸出液中Mn2+、Zn2+的浓度约为0.1 mol·L-1,根据下列数据计算,调节pH的合理范围是___________ 。(离子浓度小于1×10-5 mol·L-1即为沉淀完全)

放电时总反应为Zn+2H2O+2MnO2=Zn(OH)2+2MnOOH。从废旧碱性锌锰电池中回收Zn和MnO2的工艺如图所示:

“净化”是为了除去浸出液中的Fe2+,方法是:加入
| 化合物 | Mn(OH)2 | Zn(OH)2 | Fe(OH)3 |
| Ksp近似值 | 10-13 | 10-16 | 10-38 |
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】物质在水中可能存在电离平衡、水解平衡和沉淀溶解平衡,回答下列问题:
(1)一定温度下,向 溶液中加入
溶液中加入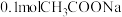 固体,则醋酸的电离平衡逆向移动;溶液中
固体,则醋酸的电离平衡逆向移动;溶液中 的值
的值_______ (填“增大”、“减小”或“不变”)。
(2)某温度下,水的离子积常数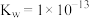 。该温度下,若100体积
。该温度下,若100体积 的
的 溶液与1体积
溶液与1体积 的
的 溶液混合后溶液呈中性,则
溶液混合后溶液呈中性,则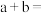
_______ 。
(3) 下,有浓度均为
下,有浓度均为 的三种溶液:a.
的三种溶液:a. ;b.
;b. ;c.
;c.
 三种溶液
三种溶液 由小到大的顺序为:
由小到大的顺序为:_______ (填序号)。
(4)已知 时,
时, ,现将足量氯化银分别放入:a.
,现将足量氯化银分别放入:a. 蒸馏水中;b.
蒸馏水中;b. 溶液中;c.
溶液中;c. 氯化铝溶液中;d.
氯化铝溶液中;d. 盐酸溶液中;充分搅拌后,相同温度下银离子浓度由大到小的顺序是
盐酸溶液中;充分搅拌后,相同温度下银离子浓度由大到小的顺序是_______ (填序号)。
(1)一定温度下,向
 溶液中加入
溶液中加入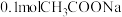 固体,则醋酸的电离平衡逆向移动;溶液中
固体,则醋酸的电离平衡逆向移动;溶液中 的值
的值(2)某温度下,水的离子积常数
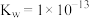 。该温度下,若100体积
。该温度下,若100体积 的
的 溶液与1体积
溶液与1体积 的
的 溶液混合后溶液呈中性,则
溶液混合后溶液呈中性,则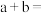
(3)
 下,有浓度均为
下,有浓度均为 的三种溶液:a.
的三种溶液:a. ;b.
;b. ;c.
;c.
 三种溶液
三种溶液 由小到大的顺序为:
由小到大的顺序为:(4)已知
 时,
时, ,现将足量氯化银分别放入:a.
,现将足量氯化银分别放入:a. 蒸馏水中;b.
蒸馏水中;b. 溶液中;c.
溶液中;c. 氯化铝溶液中;d.
氯化铝溶液中;d. 盐酸溶液中;充分搅拌后,相同温度下银离子浓度由大到小的顺序是
盐酸溶液中;充分搅拌后,相同温度下银离子浓度由大到小的顺序是
您最近一年使用:0次

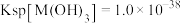 ,要使溶液中的
,要使溶液中的 降至
降至 ,则应调节溶液
,则应调节溶液


