利用铝锂钴废料(主要成分为Co3O4,还含有少量铝箔、LiCoO2等杂质)制备CoC2O4⋅2H2O)的工艺流程如图所示。

已知:Co3O4具有较强氧化性,Co3O4、LiCoO2均难溶于水。
回答下列问题:
(1)写出增大“碱溶”速率的一种方法:_______ ,“碱溶”时发生反应的离子方程式为_______ 。
(2)“酸溶”时,Co3O4发生反应的离子方程式为_______ ;从环保角度考虑,“酸溶”时的试剂_______ (填“能”或“不能”)用浓盐酸代替,简要说明理由:_______ 。
(3)已知 ,要使溶液中的Co2+完全沉淀(即Co2+浓度小于
,要使溶液中的Co2+完全沉淀(即Co2+浓度小于 ),则溶液中
),则溶液中 浓度最小为
浓度最小为_______ mol⋅L-1;简述洗涤CoC2O4⋅2H2O)的操作:_______ 。
(4)已知NH3⋅H2O的电离常数 ,
, 的电离常数
的电离常数 、
、 。则
。则 溶液中各离子浓度由大到小的顺序为
溶液中各离子浓度由大到小的顺序为_______ 。

已知:Co3O4具有较强氧化性,Co3O4、LiCoO2均难溶于水。
回答下列问题:
(1)写出增大“碱溶”速率的一种方法:
(2)“酸溶”时,Co3O4发生反应的离子方程式为
(3)已知
 ,要使溶液中的Co2+完全沉淀(即Co2+浓度小于
,要使溶液中的Co2+完全沉淀(即Co2+浓度小于 ),则溶液中
),则溶液中 浓度最小为
浓度最小为(4)已知NH3⋅H2O的电离常数
 ,
, 的电离常数
的电离常数 、
、 。则
。则 溶液中各离子浓度由大到小的顺序为
溶液中各离子浓度由大到小的顺序为
更新时间:2024-03-06 22:52:36
|
相似题推荐
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐1】现有7种短周期元素,其原子半径及主要化合价如下:
回答下列问题:
(1)B在元素周期表中的位置是_______ 。
(2)上述7种元素形成的简单离子中,离子半径最大的是_______ (用离子符号表示)。
(3)甲是由E和H两种元素组成的_______ (“离子”或“共价”)化合物,用电子式表示其形成过程:_______ 。
(4)元素E与元素F相比,非金属性较强的是_______ (用元素符号表示),下列表述中能证明这一事实的是_______ (填字母)。
a.常温下E的单质和F的单质状态不同
b.E的简单氢化物比F的简单氢化物稳定
c.单质与 化合的难易程度:E<F
化合的难易程度:E<F
(5)元素H的最高价氧化物对应的水化物的水溶液与G的单质反应的离子方程式为_______ 。
| 元素代号 | A | B | D | E | F | G | H |
| 原子半径/nm | 0.037 | 0.074 | 0.075 | 0.099 | 0.102 | 0.143 | 0.186 |
| 主要化合价 | +1 | -2 | +5,-3 | +7,-1 | +6,-2 | +3 | +1 |
(1)B在元素周期表中的位置是
(2)上述7种元素形成的简单离子中,离子半径最大的是
(3)甲是由E和H两种元素组成的
(4)元素E与元素F相比,非金属性较强的是
a.常温下E的单质和F的单质状态不同
b.E的简单氢化物比F的简单氢化物稳定
c.单质与
 化合的难易程度:E<F
化合的难易程度:E<F(5)元素H的最高价氧化物对应的水化物的水溶液与G的单质反应的离子方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】胆矾是一种常见的化合物,工业上它也是一种制取其它含铜化合物的原料,现有废铜(主要杂质为 Fe)来制备胆矾.有人设计了如下流程:

pH 值控制可参考下列数据
请根据上述流程回答下列问题:
(1) A 可选用________ (填字母).
a.稀 H2SO4b.浓 H2SO4、加热 c.浓 FeCl3溶液 d.浓 HNO3
(2) Ⅰ中加 H2O2的目的____________ .
(3) Ⅱ中加 Cu2(OH)2CO3的目的是_________ ,其优点是___________ .
(4) Ⅲ加热煮沸时发生的化学反应的离子方程式为_____________ .
(5) V 中加 H2SO4调节 pH=1 是为了____________ ,某工程师认为上述流程中所加的 A 物质并不理想,需作改进,其理由是_________ ,若你是工程师,将对所加的 A 物质作何改进?请提出建议_________ .

pH 值控制可参考下列数据
| 物质 | 开始沉淀时的 pH 值 | 完全沉淀时的 pH 值 |
| 氢氧化铁 | 2.7 | 3.7 |
| 氢氧化亚铁 | 7.6 | 9.6 |
| 氢氧化铜 | 5.2 | 6.4 |
(1) A 可选用
a.稀 H2SO4b.浓 H2SO4、加热 c.浓 FeCl3溶液 d.浓 HNO3
(2) Ⅰ中加 H2O2的目的
(3) Ⅱ中加 Cu2(OH)2CO3的目的是
(4) Ⅲ加热煮沸时发生的化学反应的离子方程式为
(5) V 中加 H2SO4调节 pH=1 是为了
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
解题方法
【推荐1】甲学生对Cl2与FeCl2和KSCN混合溶液的反应进行实验探究。
(1)B中反应的离子方程式是____ 。
(2)A中溶液变红的原因是____ 。
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在_____ 。
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是SCN—与Cl2发生了反应。
(4)甲同学猜想SCN—可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN—的电子式为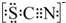
①甲同学认为SCN—中碳元素没有被氧化,理由是_________ 。
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN—中被氧化的元素是__________ 。
③通过实验证明了SCN—中氮元素转化为NO3-,他的实验方案是____ 。
④若SCN—与Cl2反应生成1 mol CO2,则转移电子的物质的量是______ mol。
| 操作 | 现象 |
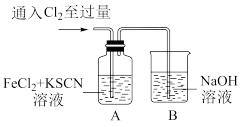 | I.A中溶液变红 II.稍后,溶液由红色变为黄色 |
(2)A中溶液变红的原因是
(3)为了探究现象II的原因,甲同学进行如下实验。
①取A中黄色溶液于试管中,加入NaOH溶液,有红褐色沉淀生成,则溶液中一定存在
②取A中黄色溶液于试管中,加入过量的KSCN溶液,最终得到红色溶液。
甲同学的实验证明产生现象Ⅱ的原因是SCN—与Cl2发生了反应。
(4)甲同学猜想SCN—可能被Cl2氧化了,他又进行了如下研究。
资料显示:SCN—的电子式为
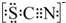
①甲同学认为SCN—中碳元素没有被氧化,理由是
②取A中黄色溶液于试管中,加入用盐酸酸化的BaCl2溶液,产生白色沉淀,由此证明SCN—中被氧化的元素是
③通过实验证明了SCN—中氮元素转化为NO3-,他的实验方案是
④若SCN—与Cl2反应生成1 mol CO2,则转移电子的物质的量是
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
名校
【推荐2】测定溶液中甘油浓度通常采用采用高碘酸氧化还原法,实验步骤如下:
i.配制准确浓度的硫代硫酸钠( )溶液
)溶液
①称取16克 ,溶于1000毫升水中,冷却,备用。
,溶于1000毫升水中,冷却,备用。
②称取0.147克基准重铬酸钾( ),置于碘量瓶中,溶于25毫升水,加2克碘化钾及20毫升
),置于碘量瓶中,溶于25毫升水,加2克碘化钾及20毫升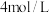 的硫酸,摇匀。于暗处放置10分钟。加75毫升水,用硫代硫酸钠溶液滴定(
的硫酸,摇匀。于暗处放置10分钟。加75毫升水,用硫代硫酸钠溶液滴定(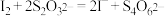 ),近终点时加1毫升0.5%指示剂,继续滴定至溶液由蓝色变为亮绿色。再重复滴定2次,平均用硫代硫酸钠溶液
),近终点时加1毫升0.5%指示剂,继续滴定至溶液由蓝色变为亮绿色。再重复滴定2次,平均用硫代硫酸钠溶液 。
。
ii.甘油含量测定
①准确量取 甘油溶液,放入
甘油溶液,放入 碘量瓶中,再加入
碘量瓶中,再加入 溶液、
溶液、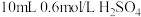 溶液、
溶液、 正己烷,盖好塞盖,摇匀,在室温下于暗处放置
正己烷,盖好塞盖,摇匀,在室温下于暗处放置 。
。
②加入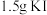 反应
反应 后,再加水
后,再加水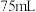 ,剩余的
,剩余的 和反应生成的
和反应生成的 被还原析出碘,析出的碘用配制好的
被还原析出碘,析出的碘用配制好的 标液滴定,滴定至颜色变亮时加入
标液滴定,滴定至颜色变亮时加入 指示剂,此时溶液呈现不透明深蓝色,继续滴至蓝色恰好消失为止。
指示剂,此时溶液呈现不透明深蓝色,继续滴至蓝色恰好消失为止。
③再重复滴定2次,平均用 溶液
溶液 。
。
回答下列问题:
(1)步骤i①的实验操作是否正确_______ (填“正确”或“错误”)。
(2)步骤i②的目的是_______ ,所用的指示剂是_______ , 溶液浓度是
溶液浓度是_______  。
。
(3)甘油( )溶液与
)溶液与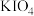 溶液反应生成甲醛、甲酸、
溶液反应生成甲醛、甲酸、 ,写出步骤ii①反应的离子方程式
,写出步骤ii①反应的离子方程式_______ 。步骤ii②中高碘酸与 反应的离子方程式为
反应的离子方程式为_______ 。
(4)步骤ii中下列因素引起测定结果偏高的是_______ 。
a.将碘量瓶换成普通锥形瓶
b.加入的 过量
过量
c.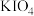 溶液浓度偏小
溶液浓度偏小
d.指示剂一褪色就停止滴定、读数
e.滴定前正视读数,滴定后仰视读数
i.配制准确浓度的硫代硫酸钠(
 )溶液
)溶液①称取16克
 ,溶于1000毫升水中,冷却,备用。
,溶于1000毫升水中,冷却,备用。②称取0.147克基准重铬酸钾(
 ),置于碘量瓶中,溶于25毫升水,加2克碘化钾及20毫升
),置于碘量瓶中,溶于25毫升水,加2克碘化钾及20毫升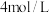 的硫酸,摇匀。于暗处放置10分钟。加75毫升水,用硫代硫酸钠溶液滴定(
的硫酸,摇匀。于暗处放置10分钟。加75毫升水,用硫代硫酸钠溶液滴定(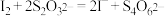 ),近终点时加1毫升0.5%指示剂,继续滴定至溶液由蓝色变为亮绿色。再重复滴定2次,平均用硫代硫酸钠溶液
),近终点时加1毫升0.5%指示剂,继续滴定至溶液由蓝色变为亮绿色。再重复滴定2次,平均用硫代硫酸钠溶液 。
。ii.甘油含量测定
①准确量取
 甘油溶液,放入
甘油溶液,放入 碘量瓶中,再加入
碘量瓶中,再加入 溶液、
溶液、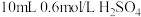 溶液、
溶液、 正己烷,盖好塞盖,摇匀,在室温下于暗处放置
正己烷,盖好塞盖,摇匀,在室温下于暗处放置 。
。②加入
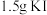 反应
反应 后,再加水
后,再加水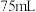 ,剩余的
,剩余的 和反应生成的
和反应生成的 被还原析出碘,析出的碘用配制好的
被还原析出碘,析出的碘用配制好的 标液滴定,滴定至颜色变亮时加入
标液滴定,滴定至颜色变亮时加入 指示剂,此时溶液呈现不透明深蓝色,继续滴至蓝色恰好消失为止。
指示剂,此时溶液呈现不透明深蓝色,继续滴至蓝色恰好消失为止。③再重复滴定2次,平均用
 溶液
溶液 。
。回答下列问题:
(1)步骤i①的实验操作是否正确
(2)步骤i②的目的是
 溶液浓度是
溶液浓度是 。
。(3)甘油(
 )溶液与
)溶液与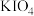 溶液反应生成甲醛、甲酸、
溶液反应生成甲醛、甲酸、 ,写出步骤ii①反应的离子方程式
,写出步骤ii①反应的离子方程式 反应的离子方程式为
反应的离子方程式为(4)步骤ii中下列因素引起测定结果偏高的是
a.将碘量瓶换成普通锥形瓶
b.加入的
 过量
过量c.
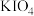 溶液浓度偏小
溶液浓度偏小d.指示剂一褪色就停止滴定、读数
e.滴定前正视读数,滴定后仰视读数
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】钼酸钠(Na2MoO4)是一种冷却水系统的金属缓蚀剂,工业上通常利用钼精矿(主要成分MoS2中硫为-2价)制备钼酸钠晶体的流程如图所示。

回答下列问题:
(1)可以提高钼精矿焙烧效率的措施有_______ 。(任写一种)
(2)NaClO的电子式_______ 。
(3)粗产品焙烧的化学方程式_______ 。
(4)实验室进行操作1所用的玻璃仪器是:烧杯_______ 、_______ ,操作2的步骤是:_______ 、_______ 过滤、洗涤、干燥。
(5)操作3中硫元素被氧化为最高价,发生反应的离子方程式为_______ 。
(6)钼的化合物间有如下转化关系。八钼酸铵的化学式为:_______ 。

(7)某温度下,BaMoO4在水中的沉淀溶解平衡曲线如图所示,要使溶液中钼酸根离子完全沉淀(浓度小于1×10-5mol/L),溶液中Ba2+的浓度应大于_______ mol/L。


回答下列问题:
(1)可以提高钼精矿焙烧效率的措施有
(2)NaClO的电子式
(3)粗产品焙烧的化学方程式
(4)实验室进行操作1所用的玻璃仪器是:烧杯
(5)操作3中硫元素被氧化为最高价,发生反应的离子方程式为
(6)钼的化合物间有如下转化关系。八钼酸铵的化学式为:

(7)某温度下,BaMoO4在水中的沉淀溶解平衡曲线如图所示,要使溶液中钼酸根离子完全沉淀(浓度小于1×10-5mol/L),溶液中Ba2+的浓度应大于

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】燃煤的过程中排放大量CO2、SO2、NOx以及固体颗粒物,对环境污染严重。请回答下列问题:
(1)将煤作为燃料常通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g) ΔH1<0 ①
途径Ⅱ:先制水煤气,后燃烧水煤气
C(s)+H2O(g) CO(g)+H2(g) ΔH2>0 ②
CO(g)+H2(g) ΔH2>0 ②
2CO(g)+O2(g)=2CO2(g) ΔH3<0 ③
2H2(g)+O2(g)=2H2O(g) ΔH4<0 ④
ΔH1、ΔH2、ΔH3、ΔH4的关系式是___________________ 。
(2)已知碳的气化反应在不同温度下平衡常数的对数值(lg K)如表:
升高温度时,反应i中H2的产率________ (填“增大”“减小”或“不变”)。在900 K时,反应CO(g)+H2O(g)=CO2(g)+H2(g)的平衡常数的对数值(lg K)为________ 。
(3)为了减少燃煤污染,可将煤燃烧产生的SO2制成自发电池,其电池总反应为2SO2+O2+2H2O=2H2SO4,该电池的负极反应式为__________________ 用这种方法处理含SO2废气的优点是______________ ;
(4)新型氨法烟气脱硫技术采用氨吸收烟气中的SO2生成亚硫酸铵和亚硫酸氢铵。亚硫酸铵又可用于燃煤烟道气脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的化学方程式________________ 。
(5)用K2CO3溶液可吸收燃煤反应中生成的CO2,常温下pH=10的K2CO3溶液中由水电离的OH-的物质的量浓度为________ 。常温下,0.1 mol·L-1 KHCO3溶液的pH>8,则溶液中c(H2CO3)________ (填“>”“=”或“<”)c(CO32-)。
(1)将煤作为燃料常通过下列两种途径:
途径Ⅰ:C(s)+O2(g)=CO2(g) ΔH1<0 ①
途径Ⅱ:先制水煤气,后燃烧水煤气
C(s)+H2O(g)
 CO(g)+H2(g) ΔH2>0 ②
CO(g)+H2(g) ΔH2>0 ②2CO(g)+O2(g)=2CO2(g) ΔH3<0 ③
2H2(g)+O2(g)=2H2O(g) ΔH4<0 ④
ΔH1、ΔH2、ΔH3、ΔH4的关系式是
(2)已知碳的气化反应在不同温度下平衡常数的对数值(lg K)如表:
| 气化反应 | lg K | ||
| 700 K | 900 K | 1 200 K | |
| i.C(s)+H2O(g)=CO(g)+H2(g) | -2.64 | -0.39 | 1.58 |
| ii. C(s)+2H2O(g)=CO2(g)+2H2(g) | -1.67 | -0.03 | 1.44 |
升高温度时,反应i中H2的产率
(3)为了减少燃煤污染,可将煤燃烧产生的SO2制成自发电池,其电池总反应为2SO2+O2+2H2O=2H2SO4,该电池的负极反应式为
(4)新型氨法烟气脱硫技术采用氨吸收烟气中的SO2生成亚硫酸铵和亚硫酸氢铵。亚硫酸铵又可用于燃煤烟道气脱氮,将氮氧化物转化为氮气,同时生成一种氮肥,形成共生系统。写出二氧化氮与亚硫酸铵反应的化学方程式
(5)用K2CO3溶液可吸收燃煤反应中生成的CO2,常温下pH=10的K2CO3溶液中由水电离的OH-的物质的量浓度为
您最近一年使用:0次
【推荐2】工业上采用 溶液吸收尾气中的
溶液吸收尾气中的 。25℃时,向
。25℃时,向 溶液中滴加NaOH溶液,
溶液中滴加NaOH溶液, 、
、 及
及 的物质的量分数
的物质的量分数 随溶液pH的变化如图1所示[
随溶液pH的变化如图1所示[ ];向
];向 溶液中滴加NaOH溶液,
溶液中滴加NaOH溶液, 、
、 及
及 的物质的量分数
的物质的量分数 随溶液pH的变化如图2所示。
随溶液pH的变化如图2所示。

回答下列问题:
(1)碳酸的二级电离常数是___________ 。
(2)在含等物质的量的 、
、 的混合溶液中,
的混合溶液中,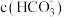
___________ 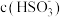 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(3)用 吸收液吸收
吸收液吸收 ,当碳以
,当碳以 形式存在(
形式存在( 和
和 忽略不计)时,硫以
忽略不计)时,硫以___________ 形式存在(填离子符号)。
(4)用 吸收液充分吸收
吸收液充分吸收 (
( 过量)。
过量)。
①发生反应的化学方程式是___________ 。
②用下图装置将充分吸收 后的吸收液电解生成NaOH、
后的吸收液电解生成NaOH、 ,以回收利用。
,以回收利用。

其中R接直流电源的___________ 极,R极上的电极反应式是___________ 。
 溶液吸收尾气中的
溶液吸收尾气中的 。25℃时,向
。25℃时,向 溶液中滴加NaOH溶液,
溶液中滴加NaOH溶液, 、
、 及
及 的物质的量分数
的物质的量分数 随溶液pH的变化如图1所示[
随溶液pH的变化如图1所示[ ];向
];向 溶液中滴加NaOH溶液,
溶液中滴加NaOH溶液, 、
、 及
及 的物质的量分数
的物质的量分数 随溶液pH的变化如图2所示。
随溶液pH的变化如图2所示。
回答下列问题:
(1)碳酸的二级电离常数是
(2)在含等物质的量的
 、
、 的混合溶液中,
的混合溶液中,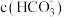
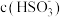 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(3)用
 吸收液吸收
吸收液吸收 ,当碳以
,当碳以 形式存在(
形式存在( 和
和 忽略不计)时,硫以
忽略不计)时,硫以(4)用
 吸收液充分吸收
吸收液充分吸收 (
( 过量)。
过量)。①发生反应的化学方程式是
②用下图装置将充分吸收
 后的吸收液电解生成NaOH、
后的吸收液电解生成NaOH、 ,以回收利用。
,以回收利用。
其中R接直流电源的
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】碳及其化合物在工农业上有重要作用。
Ⅰ、在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g) CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表所示:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表所示:
回答下列问题:
(1)该反应的化学平衡常数表达式为K=___________ 。该反应为__________ (填“吸热”或“放热”)反应。
(2)某温度下平衡浓度符合下式: c(CO2)·c(H2)=c(CO)·c(H2O),该温度下加入1 mol CO2(g)和1 mol H2(g),充分反应,达到平衡时,CO2的转化率为______________ 。
(3)在800 ℃时发生上述反应,某时刻测得容器内各物质的浓度分别为c(CO2)为2 mol/L,c(H2)为1.5 mol/L,c(CO)为1 mol/L,c(H2O)为3 mol/L,则正、逆反应速率的比较为:v正___________ v逆(填“>”“<”或“=”)。
Ⅱ、工业上用CO2和H2反应合成甲醚。已知:
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1=-53.7kJ•mol-1
CH3OCH3(g)+H2O(g)═2CH3OH(g)△H2=+23.4kJ•mol-1
则2CO2(g)+6H2(g) CH3OCH3(g)+3H2O(g)△H3=
CH3OCH3(g)+3H2O(g)△H3=_______________ kJ·mol-1。
Ⅲ、常温下用氨水吸收CO2可得到NH4HCO3溶液,在该溶液中,c(NH4+)________ (填“>”、“<”或“=”)c(HCO3—);反应NH4++HCO3—+H2O NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=__________ 。(已知常温下NH3·H2O的电离平衡常数Kb=2×10-5,H2CO3的电离平衡常数K1=4×10-7,K2=4×10-11)
Ⅰ、在一定体积的密闭容器中,进行如下化学反应:CO2(g)+H2(g)
 CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表所示:
CO(g)+H2O(g),其化学平衡常数K和温度T的关系如表所示:| T/℃ | 700 | 800 | 830 | 1000 | 1200 |
| K | 0.6 | 0.9 | 1.0 | 1.7 | 2.6 |
回答下列问题:
(1)该反应的化学平衡常数表达式为K=
(2)某温度下平衡浓度符合下式: c(CO2)·c(H2)=c(CO)·c(H2O),该温度下加入1 mol CO2(g)和1 mol H2(g),充分反应,达到平衡时,CO2的转化率为
(3)在800 ℃时发生上述反应,某时刻测得容器内各物质的浓度分别为c(CO2)为2 mol/L,c(H2)为1.5 mol/L,c(CO)为1 mol/L,c(H2O)为3 mol/L,则正、逆反应速率的比较为:v正
Ⅱ、工业上用CO2和H2反应合成甲醚。已知:
CO2(g)+3H2(g)═CH3OH(g)+H2O(g)△H1=-53.7kJ•mol-1
CH3OCH3(g)+H2O(g)═2CH3OH(g)△H2=+23.4kJ•mol-1
则2CO2(g)+6H2(g)
 CH3OCH3(g)+3H2O(g)△H3=
CH3OCH3(g)+3H2O(g)△H3=Ⅲ、常温下用氨水吸收CO2可得到NH4HCO3溶液,在该溶液中,c(NH4+)
 NH3·H2O+H2CO3的平衡常数K=
NH3·H2O+H2CO3的平衡常数K=
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐1】已知草酸镍晶体(NiC2O4·2H2O)难溶于水,工业上从废镍催化剂(主要成分为Ni,含有一定量的Al2O3、FeO、SiO2以及少量Ca)制备草酸镍晶体的流程如下图所示:

已知:相关金属离子生成氢氧化物沉淀的pH见表中数据:
回答下列问题:
(1)滤渣1的主要成分是_______ (写化学式)。
(2)步骤II加入H2O2“氧化”的目的是_______ ;试剂a“调pH”时pH的调控范围为_______ ;为检验滤液2中是否含有Fe3+,可选用的化学试剂是_______ 。
(3)当离子浓度小于1×10-5mol·L-1时,视为完全沉淀。“沉钙”后,当溶液c(F-)=1×10-3mol·L-1,Ca2+是否沉淀完全?_______ (填“是”或“否”),理由是_______ [Ksp(CaF2)=1.46×10-10]。
(4)操作a包括过滤、洗涤、110°C下烘干等,其中干燥温度不能超过110°C的原因是_______ ;检验草酸镍晶体已经洗涤干净的实验操作及现象是_______ 。
(5)测定草酸镍晶体的纯度:取mg样品加入过量稀硫酸完全溶解,配成100mL溶液,量取25.00mL溶液用cmol·L-1的KMnO4标准溶液进行滴定(C2O →CO2、MnO
→CO2、MnO →Mn2+),相同条件下,重复滴定三次,平均消耗KMnO4标准溶液VmL。
→Mn2+),相同条件下,重复滴定三次,平均消耗KMnO4标准溶液VmL。
①滴定至终点的现象是_______ 。
②草酸镍晶体的纯度为_______ (NiC2O4·2H2O的摩尔质量M g·mol-1)。

已知:相关金属离子生成氢氧化物沉淀的pH见表中数据:
| 金属离子 | Fe3+ | Fe2+ | Al3+ | Ni2+ |
| 开始沉淀的pH | 1.1 | 5.8 | 3.0 | 6.8 |
| 完全沉淀的pH | 3.2 | 8.8 | 5.0 | 9.5 |
(1)滤渣1的主要成分是
(2)步骤II加入H2O2“氧化”的目的是
(3)当离子浓度小于1×10-5mol·L-1时,视为完全沉淀。“沉钙”后,当溶液c(F-)=1×10-3mol·L-1,Ca2+是否沉淀完全?
(4)操作a包括过滤、洗涤、110°C下烘干等,其中干燥温度不能超过110°C的原因是
(5)测定草酸镍晶体的纯度:取mg样品加入过量稀硫酸完全溶解,配成100mL溶液,量取25.00mL溶液用cmol·L-1的KMnO4标准溶液进行滴定(C2O
 →CO2、MnO
→CO2、MnO →Mn2+),相同条件下,重复滴定三次,平均消耗KMnO4标准溶液VmL。
→Mn2+),相同条件下,重复滴定三次,平均消耗KMnO4标准溶液VmL。①滴定至终点的现象是
②草酸镍晶体的纯度为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】某油脂厂废弃的油脂加氢镍催化剂主要含金属Ni、Al、Fe及其氧化物,还有少量其他不溶性物质。采用如下工艺流程回收其中的镍制备硫酸镍晶体(NiSO4·7H2O):
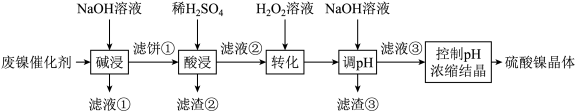
溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
回答下列问题:
(1)为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式___________ 。
(2)“滤液②”中含有的金属离子是___________ 。
(3)“转化”中可替代H2O2的物质是___________ 。若工艺流程改为先“调pH”后“转化”,即如图所示,“滤液③”中可能含有的杂质离子为___________ 。
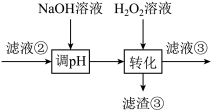
(4)如果“转化”后的溶液中Ni2+浓度为1.0mol·L−1,则“调pH”应控制的pH范围是___________ 。
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式___________ 。
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是___________ 。

溶液中金属离子开始沉淀和完全沉淀的pH如表所示:
| 金属离子 | Ni2+ | Al3+ | Fe3+ | Fe2+ |
| 开始沉淀时(c=0.01mol·L−1)的pH | 7.2 | 3.7 | 2.2 | 7.5 |
| 沉淀完全时(c=1.0×10−5mol·L−1)的pH | 8.7 | 4.7 | 3.2 | 9.0 |
(1)为回收金属,用稀硫酸将“滤液①”调为中性,生成沉淀。写出该反应的离子方程式
(2)“滤液②”中含有的金属离子是
(3)“转化”中可替代H2O2的物质是

(4)如果“转化”后的溶液中Ni2+浓度为1.0mol·L−1,则“调pH”应控制的pH范围是
(5)硫酸镍在强碱溶液中用NaClO氧化,可沉淀出能用作镍镉电池正极材料的NiOOH。写出该反应的离子方程式
(6)将分离出硫酸镍晶体后的母液收集、循环使用,其意义是
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐3】半导体芯片行业是金属靶材的主要应用领域之一。利用镍铂靶材废料(主要成分为 、
、 以及微量
以及微量 、
、 的单质)采用选择性溶解法回收铂并制备硫酸镍晶体的一种工艺流程如图:
的单质)采用选择性溶解法回收铂并制备硫酸镍晶体的一种工艺流程如图:

已知:①王水是按浓盐酸和浓硝酸的体积比为3∶1配制而成
②氧化性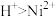
③溶液中金属离子开始沉淀和完全沉淀的 如表所示:
如表所示:
(1)工业上常将废料粉碎后再“酸浸”,其目的是____________________________ 。
(2)“转化”时发生反应的离子方程式为____________________________ 。
(3)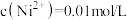 ,则调
,则调 应控制的
应控制的 范围是
范围是______________ 。
(4)在王水中生成二元强酸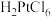 ,其中
,其中 元素的化合价为
元素的化合价为______ 。沉铂过程中发生的可逆反应的化学方程式为______ ,结合平衡移动原理分析 沉淀率随温度升高而
沉淀率随温度升高而______ (填“增大”、“减小”或“不变”)。
(5)“操作1”中包括过滤及沉淀的洗涤,洗涤沉淀时最好选用下列哪种试剂_______。
(6)“酸浸”过程中镍的浸出率与温度和时间的关系如图所示,“酸浸”的最佳温度和时间是_____ 。

 、
、 以及微量
以及微量 、
、 的单质)采用选择性溶解法回收铂并制备硫酸镍晶体的一种工艺流程如图:
的单质)采用选择性溶解法回收铂并制备硫酸镍晶体的一种工艺流程如图:
已知:①王水是按浓盐酸和浓硝酸的体积比为3∶1配制而成
②氧化性
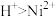
③溶液中金属离子开始沉淀和完全沉淀的
 如表所示:
如表所示:金属离子 |
|
|
|
|
开始沉淀时( | 7.2 | 3.7 | 2.2 | 7.5 |
沉淀完全时( | 8.7 | 4.7 | 3.2 | 9.0 |
(1)工业上常将废料粉碎后再“酸浸”,其目的是
(2)“转化”时发生反应的离子方程式为
(3)
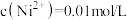 ,则调
,则调 应控制的
应控制的 范围是
范围是(4)在王水中生成二元强酸
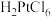 ,其中
,其中 元素的化合价为
元素的化合价为 沉淀率随温度升高而
沉淀率随温度升高而(5)“操作1”中包括过滤及沉淀的洗涤,洗涤沉淀时最好选用下列哪种试剂_______。
| A.蒸馏水 | B.浓盐酸 | C.饱和氯化铵溶液 | D.王水 |

您最近一年使用:0次

 ,
, ,
, ,取样于三支试管中,分别进行如下实验:①加入适量盐酸,有气泡放出;②加入硝酸银溶液,生成黄色沉淀;③加氯水和淀粉后,变为蓝色。
,取样于三支试管中,分别进行如下实验:①加入适量盐酸,有气泡放出;②加入硝酸银溶液,生成黄色沉淀;③加氯水和淀粉后,变为蓝色。







