一定温度下, 在不同pH的
在不同pH的 溶液中存在形式不同,
溶液中存在形式不同, 溶液中pM[
溶液中pM[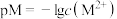 ]随pH的变化如图1,
]随pH的变化如图1, 溶液中含A微粒的物质的量分数随pH的变化如图2。
溶液中含A微粒的物质的量分数随pH的变化如图2。
①MA, 均为难溶物;
均为难溶物;
②初始 。
。
下列说法错误的是
 在不同pH的
在不同pH的 溶液中存在形式不同,
溶液中存在形式不同, 溶液中pM[
溶液中pM[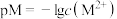 ]随pH的变化如图1,
]随pH的变化如图1, 溶液中含A微粒的物质的量分数随pH的变化如图2。
溶液中含A微粒的物质的量分数随pH的变化如图2。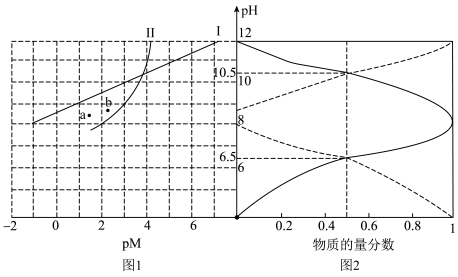
①MA,
 均为难溶物;
均为难溶物;②初始
 。
。下列说法错误的是
A.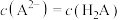 时,pH=8.5 时,pH=8.5 |
B.初始状态a点主要发生反应: |
C.Ⅰ曲线上的点满足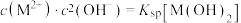 |
D.初始状态的b点,平衡后溶液中存在 |
更新时间:2024-05-25 13:39:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列说法正确的个数为( )
①pH=0的溶液中Fe3+与S2−因发生双水解而不共存
②MgCl2溶液蒸干灼烧后得MgO固体,如果想要得到MgCl2固体应通入HCl的气流
③将0.1mol的Na2CO3溶于水中,形成溶液中阴离子总数小于0.1NA
④HCO 和AlO
和AlO 在溶液中因为互相抑制水解而大量共存
在溶液中因为互相抑制水解而大量共存
⑤pH=2的盐酸和醋酸,均稀释到pH=5,醋酸加水量大
⑥NaHSO3溶液中加入少量NaOH固体, 将增大
将增大
①pH=0的溶液中Fe3+与S2−因发生双水解而不共存
②MgCl2溶液蒸干灼烧后得MgO固体,如果想要得到MgCl2固体应通入HCl的气流
③将0.1mol的Na2CO3溶于水中,形成溶液中阴离子总数小于0.1NA
④HCO
 和AlO
和AlO 在溶液中因为互相抑制水解而大量共存
在溶液中因为互相抑制水解而大量共存⑤pH=2的盐酸和醋酸,均稀释到pH=5,醋酸加水量大
⑥NaHSO3溶液中加入少量NaOH固体,
 将增大
将增大| A.2个 | B.3个 | C.4个 | D.5个 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知AG=lg ,电离度(α)=
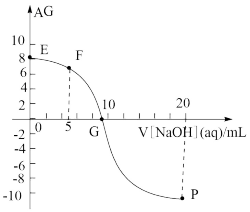
,电离度(α)= ×100%。常温下,向10mL 0.1mol•L﹣1HR溶液中滴加pH=13的NaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。下列说法错误的是
×100%。常温下,向10mL 0.1mol•L﹣1HR溶液中滴加pH=13的NaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。下列说法错误的是
 ,电离度(α)=
,电离度(α)= ×100%。常温下,向10mL 0.1mol•L﹣1HR溶液中滴加pH=13的NaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。下列说法错误的是
×100%。常温下,向10mL 0.1mol•L﹣1HR溶液中滴加pH=13的NaOH溶液,混合溶液中AG与滴加NaOH溶液体积的关系如图所示。下列说法错误的是
| A.F点溶液pH<7 |
| B.水的电离程度G>P>F>E |
C.点P前随着NaOH溶液的加入, 增大 增大 |
| D.常温下,HR的电离度约为1% |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】已知NA为阿伏加德罗常数的值,下列叙述不正确的是
| A.12 g石墨烯(单层石墨)和12g金刚石中含有的碳碳键数前者小于后者 |
| B.常温下,1L 0.1mol·L-1氯化铵溶液中加入氨水至溶液为中性,则溶液含铵根离子数小于0.1NA |
| C.用惰性电极电解CuSO4溶液一段时间后,若加入9.8 g Cu(OH)2能使溶液复原,则电解过程中转移电子的数目为0.4NA |
| D.10g质量分数为46%的甲酸水溶液中含有的氢原子数为0.8NA |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】某矿物含Al2O3、MgO,工业上先用过量烧碱溶液处理该矿物,然后过滤。再往所得滤液中逐滴加入NaHCO3溶液,测得溶液pH和生成Al(OH)3的物质的量与所加入NaHCO3溶液体积变化的曲线见下图。点e的坐标为(40,32)。
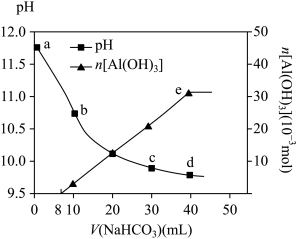
有关说法错误的是

有关说法错误的是
A.生成沉淀时的离子方程式:HCO +AlO +AlO +H2O →Al(OH)3↓+CO +H2O →Al(OH)3↓+CO |
B.NaHCO3溶液中:c(H2CO3)+c(HCO )+c(CO )+c(CO )=0.8mol/L )=0.8mol/L |
C.a点溶液存在:c(Na+)+c(H+)=c(AlO )+c(OH-) )+c(OH-) |
| D.水的电离程度:点a <点b |
您最近一年使用:0次
【推荐1】利用镍铂靶材废料(主要成分为 以及微量
以及微量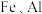 的单质)回收铂的一种工艺流程如图所示.下列说法错误的是
的单质)回收铂的一种工艺流程如图所示.下列说法错误的是 ;
;
②室温下: .
.
 以及微量
以及微量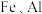 的单质)回收铂的一种工艺流程如图所示.下列说法错误的是
的单质)回收铂的一种工艺流程如图所示.下列说法错误的是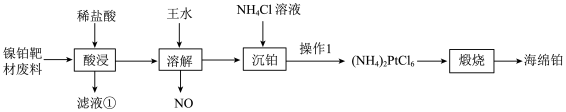
 ;
;②室温下:
 .
.| A.“酸浸”时为加快化学反应速率,须在较高温度下进行 |
B.“沉铂”时,若向 的溶液中加入等体积的 的溶液中加入等体积的 溶液,使 溶液,使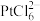 沉淀完全,则 沉淀完全,则 溶液的最小浓度为 溶液的最小浓度为 (忽略溶液混合后体积的变化) (忽略溶液混合后体积的变化) |
C.“操作1”中包括过滤及沉淀的洗涤、干燥,洗涤沉淀时最好选用饱和 溶液 溶液 |
D.隔绝空气“煅烧”时每生成 ,理论上产生标准状况下 ,理论上产生标准状况下 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】已知Ksp(Mg(OH)2)=1.8×10-11,则:Mg(OH)2在水中的溶解的浓度为
| A.2.6×10-4mol/L | B.1.7×10-4mol/L | C.4.2×10-6mol/L | D.3.2×10-22mol/L |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐3】25℃时,向10mL0.10mol/LBaCl2溶液中滴加0.10mol/LNa2CO3溶液,滴加过程中溶液中-lgc(Ba2+)与Na2CO3溶液体积(V)的关系如图所示;Ksp=(BaSO4)=10-9.96,下列说法不正确的是


| A.Ksp(BaCO3)=10-8.58 |
B.b点溶液中:c( )+c( )+c( )+c(H2CO3)= )+c(H2CO3)= c(Na+) c(Na+) |
| C.若改用0.20mol/LNa2CO3溶液来滴定,则恰好反应点由b向左平移 |
| D.若把Na2CO3溶液换成等浓度Na2SO4溶液,则曲线变为Ⅰ |
您最近一年使用:0次

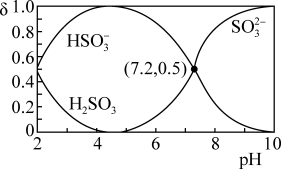
 时,溶液中H2SO3、HSO
时,溶液中H2SO3、HSO 的物质的量分数随pH的分布如图所示。下列叙述错误的是
的物质的量分数随pH的分布如图所示。下列叙述错误的是