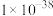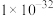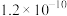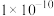自然界中化合态硫主要以FeS2(黄铁矿)、CuFeS2(黄铜矿)等矿物形式存在。用黄铜矿炼铜的总反应为: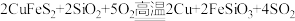 。
。
(1)该反应中_______ 元素被还原,如果在反应中生成1molCu,转移电子数为____ (用NA表示阿伏加德罗常数)。
(2)上述产生的SO2是一种大气污染物,不能直接排放到大气中,目前工业上常用的处理方法有多种。
I、用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4
①写出上述转化中生成NH4HSO3的化学方程式_______ (用一个方程式表示)若想提高该过程中SO2的除去速率,可采取的措施为_______ (填序号)
②25℃时0.lmol·L—1 (NH4)2SO4溶液的pH=5,其原因是_______ (用离子方程式表示),若水解常数用Kb表示,则该溶液中铵根离子的水解常数Kb约为______________ .
Ⅱ、“钠碱法”:用NaOH溶液作吸收剂吸收SO2
③当n(NaOH)∶n(SO2)=_______ 时,吸收SO2的成本最低,所得吸收液中各离子浓度大小关系是_______ ,向吸收液中加入NaOH可得到_______ 。
A. 增大氨水浓度
B. 升高反应温度
C. 使气体与氨水充分接触
D. 通入空气使HSO 转化为SO
转化为SO
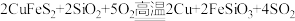 。
。(1)该反应中
(2)上述产生的SO2是一种大气污染物,不能直接排放到大气中,目前工业上常用的处理方法有多种。
I、用氨水将SO2转化为NH4HSO3,再氧化成(NH4)2SO4
①写出上述转化中生成NH4HSO3的化学方程式
②25℃时0.lmol·L—1 (NH4)2SO4溶液的pH=5,其原因是
Ⅱ、“钠碱法”:用NaOH溶液作吸收剂吸收SO2
③当n(NaOH)∶n(SO2)=
A. 增大氨水浓度
B. 升高反应温度
C. 使气体与氨水充分接触
D. 通入空气使HSO
 转化为SO
转化为SO
更新时间:2016-12-09 07:43:41
|
相似题推荐
解答题-实验探究题
|
适中
(0.65)
【推荐1】实验室里除了用二氧化锰和浓盐酸加热制取氯气,也可以在常温下利用反应: 制取并收集纯净、干燥的氯气,装置如图所示:
制取并收集纯净、干燥的氯气,装置如图所示:
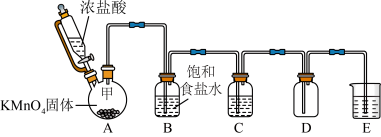
(1)①装置A中甲仪器的名称是_______ 。
②装置B的作用是_______ 。
③装置C中盛装的药品是_______ 。
④装置E中发生反应的化学方程是_______ 。
(2) 。若产生
。若产生 ,则转移的电子数目为
,则转移的电子数目为_______ ,浓盐酸体现了_______ 性质(选填字母编号)。
A.酸性 B.碱性 C.氧化性 D.还原性
(3)在该反应中,被还原的元素是_______ ,氧化剂与还原剂的物质的量之比为_______ 。
 制取并收集纯净、干燥的氯气,装置如图所示:
制取并收集纯净、干燥的氯气,装置如图所示:
(1)①装置A中甲仪器的名称是
②装置B的作用是
③装置C中盛装的药品是
④装置E中发生反应的化学方程是
(2)
 。若产生
。若产生 ,则转移的电子数目为
,则转移的电子数目为A.酸性 B.碱性 C.氧化性 D.还原性
(3)在该反应中,被还原的元素是
您最近一年使用:0次
【推荐2】二硫化钨(WS2,WS2中W的化合价为+4)可用作润滑剂及石油化工领域中的催化剂。由钨铁矿(其主要成分是FeWO4,还含少量Al2O3)制备二硫化钨的工艺流程如下:
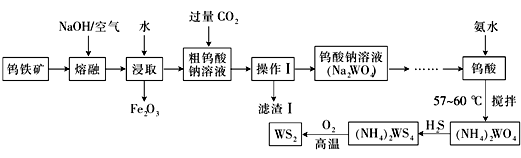
请回答下列问题:
(1)已知:W元素的原子序数是74,请写出W元素在周期表中的位置:_________________
(2)操作Ⅰ中用到的玻璃仪器有________________________________
(3)写出FeWO4在碱熔过程中发生反应的化学方程式:_________________________________
(4)滤渣Ⅰ中主要成分的形成可用离子方程式表示为:_________________________________
(5)钨丝灯管中的W在使用过程中缓慢挥发而使灯丝变细,加入碘单质可以延长使用寿命,其原理为:W(s)+2I2(g) WI4(g)下列说法正确的有_______
WI4(g)下列说法正确的有_______
(6)已知常温下,Ksp(CaWO4) =1×10-10,浓度为x mol/L的Na2WO4溶液与浓度为1×10-4 mol/L的CaCl2溶液按体积比2:1混合,产生CaWO4沉淀,则x≥___________
(7)已知生成二硫化钨的化学方程式为:2(NH4)2WS4+3O2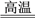 2WS2+4NH3+2S+2SO2+2H2O,若生成124克WS2,则反应所转移的电子数目为
2WS2+4NH3+2S+2SO2+2H2O,若生成124克WS2,则反应所转移的电子数目为________________

请回答下列问题:
(1)已知:W元素的原子序数是74,请写出W元素在周期表中的位置:
(2)操作Ⅰ中用到的玻璃仪器有
(3)写出FeWO4在碱熔过程中发生反应的化学方程式:
(4)滤渣Ⅰ中主要成分的形成可用离子方程式表示为:
(5)钨丝灯管中的W在使用过程中缓慢挥发而使灯丝变细,加入碘单质可以延长使用寿命,其原理为:W(s)+2I2(g)
 WI4(g)下列说法正确的有_______
WI4(g)下列说法正确的有_______| A.灯管内的I2可以循环使用 |
| B.WI4在灯丝上分解,产生的W又在灯丝上沉积 |
| C.温度升高时,WI4的分解速率加快,而W和I2的合成速率减慢 |
| D.WI4在灯管壁上分解,使灯管寿命延长 |
(7)已知生成二硫化钨的化学方程式为:2(NH4)2WS4+3O2
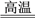 2WS2+4NH3+2S+2SO2+2H2O,若生成124克WS2,则反应所转移的电子数目为
2WS2+4NH3+2S+2SO2+2H2O,若生成124克WS2,则反应所转移的电子数目为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。
常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。 和
和 (亚氯酸钠)均具有漂白性,工业上由
(亚氯酸钠)均具有漂白性,工业上由 气体制取
气体制取 固体的工艺流程如图所示:
固体的工艺流程如图所示:

请回答下列问题:
(1)吸收器中生成 的离子方程式为(补充完整):
的离子方程式为(补充完整):_____ 。
①______ ______
______ ______=______
______=______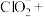 ______
______ ______
______
②此氧化还原反应中,双氧水表现______ 性;若 完全反应,
完全反应,______ (填“得到”或“失去”)的电子数为______ 个,生成的气体产物的体积为__________ (标况下)。
(2)为了探究 和
和 的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有:
的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有: 溶液、KI溶液、淀粉溶液、
溶液、KI溶液、淀粉溶液、 酸性溶液
酸性溶液
(3)工业上可以用草酸( ,二元弱酸)还原
,二元弱酸)还原 的方法生产
的方法生产 ,草酸被氧化为
,草酸被氧化为 ,请写出该反应的离子方程式
,请写出该反应的离子方程式__________________ 。
(4)工业上制取 (亚氯酸钠)固体,理论上至少需要常温常压下
(亚氯酸钠)固体,理论上至少需要常温常压下 气体的体积为
气体的体积为______ L。(常温常压下,气体摩尔体积为24.5L/mol,计算结果保留两位小数)。
 常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。
常温下为黄色气体,易溶于水,其水溶液是一种广谱杀菌剂。 和
和 (亚氯酸钠)均具有漂白性,工业上由
(亚氯酸钠)均具有漂白性,工业上由 气体制取
气体制取 固体的工艺流程如图所示:
固体的工艺流程如图所示:
请回答下列问题:
(1)吸收器中生成
 的离子方程式为(补充完整):
的离子方程式为(补充完整):①______
 ______
______ ______=______
______=______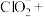 ______
______ ______
______②此氧化还原反应中,双氧水表现
 完全反应,
完全反应,(2)为了探究
 和
和 的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有:
的氧化性或还原性,某兴趣小组进行下列2个实验,请完成实验报告。实验②可供选用的试剂有: 溶液、KI溶液、淀粉溶液、
溶液、KI溶液、淀粉溶液、 酸性溶液
酸性溶液序号 | 实验操作 | 实验现象 | 实验结论 |
① | 将 通入足量KI溶液中,加入稀硫酸,再加入几滴淀粉溶液 通入足量KI溶液中,加入稀硫酸,再加入几滴淀粉溶液 | ||
② |  溶液 溶液 |
|
 ,二元弱酸)还原
,二元弱酸)还原 的方法生产
的方法生产 ,草酸被氧化为
,草酸被氧化为 ,请写出该反应的离子方程式
,请写出该反应的离子方程式(4)工业上制取
 (亚氯酸钠)固体,理论上至少需要常温常压下
(亚氯酸钠)固体,理论上至少需要常温常压下 气体的体积为
气体的体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】我国力争于2030年前做到碳达峰,2060年前实现碳中和。资源化利用碳氧化合物能有效减少 排放,实现自然界中的碳循环。
排放,实现自然界中的碳循环。
(1)以 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:
I.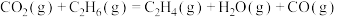
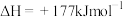 (主反应)
(主反应)
II.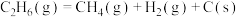
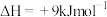 (副反应)
(副反应)
反应 的反应历程可分为如下两步:
的反应历程可分为如下两步:
i.

ii.
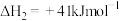
①
______ 。
②相比于提高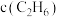 ,提高
,提高 对反应
对反应 速率影响更大,可能的原因是
速率影响更大,可能的原因是______ 。
③ 时,向一恒容密闭容器中充入物质的量之比为
时,向一恒容密闭容器中充入物质的量之比为 的
的 和
和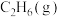 ,反应物转化率与反应温度的关系如图所示。在
,反应物转化率与反应温度的关系如图所示。在 ,
, 得选择性
得选择性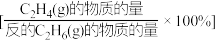 为
为______ 。

(2) 可制甲烷化,
可制甲烷化, 可制甲烷化过程中,
可制甲烷化过程中, 活化的可能途径如图所示。
活化的可能途径如图所示。 是
是 活化的优势中间体,可能的原因是
活化的优势中间体,可能的原因是______ 。

(3) 可用
可用 吸收,发生反应:
吸收,发生反应: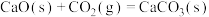 。在不同温度下,达到平衡时体系中
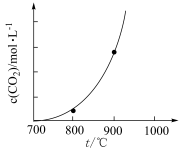
。在不同温度下,达到平衡时体系中 物质的量浓度[
物质的量浓度[ ]与温度的关系如图所示。
]与温度的关系如图所示。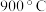 下的
下的 远大于
远大于 下的
下的 ,其原因是
,其原因是______ 。
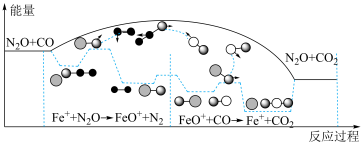
(4)研究表明 与
与 在
在 作用下发生反应的能量变化及反应过程如图所示,下列说法正确的是___________。
作用下发生反应的能量变化及反应过程如图所示,下列说法正确的是___________。
 排放,实现自然界中的碳循环。
排放,实现自然界中的碳循环。(1)以
 为原料合成
为原料合成 涉及的主要反应如下:
涉及的主要反应如下:I.
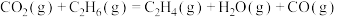
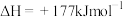 (主反应)
(主反应)II.
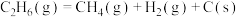
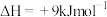 (副反应)
(副反应)反应
 的反应历程可分为如下两步:
的反应历程可分为如下两步:i.


ii.

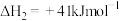
①

②相比于提高
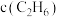 ,提高
,提高 对反应
对反应 速率影响更大,可能的原因是
速率影响更大,可能的原因是③
 时,向一恒容密闭容器中充入物质的量之比为
时,向一恒容密闭容器中充入物质的量之比为 的
的 和
和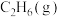 ,反应物转化率与反应温度的关系如图所示。在
,反应物转化率与反应温度的关系如图所示。在 ,
, 得选择性
得选择性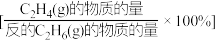 为
为
(2)
 可制甲烷化,
可制甲烷化, 可制甲烷化过程中,
可制甲烷化过程中, 活化的可能途径如图所示。
活化的可能途径如图所示。 是
是 活化的优势中间体,可能的原因是
活化的优势中间体,可能的原因是
(3)
 可用
可用 吸收,发生反应:
吸收,发生反应: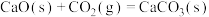 。在不同温度下,达到平衡时体系中
。在不同温度下,达到平衡时体系中 物质的量浓度[
物质的量浓度[ ]与温度的关系如图所示。
]与温度的关系如图所示。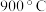 下的
下的 远大于
远大于 下的
下的 ,其原因是
,其原因是
(4)研究表明
 与
与 在
在 作用下发生反应的能量变化及反应过程如图所示,下列说法正确的是___________。
作用下发生反应的能量变化及反应过程如图所示,下列说法正确的是___________。
A. 是催化剂, 是催化剂,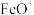 是中间产物 是中间产物 |
B.增大压强可以提高 与 与 的反应速率和平衡转化率 的反应速率和平衡转化率 |
C.每当有 生成时,转移 生成时,转移 电子 电子 |
D. 与 与 转变成 转变成 和 和 的总过程,温度升高,平衡常数K增大 的总过程,温度升高,平衡常数K增大 |
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
【推荐2】工业上设计将VOSO4中的K2SO4、SiO2杂质除去并回收得到V2O5流程:

(1)步骤①所得废渣的成分是____________ (写化学式),操作I的名称__________ ;
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):R2(SO4)n (水层)+ 2nHA(有机层) 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层)
②中萃取时必须加入适量碱,其原因是_____________________________ ;
③中X试剂为(写化学式)______________________________________ ;
(3)④的离子方程式为___________________________________________ ;
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间关系如下表:
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为____________ ;若钒沉淀率为93.1%时不产生Fe(OH)3沉淀,则溶液中c(Fe3+)< _____________ ;(已知:25℃时,Ksp[Fe(OH)3]=2.6×10-39)
(5)该工艺流程中,可以循环利用的物质有__________ 和_______________ 。

(1)步骤①所得废渣的成分是
(2)步骤②、③的变化过程可简化为(下式R表示VO2+,HA表示有机萃取剂):R2(SO4)n (水层)+ 2nHA(有机层)
 2RAn(有机层) + nH2SO4 (水层)
2RAn(有机层) + nH2SO4 (水层) ②中萃取时必须加入适量碱,其原因是
③中X试剂为(写化学式)
(3)④的离子方程式为
(4)25℃时,取样进行实验分析,得到钒沉淀率和溶液pH之间关系如下表:
pH | 1.3 | 1.4 | 1.5 | 1.6 | 1.7 | 1.8 | 1.9 | 2.0 | 2.1 |
钒沉淀率% | 88.1 | 94.8 | 96.5 | 98.0 | 98.8 | 98.8 | 96.4 | 93.1 | 89.3 |
结合上表,在实际生产中,⑤中加入氨水,调节溶液的最佳pH为
(5)该工艺流程中,可以循环利用的物质有
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】以电镀废水(主要成分为 及少量
及少量 )为原料获得
)为原料获得 的过程如下:
的过程如下:
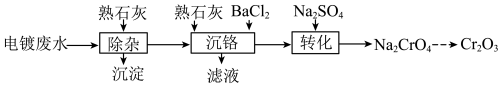
已知:①常温下, 易溶于水。
易溶于水。
部分难溶物的溶度积常数如下表:
|
|
|
| |
|
|
|
|
|
②Cr(Ⅵ)在酸性条件下主要以 (橙红色)的形式存在,pH增大转化为
(橙红色)的形式存在,pH增大转化为 (黄色)。
(黄色)。 ,Cr(Ⅵ)较易还原生成
,Cr(Ⅵ)较易还原生成 (绿色)。
(绿色)。
③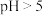 时
时 完全转化为
完全转化为 ,
,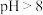 时
时 开始转化为
开始转化为 。
。
(1)“除杂”时调节废水pH将其中
 除去(浓度小于
除去(浓度小于 mol⋅L
mol⋅L ),需加入熟石灰控制废水pH大于
),需加入熟石灰控制废水pH大于(2)“沉铬”时先加入
 调节废水pH,再加入
调节废水pH,再加入 使废水中的Cr(Ⅵ)转化为
使废水中的Cr(Ⅵ)转化为 。调节后的废水pH对Cr(Ⅵ)沉淀率的影响如图所示。
。调节后的废水pH对Cr(Ⅵ)沉淀率的影响如图所示。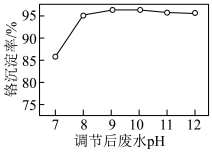
①沉铬过程中将 转化为
转化为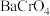 反应的化学方程式为
反应的化学方程式为
②废水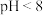 时,铬沉淀率随pH减小而下降的原因是
时,铬沉淀率随pH减小而下降的原因是
③在废水中加入 沉淀前后废水pH
沉淀前后废水pH
(3)“转化”时将
 转化为
转化为 。
。 的转化率随着
的转化率随着 浓度的变化如图所示。当
浓度的变化如图所示。当 浓度超过0.450 mol⋅L
浓度超过0.450 mol⋅L 时,Cr(Ⅵ)的转化率随
时,Cr(Ⅵ)的转化率随 浓度增大变化不明显,其原因是
浓度增大变化不明显,其原因是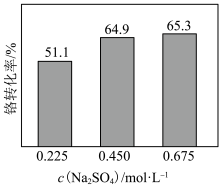
(4)请补充完整由
 溶液制取
溶液制取 的实验方案:向
的实验方案:向 溶液中,
溶液中, 。(可选用的仪器与药品:
。(可选用的仪器与药品: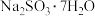 、稀
、稀 、NaOH溶液)
、NaOH溶液)
您最近一年使用:0次
解答题-实验探究题
|
适中
(0.65)
【推荐1】铁及其化合物在日常生产生活中用途广泛,利用FeSO4制备还原铁粉的工业流程如图:

实验室中可用FeSO4(用铁粉和稀硫酸反应制得)和NH4HCO3在如图装置模拟上述流程中的“转化”环节。

(1)装置A的名称是__ ,装置B中盛放的药品是___ ,NH4HCO3盛放在装置___ 中。
(2)实验过程中,欲将生成的FeSO4溶液和NH4HCO3溶液混合,操作方法是___ ,发生主要反应的离子方程式为___ 。
(3)FeSO4溶液要现用现配制的原因是___ 。
(4)干燥过程的主要目的是脱去游离水,该过程中会有少量FeCO3在空气中被氧化为FeOOH,该反应的化学方程式为___ ,取干燥后的FeCO3样品12.49g,与炭混合后焙烧,最终得到还原铁粉6.16g,计算样品中杂质FeOOH的质量:__ g。

实验室中可用FeSO4(用铁粉和稀硫酸反应制得)和NH4HCO3在如图装置模拟上述流程中的“转化”环节。

(1)装置A的名称是
(2)实验过程中,欲将生成的FeSO4溶液和NH4HCO3溶液混合,操作方法是
(3)FeSO4溶液要现用现配制的原因是
(4)干燥过程的主要目的是脱去游离水,该过程中会有少量FeCO3在空气中被氧化为FeOOH,该反应的化学方程式为
您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
名校
解题方法
【推荐2】以镁铝复合氧化物(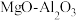 )为载体的负载型镍铜双金属催化剂(
)为载体的负载型镍铜双金属催化剂(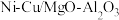 )是一种新型的高效加氢或脱氢催化剂,其制备流程如图:
)是一种新型的高效加氢或脱氢催化剂,其制备流程如图:
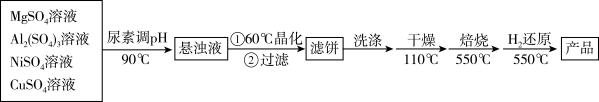
已知:常温下, 。
。
回答下列问题:
(1)在元素周期表中, 在
在_______ (填“s”“p”“d“f”或“ds”)区。
(2)在加热条件下,尿素( )在水中发生水解反应,放出
)在水中发生水解反应,放出 和
和 两种气体。
两种气体。
①尿素中C原子的杂化轨道类型为_______ ;尿素分子中 键与
键与 键的数目之比为
键的数目之比为_______ 。
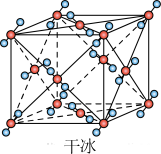
②如图为干冰的晶胞结构示意图,一个二氧化碳晶胞中含有_______ 个二氧化碳分子。
(3)“晶化”过程中,需保持恒温 ,可采用的加热方式为
,可采用的加热方式为_______ 。
(4)常温下,若“悬浊液”中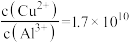 ,则溶液的
,则溶液的
_______ 。
(5) 在消防工业中常用于与小苏打、发泡剂组成泡沫灭火剂,请写出其灭火原理:
在消防工业中常用于与小苏打、发泡剂组成泡沫灭火剂,请写出其灭火原理:_______ (用离子方程式表示)。
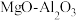 )为载体的负载型镍铜双金属催化剂(
)为载体的负载型镍铜双金属催化剂(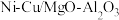 )是一种新型的高效加氢或脱氢催化剂,其制备流程如图:
)是一种新型的高效加氢或脱氢催化剂,其制备流程如图:
已知:常温下,
 。
。回答下列问题:
(1)在元素周期表中,
 在
在(2)在加热条件下,尿素(
 )在水中发生水解反应,放出
)在水中发生水解反应,放出 和
和 两种气体。
两种气体。①尿素中C原子的杂化轨道类型为
 键与
键与 键的数目之比为
键的数目之比为②如图为干冰的晶胞结构示意图,一个二氧化碳晶胞中含有

(3)“晶化”过程中,需保持恒温
 ,可采用的加热方式为
,可采用的加热方式为(4)常温下,若“悬浊液”中
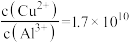 ,则溶液的
,则溶液的
(5)
 在消防工业中常用于与小苏打、发泡剂组成泡沫灭火剂,请写出其灭火原理:
在消防工业中常用于与小苏打、发泡剂组成泡沫灭火剂,请写出其灭火原理:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐3】回答下列问题:
(1)①取20 mL pH=3的CH3COOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电性变化如图1,则加入氨水前CH3COOH的电离度(分子电离的百分数)为_______ ,加入0~10 mL的氨水导电能力增强的原因_______ 。

②将醋酸铵固体溶于水,配成0.1 mol·L-1溶液,请写出醋酸铵水解的离子方程式_______ 。
(2)在25℃时,碳酸钙在水中的沉淀溶解平衡曲线如图2所示,已知25℃时硫酸钙的Ksp=9.1×10-6。

①通过蒸发,可使稀溶液由_______ 点变化到_______ 点。
②在25℃时,反应CaSO4(s)+ (aq)⇌CaCO3(s)+
(aq)⇌CaCO3(s)+ (aq)的平衡常数K
(aq)的平衡常数K_______
(3)某带盐桥的原电池构造如图3所示。

该原电池工作时,银电极的电极反应式为_______ ,当外电路中每通过0.2 mol电子,铜电极的质量减小_______ g。
(1)①取20 mL pH=3的CH3COOH溶液,加入0.2 mol·L-1的氨水,测得溶液导电性变化如图1,则加入氨水前CH3COOH的电离度(分子电离的百分数)为

②将醋酸铵固体溶于水,配成0.1 mol·L-1溶液,请写出醋酸铵水解的离子方程式
(2)在25℃时,碳酸钙在水中的沉淀溶解平衡曲线如图2所示,已知25℃时硫酸钙的Ksp=9.1×10-6。

①通过蒸发,可使稀溶液由
②在25℃时,反应CaSO4(s)+
 (aq)⇌CaCO3(s)+
(aq)⇌CaCO3(s)+ (aq)的平衡常数K
(aq)的平衡常数K(3)某带盐桥的原电池构造如图3所示。

该原电池工作时,银电极的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】填空题
(1)氯化铁水溶液呈酸性的原因是___________ (用离子方程式表示)。
(2)在25℃时,1mol/L的① 、②
、② 、③
、③ 溶液中,
溶液中, 由小到大的顺序是
由小到大的顺序是___________ 。(填序号)
(3)某浓度的氨水中存在平衡: ,如想增大
,如想增大 的浓度而不增大
的浓度而不增大 的浓度,应采取的措施是
的浓度,应采取的措施是___________ (填字母)。
a.适当升高温度 b.加入 固体 c.通入
固体 c.通入 d.加入少量浓盐酸
d.加入少量浓盐酸
(4)常温下,用NaOH溶液吸收 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡___________ (填“向左”“向右”或“不”)移动。试计算溶液中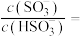
___________ (常温下 的电离平衡常数
的电离平衡常数 ,
, )。
)。
(1)氯化铁水溶液呈酸性的原因是
(2)在25℃时,1mol/L的①
 、②
、② 、③
、③ 溶液中,
溶液中, 由小到大的顺序是
由小到大的顺序是(3)某浓度的氨水中存在平衡:
 ,如想增大
,如想增大 的浓度而不增大
的浓度而不增大 的浓度,应采取的措施是
的浓度,应采取的措施是a.适当升高温度 b.加入
 固体 c.通入
固体 c.通入 d.加入少量浓盐酸
d.加入少量浓盐酸(4)常温下,用NaOH溶液吸收
 得到
得到 的
的 溶液,吸收过程中水的电离平衡
溶液,吸收过程中水的电离平衡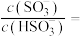
 的电离平衡常数
的电离平衡常数 ,
, )。
)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐2】氮的化合物是重要的工业原料,也是主要的大气污染来源,研究氮的化合物的反应具有重要意义,回答下列问题:
(1)工业上利用NH3与金属镓(Ga)在高温条件下合成固体半导体材料氮化镓(GaN),反应的热化学方程式为2Ga(s)+ 2NH3(g) 2GaN(s)+3H2(g) ΔH=-30.8kJ/mol。下列说法正确的是___________(填标号)。
2GaN(s)+3H2(g) ΔH=-30.8kJ/mol。下列说法正确的是___________(填标号)。
(2)肼(N2H4,液态)与四氧化二氮(N2O4)分别是火箭发射器中最常用的燃料与氧化剂,涉及的反应有:
Ⅰ.N2(g) +2O2(g)=2NO2(g) ΔH= +66.4kJ/mol;
Ⅱ.N2H4(l) +O2(g)=N2(g)+2H2O(g) ΔH=-534kJ/mol;
Ⅲ.2NO2(g)=N2O4(g) ΔH=-56.9kJ/mol;
①常温下,表示肼燃烧热的热化学方程式为___________ [已知: H2O(l)=H2O(g) ΔH=+44kJ/mol]。
②N2H4(l)和四氧化二氮(N2O4)反应生成N2和H2O(g)的热化学方程式为___________ 。
③反应Ⅰ的能量变化与下列物质间的能量变化相符的是___________ (填标号)。
A.铝热反应 B.氯化铵与氢氧化钡晶体的反应
C. C与二氧化碳生成一氧化碳的反应 D.金属钠与水的反应
(3)可利用如图电解装置将硝酸工业尾气中的NO转化为NH4NO3(假设两电极均为惰性电极)。

①N电极上发生___________ (填“氧化”或“还原”)反应,判断的理由为___________ 。
②M电极上的电极反应式为___________ 。
③常温下,0.1mol/L的NH4NO3溶液的pH约为___________ (保留2位有效数字),该溶液中各离子的浓度由大到小的顺序为___________ [Kb(NH3·H2O)≈2×10-5,lg2≈0.3]
(1)工业上利用NH3与金属镓(Ga)在高温条件下合成固体半导体材料氮化镓(GaN),反应的热化学方程式为2Ga(s)+ 2NH3(g)
 2GaN(s)+3H2(g) ΔH=-30.8kJ/mol。下列说法正确的是___________(填标号)。
2GaN(s)+3H2(g) ΔH=-30.8kJ/mol。下列说法正确的是___________(填标号)。| A.每断裂6 mol N- H键,同时放出 30.8 kJ热量 |
| B.每生成0.2 mol GaN(s),同时生成6.72 L H2(g) |
| C.该反应的反应物的总能量大于生成物的总能量 |
| D.当ΔH的大小不再随时间而改变时,该反应达到平衡状态 |
(2)肼(N2H4,液态)与四氧化二氮(N2O4)分别是火箭发射器中最常用的燃料与氧化剂,涉及的反应有:
Ⅰ.N2(g) +2O2(g)=2NO2(g) ΔH= +66.4kJ/mol;
Ⅱ.N2H4(l) +O2(g)=N2(g)+2H2O(g) ΔH=-534kJ/mol;
Ⅲ.2NO2(g)=N2O4(g) ΔH=-56.9kJ/mol;
①常温下,表示肼燃烧热的热化学方程式为
②N2H4(l)和四氧化二氮(N2O4)反应生成N2和H2O(g)的热化学方程式为
③反应Ⅰ的能量变化与下列物质间的能量变化相符的是
A.铝热反应 B.氯化铵与氢氧化钡晶体的反应
C. C与二氧化碳生成一氧化碳的反应 D.金属钠与水的反应
(3)可利用如图电解装置将硝酸工业尾气中的NO转化为NH4NO3(假设两电极均为惰性电极)。

①N电极上发生
②M电极上的电极反应式为
③常温下,0.1mol/L的NH4NO3溶液的pH约为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】醋酸是日常生活中最常见的调味剂和重要的化工原料,醋酸钾是其常见的盐。请回答下列问题:
(1)0. 2 mol· L-1CH3COOK溶液中离子浓度由大到小的顺序为___________ 。
(2)物质的量浓度均为0.2 mol·L-1的CH3COOH和CH3COOK溶液等体积混合(混合前后忽略溶液体积变化),混合液中的下列关系式正确的是___________ (填字母)。
A. c(CH3COOH) +c(H+ )= c(CH3COO- ) +c(OH- )
B.c(H+)+c(K+ )=c(CH3COO- ) +c(OH- )
C.c(CH3COO- )+c(CH3COOH)=0.2 mol·L-1
(3)常温下0. 1 mol·L-1的CH3COOH溶液加水稀释的过程,下列表达式的数值一定变大的是______(填字母)。
(4)常温时,pH=3的醋酸溶液和pH=11的KOH溶液等体积混合后,溶液中c(K+)___________ c(CH3COO-)(填“>”“<”或“=”,下同)。
(5)常温时,将m mol· L-1的醋酸溶液和n mol·L-1的KOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m___________ n。
(6)已知25° C时,三种酸的电离平衡常数如下:
下列四种离子结合H+能力最强的是___________ (填字 母)。
A. HCO B. CO
B. CO C. ClO- D. CH3COO-
C. ClO- D. CH3COO-
写出HClO+Na2CO3 (少量)反应离子方程式:___________ 。
(1)0. 2 mol· L-1CH3COOK溶液中离子浓度由大到小的顺序为
(2)物质的量浓度均为0.2 mol·L-1的CH3COOH和CH3COOK溶液等体积混合(混合前后忽略溶液体积变化),混合液中的下列关系式正确的是
A. c(CH3COOH) +c(H+ )= c(CH3COO- ) +c(OH- )
B.c(H+)+c(K+ )=c(CH3COO- ) +c(OH- )
C.c(CH3COO- )+c(CH3COOH)=0.2 mol·L-1
(3)常温下0. 1 mol·L-1的CH3COOH溶液加水稀释的过程,下列表达式的数值一定变大的是______(填字母)。
| A.c(H+ ) | B. |
| C.c(H+) · c(OH -) | D.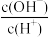 |
(5)常温时,将m mol· L-1的醋酸溶液和n mol·L-1的KOH溶液等体积混合后,所得溶液的pH=7,则m与n的大小关系是m
(6)已知25° C时,三种酸的电离平衡常数如下:
| 化学式 | CH3COOH | H2CO3 | HClO |
| Ka1 | 1.8 ×10-5 | 4.3 ×10-7 | 3.0 ×10-8 |
| Ka2 | — | 5.6 ×10-11 | — |
A. HCO
 B. CO
B. CO C. ClO- D. CH3COO-
C. ClO- D. CH3COO-写出HClO+Na2CO3 (少量)反应离子方程式:
您最近一年使用:0次