元素周期表是元素周期律的具体表现形式。下表是元素周期表的短周期部分:
用编号对应的元素微粒符号回答下列问题:
(1)元素②的原子核外电子排布式_________ ,元素③的气态氢化物的电子式______ 。
(2)元素④⑤⑥的原子半径由大到小的顺序是_______________ 。
(3)元素⑥的最高价氧化物对应水化物与强碱溶液反应的离子方程式_____________ 。
(4)元素②与④形成的化合物的熔点比②与⑧形成的化合物熔点______ (填“高或低”),理由是_____________________ 。
(5)某温度下,在2.0L的密闭容器中,加入一定量的①③的单质发生反应,20min达到平衡,此时容器中产物为68.0g。用单质③表示该反应的平均速率为____________ 。下列描述中能说明上述反应已达平衡的是_______ 。
a.c(N2):c(H2):c(NH3)=1:3:2 b.容器中气体密度不变
c.容器中压强不变 d.3v正(H2)=2v逆(NH3)
达到平衡后,若使平衡常数K值增大,则________ (填“正反应”或“逆反应”)的速率变化更大。
| ① | |||||||
| ② | ③ | ④ | |||||
| ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
用编号对应的元素微粒符号回答下列问题:
(1)元素②的原子核外电子排布式
(2)元素④⑤⑥的原子半径由大到小的顺序是
(3)元素⑥的最高价氧化物对应水化物与强碱溶液反应的离子方程式
(4)元素②与④形成的化合物的熔点比②与⑧形成的化合物熔点
(5)某温度下,在2.0L的密闭容器中,加入一定量的①③的单质发生反应,20min达到平衡,此时容器中产物为68.0g。用单质③表示该反应的平均速率为
a.c(N2):c(H2):c(NH3)=1:3:2 b.容器中气体密度不变
c.容器中压强不变 d.3v正(H2)=2v逆(NH3)
达到平衡后,若使平衡常数K值增大,则
更新时间:2018-01-11 09:02:11
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】从衣食住行到探索浩瀚宇宙,都有氮及其化合物的参与,但同时有毒含氮化合物的排放,也对环境产生污染。如何实现环境保护与资源利用的和谐统一,已成为我们的重要研究课题。
(1)工业上利用N2和H2可以合成NH3,NH3又可以进一步制备火箭燃料肼(N2H4)。
① △H1
△H1
② △H2
△H2
③ △H3
△H3
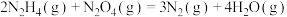 的反应热△H=
的反应热△H=______ (写出表达式)。
(2) N2H4的水溶液呈弱碱性,室温下其电离常数 ,则0.01 mol∙L-1的N2H4水溶液pH等于
,则0.01 mol∙L-1的N2H4水溶液pH等于______ (忽略N2H4的二级电离和H2O的电离,lg4=0.6)。
(3)利用测压法在刚性密闭容器中研究T1℃时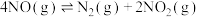 (△H<0)的分解反应,现将一定量的NO充入该密闭容器中,测得体系的总压强随时间的变化如下表所示:
(△H<0)的分解反应,现将一定量的NO充入该密闭容器中,测得体系的总压强随时间的变化如下表所示:
①0~20 min时,v(NO2)=______ MPa∙min-1。
②T1℃时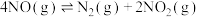 反应的平衡常数Kx=
反应的平衡常数Kx=______ (Kx为以物质的量分数表示的平衡常数)。若升高温度,N2的物质的量分数将______ (填“增大”“减小”或“不变”)。
(4)将等物质的量的NO和CO分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应 △H<0,经过相同时间测得NO的转化率如图所示,图中cd段转化率下降的可能原因是(答2条):
△H<0,经过相同时间测得NO的转化率如图所示,图中cd段转化率下降的可能原因是(答2条):
①________________________________________________ ;
②________________________________________________ 。

(1)工业上利用N2和H2可以合成NH3,NH3又可以进一步制备火箭燃料肼(N2H4)。
①
 △H1
△H1②
 △H2
△H2③
 △H3
△H3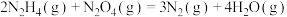 的反应热△H=
的反应热△H=(2) N2H4的水溶液呈弱碱性,室温下其电离常数
 ,则0.01 mol∙L-1的N2H4水溶液pH等于
,则0.01 mol∙L-1的N2H4水溶液pH等于(3)利用测压法在刚性密闭容器中研究T1℃时
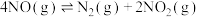 (△H<0)的分解反应,现将一定量的NO充入该密闭容器中,测得体系的总压强随时间的变化如下表所示:
(△H<0)的分解反应,现将一定量的NO充入该密闭容器中,测得体系的总压强随时间的变化如下表所示:| 反应时间/min | 0 | 10 | 20 | 30 | 40 |
| 压强/MPa | 15.00 | 14.02 | 13.20 | 12.50 | 12.50 |
②T1℃时
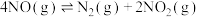 反应的平衡常数Kx=
反应的平衡常数Kx=(4)将等物质的量的NO和CO分别充入盛有催化剂①和②的体积相同的刚性容器,进行反应
 △H<0,经过相同时间测得NO的转化率如图所示,图中cd段转化率下降的可能原因是(答2条):
△H<0,经过相同时间测得NO的转化率如图所示,图中cd段转化率下降的可能原因是(答2条):①
②

您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】烟气中含有大量氮氧化物NOx,工业脱硝技术成为研究热点。
(1)汽车尾气中NO和CO可利用车载催化剂转化为无毒物质排放。
已知:N2(g)+O2(g)=2NO(g) △H1=+183 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-565 kJ·mol-1
写出催化转化的热化学方程式_________ 。
(2)臭氧氧化-碱吸收法可有效脱除NO,氧化原理为:NO(g)+O3(g) NO2(g)+O2(g) △H=-200.9 kJ·mol-1。在容积为2L的密闭容器中充入含1.0 mol NO的模拟烟气和2.0 mol O3,在不同温度,经过相同时间(10min)NO的转化率如图所示。
NO2(g)+O2(g) △H=-200.9 kJ·mol-1。在容积为2L的密闭容器中充入含1.0 mol NO的模拟烟气和2.0 mol O3,在不同温度,经过相同时间(10min)NO的转化率如图所示。
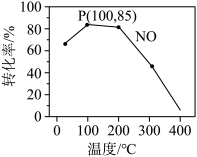
①100℃时,从开始反应到P点的平均反应速率v(NO)=__________ 。
②反应时同时发生副反应:2O3 3O2,共有15%的O3自身分解为O2。则P点时O3的物质的量为
3O2,共有15%的O3自身分解为O2。则P点时O3的物质的量为________ mol。
(3)选择性催化还原技术(NCR)可在较低温度下脱硝,原理如图I,天然锰矿可作催化剂。
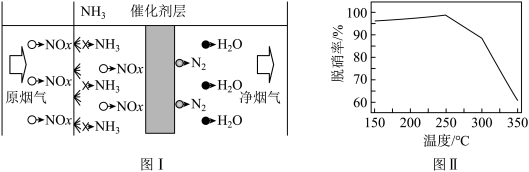
以NO代表氮氧化物,写出反应方程式_____________________ ;实验测得脱硝率随温度的变化如图II所示,请分析温度高于250℃时脱硝率下降的原因可能是______________ 。
(1)汽车尾气中NO和CO可利用车载催化剂转化为无毒物质排放。
已知:N2(g)+O2(g)=2NO(g) △H1=+183 kJ·mol-1
2CO(g)+O2(g)=2CO2(g) △H2=-565 kJ·mol-1
写出催化转化的热化学方程式
(2)臭氧氧化-碱吸收法可有效脱除NO,氧化原理为:NO(g)+O3(g)
 NO2(g)+O2(g) △H=-200.9 kJ·mol-1。在容积为2L的密闭容器中充入含1.0 mol NO的模拟烟气和2.0 mol O3,在不同温度,经过相同时间(10min)NO的转化率如图所示。
NO2(g)+O2(g) △H=-200.9 kJ·mol-1。在容积为2L的密闭容器中充入含1.0 mol NO的模拟烟气和2.0 mol O3,在不同温度,经过相同时间(10min)NO的转化率如图所示。
①100℃时,从开始反应到P点的平均反应速率v(NO)=
②反应时同时发生副反应:2O3
 3O2,共有15%的O3自身分解为O2。则P点时O3的物质的量为
3O2,共有15%的O3自身分解为O2。则P点时O3的物质的量为(3)选择性催化还原技术(NCR)可在较低温度下脱硝,原理如图I,天然锰矿可作催化剂。

以NO代表氮氧化物,写出反应方程式
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】Ⅰ、某实验小组对H2O2的分解做了如下探究:将质量相同但状态不同的MnO2分别加入盛有15mL5%的H2O2溶液的大试管中,并用带火星的木条测试。下表是该实验小组研究影响H2O2分解速率的因素时记录的一组数据:
(1)写出大试管中发生反应的化学方程式:___________ ,
(2)实验结果表明,催化剂的催化效果与___________ 有关。
Ⅱ、某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。
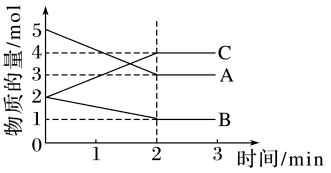
(3)该反应的化学方程式为___________ 。
(4)能说明该反应已达到平衡状态的是___________ (填字母)。
a、v(A)=2v(B)
b、容器内压强保持不变
c、混合气体的平均摩尔质量保持不变
d、容器内混合气体的密度保持不变
e、B的体积分数不变
(5)在密闭容器里,通入amolA(g)、bmolB(g)、cmolC(g),发生上述反应,当改变下列条件时,反应速率会减小的是___________ (填序号)。
①降低温度②加入催化剂③增大容器体积④移走部分A⑤恒容时,充入氦气
(6)一定温度下,氧化铁可与一氧化碳发生反应:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)。在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成单质铁11.2g。10min内v(CO)=___________ 。
(7)下列4个数据是在不同条件下测得的合成氨反应速率,其中反应最快的是___________(填字母)。
(8)在2Z(g)+Y(g) 3X(s)中,恒容时,下列情况能说明该反应已达到平衡状态的是
3X(s)中,恒容时,下列情况能说明该反应已达到平衡状态的是___________ (填字母)。
a、v(Z)正=2v(Y)逆
b、容器内压强保持不变
c、混合气体的平均摩尔质量保持不变
d、容器内混合气体的密度保持不变
e、Z的物质的量分数不变
| MnO2 | 触摸试管情况 | 观察结果 | 反应完成所需的时间 |
| 粉末状 | 很烫 | 剧烈反应,带火星的木条复燃 | 3.5min |
| 块状 | 微热 | 反应较慢,火星红亮但木条未复燃 | 30min |
(2)实验结果表明,催化剂的催化效果与
Ⅱ、某可逆反应在体积为5L的密闭容器中进行,0~3min内各物质的物质的量的变化情况如图所示(A、B、C均为气体)。

(3)该反应的化学方程式为
(4)能说明该反应已达到平衡状态的是
a、v(A)=2v(B)
b、容器内压强保持不变
c、混合气体的平均摩尔质量保持不变
d、容器内混合气体的密度保持不变
e、B的体积分数不变
(5)在密闭容器里,通入amolA(g)、bmolB(g)、cmolC(g),发生上述反应,当改变下列条件时,反应速率会减小的是
①降低温度②加入催化剂③增大容器体积④移走部分A⑤恒容时,充入氦气
(6)一定温度下,氧化铁可与一氧化碳发生反应:Fe2O3(s)+3CO(g)=2Fe(s)+3CO2(g)。在2L盛有Fe2O3粉末的密闭容器中通入CO气体,10min后,生成单质铁11.2g。10min内v(CO)=
(7)下列4个数据是在不同条件下测得的合成氨反应速率,其中反应最快的是___________(填字母)。
| A.v(H2)=0.1mol/(L∙min) | B.v(N2)=0.1mol/(L∙min) |
| C.v(NH3)=0.15mol/(L∙min) | D.v(N2)=0.002mol/(L∙s) |
 3X(s)中,恒容时,下列情况能说明该反应已达到平衡状态的是
3X(s)中,恒容时,下列情况能说明该反应已达到平衡状态的是a、v(Z)正=2v(Y)逆
b、容器内压强保持不变
c、混合气体的平均摩尔质量保持不变
d、容器内混合气体的密度保持不变
e、Z的物质的量分数不变
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】合成气(CO+H2)在煤化工和天然气化工中有着十分重要的地位,由合成气可合成多种有机基础原料和产品。
(1)煤化工中生产合成气的反应为: ,
,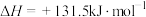
①该反应的平衡常数表达式为___________
②判断该反应的自发性___________
③在恒温恒容下,同时放入 、
、 、
、 、
、 四种物质,下列事实能够说明反应
四种物质,下列事实能够说明反应 已达到平衡的是
已达到平衡的是___________ 。
A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有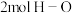 键断裂的同时有
键断裂的同时有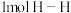 键断裂
键断裂
D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为: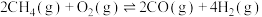 ,
, ,在恒容容器中按物质的量之比1∶2加入一定量的
,在恒容容器中按物质的量之比1∶2加入一定量的 和
和 ,在压强为
,在压强为 、不同温度下测得
、不同温度下测得 的平衡转化率如下图所示:
的平衡转化率如下图所示:

①请在图中画出压强为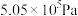 时
时 的平衡转化率随温度的变化曲线
的平衡转化率随温度的变化曲线___________ 。
②现有实验测得反应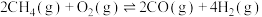 在750℃下,以不同碳氧比[
在750℃下,以不同碳氧比[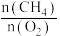 ]投料时反应达平衡后
]投料时反应达平衡后 的转化率及
的转化率及 、CO的选择性,所测数据如表所示。
、CO的选择性,所测数据如表所示。
已知:选择性=目标产物的产率/反应原料的转化率
最佳碳氧比[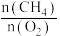 ]为
]为___________ 。
假设按碳氧比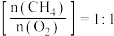 投料,反应容器的体积为VL,通入
投料,反应容器的体积为VL,通入 和
和 各amol,请列式表示平衡时容器内CO的浓度
各amol,请列式表示平衡时容器内CO的浓度___________ (用a、V的代数式表示)
(1)煤化工中生产合成气的反应为:
 ,
,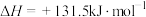
①该反应的平衡常数表达式为
②判断该反应的自发性
③在恒温恒容下,同时放入
 、
、 、
、 、
、 四种物质,下列事实能够说明反应
四种物质,下列事实能够说明反应 已达到平衡的是
已达到平衡的是A.反应体系中,混合气体的密度不再改变
B.反应体系中,各组分的物质的量相等
C.反应体系中,当有
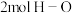 键断裂的同时有
键断裂的同时有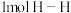 键断裂
键断裂D.混合气体的平均相对分子质量保持不变
(2)天然气化工中生产合成气的主要反应为:
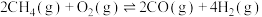 ,
, ,在恒容容器中按物质的量之比1∶2加入一定量的
,在恒容容器中按物质的量之比1∶2加入一定量的 和
和 ,在压强为
,在压强为 、不同温度下测得
、不同温度下测得 的平衡转化率如下图所示:
的平衡转化率如下图所示:
①请在图中画出压强为
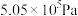 时
时 的平衡转化率随温度的变化曲线
的平衡转化率随温度的变化曲线②现有实验测得反应
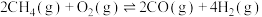 在750℃下,以不同碳氧比[
在750℃下,以不同碳氧比[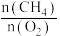 ]投料时反应达平衡后
]投料时反应达平衡后 的转化率及
的转化率及 、CO的选择性,所测数据如表所示。
、CO的选择性,所测数据如表所示。已知:选择性=目标产物的产率/反应原料的转化率
碳氧比[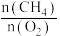 ] ] | 1∶0.25 | 1∶0.5 | 1∶1 | 1∶1.25 |
 转化率 转化率 | 0.40 | 0.88 | 0.98 | 0.99 |
 选择性 选择性 | 0.98 | 0.93 | 0.67 | 0.40 |
| CO选择性 | 0.99 | 0.94 | 0.65 | 0.32 |
最佳碳氧比[
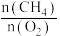 ]为
]为假设按碳氧比
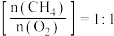 投料,反应容器的体积为VL,通入
投料,反应容器的体积为VL,通入 和
和 各amol,请列式表示平衡时容器内CO的浓度
各amol,请列式表示平衡时容器内CO的浓度
您最近一年使用:0次
【推荐2】2020年9月,习近平主席在第75届联合国大会提出我国要实现2030年前碳达峰、2060年前碳中和的目标。因此CO2的捕集、利用与封存成为科学家研究的重要课题。
Ⅰ.工业上可以利用CO2和H2合成CH3OH,CO2(g)+3H2(g) CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
(1)达到平衡时,反应a、b对比: 的体积分数
的体积分数
_______ 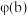 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。
(2)下列不能说明反应a达到平衡状态的是_______(填标号)。
Ⅱ.CH4与CO2催化重整是实现碳中和的热点研究课题。该催化重整反应体系主要涉及以下反应:
主反应:CH4(g)+CO2(g) 2CO(g)+2H2(g) ΔH1
2CO(g)+2H2(g) ΔH1
副反应:CO2(g)+H2(g) CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2
(3)已知H2(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0lkJ·mol-1,H2O(l)= H2O(g) ΔH5=+44kJ·mol-1,则副反应的ΔH2=_______ kJ·mol-1。
(4)一定温度下,向一恒容密闭容器中充入 和
和 ,若只发生上述主反应,初始时
,若只发生上述主反应,初始时 和
和 的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数
的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数
_______  (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
Ⅲ.以铅蓄电池为电源可将 转化为乙烯,其原理如下图所示,电解所用电极材料均为惰性电极。
转化为乙烯,其原理如下图所示,电解所用电极材料均为惰性电极。

(5)阴极上的电极反应式为_______ 。
Ⅰ.工业上可以利用CO2和H2合成CH3OH,CO2(g)+3H2(g)
 CH3OH(g)+H2O(g)
CH3OH(g)+H2O(g)  。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表:
。该反应在起始温度和体积均相同(T℃、1L)的两个密闭容器中分别进行,反应物起始物质的量见下表: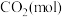 |  |  | 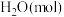 | |
| 反应a(恒温恒容) | 1 | 3 | 0 | 0 |
| 反应b(绝热恒容) | 0 | 0 | 1 | 1 |
(1)达到平衡时,反应a、b对比:
 的体积分数
的体积分数
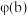 (填“>”“<”或“=”)。
(填“>”“<”或“=”)。(2)下列不能说明反应a达到平衡状态的是_______(填标号)。
A. |
| B.混合气体的平均摩尔质量不再改变 |
C.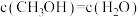 |
| D.容器内压强不再改变 |
Ⅱ.CH4与CO2催化重整是实现碳中和的热点研究课题。该催化重整反应体系主要涉及以下反应:
主反应:CH4(g)+CO2(g)
 2CO(g)+2H2(g) ΔH1
2CO(g)+2H2(g) ΔH1 副反应:CO2(g)+H2(g)
 CO(g)+H2O(g) ΔH2
CO(g)+H2O(g) ΔH2 (3)已知H2(g)、CO(g)的燃烧热ΔH分别为-285.8kJ·mol-1、-283.0lkJ·mol-1,H2O(l)= H2O(g) ΔH5=+44kJ·mol-1,则副反应的ΔH2=
(4)一定温度下,向一恒容密闭容器中充入
 和
和 ,若只发生上述主反应,初始时
,若只发生上述主反应,初始时 和
和 的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数
的分压分别为14kPa、16kPa,一段时间达到平衡后,测得体系压强是起始时的1.4倍,则该反应的平衡常数
 (用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。
(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数)。Ⅲ.以铅蓄电池为电源可将
 转化为乙烯,其原理如下图所示,电解所用电极材料均为惰性电极。
转化为乙烯,其原理如下图所示,电解所用电极材料均为惰性电极。
(5)阴极上的电极反应式为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】完成下列问题。
(1)在图1和图2中出现的所有物质都为气体,分析图1和图2,可推测:
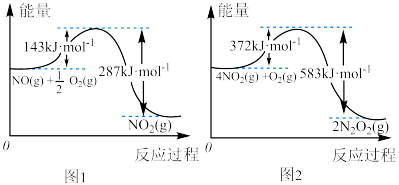
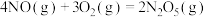

___________ 。
(2)在一个容积不变的密闭容器中,发生反应: 。当
。当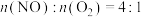 时,
时, 的转化率随时间的变化关系如图所示。
的转化率随时间的变化关系如图所示。

(a)A点的正反应速率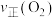
___________ B点的逆反应速率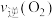 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。
(b)NO的平衡转化率为___________ ;当达到B点后往容器中再以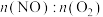 为4∶1加入一些NO和
为4∶1加入一些NO和 ,当达到新平衡时,NO的百分含量
,当达到新平衡时,NO的百分含量___________ B点NO的百分含量(填“大于”“小于”或“等于”)。
(c)到达B点后,下列关系正确的是___________ 。
A.容器内气体颜色不再变化
B.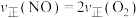
C.气体平均摩尔质量在此条件下达到最小
D.容器内气体密度不再变化
(1)在图1和图2中出现的所有物质都为气体,分析图1和图2,可推测:

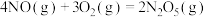

(2)在一个容积不变的密闭容器中,发生反应:
 。当
。当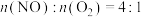 时,
时, 的转化率随时间的变化关系如图所示。
的转化率随时间的变化关系如图所示。
(a)A点的正反应速率
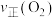
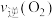 (填“大于”“小于”或“等于”)。
(填“大于”“小于”或“等于”)。(b)NO的平衡转化率为
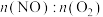 为4∶1加入一些NO和
为4∶1加入一些NO和 ,当达到新平衡时,NO的百分含量
,当达到新平衡时,NO的百分含量(c)到达B点后,下列关系正确的是
A.容器内气体颜色不再变化
B.
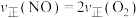
C.气体平均摩尔质量在此条件下达到最小
D.容器内气体密度不再变化
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
【推荐1】下表是元素周期表的一部分,回答相关的问题。
(1)写出④的元素符号___________ ,①的氢化物化学式___________ 。
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式:___________ 。
(3)在这些元素中,最高价氧化物的水化物酸性最强的是___________ (填相应化学式)。
(4)这些元素中(除⑨外),原子半径最小的是___________ (填元素符号)。
(5)②的单质与③的最高价氧化物的水化物的溶液反应,其产物之一是OX2,(O、X分别表示氧和②的元素符号,即OX2代表该化学式),该反应的离子方程式为___________ (方程式中用具体元素符号表示)。
| 族 周期 | ⅠA | ⅡA | ⅢA | ⅣA | ⅤA | ⅥA | ⅦA | 0 |
| 2 | ① | ② | ||||||
| 3 | ③ | ④ | ⑤ | ⑥ | ⑦ | ⑧ | ⑨ |
(2)在这些元素中,最活泼的金属元素与水反应的离子方程式:
(3)在这些元素中,最高价氧化物的水化物酸性最强的是
(4)这些元素中(除⑨外),原子半径最小的是
(5)②的单质与③的最高价氧化物的水化物的溶液反应,其产物之一是OX2,(O、X分别表示氧和②的元素符号,即OX2代表该化学式),该反应的离子方程式为
您最近一年使用:0次
解答题-无机推断题
|
适中
(0.65)
解题方法
【推荐2】A、B、C、D四种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)B元素的名称________ ;B在周期表中的位置________________ ;
(2)A、C形成的化合物的成键方式为_________ (填“离子键”、“极性共价键”或“非极性共价键”);
(3)D的最高价氧化物对应的水化物的化学式________ ;
(4)写出工业上制备C元素的最高价氧化物的化学反应方程式_________ 。
(1)B元素的名称
(2)A、C形成的化合物的成键方式为
(3)D的最高价氧化物对应的水化物的化学式
(4)写出工业上制备C元素的最高价氧化物的化学反应方程式
您最近一年使用:0次
【推荐3】下表是元素周期表前五周期的一部分,X、Y、Z、R、W、J是6种元素的代号。其中J为0族元素。
请回答下列问题(除特别说明外,凡涉及用元素回答的问题均用具体元素符号表示):
(1)R原子的电子排布图为__________ 。
(2)在化合物YZ2中Y的化合价为__________ ;Y2-与Na+的半径大小为__________ 。
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是__________ ;X与Y的第一电离能:X__________ Y(填“<”、“>”或“=”),其理由是__________________________________________________________ 。
| X | Y | Z | |
| R | |||
| W | |||
| J |
(1)R原子的电子排布图为
(2)在化合物YZ2中Y的化合价为
(3)在X、Y、Z三种元素中,电负性由大到小的顺序是
您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐1】过渡金属元素在日常生活中有广泛的应用。
(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价层电子的排布式为__________ ;基态 Mn原子核外有____ 种运动状态不同的电子,M层的电子云有_______ 种不同的伸展方向。
(2)第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,原因是____________________________________
(3)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验 K+的存在。与NO2-互为等电子体的微粒__________ (写出一种),K3[Co(NO2)6]中存在的作用力有___________ a.σ键 b.π键 c.配位键 d.离子键 e.范德华力
(4)锰的一种配合物的化学式为 Mn(BH4)2(THF)3,BH4-的空间构型为____________
(5)FeO 是离子晶体,其晶格能可通过下图中的 Born—Haber 循环计算得到。
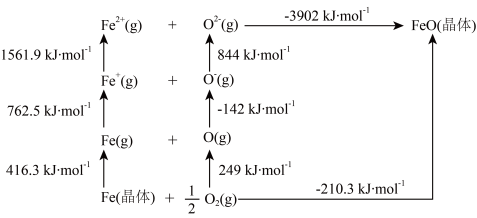
可知,O原子的第一电子亲和能为________ kJ•mol-1,FeO晶格能为________ kJ•mol-1。
(6)铜与氧可形成如图所示的晶胞结构,其中 Cu 均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(1/2,1/2,1/2),则 d 点的坐标参数为_______________ ,已知该晶体的密度为ρg•cm-3,NA是阿伏加 德罗常数的值,则晶胞参数为_________ pm(列出计算式即可)

(1)金属钒在材料科学上有重要作用,被称为“合金的维生素”,基态钒原子的价层电子的排布式为
(2)第四周期元素的第一电离能随原子序数增大,总趋势是逐渐增大的,但Ga的第一电离能明显低于Zn,原因是
(3)NO2-与钴盐形成的配离子[Co(NO2)6]3-可用于检验 K+的存在。与NO2-互为等电子体的微粒
(4)锰的一种配合物的化学式为 Mn(BH4)2(THF)3,BH4-的空间构型为
(5)FeO 是离子晶体,其晶格能可通过下图中的 Born—Haber 循环计算得到。

可知,O原子的第一电子亲和能为
(6)铜与氧可形成如图所示的晶胞结构,其中 Cu 均匀地分散在立方体内部,a、b的坐标参数依次为(0,0,0)、(1/2,1/2,1/2),则 d 点的坐标参数为

您最近一年使用:0次
解答题-结构与性质
|
适中
(0.65)
名校
解题方法
【推荐2】二氟草酸硼酸锂(LiBF2C2O4)是新型锂离子电池电解质,乙酸锰[(CH3COO)3Mn]可用于制造离子电池的负极材料。合成方程式如下:
2H2C2O4+SiCl4+2LiBF4=2LiBF2C2O4+SiF4+4HCl
4Mn(NO3)2•6H2O+26(CH3CO)2O=4[(CH3COO)3Mn]+8HNO2+3O2↑+40CH3COOH
(1)基态Mn原子的核外电子排布式为____ 。
(2)SiF4中Si的杂化方式为____ 。
(3)CH3COOH易溶于水,原因除了它是极性分子外,还有___ 。
(4)向硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间结构都是三角锥形,但NF3不易与Cu2+形成配离子的原因是____ 。
(5)硼氢化钠的晶胞结构如图所示,该晶胞中Na+的配位数为____ 。若硼氢化钠晶体的密度为dg•cm-3,NA表示阿伏加德罗常数的值,则a=____ (用含d、NA的代数式表示);若硼氢化钠晶胞上、下底心处的Na+被Li+取代,则得到的晶体的化学式为____ 。

2H2C2O4+SiCl4+2LiBF4=2LiBF2C2O4+SiF4+4HCl
4Mn(NO3)2•6H2O+26(CH3CO)2O=4[(CH3COO)3Mn]+8HNO2+3O2↑+40CH3COOH
(1)基态Mn原子的核外电子排布式为
(2)SiF4中Si的杂化方式为
(3)CH3COOH易溶于水,原因除了它是极性分子外,还有
(4)向硫酸铜溶液中加入过量氨水,可生成[Cu(NH3)4]2+配离子。已知NF3与NH3的空间结构都是三角锥形,但NF3不易与Cu2+形成配离子的原因是
(5)硼氢化钠的晶胞结构如图所示,该晶胞中Na+的配位数为

您最近一年使用:0次
解答题-工业流程题
|
适中
(0.65)
解题方法
【推荐3】氢氧化氧镍是高性能一次电池的电极材料。某工厂利用含镍废渣(主要含NiO及少量Fe2O3、FeO、CuO、CaO、SiO2)为原料制备氢氧化氧镍的工艺流程如图:

已知:常温下,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)2]=8.0×10-16,Ksp[Ni(OH)2]=2.0×10-15,当溶液中离子浓度低于1.0×10-5mol/L时,认为沉淀完全。
回答下列问题:
(1)基态Ni原子的价电子排布式为______ ,其电子占据的最高能层的符号为______ 。
(2)写出一种提高“酸浸”速率的措施______ 。
(3)“沉铜”过程中生成单质S的离子方程式为______ 。
(4)有人提出用绿色试剂H2O2代替NaClO也可以达到“氧化”效果,但实践发现所用的H2O2远高于理论用量。试分析造成这一结果的原因是______ 。
(5)当调节pH=5.5时,______ (填“能”或“不能”)达到沉铁目的。
(6)“氧化”生成氢氧化氧镍的离子方程式为______ 。

已知:常温下,Ksp[Fe(OH)3]=4.0×10-38,Ksp[Fe(OH)2]=8.0×10-16,Ksp[Ni(OH)2]=2.0×10-15,当溶液中离子浓度低于1.0×10-5mol/L时,认为沉淀完全。
回答下列问题:
(1)基态Ni原子的价电子排布式为
(2)写出一种提高“酸浸”速率的措施
(3)“沉铜”过程中生成单质S的离子方程式为
(4)有人提出用绿色试剂H2O2代替NaClO也可以达到“氧化”效果,但实践发现所用的H2O2远高于理论用量。试分析造成这一结果的原因是
(5)当调节pH=5.5时,
(6)“氧化”生成氢氧化氧镍的离子方程式为
您最近一年使用:0次



