某温度下HF的电离常数Ka=4×10-4 ,CaF2的溶度积常数Ksp=1.46×10-10。在该温度下取浓度为0.25 mol·L-1的HF与浓度为0.002 mol·L-1的CaCl2溶液等体积混合。下列说法正确的是
| A.该温度下,0.25 mol·L-1的HF溶液的pH=2 |
| B.升高温度或增大浓度,HF的电离平衡常数都将增大 |
| C.两溶液混合不会产生沉淀 |
| D.向饱和的CaF2溶液中加入少量CaCl2固体后,溶度积常数Ksp一定比之前减小 |
更新时间:2018-02-25 10:29:59
|
相似题推荐
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】下列图示与对应叙述正确的是


| A.图甲表示在有、无催化剂时H2O2分解反应的能量变化曲线,曲线b表示有催化剂时的反应 |
B.图乙表示在一定条件下进行的反应2SO2+O2 2SO3中各成分的物质的量浓度变化,t2时刻改变的条件是缩小容器的体积 2SO3中各成分的物质的量浓度变化,t2时刻改变的条件是缩小容器的体积 |
| C.图丙表示25℃时,分别加水稀释体积均为100mL、pH=2的CH3COOH溶液和一元酸HX溶液,则该温度下HX的电离平衡常数大于CH3COOH |
| D.图丁表示用0.1000mol·L-1HCl溶液滴定0.1000mol·L-1NaOH溶液 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列实验装置或操作不能达到实验目的的是
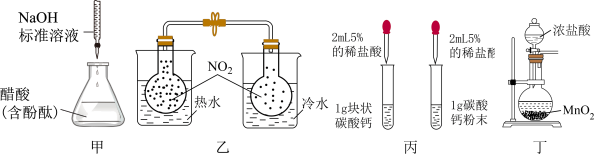

| A.图甲:测定醋酸的浓度 |
| B.图乙:探究温度对化学平衡的影响 |
| C.图丙:探究反应物的接触面积对反应速率的影响 |
| D.图丁:实验室制取氯气 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】测定水的总硬度一般采用配位滴定法, 即在pH=10的氨性溶液中,以铬黑T (EBT)作为指示剂,用EDTA(乙二胺四乙酸二钠,Na2H2Y)标准溶液直接滴定水中的Ca2+、Mg2+,测定中涉及的反应有:
①Mg2++EBT (蓝色)→Mg-EBT (酒红色)
②M2+ (金属离子Ca2+、Mg2+) +Y4- → MY2-
③Mg-EBT+Y4-→MgY2- + EBT
下列说法正确的是
①Mg2++EBT (蓝色)→Mg-EBT (酒红色)
②M2+ (金属离子Ca2+、Mg2+) +Y4- → MY2-
③Mg-EBT+Y4-→MgY2- + EBT
下列说法正确的是
| A.配合物Mg-EBT的稳定性大于MgY2- |
| B.在滴定过程中眼睛要随时观察滴定管中液面的变化 |
| C.达到滴定终点的现象是溶液恰好由酒红色变为蓝色,且半分钟内不恢复原色 |
| D.实验时装EDTA标准液的滴定管只用蒸馏水洗涤而未用标准液润洗,测定结果将偏小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】宏观辨识与微观探析是化学学科核心素养之一、下列反应的离子方程式正确的是
A.向 溶液中通入少量的 溶液中通入少量的 : :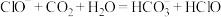 [已知: [已知: 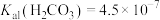 , ,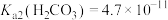 , ,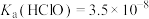 ] ] |
B.泡沫灭火器反应原理: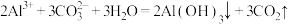 |
C.草酸与酸性高锰酸钾溶液反应: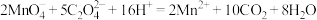 |
D.明矾溶液中加入足量氢氧化钡溶液: |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】已知某二元酸 在溶液中存在电离:
在溶液中存在电离: ,
, ,
, ,设NA为阿伏加德罗常数的值。关于常温下
,设NA为阿伏加德罗常数的值。关于常温下 的
的 溶液,下列说法正确的是
溶液,下列说法正确的是
 在溶液中存在电离:
在溶液中存在电离: ,
, ,
, ,设NA为阿伏加德罗常数的值。关于常温下
,设NA为阿伏加德罗常数的值。关于常温下 的
的 溶液,下列说法正确的是
溶液,下列说法正确的是| A.该溶液与足量NaOH溶液反应的离子方程式是H2A + 2OH- = A2- + 2H2O |
| B.该溶液的c(H+)< 0.001mol/L |
C.该溶液中存在的粒子有 、 、 、 、 、 、 、 、 |
D. |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐3】广安市某中学的化学课外兴趣小组,利用手持技术,进行了酸碱中和滴定实验: 25°C时,向10.00mL 0.10mol/LCH3COOH溶液中,逐滴加入0.10mol/L NaOH溶液,通过pH传感器,在电脑上得到了pH变化曲线如图所示。下列说法正确的是
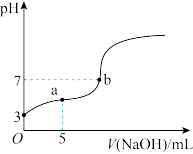

| A.25°C时,CH3COOH的电离平衡常数Ka=1.0 ×10-6 |
| B.b点表示的溶液中c(Na+) < c(CH3COO-) |
| C.a点表示的溶液中2c(Na+)=c(CH3COO-)+c(CH3COOH) |
| D.a、b两点所示的溶液中水的电离程度较大的是a点 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐1】在一定条件下,Na2S溶液中存在水解平衡:S2-+H2O⇌HS-+OH-。下列说法正确的是
| A.加水稀释,所有离子浓度均减小 |
| B.保持温度不变,加入浓盐酸,S2-的水解平衡常数增大 |
C.升高温度, 减小 减小 |
| D.加入AlCl3固体,溶液pH减小 |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
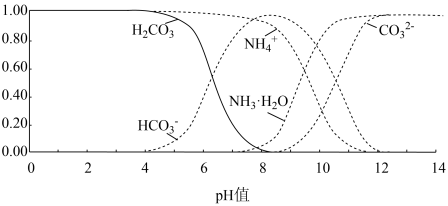
【推荐2】常温下,现有0.1 mol/L碳酸氢铵溶液pH=7.8,已知含氮(或含碳)各微粒的分布分数与pH的关系如下图所示,下列说法正确的是

A.NH4HCO3溶液中存在下列关系: |
B.当溶液的pH=9时,溶液中存在下列关系: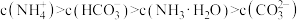 |
C.通过分析可知常温下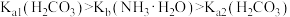 |
D.分析可知,常温下水解平衡常数 的数量级为10-10 的数量级为10-10 |
您最近一年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】下列离子方程式书写不正确的是
A. 与稀硫酸混合: 与稀硫酸混合: |
B. 悬浊液中加入足量的 悬浊液中加入足量的 溶液: 溶液: |
C. 与稀硝酸反应: 与稀硝酸反应: |
D.用足量的氨水吸收烟气中的 : :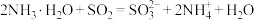 |
您最近一年使用:0次
单选题
|
适中
(0.65)
【推荐2】下列陈述Ⅰ、Ⅱ正确并且有因果关系的是( )
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 氧化性:Fe3+>Cu2+ | 还原性:Fe2+>Cu |
| B | 纯银器表面在空气中渐渐变暗 | Ag发生了化学腐蚀 |
| C | SiO2能与氢氟酸及碱反应 | SiO2是两性氧化物 |
| D | BaSO4饱和溶液中加入饱和Na2CO3溶液有白色沉淀 | 说明Ksp(BaSO4)大于Ksp(BaCO3) |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐3】分别依据下列实验事实,得出的结论正确的是
| 实验事实 | 结论 | |
| A | 苯酚和水的浊液中,加碳酸钠溶液,溶液变澄清 | 苯酚的酸性比碳酸强 |
| B | 将“84”消毒液(含NaClO)滴入品红溶液中,褪色缓慢,若同时加入食醋,红色很快褪为无色 | 随溶液pH减小,“84”消毒液的氧化能力增强 |
| C | 铜放入稀硫酸中,无明显现象,再加入硝酸钠固体,溶液变蓝,有明显的气泡放出,铜溶解 | 硝酸钠可以加快铜与稀硫酸的反应速率 |
| D | 向2 mL 0.1 mol/L的硝酸银溶液中加入1 mL0.1 mol/L NaCl溶液,出现白色沉淀,再加入几滴0.1 mol/L Na2S溶液,有黑色沉淀生成 | 氯化银的溶解度大于硫化银 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次




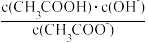 的值更大
的值更大

