常温下,电解质溶液中的下列关系式不正确的是
| A.已知A-+H2B(过量)═HA+HB-,则结合H+的能力:A-<HB-<B2- |
| B.在0.1 mol·L﹣1的氨水中滴加0.1 mol·L-1盐酸,恰好完全中和时溶液的pH=a,则由水电离产生的c(OH-)=10-a mol·L﹣1 |
C.将c mol·L﹣1的醋酸溶液与0.02 mol·L﹣1NaOH溶液等体积混合后溶液恰好呈中性,用含c的代数式表示CH3COOH的电离常数Ka= |
| D.将0.2 mol•L﹣1盐酸与0.1 mol•L﹣1的KAlO2溶液等体积混合,溶液中离子浓度由大到小的顺序:c(Cl-)>c(K+)>c(Al3+)>c(H+)>c(OH-) |
更新时间:2018-03-01 14:43:47
|
相似题推荐
单选题
|
适中
(0.65)
【推荐1】某工业废水中Pb2+及其与OH-形成的微粒的浓度分数a随溶液pH变化的关系如图所示。已知NH3·H2O的Kb=1.74×10-5。向Pb(NO3)2溶液中滴加氨水,关于该过程的说法错误的是


A.c(NO )与c(Pb2+)的比值减小后增大,pH>10后不变 )与c(Pb2+)的比值减小后增大,pH>10后不变 |
| B.Pb2+的浓度分数值减小 |
C.pH=7时,存在的阳离子仅有Pb2+、Pb(OH)+、H+以及NH |
D.溶液中Pb2+与Pb(OH)2浓度相等时,氨主要以NH 的形式存在 的形式存在 |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,通过下列实验探究 、
、 溶液的性质。
溶液的性质。
下列有关说法正确的是
 、
、 溶液的性质。
溶液的性质。| 实验 | 实验操作和现象 |
| 1 | 用pH试纸测定浓度为 溶液的pH,pH约为10 溶液的pH,pH约为10 |
| 2 | 用pH试纸测定浓度为 溶液的pH,pH约为4 溶液的pH,pH约为4 |
| 3 | 向 溶液中滴加酸性高锰酸钾溶液,溶液紫红色褪去 溶液中滴加酸性高锰酸钾溶液,溶液紫红色褪去 |
| 4 | 向 溶液中滴加几滴 溶液中滴加几滴 溶液,产生白色沉淀 溶液,产生白色沉淀 |
A.实验1可得 溶液中: 溶液中: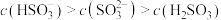 |
B.实验2可得 溶液中: 溶液中: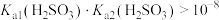 |
C.实验3说明 溶液具有漂白性 溶液具有漂白性 |
D.实验4中发生反应的离子方程式为: |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐1】25℃时,向 溶液中滴入
溶液中滴入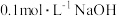 溶液,溶液中由水电离出的
溶液,溶液中由水电离出的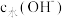 的负对数
的负对数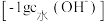 与所加
与所加 溶液体积的关系如图所示.下列说法中正确的是
溶液体积的关系如图所示.下列说法中正确的是
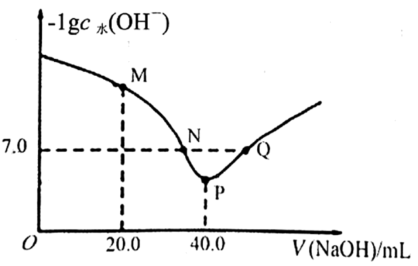
 溶液中滴入
溶液中滴入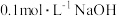 溶液,溶液中由水电离出的
溶液,溶液中由水电离出的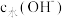 的负对数
的负对数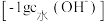 与所加
与所加 溶液体积的关系如图所示.下列说法中正确的是
溶液体积的关系如图所示.下列说法中正确的是
A.M点时: |
B.N点时: |
C.P点时: |
D.水的电离程度: |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐2】下列溶液中粒子的物质的量浓度关系正确的是( )
| A.0.1mol/L NaHCO3溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(Na+)>c(CO32-)>c(HCO3-)>c(OH-) |
| B.20ml 0.1mol/LCH3COONa溶液与10ml 0.1mol/LHCl溶液混合后呈酸性,所得溶液中:c(CH3COO-)>c(Cl-)>c(CH3COOH)>c(OH-) |
| C.室温下,pH=2的盐酸与pH=12的氨水等体积混合,所得溶液中:c(Cl-)>c(H+)>c(NH4+)>c(OH-) |
| D.0.1mol/LCH3COOH溶液与0.1mol/LNaOH溶液等体积混合,所得溶液中:c(OH-)>c(H+)+ c(CH3COOH) |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】室温下,将0.10 mol/LNaOH溶液滴加到0.10 mol/LHA溶液中,溶液的pH与粒子浓度比值的对数 关系如图所示。下列叙述正确的是
关系如图所示。下列叙述正确的是

 关系如图所示。下列叙述正确的是
关系如图所示。下列叙述正确的是
| A.溶液中水的电离程度∶N>P>Q |
| B.室温下,NaA的水解平衡常数K=10-4.75 |
| C.P点溶液中∶c(Na+)=c(OH-)+c(HA)-c(H+) |
| D.Q点溶液中∶c(Na+)>c(A-)>c(HA) |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐2】下列与实验相关的叙述正确的是
| A.取一定体积浓硫酸配制稀硫酸,从量筒中倒出浓硫酸后未冲洗量筒,所配溶液浓度偏低 |
B.将 溶液从20℃升温至30℃,溶液中 溶液从20℃升温至30℃,溶液中 减小 减小 |
| C.酸碱滴定时,若加入待测液前用待测液润洗锥形瓶,将导致测定结果偏低 |
D.将 沉淀转入表面皿中,加入足量稀盐酸,加热蒸干得无水 沉淀转入表面皿中,加入足量稀盐酸,加热蒸干得无水 固体 固体 |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐3】 时,
时, 与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH的关系如下图所示。下列有关叙述正确的是:
与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH的关系如下图所示。下列有关叙述正确的是:
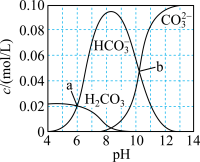
 时,
时, 与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH的关系如下图所示。下列有关叙述正确的是:
与盐酸混合所得的一组体积为1L的溶液,溶液中部分微粒与pH的关系如下图所示。下列有关叙述正确的是: 
A.随pH增大,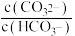 数值先减小后增大 数值先减小后增大 |
B.b点所示的溶液中: |
C. 时,碳酸的第一步电离常数 时,碳酸的第一步电离常数 |
D.溶液呈中性时: |
您最近半年使用:0次


 增大
增大 浓度也相同
浓度也相同 )由大到小的顺序是:①>②>③>④
)由大到小的顺序是:①>②>③>④

