将E和F加入密闭容器中,在一定条件下发生反应:E(g)+F(s)  2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
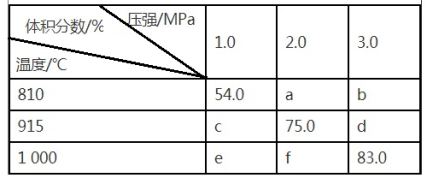
① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1 000℃)>K(810℃) 上述①~④中正确的有( )
 2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
2G(g)。忽略固体体积,平衡时G的体积分数(%)随温度和压强的变化如下表所示:
① b<f ② 915℃、2.0 MPa时E的转化率为60% ③ 增大压强平衡左移 ④ K(1 000℃)>K(810℃) 上述①~④中正确的有( )
| A.4个 | B.3个 | C.2个 | D.1个 |
更新时间:2018-11-16 08:46:45
|
相似题推荐
单选题
|
较难
(0.4)
名校
【推荐1】反应:2X(g)+Y(g)⇌2Z(g)在不同温度和压强下的产物Z的物质的量和反应时间t的关系如图所示,下列判断正确的是( )
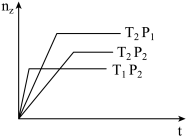

| A.P1>P2 T1>T2 ΔH<0 |
| B.P1>P2 T1<T2 ΔH<0 |
| C.P1<P2 T1>T2 ΔH>0 |
| D.P1<P2 T1<T2 ΔH>0 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】使用合适的催化剂进行乙酸直接加氢可制备乙醇,反应原理如下:
主反应:

副反应:
 (热效应小可忽略)
(热效应小可忽略)
在密闭容器中控制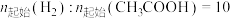 。
。 下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为
下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为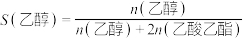 。下列说法正确的是
。下列说法正确的是
主反应:


副反应:

 (热效应小可忽略)
(热效应小可忽略)在密闭容器中控制
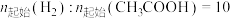 。
。 下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为
下平衡时S(乙醇)和S(乙酸乙酯)随温度的变化与250℃下平衡时S(乙醇)和S(乙酸乙酯)随压强的变化如图所示。乙醇的选择性可表示为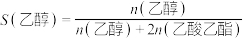 。下列说法正确的是
。下列说法正确的是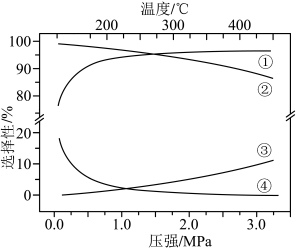
A.反应  |
| B.曲线②变化的原因是随温度升高,副反应正向进行的程度减小 |
| C.图中曲线③表示250℃,乙醇选择性随压强变化的曲线 |
D.300℃、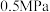 下,反应足够长时间,S(乙醇) 下,反应足够长时间,S(乙醇)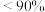 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐3】二硫化碳 是一种重要的溶剂,对
是一种重要的溶剂,对 在内的许多物质具有特殊的溶解能力。在工业生产中用硫
在内的许多物质具有特殊的溶解能力。在工业生产中用硫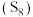 与
与 为原料制备
为原料制备 ,发生以下两个连续反应:反应Ⅰ:
,发生以下两个连续反应:反应Ⅰ: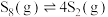 ;反应Ⅱ:
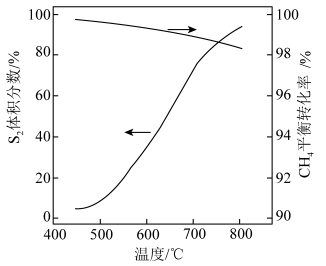
;反应Ⅱ: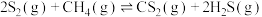 。一定条件下,
。一定条件下, 分解产生
分解产生 的体积分数、
的体积分数、 与
与 反应中
反应中 的平衡转化率与温度的关系如图所示。下列说法不正确的是
的平衡转化率与温度的关系如图所示。下列说法不正确的是
 是一种重要的溶剂,对
是一种重要的溶剂,对 在内的许多物质具有特殊的溶解能力。在工业生产中用硫
在内的许多物质具有特殊的溶解能力。在工业生产中用硫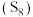 与
与 为原料制备
为原料制备 ,发生以下两个连续反应:反应Ⅰ:
,发生以下两个连续反应:反应Ⅰ: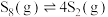 ;反应Ⅱ:
;反应Ⅱ: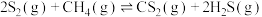 。一定条件下,
。一定条件下, 分解产生
分解产生 的体积分数、
的体积分数、 与
与 反应中
反应中 的平衡转化率与温度的关系如图所示。下列说法不正确的是
的平衡转化率与温度的关系如图所示。下列说法不正确的是
| A.反应Ⅱ的正反应为放热反应 |
B.通过增大 的浓度可以提高 的浓度可以提高 的转化率 的转化率 |
C.增加压强既能提高 的反应速率,又能提高 的反应速率,又能提高 的转化率 的转化率 |
D.制备 时温度需高于600℃的原因是:此温度 时温度需高于600℃的原因是:此温度 平衡转化率已很高,低于此温度, 平衡转化率已很高,低于此温度, 浓度小,反应速率慢 浓度小,反应速率慢 |
您最近一年使用:0次
单选题
|
较难
(0.4)
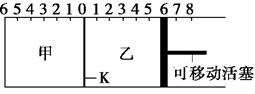
【推荐1】如图所示,甲、乙之间的隔板K可以左右移动,甲中充入2 mol A和1 mol B,乙中充入2 mol C和1 mol He,此时K停在0处。在一定条件下发生可逆反应:2A(g)+B(g) 2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是
2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是
 2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是
2C(g),反应达到平衡后,恢复到反应发生前时的温度。下列有关说法不正确的是
| A.根据隔板K滑动与否可判断左右两边的反应是否达到平衡 |
| B.达到平衡后,隔板K最终停留在左侧刻度0~2之间 |
| C.达到平衡时,甲容器中C的物质的量大于乙容器中C的物质的量 |
| D.若平衡时K停留在左侧1处,则活塞仍停留在右侧6处 |
您最近一年使用:0次
单选题
|
较难
(0.4)
【推荐2】向温度为300℃的2 L密闭容器中充入2 mol SO2和1 mol O2,发生反应2SO2 (g)+ O2 (g)  2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
 2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是
2SO3(g)△H<0,体系达到平衡状态后SO2的浓度为0.1 mol/L,下列说法错误的是| A.该温度下,反应的平衡常数K =1620 |
| B.SO2和O2的平衡转化率相等 |
| C.平衡后保持温度和容器体积不变,再充入SO3(g),平衡常数不变 |
| D.若不再向容器中加入任何物质,仅改变条件不可能使SO2的浓度达到1 mol/L |
您最近一年使用:0次
【推荐1】用含少量 的废铁屑制备三草酸合铁酸钾晶体
的废铁屑制备三草酸合铁酸钾晶体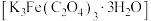 ,流程如图。
,流程如图。
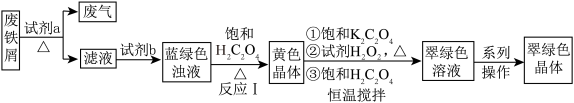
已知:① 为蓝绿色晶体,
为蓝绿色晶体, 为黄色晶体,
为黄色晶体,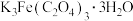 为翠绿色晶体。
为翠绿色晶体。
② 时,
时,
下列说法错误的是
 的废铁屑制备三草酸合铁酸钾晶体
的废铁屑制备三草酸合铁酸钾晶体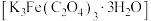 ,流程如图。
,流程如图。
已知:①
 为蓝绿色晶体,
为蓝绿色晶体, 为黄色晶体,
为黄色晶体,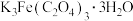 为翠绿色晶体。
为翠绿色晶体。②
 时,
时,
下列说法错误的是
A.试剂 和 和 分别为稀硫酸、氨水 分别为稀硫酸、氨水 |
B.“反应I”的离子方程式为: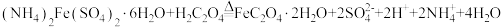 |
| C.“系列操作”包括蒸发浓缩、冷却结晶、过滤、洗涤(乙醇)、干燥 |
| D.可以用KSCN溶液检测所得晶体中铁元素的价态 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐2】某温度下,密闭容器中X、Y、Z、W四种气体的初始浓度和平衡浓度如下表,下列说法错误的是

| A.反应达到平衡时,X的转化率为80% |
B.该反应的平衡常数表达式为K=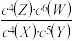 |
| C.增大压强其平衡常数不变,但使平衡向生成Z的方向移动 |
| D.改变温度可以改变此反应的平衡常数 |
您最近一年使用:0次
【推荐3】向三个体积均为3 L的恒容绝热容器中,按不同方式投入反应物,500 ℃条件下开始发生如下反应:H2(g)+Br2(g)  2HBr(g) ΔH<0,测得达平衡时有关数据如下:
2HBr(g) ΔH<0,测得达平衡时有关数据如下:
下列说法正确的是
 2HBr(g) ΔH<0,测得达平衡时有关数据如下:
2HBr(g) ΔH<0,测得达平衡时有关数据如下:容器 | Ⅰ | Ⅱ | Ⅲ |
反应物投入量 | 1 mol H2、1 mol Br2 | 2 mol HBr | 2 mol H2、2 mol Br2 |
平衡时正反应速率 | v1 | v2 | v3 |
平衡常数 | K1 | K2 | K3 |
平衡时H2的物质的量 | n1 | n2 | n3 |
反应物的转化率 | α1 | α2 | α3 |
| A.v1=v2 | B.K1=K3 |
| C.n1>n2 | D.α1+α2>1 |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
【推荐1】恒温恒容的密闭容器中,在某催化剂表面上发生反应: ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法不正确 的是
 ,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法
,测得不同起始浓度和催化剂表面积下氨浓度随时间的变化,如下表所示,下列说法| 编号 | 时间/min 表面积/cm2 | 0 | 20 | 40 | 60 | 80 |
| ① | a | 2.40 | 2.00 | 1.60 | 1.20 | 0.80 |
| ② | a | 1.20 | 0.80 | 0.40 | ||
| ③ | 2a | 2.40 | 1.60 | 0.80 | 0.40 | 0.40 |
A.由实验①、③可知催化剂表面积越大,反应速率越快, 的平衡转化率不变 的平衡转化率不变 |
| B.由实验数据可知相同条件下,增加氨的浓度,该反应速率不一定增大 |
C.实验①、②达到平衡后, 的体积分数①<② 的体积分数①<② |
D.实验③达到平衡后, 的体积分数约为22.7% 的体积分数约为22.7% |
您最近一年使用:0次
单选题
|
较难
(0.4)
名校
解题方法
【推荐2】在25℃时,密闭容器中X、Y、Z三种气体的初始浓度和平衡浓度如下表:
下列说法错误的是( )
| 物质 | X | Y | Z |
| 初始浓度/mol·L-1 | 0.1 | 0.2 | 0 |
| 平衡浓度/mol·L-1 | 0.05 | 0.05 | 0.1 |
| A.增大压强使平衡向生成Z的方向移动,平衡常数增大 |
B.反应可表示为X+3Y 2Z,其平衡常数为1600 2Z,其平衡常数为1600 |
| C.反应达到平衡时,X的转化率为50% |
| D.增大X的浓度,Y的转化率增大 |
您最近一年使用:0次

 密闭容器中充入
密闭容器中充入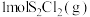 和
和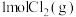 ,发生反应:
,发生反应: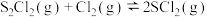 。
。 的消耗速率
的消耗速率 、
、 的消耗速率
的消耗速率 三者的关系如图所示。下列说法正确的是
三者的关系如图所示。下列说法正确的是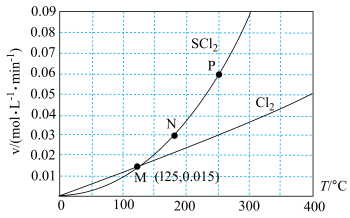
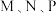 三点对应状态下,达到平衡状态的是
三点对应状态下,达到平衡状态的是
 增大
增大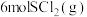 ,平衡时
,平衡时 的体积分数增大
的体积分数增大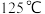 时,平衡时
时,平衡时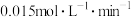

 。实验测得:
。实验测得: ,
,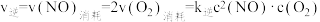 ,
, 、
、 为速率常数,受温度影响。下列说法正确的是
为速率常数,受温度影响。下列说法正确的是 )
)


 ,且
,且 ,则
,则
 的转化率比容器I中的大
的转化率比容器I中的大

