下列说法不正确的是
| A.Na2CO3溶液中c(Na+)与c(CO32-)之比大于2:1 |
| B.蒸发氯化铝溶液要不断通入氯化氢气体方可得到氯化铝晶体 |
| C.1 L 0.3 mol/L醋酸溶液中H+个数与3 L 0.1 mol/L醋酸溶液中H+个数之比为1:1 |
| D.0.1 mol·L-1 Na2SO3溶液中:c(OH-)-c(H+)=2c(H2SO3)+c(HSO3-) |
更新时间:2019-01-01 12:12:45
|
相似题推荐
单选题
|
适中
(0.65)
名校
【推荐1】下列溶液中微粒的物质的量浓度关系正确的是
| A.25℃时,向0.1mol·L-1NH4HSO4溶液中滴加NaOH溶液至中性:c(Na+)>c(NH4+)>c(SO42-)>c(OH-)=c(H+) |
| B.25℃时,NaB溶液的pH=8,c(Na+)- c(B-)=9.9×10-7 mol·L-1 |
| C.0.1 mol·L-1NaHCO3溶液:c(Na+)>c(oH-)>c(HCO3-)>c(H+) |
| D.相同物质的量浓度的CH3COONa和NaClO的混合液中,各离子浓度的大小关系是:c(Na+)>c(ClO-)>c(CH3COO-)>c(OH-)>c(H+) |
您最近半年使用:0次
单选题
|
适中
(0.65)
【推荐2】 时,由弱酸
时,由弱酸 及其盐
及其盐 组成的混合溶液,起始浓度均为
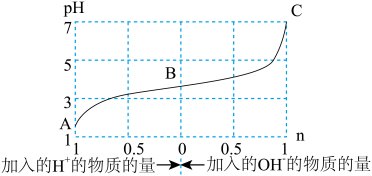
组成的混合溶液,起始浓度均为 。如图为向该溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入
。如图为向该溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入 或
或 的物质的量而变化的曲线。下列说法中,不正确的是
的物质的量而变化的曲线。下列说法中,不正确的是
 时,由弱酸
时,由弱酸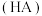 及其盐
及其盐 组成的混合溶液,起始浓度均为
组成的混合溶液,起始浓度均为 。如图为向该溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入
。如图为向该溶液中通入HCl气体或加入NaOH固体时,溶液pH随加入 或
或 的物质的量而变化的曲线。下列说法中,不正确的是
的物质的量而变化的曲线。下列说法中,不正确的是
| A.A、B、C三点所表示的溶液中水的电离程度依次增大 |
B.加入1 mol NaOH后,溶液中 |
C.通入HCl, 的水解程度增大,HA的电离常数减小 的水解程度增大,HA的电离常数减小 |
D.未加HCl和NaOH时,溶液中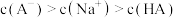 |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
【推荐1】向0.1 mol•L-1醋酸溶液中逐滴滴入0.1 mol•L-1氢氧化钠溶液,所得溶液离子浓度大小顺序一定不正确的是
①c(H+)>c(CH3COO-)>c(OH-)>c(Na+)
②c(CH3COO-)>c(Na+)=c(H+)>c(OH-)
③c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
④c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
⑤c(Na+)>c(CH3COO-)=c(OH-)>c(H+)
⑥c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
⑦c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
①c(H+)>c(CH3COO-)>c(OH-)>c(Na+)
②c(CH3COO-)>c(Na+)=c(H+)>c(OH-)
③c(CH3COO-)>c(Na+)>c(H+)>c(OH-)
④c(CH3COO-)=c(Na+)>c(H+)=c(OH-)
⑤c(Na+)>c(CH3COO-)=c(OH-)>c(H+)
⑥c(Na+)>c(CH3COO-)>c(H+)>c(OH-)
⑦c(Na+)>c(OH-)>c(CH3COO-)>c(H+)
| A.②③④ | B.只有⑥ | C.①⑥ | D.②④⑤⑥ |
您最近半年使用:0次
单选题
|
适中
(0.65)
解题方法
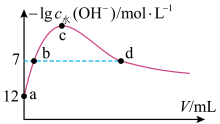
【推荐2】常温下,将 通入
通入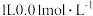 的某一元碱MOH溶液中,溶液中水电离出的
的某一元碱MOH溶液中,溶液中水电离出的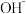 离子浓度
离子浓度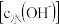 与通入的
与通入的 的体积
的体积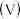 的关系如图所示,下列叙述错误的是
的关系如图所示,下列叙述错误的是
 通入
通入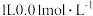 的某一元碱MOH溶液中,溶液中水电离出的
的某一元碱MOH溶液中,溶液中水电离出的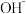 离子浓度
离子浓度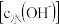 与通入的
与通入的 的体积
的体积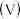 的关系如图所示,下列叙述错误的是
的关系如图所示,下列叙述错误的是
| A.MOH为一元强碱 |
B.b点溶液中: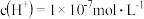 |
C.c点溶液中: |
D.d点溶液中: |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐1】常温下,通过下列实验探究 、
、 溶液的性质。
溶液的性质。
实验1:向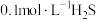 溶液中通入一定体积
溶液中通入一定体积 ,测得溶液
,测得溶液 为7
为7
实验2:向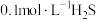 溶液中加等体积同浓度
溶液中加等体积同浓度 溶液,充分反应后再滴入2滴酚酞,溶液呈红色
溶液,充分反应后再滴入2滴酚酞,溶液呈红色
实验3:向 溶液中逐滴滴加等体积同浓度的盐酸,无明显现象
溶液中逐滴滴加等体积同浓度的盐酸,无明显现象
实验4:向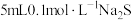 溶液中滴入
溶液中滴入 溶液,产生白色沉淀;再滴入几滴
溶液,产生白色沉淀;再滴入几滴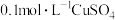 溶液,立即出现黑色沉淀
溶液,立即出现黑色沉淀
下列说法正确的是
 、
、 溶液的性质。
溶液的性质。实验1:向
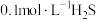 溶液中通入一定体积
溶液中通入一定体积 ,测得溶液
,测得溶液 为7
为7实验2:向
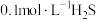 溶液中加等体积同浓度
溶液中加等体积同浓度 溶液,充分反应后再滴入2滴酚酞,溶液呈红色
溶液,充分反应后再滴入2滴酚酞,溶液呈红色实验3:向
 溶液中逐滴滴加等体积同浓度的盐酸,无明显现象
溶液中逐滴滴加等体积同浓度的盐酸,无明显现象实验4:向
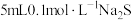 溶液中滴入
溶液中滴入 溶液,产生白色沉淀;再滴入几滴
溶液,产生白色沉淀;再滴入几滴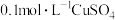 溶液,立即出现黑色沉淀
溶液,立即出现黑色沉淀下列说法正确的是
A.实验1得到的溶液中存在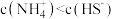 |
B.由实验2可得出: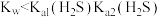 |
C.实验3得到的溶液中存在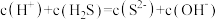 |
D.由实验4可得出: |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】常温下,用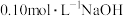 溶液滴定
溶液滴定 溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列叙述错误的是
溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列叙述错误的是
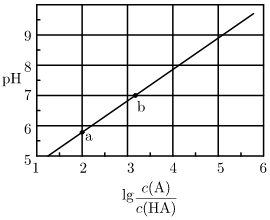
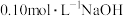 溶液滴定
溶液滴定 溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列叙述错误的是
溶液,混合溶液的pH与离子浓度变化的关系如图所示,下列叙述错误的是
A. 的数量级为 的数量级为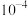 |
| B.b点时消耗NaOH溶液的体积小于20mL |
C.b点溶液中离子浓度: |
D.混合溶液的导电能力: |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
【推荐1】设NA为阿伏加德罗常数的值。下列说法正确的是
| A.将0.1molFeCl3溶液于1L水中,所得溶液含Fe3+离子数目为0.1NA |
| B.1 mol的羟基与1 mol的氢氧根离子所含电子数均为10NA |
| C.常温、常压下,4.6 g NO2和N2O4混合气体中含有的氧原子数目为0.2NA |
| D.在高温下,有1 mol Fe与足量的水蒸气反应,转移电子的数目为3NA |
您最近半年使用:0次
单选题
|
适中
(0.65)
名校
解题方法
【推荐2】室温下,下列各组离子在指定溶液中一定能大量共存的是( )
A.能使甲基橙试液显红色的溶液中:NH 、Mg2+、ClO-、NO 、Mg2+、ClO-、NO |
B.0.1 mol·L的NH4Al(SO4)2溶液中:K+、Na+、CO 、Cl- 、Cl- |
C.透明的溶液中:Cu2+、Fe3+、SO 、Cr3+ 、Cr3+ |
D.常温下, 的溶液中:Fe2+、Al3+、NO 的溶液中:Fe2+、Al3+、NO 、SO 、SO |
您最近半年使用:0次


 与
与 混合所得的碱性溶液中:
混合所得的碱性溶液中:
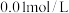 的
的 和
和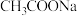 的混合溶液中
的混合溶液中
 溶液、
溶液、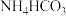 溶液、
溶液、 溶液中
溶液中 :
:
 为阿伏加德罗常数的值,下列说法正确的是
为阿伏加德罗常数的值,下列说法正确的是 与
与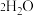 (标准状况下)中所含质子数目为2.5
(标准状况下)中所含质子数目为2.5 离子数目为0.1
离子数目为0.1 浓度均为
浓度均为 的
的 和
和 混合溶液中逐滴加入
混合溶液中逐滴加入 某一元碱
某一元碱 溶液,溶液的导电能力随
溶液,溶液的导电能力随
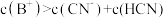
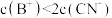 ,则
,则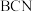 溶液显碱性
溶液显碱性



