研究碳、氮、硫等元素化合物的性质或转化对建设生态文明、美丽中国具有重要意义。
(1)海水中无机碳的存在形式及分布如下图所示:用离子方程式表示海水呈弱碱性的原因_________ 。已知春季海水pH=8.1,预测夏季海水碱性将会_________ (填写“增强”或“减弱”),理由是________ (写出1条即可)
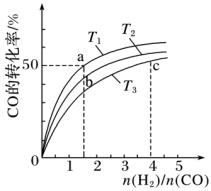
(2)工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g) CH3OH(g)△H<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为lmol)与CO平衡转化率的关系。下列说法正确的是
CH3OH(g)△H<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为lmol)与CO平衡转化率的关系。下列说法正确的是_________ (a、b点横坐标相同,a在曲线T1上,b在曲线T2上)
A.a、b、c三点H2转化率:c>a>b
B.上述三种温度之间关系为T1>T2>T3
C.a点(1.5,50)状态下再通入0.5 mol CO和0.5 mol CH3OH,平衡不移动
D.c点状态下再通入1 molCO和4molH2,新平衡中H2的体积分数增大
(3)NO加速臭氧层被破坏,其反应过程如图所示:
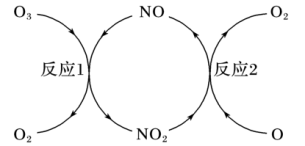
①NO的作用是__________________ 。
②已知:O3(g)+O(g)=2O2(g)△H =-143kJ·mol-1
反应1: O3(g)+NO(g) NO2(g)+O2(g)△H1=-200.2kJ·mol-1
NO2(g)+O2(g)△H1=-200.2kJ·mol-1
反应2:热化学方程式为______________________ 。
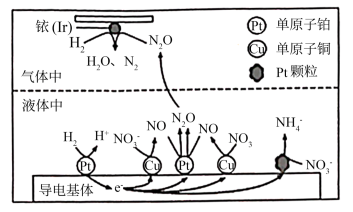
(4)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-)从而降低水体中的氮含量,其工作原理如下图所示
①Ir表面发生反应的方程式为__________________________ 。
②若导电基体上的Pt颗粒增多,造成的后果是__________________________ 。
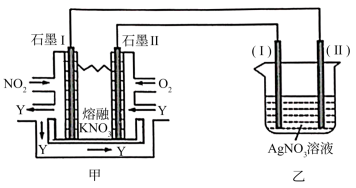
(5)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来精炼银,装置如图所示,甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用,则石墨II附近发生的电极反应式为__________________________ 。
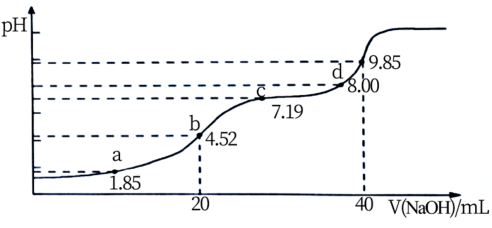
(6)大气污染物SO2可用NaOH吸收。已知pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。该温度下用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液的滴定曲线如下图所示。b点所得溶液中各离子浓度由大到小的顺序是__________________________ ;c点所得溶液中:c(Na+)__________ 3c(HSO3-)(填“>”、“<”或“=”)
(1)海水中无机碳的存在形式及分布如下图所示:用离子方程式表示海水呈弱碱性的原因
| 无机碳 | HCO3- | 90% |
| CO32- | 9% | |
| CO2 | 1% | |
| H2CO3 | ||
| 其中H2CO3仅为CO2的0.2% | ||

(2)工业上以CO和H2为原料合成甲醇的反应:CO(g)+2H2(g)
 CH3OH(g)△H<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为lmol)与CO平衡转化率的关系。下列说法正确的是
CH3OH(g)△H<0,在容积为1L的恒容容器中,分别在T1、T2、T3三种温度下合成甲醇。如图是上述三种温度下不同H2和CO的起始组成比(起始时CO的物质的量均为lmol)与CO平衡转化率的关系。下列说法正确的是A.a、b、c三点H2转化率:c>a>b
B.上述三种温度之间关系为T1>T2>T3
C.a点(1.5,50)状态下再通入0.5 mol CO和0.5 mol CH3OH,平衡不移动
D.c点状态下再通入1 molCO和4molH2,新平衡中H2的体积分数增大
(3)NO加速臭氧层被破坏,其反应过程如图所示:

①NO的作用是
②已知:O3(g)+O(g)=2O2(g)△H =-143kJ·mol-1
反应1: O3(g)+NO(g)
 NO2(g)+O2(g)△H1=-200.2kJ·mol-1
NO2(g)+O2(g)△H1=-200.2kJ·mol-1反应2:热化学方程式为
(4)近年来,地下水中的氮污染已成为一个世界性的环境问题。在金属Pt、Cu和铱(Ir)的催化作用下,密闭容器中的H2可高效转化酸性溶液中的硝态氮(NO3-)从而降低水体中的氮含量,其工作原理如下图所示
①Ir表面发生反应的方程式为
②若导电基体上的Pt颗粒增多,造成的后果是


(5)利用电化学原理,将NO2、O2和熔融KNO3制成燃料电池,模拟工业电解法来精炼银,装置如图所示,甲池工作时,NO2转变成绿色硝化剂Y,Y是N2O5,可循环使用,则石墨II附近发生的电极反应式为
(6)大气污染物SO2可用NaOH吸收。已知pKa=-lgKa,25℃时,H2SO3的pKa1=1.85,pKa2=7.19。该温度下用0.1mol·L-1NaOH溶液滴定20mL0.1mol·L-1H2SO3溶液的滴定曲线如下图所示。b点所得溶液中各离子浓度由大到小的顺序是

更新时间:2019-07-04 15:42:31
|
相似题推荐
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】为尽快实现“碳达峰”“碳中和”,碳化学研究已成为当前科学研究的热点。由 合成淀粉的部分流程如图所示:
合成淀粉的部分流程如图所示:
①
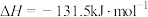
②
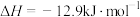
③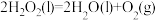
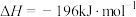
④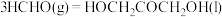
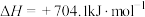
回答下列问题:
(1)反应①中,反应物的总能量_______ (填“大于”、“小于”或“等于”,下同)生成物的总能量,反应④中,反应物的总键能_______ 生成物的总键能。
(2)反应①中使用催化剂的作用有_______ (填标号);将3mol 和1mol
和1mol 通过催化剂发生反应①,经过2次循环后测得
通过催化剂发生反应①,经过2次循环后测得 的转化率为36%,则经过4次循环后
的转化率为36%,则经过4次循环后 的转化率为
的转化率为_______ 。
a.有效降低了反应活化能
b.提高了 的平衡转化率
的平衡转化率
c.加快了反应①的反应速率
(3)已知 的燃烧热(
的燃烧热( )为
)为 ,则
,则 的燃烧热(
的燃烧热( )为
)为_______ 。
(4) 合成淀粉过程中,当有1kg
合成淀粉过程中,当有1kg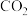 转化为
转化为 时,理论上反应体系共需向外界
时,理论上反应体系共需向外界_______ (填“吸收”或“放出”)的热量为_______ kJ。(所有能量均充分利用,且不考虑能量的损耗)
(5)几个有关CO的热化学方程式为
 ;
;
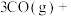
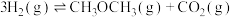
 ;
;

 ;
;
则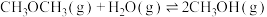

_______ (用含 、
、 、
、 的代数式表示)。
的代数式表示)。
 合成淀粉的部分流程如图所示:
合成淀粉的部分流程如图所示: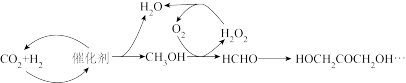
①

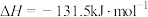
②

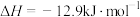
③
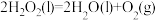
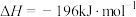
④
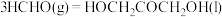
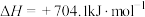
回答下列问题:
(1)反应①中,反应物的总能量
(2)反应①中使用催化剂的作用有
 和1mol
和1mol 通过催化剂发生反应①,经过2次循环后测得
通过催化剂发生反应①,经过2次循环后测得 的转化率为36%,则经过4次循环后
的转化率为36%,则经过4次循环后 的转化率为
的转化率为a.有效降低了反应活化能
b.提高了
 的平衡转化率
的平衡转化率c.加快了反应①的反应速率
(3)已知
 的燃烧热(
的燃烧热( )为
)为 ,则
,则 的燃烧热(
的燃烧热( )为
)为(4)
 合成淀粉过程中,当有1kg
合成淀粉过程中,当有1kg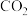 转化为
转化为 时,理论上反应体系共需向外界
时,理论上反应体系共需向外界(5)几个有关CO的热化学方程式为

 ;
;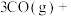
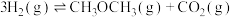
 ;
;
 ;
;则
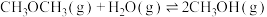

 、
、 、
、 的代数式表示)。
的代数式表示)。
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐2】碳资源的合理利用和控制储存具有重要意义。
(1)工业上制备甲醇的主要反应有:
反应Ⅰ. 平衡常数K1
平衡常数K1
反应Ⅱ.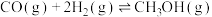 平衡常数K2
平衡常数K2
反应Ⅲ. 平衡常数K3
平衡常数K3
K3=___________ 。(用K1、K2表示)
(2)乙烷直接热解脱氢制乙烯。热化学方程式为: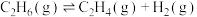 △H
△H
△H=___________ kJ∙mol-1 (填数值,相关键能数据如下表)。
(3)已知草酸( )为二元弱酸,
)为二元弱酸, 、
、 、
、 三种微粒的物质的量分数(
三种微粒的物质的量分数( )与溶液pH的关系如下图所示。
)与溶液pH的关系如下图所示。
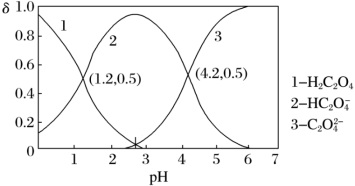
①用已知浓度的酸性KMnO4溶液滴定未知浓度草酸溶液,终点判断:当滴入最后半滴KMnO4溶液时,___________ ,停止滴定,并记录KMnO4溶液的体积,重复操作2~3次。
②硫酸酸化的KMnO4溶液滴定H2C2O4溶液的离子方程式为___________ 。
③结合图中信息,pH=2.7的溶液中: =
=___________ 。(填数值)
(1)工业上制备甲醇的主要反应有:
反应Ⅰ.
 平衡常数K1
平衡常数K1反应Ⅱ.
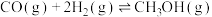 平衡常数K2
平衡常数K2反应Ⅲ.
 平衡常数K3
平衡常数K3K3=
(2)乙烷直接热解脱氢制乙烯。热化学方程式为:
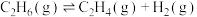 △H
△H△H=
| 化学键 |  |  |  |  |
键能/ | 348 | 615 | 413 | 436 |
(3)已知草酸(
 )为二元弱酸,
)为二元弱酸, 、
、 、
、 三种微粒的物质的量分数(
三种微粒的物质的量分数( )与溶液pH的关系如下图所示。
)与溶液pH的关系如下图所示。
①用已知浓度的酸性KMnO4溶液滴定未知浓度草酸溶液,终点判断:当滴入最后半滴KMnO4溶液时,
②硫酸酸化的KMnO4溶液滴定H2C2O4溶液的离子方程式为
③结合图中信息,pH=2.7的溶液中:
 =
=
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
【推荐3】当今世界多国相继规划了碳达峰、碳中和的时间节点。因此,研发二氧化碳利用技术,降低空气中二氧化碳含量成为研究热点。其中用 、
、 为原料合成甲醇(
为原料合成甲醇( )过程主要涉及以下反应:
)过程主要涉及以下反应:
反应Ⅰ:

反应Ⅱ:

反应Ⅲ:
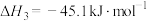
(1)根据盖斯定律,反应Ⅰ的
_______ 。
(2)我国学者结合实验与计算机模拟结果,研究了 与
与 在
在 /Cu催化剂表面生成
/Cu催化剂表面生成 和
和 的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
_______ eV。并写出该历程的化学方程式_______ 。
(3)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______(填字母)。
(4)加压,甲醇产率将_______ (填“升高”“不变”“降低”或“无法确定”);若原料二氧化碳中掺混一氧化碳,随一氧化碳含量的增加,甲醇产率将_______ (填“升高”“不变”“降低”或“无法确定”)。
(5)加入新催化剂使1mol 和3mol
和3mol  在1L密闭容器中只发生反应Ⅰ、Ⅱ,
在1L密闭容器中只发生反应Ⅰ、Ⅱ, 平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的
平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的 物质的量分数)与温度的变化趋势如图所示。
物质的量分数)与温度的变化趋势如图所示。_______ (填“473K”“513K”或“553K”)。
②553K时,若反应后体系的总压为p,反应Ⅰ的
_______ (列出计算式)。( 为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
 、
、 为原料合成甲醇(
为原料合成甲醇( )过程主要涉及以下反应:
)过程主要涉及以下反应:反应Ⅰ:


反应Ⅱ:


反应Ⅲ:

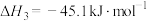
(1)根据盖斯定律,反应Ⅰ的

(2)我国学者结合实验与计算机模拟结果,研究了
 与
与 在
在 /Cu催化剂表面生成
/Cu催化剂表面生成 和
和 的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。
的部分反应历程,如图所示,其中吸附在催化剂表面的物种用*标注。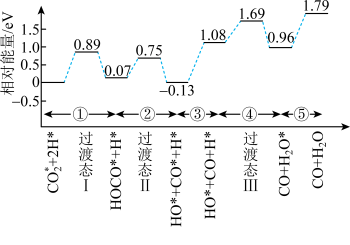

(3)上述反应体系在一定条件下建立平衡后,下列说法正确的有_______(填字母)。
| A.升高温度,反应Ⅱ正向移动,反应Ⅲ逆向移动 |
| B.加入反应Ⅰ的催化剂,可以降低反应的活化能及反应热 |
C.增大 的浓度,有利于提高 的浓度,有利于提高 的平衡转化率 的平衡转化率 |
D.及时分离出 ,可以使得反应Ⅰ的正反应速率增大 ,可以使得反应Ⅰ的正反应速率增大 |
(4)加压,甲醇产率将
(5)加入新催化剂使1mol
 和3mol
和3mol  在1L密闭容器中只发生反应Ⅰ、Ⅱ,
在1L密闭容器中只发生反应Ⅰ、Ⅱ, 平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的
平衡转化率和甲醇选择率(甲醇选择率是指转化生成甲醇的 物质的量分数)与温度的变化趋势如图所示。
物质的量分数)与温度的变化趋势如图所示。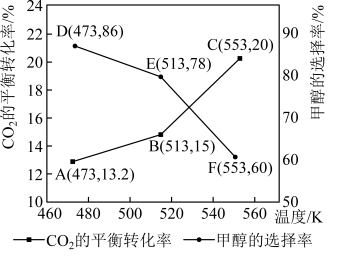
②553K时,若反应后体系的总压为p,反应Ⅰ的

 为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
为压强平衡常数,其表达式写法:在浓度平衡常数表达式中用气体分压代替浓度,气体的分压等于总压乘以物质的量分数。)
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐1】 回收与利用是环境科学家研究的热点课题。利用
回收与利用是环境科学家研究的热点课题。利用 制备合成气(
制备合成气( ),再制备高值产品,如甲醇等,也可以利用
),再制备高值产品,如甲醇等,也可以利用 直接制备甲醇等产品。
直接制备甲醇等产品。
(1)已知几种反应的正反应活化能(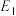 )、逆反应活化能(
)、逆反应活化能(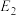 )如表所示:
)如表所示:
上述反应,其中属于吸热反应的有______ (填序号),氢气的标准燃烧热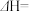
_________  。
。
(2) 下,在
下,在 恒容密闭容器中充入
恒容密闭容器中充入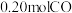 和
和 合成
合成 ,发生反应:
,发生反应: 经
经 恰好达到平衡,
恰好达到平衡, 的浓度是
的浓度是 。
。
① 时,以
时,以 表示的反应的平均速率为
表示的反应的平均速率为_______________ 。
②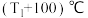 时,在1L恒容密闭容器中充入
时,在1L恒容密闭容器中充入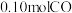 、
、 和
和 此时速率
此时速率
________  (填“>”“<”“=”)
(填“>”“<”“=”)
(3) 和
和 在催化剂作用下,可以直接合成甲醇,其反应原理可用方程式表示为
在催化剂作用下,可以直接合成甲醇,其反应原理可用方程式表示为
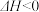 ,测得反应开始相同时间内甲醇产率与温度的关系如图所示。
,测得反应开始相同时间内甲醇产率与温度的关系如图所示。

分析温度在 时(催化剂有效)甲醇产率最高的主要原因是
时(催化剂有效)甲醇产率最高的主要原因是_______________ 。
 回收与利用是环境科学家研究的热点课题。利用
回收与利用是环境科学家研究的热点课题。利用 制备合成气(
制备合成气( ),再制备高值产品,如甲醇等,也可以利用
),再制备高值产品,如甲醇等,也可以利用 直接制备甲醇等产品。
直接制备甲醇等产品。(1)已知几种反应的正反应活化能(
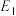 )、逆反应活化能(
)、逆反应活化能(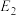 )如表所示:
)如表所示:| 序号 | 化学反应 |  |  |
| ① | 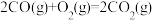 | 1954 | 2519 |
| ② |  | 685 | 970 |
| ③ |  | 4978 | 3526 |
上述反应,其中属于吸热反应的有
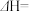
 。
。(2)
 下,在
下,在 恒容密闭容器中充入
恒容密闭容器中充入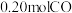 和
和 合成
合成 ,发生反应:
,发生反应: 经
经 恰好达到平衡,
恰好达到平衡, 的浓度是
的浓度是 。
。①
 时,以
时,以 表示的反应的平均速率为
表示的反应的平均速率为②
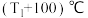 时,在1L恒容密闭容器中充入
时,在1L恒容密闭容器中充入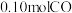 、
、 和
和 此时速率
此时速率
 (填“>”“<”“=”)
(填“>”“<”“=”)(3)
 和
和 在催化剂作用下,可以直接合成甲醇,其反应原理可用方程式表示为
在催化剂作用下,可以直接合成甲醇,其反应原理可用方程式表示为
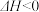 ,测得反应开始相同时间内甲醇产率与温度的关系如图所示。
,测得反应开始相同时间内甲醇产率与温度的关系如图所示。
分析温度在
 时(催化剂有效)甲醇产率最高的主要原因是
时(催化剂有效)甲醇产率最高的主要原因是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】某实验小组研究可逆反应AsO43-+2I-+2H+ AsO33-+I2+H2O时,设计了如图所示的原电池:
AsO33-+I2+H2O时,设计了如图所示的原电池:
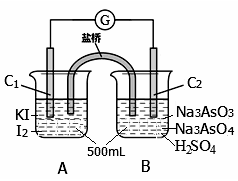
(1)电池工作中,盐桥中的阴离子向________________ 填“C1”或“C2”)极移动;若向B池滴加NaOH溶液,平衡向_________________ 方向移动,此时C2极的电极反应式为____________________________________________________________________ 。
(2)下列判断正确的是_________________ 。
a.微安表指针为0时,该反应处于平衡状态
b.向A池中加入淀粉溶液,溶液变蓝说明该反应处于平衡状态
c.AsO43-、AsO33-浓度相等时,该反应处于平衡状态
(3)该反应的平衡常数表达式K=______ 。若升高温度,K值增大,则正反应的∆H_____ (填“>”“<”或“=”)0。
(4)已知反应达到平衡时,AsO43-的转化率为25%,则I-的转化率_________________ 。
A.大于25% b.小于25%
c.等于25% d.无法确定
 AsO33-+I2+H2O时,设计了如图所示的原电池:
AsO33-+I2+H2O时,设计了如图所示的原电池:
(1)电池工作中,盐桥中的阴离子向
(2)下列判断正确的是
a.微安表指针为0时,该反应处于平衡状态
b.向A池中加入淀粉溶液,溶液变蓝说明该反应处于平衡状态
c.AsO43-、AsO33-浓度相等时,该反应处于平衡状态
(3)该反应的平衡常数表达式K=
(4)已知反应达到平衡时,AsO43-的转化率为25%,则I-的转化率
A.大于25% b.小于25%
c.等于25% d.无法确定
您最近一年使用:0次
【推荐3】工业生产和社会生活重要应用。
Ⅰ.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g) CH3OH(g)。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OHg的浓度随时间变化。请回答下列问题:
CH3OH(g)。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OHg的浓度随时间变化。请回答下列问题:
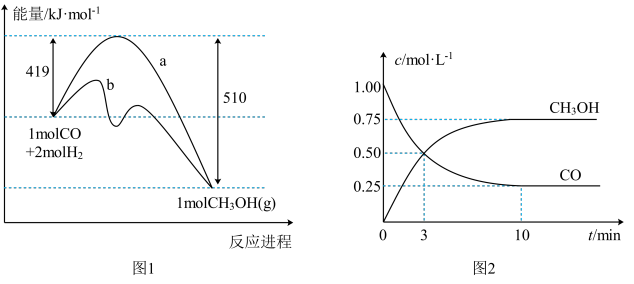
(1)在图1中,曲线___________ (填“a”或“b”)表示使用了催化剂。
(2)该反应属于___________ (填“吸热”或“放热”)反应。
(3)增大反应体系压强,则该反应化学平衡常数___________ (填“增大”“减小”或“不变”)。
(4)下列说法中正确的是___________
Ⅱ.CuSO4溶液是一种重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(5)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是___________ (填字母)。
a.溶液中Cu2+向阳极移动
b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小
d.利用阳极泥可回收Ag、Pt、Au等金属
(6)下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜:
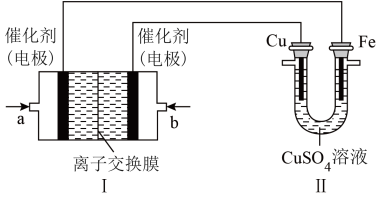
①b处通入的是___________ (填“CH4”或“O2”),a处的电极反应式为___________ 。
②当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为___________ 。
Ⅰ.工业上用CO生产燃料甲醇,一定条件下发生反应:CO(g)+2H2(g)
 CH3OH(g)。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OHg的浓度随时间变化。请回答下列问题:
CH3OH(g)。图1表示反应中能量变化;图2表示一定温度下,在容积为2L的密闭容器中加入4molH2和一定量的CO后,CO和CH3OHg的浓度随时间变化。请回答下列问题:
(1)在图1中,曲线
(2)该反应属于
(3)增大反应体系压强,则该反应化学平衡常数
(4)下列说法中正确的是___________
| A.起始充入的CO为1mol |
| B.增加CO的浓度,CO的转化率增大 |
| C.容器中压强恒定时,反应已达化学平衡状态 |
D.保持温度和密闭容器体积不变,再冲入1molCO和2molH2,再次达到平衡时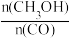 会减小 会减小 |
Ⅱ.CuSO4溶液是一种重要的铜盐试剂,在电镀、印染、颜料、农药等方面有广泛应用。某同学利用CuSO4溶液进行以下实验探究:
(5)以CuSO4溶液为电解质溶液进行粗铜(含Al、Zn、Ag、Pt、Au等杂质)的电解精炼,下列说法正确的是
a.溶液中Cu2+向阳极移动
b.粗铜接电源正极,发生还原反应
c.电解后CuSO4溶液的浓度减小
d.利用阳极泥可回收Ag、Pt、Au等金属
(6)下图中,Ⅰ是甲烷燃料电池(电解质溶液为KOH溶液)的结构示意图,该同学想在Ⅱ中实现铁上镀铜:

①b处通入的是
②当铜电极的质量减轻3.2g,则消耗的CH4在标准状况下的体积为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
【推荐1】CO2耦合乙苯(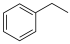 )脱氢制备苯乙烯(
)脱氢制备苯乙烯( )是综合利用CO2的热点研究领域,制备苯乙烯涉及的主要反应如下:
)是综合利用CO2的热点研究领域,制备苯乙烯涉及的主要反应如下:
反应I. (g)⇌
(g)⇌  (g)+H2(g) △H1
(g)+H2(g) △H1
 △H2>0
△H2>0反应Ⅲ. (g)+CO2(g)⇌
(g)+CO2(g)⇌ (g)+CO(g)+H2O(g)△H3>0
(g)+CO(g)+H2O(g)△H3>0
| 化学键 | H-H | C-H | C-C | C=C |
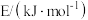 | 436 | 413 | 348 | 615 |
利用上表数据计算△H1为 的平衡转化率,可采取的措施为
的平衡转化率,可采取的措施为
 随温度变化关系如图所示。三种原料气配比分别为:I.只有乙苯、Ⅱ.n(乙苯):n(CO2)=1:5、Ⅲ.n(乙苯):n(Ar)=1:5
随温度变化关系如图所示。三种原料气配比分别为:I.只有乙苯、Ⅱ.n(乙苯):n(CO2)=1:5、Ⅲ.n(乙苯):n(Ar)=1:5
②恒压条件下,若B表示原料气只有乙苯的曲线,则原料气配比n(乙苯):n(CO2)=1:5的曲线为
(3)向恒容密闭容器中,投入乙苯和CO2各1mol,此时气体压强为P0,催化脱氢制备苯乙烯,除上述反应外,还发生副反应:
 (g)+H2(g)
(g)+H2(g)
 (g)+CH4(g) △H4<0,测得反应体系中甲苯的选择性s(
(g)+CH4(g) △H4<0,测得反应体系中甲苯的选择性s( )、乙苯的平衡转化率、CO2的平衡转化率随温度的变化关系如图所示。表示乙苯的平衡转化率的曲线是
)、乙苯的平衡转化率、CO2的平衡转化率随温度的变化关系如图所示。表示乙苯的平衡转化率的曲线是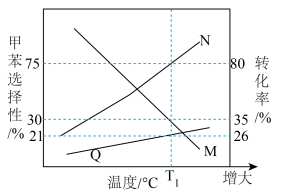
您最近一年使用:0次
【推荐2】高纯硅晶体是信息技术的重要材料。
(1)在周期表的以下区域中可以找到类似硅的半导体材料的是______ (填字母)。
A.过渡元素区域 B.金属和非金属元素的分界线附近
(2)工业上用石英和焦炭可以制得粗硅。已知:

写出用石英和焦炭制取粗硅的热化学方程式____________________ 。
(3)某同学设计下列流程制备高纯硅:

①Y的化学式为______ 。
②写出反应Ⅰ的离子方程式______________ 。
③写出反应Ⅳ的化学方程式______________ 。
④步骤Ⅵ中硅烷(SiH4)分解生成高纯硅,已知甲烷分解的温度远远高于硅烷,用原子结构解释其原因是______________ 。
(4)将粗硅转化成三氯硅烷(SiHCl3),进一步反应也可以制得粗硅。其反应:
SiHCl3 (g) + H2(g) Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是
Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是______________ (填字母)。

A.该反应是放热反应
B.横坐标表示的投料比应该是
C.该反应的平衡常数随温度升高而增大
D.实际生产中为提高SiHCl3的利用率,可以适当增大压强
(1)在周期表的以下区域中可以找到类似硅的半导体材料的是
A.过渡元素区域 B.金属和非金属元素的分界线附近
(2)工业上用石英和焦炭可以制得粗硅。已知:

写出用石英和焦炭制取粗硅的热化学方程式
(3)某同学设计下列流程制备高纯硅:

①Y的化学式为
②写出反应Ⅰ的离子方程式
③写出反应Ⅳ的化学方程式
④步骤Ⅵ中硅烷(SiH4)分解生成高纯硅,已知甲烷分解的温度远远高于硅烷,用原子结构解释其原因是
(4)将粗硅转化成三氯硅烷(SiHCl3),进一步反应也可以制得粗硅。其反应:
SiHCl3 (g) + H2(g)
 Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是
Si(s) + 3HCl(g),不同温度下,SiHCl3的平衡转化率随反应物的投料比(反应初始时各反应物的物质的量之比)的变化关系如图所示。下列说法正确的是
A.该反应是放热反应
B.横坐标表示的投料比应该是

C.该反应的平衡常数随温度升高而增大
D.实际生产中为提高SiHCl3的利用率,可以适当增大压强
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】甲醇是一种重要的化工原料,具有广阔的开发和应用前景。工业上使用水煤气(CO与H2的混合气体)转化成甲醇(CH3OH)。
(1)已知一定条件下,发生反应:
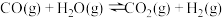
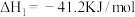
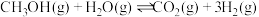
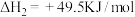
该条件下,水煤气(CO与H2的混合气体)转化成甲醇的热化学方程式是_______ 。
(2)工业上使用水煤气转化成甲醇,CO的平衡转化率与温度、压强的关系如图所示:
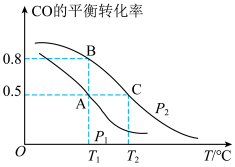
①要使A点变到B点除增大压强外还可以_______ 。
②A、C两点的平衡转化率相等的原因是_______ 。
③C点条件下假设压强为P2千帕,往容器内充入1molCO与2.5molH2发生反应。平衡时H2的体积分数是_______ 、Kp=_______ 。
(3)工业上也可以用CO2和H2合成甲醇: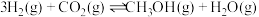
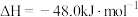 。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下。
。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下。
①若x=19.2,则α1=_______ 。
②下列说法正确的是_______ (填选项字母)。
A. 2c2<c3 B. z>2y,x=y C. p3<2p1 D. a1=a2
③若反应 在四种不同情况下的反应速率分别为:
在四种不同情况下的反应速率分别为:
A. B.
B. 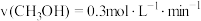
C.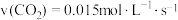 D.
D. 
该反应进行由慢到快的顺序为_______ (填选项字母)。
(1)已知一定条件下,发生反应:
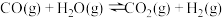
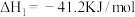
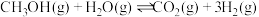
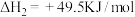
该条件下,水煤气(CO与H2的混合气体)转化成甲醇的热化学方程式是
(2)工业上使用水煤气转化成甲醇,CO的平衡转化率与温度、压强的关系如图所示:

①要使A点变到B点除增大压强外还可以
②A、C两点的平衡转化率相等的原因是
③C点条件下假设压强为P2千帕,往容器内充入1molCO与2.5molH2发生反应。平衡时H2的体积分数是
(3)工业上也可以用CO2和H2合成甲醇:
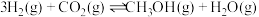
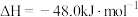 。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下。
。在T℃时,甲、乙、丙三个2L的恒容密闭容器中,按不同方式投入反应物,测得平衡时有关数据如下。| 容器 | 甲 | 乙 | 丙 | |
| 起始反应物投入量 | 3molH2(g) 1molCO2(g) | 1molCH3OH(g) 1molH2O(g) | 2molCH3OH(g) 2molH2O(g) | |
| 平衡数据 | 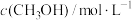 | c1 | c2 | c3 |
| 反应的能量变化/kJ | x | y | z | |
| 体系压强/Pa | p1 | p2 | p3 | |
| 反应物转化率 | a1 | a2 | a3 | |
②下列说法正确的是
A. 2c2<c3 B. z>2y,x=y C. p3<2p1 D. a1=a2
③若反应
 在四种不同情况下的反应速率分别为:
在四种不同情况下的反应速率分别为:A.
 B.
B. 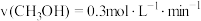
C.
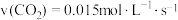 D.
D. 
该反应进行由慢到快的顺序为
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐1】I.25℃时,有关物质的电离平衡常数如下:
(1)将等物质的量浓度、等体积的 溶液与KOH溶液混合,离子方程式是
溶液与KOH溶液混合,离子方程式是_______ 。溶液显性_______ (填“酸性”、“碱性”或“中性”)。
(2)写出向 溶液中通入少量
溶液中通入少量 的离子方程式
的离子方程式_______ 。
(3)常温下0.1mol/L的 溶液,该溶液中各微粒浓度之间关系式错误的是_______
溶液,该溶液中各微粒浓度之间关系式错误的是_______
II.室温下,某一元弱酸HA的电离常数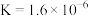 。向20.00mL浓度约为0.1
。向20.00mL浓度约为0.1 HA溶液中逐滴加入0.1000
HA溶液中逐滴加入0.1000 的标准KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
的标准KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:

(4)a点溶液中 电离出的
电离出的 为
为_______ mol/L。
(5)a、b、c、d四点中水的电离程度最大的是_______ 点。
| 化学式 |  |  |  | HClO |  |
| 电离平衡常数 | 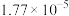 |  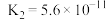 |  |  |   |
 溶液与KOH溶液混合,离子方程式是
溶液与KOH溶液混合,离子方程式是(2)写出向
 溶液中通入少量
溶液中通入少量 的离子方程式
的离子方程式(3)常温下0.1mol/L的
 溶液,该溶液中各微粒浓度之间关系式错误的是_______
溶液,该溶液中各微粒浓度之间关系式错误的是_______A.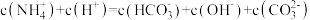 |
B. |
C.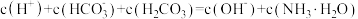 |
D. |
II.室温下,某一元弱酸HA的电离常数
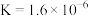 。向20.00mL浓度约为0.1
。向20.00mL浓度约为0.1 HA溶液中逐滴加入0.1000
HA溶液中逐滴加入0.1000 的标准KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
的标准KOH溶液,其pH变化曲线如图所示(忽略温度变化)。请回答下列有关问题:
(4)a点溶液中
 电离出的
电离出的 为
为(5)a、b、c、d四点中水的电离程度最大的是
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
解题方法
【推荐2】已知在25℃时,醋酸、碳酸和亚硫酸的电离平衡常数如下表所示:
(1)根据上表,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3_____ Na2SO3。(填“>” “<”或 “=”,下同)。
(2)向0.1 mol∙L−1的CH3COONa溶液中加入少量下列物质,其水解程度增大的是______。
(3)已知常温下NH3∙H2O的电离常数 ,则常温下CH3COONH4溶液的pH
,则常温下CH3COONH4溶液的pH____ 7。
(4)将pH=4的 溶液加水稀释,图中的纵坐标可以是
溶液加水稀释,图中的纵坐标可以是_____ 。
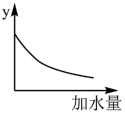
a.溶液的pH b.醋酸的电离平衡常数
c.溶液的导电能力 d.醋酸的电离程度
(5)NaHSO3是中学化学常见的物质。 在水溶液中存在如下两个平衡:
在水溶液中存在如下两个平衡:
 Ka2
Ka2
 Kh2 (水解平衡常数,表示水解程度)
Kh2 (水解平衡常数,表示水解程度)
已知25 ℃时,Ka2 > Kh2,则0.1 mol∙L−1 NaHSO3溶液:
①溶液呈__________ (填“酸性”“碱性”或“中性”);
②写出该溶液中的守恒式:电荷守恒:_________ ,质子守恒:__________ 。
| 酸 | 电离平衡常数 |
| 醋酸 |  |
| 碳酸 |  ; ; |
| 亚硫酸 | 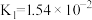 ; ;  |
(1)根据上表,在相同条件下,试比较Na2CO3、Na2SO3溶液的pH:Na2CO3
(2)向0.1 mol∙L−1的CH3COONa溶液中加入少量下列物质,其水解程度增大的是______。
| A.NaCl溶液 | B.Na2CO3固体 | C.NH4Cl溶液 | D.CH3COONa固体 |
 ,则常温下CH3COONH4溶液的pH
,则常温下CH3COONH4溶液的pH(4)将pH=4的
 溶液加水稀释,图中的纵坐标可以是
溶液加水稀释,图中的纵坐标可以是
a.溶液的pH b.醋酸的电离平衡常数
c.溶液的导电能力 d.醋酸的电离程度
(5)NaHSO3是中学化学常见的物质。
 在水溶液中存在如下两个平衡:
在水溶液中存在如下两个平衡: Ka2
Ka2 Kh2 (水解平衡常数,表示水解程度)
Kh2 (水解平衡常数,表示水解程度)已知25 ℃时,Ka2 > Kh2,则0.1 mol∙L−1 NaHSO3溶液:
①溶液呈
②写出该溶液中的守恒式:电荷守恒:
您最近一年使用:0次
解答题-原理综合题
|
适中
(0.65)
名校
解题方法
【推荐3】1.硫化氢(H2S)的转化是资源利用和环境保护的重要研究课题。
(1)H2S和CO混合加热可制得羰基硫(COS),羰基疏可作粮食熏蒸剂,能防止其些昆虫、线虫和真菌的危害。反应方程式为CO(g)+H2S(g)=COS(g)+H2(g)。
①羰基硫的电子式为__________ 。
②下列能说明碳与硫两元素非金属性相对强弱的是_______ (填字母代号)。
a.相同条件下水溶液的pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.S与H2的化合比C与H2的化合更容易
(2)H2S具有还原性,在酸性条件下,能与KMnO4反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式____________ 。
(3)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10mol·L-1 H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。
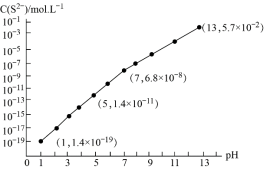
①pH=13时,溶液中的c(H2S)+c(HS-)=______ mol·L-1。
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH=_______ 时,Mn2+开始沉淀。[已知:Ksp(MnS)=2.8×10-13]。
(4)H2S的废气可用烧碱溶液吸收,将烧碱吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2--2e-=S↓ (n-1)S+S2- Sn2-写出电解时阴极的电极反应式:
Sn2-写出电解时阴极的电极反应式:______________________ 。

1.(5)一定温度下将NH4HS固体放入定容真空密闭容器中,可部分分解为硫化氢和氨气:NH4HS(s) H2S(g)+NH3(g)。
H2S(g)+NH3(g)。
①可以判断上述分解反应已经达到化学平衡状态的是_______ (填字母代号)
A.v(H2S)=v(NH3) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②当上述反应达平衡时:p(NH3)×p(H2S)=a(Pa2),则平衡时容器中的总压为_______ Pa( 用含a 的代数式表示).[p(NH3)、p(H2S)分别代表NH3、H2S的压强,Pa为压强的单位]
(1)H2S和CO混合加热可制得羰基硫(COS),羰基疏可作粮食熏蒸剂,能防止其些昆虫、线虫和真菌的危害。反应方程式为CO(g)+H2S(g)=COS(g)+H2(g)。
①羰基硫的电子式为
②下列能说明碳与硫两元素非金属性相对强弱的是
a.相同条件下水溶液的pH:Na2CO3>Na2SO4
b.酸性:H2SO3>H2CO3
c.S与H2的化合比C与H2的化合更容易
(2)H2S具有还原性,在酸性条件下,能与KMnO4反应生成S、MnSO4、K2SO4和H2O,写出该反应的化学方程式
(3)H2S气体溶于水形成的氢硫酸是一种二元弱酸,25℃时,在0.10mol·L-1 H2S溶液中,通入HCl气体或加入NaOH固体以调节溶液pH,溶液pH与c(S2-)关系如图所示(忽略溶液体积的变化、H2S的挥发)。

①pH=13时,溶液中的c(H2S)+c(HS-)=
②某溶液含0.020 mol·L-1Mn2+、0.10 mol·L-1H2S,当溶液pH=
(4)H2S的废气可用烧碱溶液吸收,将烧碱吸收H2S后的溶液加入到如图所示的电解池的阳极区进行电解。电解过程中阳极区发生如下反应:S2--2e-=S↓ (n-1)S+S2-
 Sn2-写出电解时阴极的电极反应式:
Sn2-写出电解时阴极的电极反应式:
1.(5)一定温度下将NH4HS固体放入定容真空密闭容器中,可部分分解为硫化氢和氨气:NH4HS(s)
 H2S(g)+NH3(g)。
H2S(g)+NH3(g)。①可以判断上述分解反应已经达到化学平衡状态的是
A.v(H2S)=v(NH3) B.密闭容器中总压强不变
C.密闭容器中混合气体的密度不变 D.密闭容器中氨气的体积分数不变
②当上述反应达平衡时:p(NH3)×p(H2S)=a(Pa2),则平衡时容器中的总压为
您最近一年使用:0次



