常温下,向浓度为0.1 mol·L-1、体积为V L的氨水中逐滴加入一定浓度的盐酸,用pH计测溶液的pH随盐酸的加入量而降低的滴定曲线,d点两种溶液恰好完全反应。据图信息回答:
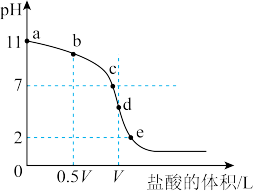
(1)该温度时NH3·H2O的电离常数K=________ 。
(2)比较b、c、d三点时的溶液中,由水电离出的c(OH-)大小顺序为________ 。

(1)该温度时NH3·H2O的电离常数K=
(2)比较b、c、d三点时的溶液中,由水电离出的c(OH-)大小顺序为
更新时间:2019-12-13 18:04:36
|
相似题推荐
填空题
|
适中
(0.65)
【推荐1】甲胺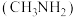 是一种一元弱碱。已知:
是一种一元弱碱。已知: 时,甲胺的电离常数
时,甲胺的电离常数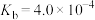 ,
, 。
。 时,向
时,向 溶液中滴加
溶液中滴加 的盐酸,混合溶液的
的盐酸,混合溶液的 、导电能力与加入盐酸体积
、导电能力与加入盐酸体积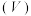 的关系如图所示。试回答下列问题:
的关系如图所示。试回答下列问题:

(1) 属于
属于_____ (填“强”或“弱”)电解质, 在水中的电离过程与
在水中的电离过程与 相似,写出
相似,写出 在水中的电离方程式:
在水中的电离方程式:_____ 。
(2) 时,
时, 点溶液呈
点溶液呈_____ (填“酸性”、“碱性”或“中性”)。
(3)已知:图中 点对应的溶液导电能力最强。则b、d、e三点对应的溶液中,水的电离程度由大到小的顺序为
点对应的溶液导电能力最强。则b、d、e三点对应的溶液中,水的电离程度由大到小的顺序为_____ , 的电离程度由大到小的顺序为
的电离程度由大到小的顺序为_____ 。
(4)图中
_____ (填“=”、“<”或“>”)20.00,b点对应的溶液中各离子浓度由大到小的顺序为_____ 。
(5) 点对应的溶液中
点对应的溶液中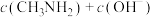
_____ (填“=”、“<”或“>”) 。
。
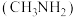 是一种一元弱碱。已知:
是一种一元弱碱。已知: 时,甲胺的电离常数
时,甲胺的电离常数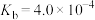 ,
, 。
。 时,向
时,向 溶液中滴加
溶液中滴加 的盐酸,混合溶液的
的盐酸,混合溶液的 、导电能力与加入盐酸体积
、导电能力与加入盐酸体积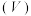 的关系如图所示。试回答下列问题:
的关系如图所示。试回答下列问题:
(1)
 属于
属于 在水中的电离过程与
在水中的电离过程与 相似,写出
相似,写出 在水中的电离方程式:
在水中的电离方程式:(2)
 时,
时, 点溶液呈
点溶液呈(3)已知:图中
 点对应的溶液导电能力最强。则b、d、e三点对应的溶液中,水的电离程度由大到小的顺序为
点对应的溶液导电能力最强。则b、d、e三点对应的溶液中,水的电离程度由大到小的顺序为 的电离程度由大到小的顺序为
的电离程度由大到小的顺序为(4)图中

(5)
 点对应的溶液中
点对应的溶液中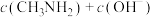
 。
。
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐2】现有常温下甲、乙、丙三种溶液,其中,甲为0.1mol·L-1的NaOH溶液,乙为0.1mol·L-1的H2SO4溶液,丙为0.1mol·L-1的CH3COOH溶液,试回答下列问题:
(1)甲溶液的pH=______ 。
(2)丙溶液中存在的电离平衡为______ 、______ (用电离方程式表示)。
(3)常温下,用水稀释0.1mol·L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是______ (填序号)。
①n(H+) ②c(OH-) ③ ④c(H+)·c(OH-)
④c(H+)·c(OH-)
(4)甲、乙、丙三种溶液中由水电离出的c(OH-)的由大到小的顺序为______ 。
(1)甲溶液的pH=
(2)丙溶液中存在的电离平衡为
(3)常温下,用水稀释0.1mol·L-1的CH3COOH溶液时,下列各量随水量的增加而增大的是
①n(H+) ②c(OH-) ③
 ④c(H+)·c(OH-)
④c(H+)·c(OH-)(4)甲、乙、丙三种溶液中由水电离出的c(OH-)的由大到小的顺序为
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐1】已知 时,三种酸的平衡常数分别为:
时,三种酸的平衡常数分别为: 的
的 ;
; 的
的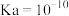 ;
; 的
的 ;
;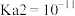 回答下列问题:
回答下列问题:
(1)将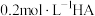 溶液与
溶液与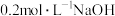 溶液等体积混合,测得混合溶液中
溶液等体积混合,测得混合溶液中 ,混合溶液中
,混合溶液中
_______  ;
;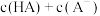
_____  (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。
(2)将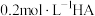 溶液与
溶液与 氨水等体积混合,反应后溶液呈中性。(1)和(2)反应后的溶液中,由水电离出的
氨水等体积混合,反应后溶液呈中性。(1)和(2)反应后的溶液中,由水电离出的 较大的是
较大的是________ (填(1)或(2))。
(3) 相同的
相同的 两溶液稀释后
两溶液稀释后 仍相同,加水量:
仍相同,加水量:
________  (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。
(4) 溶液与
溶液与 溶液混合,当溶液中
溶液混合,当溶液中 时,溶液的
时,溶液的
___________ 。
(5)同浓度的四种溶液:① ②
② ③
③ 溶液,
溶液, 由大到小的顺序是
由大到小的顺序是___________ 。
(6)写出 的
的 表达式
表达式___________ 。
 时,三种酸的平衡常数分别为:
时,三种酸的平衡常数分别为: 的
的 ;
; 的
的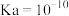 ;
; 的
的 ;
;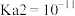 回答下列问题:
回答下列问题:(1)将
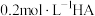 溶液与
溶液与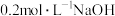 溶液等体积混合,测得混合溶液中
溶液等体积混合,测得混合溶液中 ,混合溶液中
,混合溶液中
 ;
;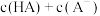
 (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。(2)将
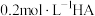 溶液与
溶液与 氨水等体积混合,反应后溶液呈中性。(1)和(2)反应后的溶液中,由水电离出的
氨水等体积混合,反应后溶液呈中性。(1)和(2)反应后的溶液中,由水电离出的 较大的是
较大的是(3)
 相同的
相同的 两溶液稀释后
两溶液稀释后 仍相同,加水量:
仍相同,加水量:
 (填“<”、“>”或“=”)。
(填“<”、“>”或“=”)。(4)
 溶液与
溶液与 溶液混合,当溶液中
溶液混合,当溶液中 时,溶液的
时,溶液的
(5)同浓度的四种溶液:①
 ②
② ③
③ 溶液,
溶液, 由大到小的顺序是
由大到小的顺序是(6)写出
 的
的 表达式
表达式
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】运用所学知识,解决下列问题。
(1)现欲测定100℃沸水的pH及酸碱性,溶液呈___________ (填“酸”、“碱”或“中”)性;若用pH计测定,则pH___________ (填“>”、“<”或“=”)7。
(2)25℃时欲使水电离产生的c(H+)=10-13mol·L-1,配制1L溶液,应向其中加入5.0mol·L-1的盐酸溶液___________ L。
(3)25℃时,将①H+、②Fe3+、③Al3+、④Na+、⑤HS-、⑥CH3COO-、⑦CO 、⑧NH
、⑧NH 分别加入H2O中,基本上不影响水的电离平衡的是
分别加入H2O中,基本上不影响水的电离平衡的是___________ (填入相应序号)。
(4)请在下列题目中填入“增大”、“减小”或“不变”。
①0.1mol·L-1CH3COOH溶液加水稀释,CH3COOH的电离度___________ 。
②常温下,用蒸馏水不断稀释醋酸,溶液中 的值
的值___________ 。
(1)现欲测定100℃沸水的pH及酸碱性,溶液呈
(2)25℃时欲使水电离产生的c(H+)=10-13mol·L-1,配制1L溶液,应向其中加入5.0mol·L-1的盐酸溶液
(3)25℃时,将①H+、②Fe3+、③Al3+、④Na+、⑤HS-、⑥CH3COO-、⑦CO
 、⑧NH
、⑧NH 分别加入H2O中,基本上不影响水的电离平衡的是
分别加入H2O中,基本上不影响水的电离平衡的是(4)请在下列题目中填入“增大”、“减小”或“不变”。
①0.1mol·L-1CH3COOH溶液加水稀释,CH3COOH的电离度
②常温下,用蒸馏水不断稀释醋酸,溶液中
 的值
的值
您最近一年使用:0次
填空题
|
适中
(0.65)
【推荐3】在氨水中存在下列电离平衡:NH3·H2O
 +OH-。
+OH-。
(1)下列情况能引起电离平衡正向移动的有___________ (填字母,下同)。
①加NH4Cl固体;②加NaOH溶液;③通入HCl;④加CH3COOH溶液;⑤加水;⑥加热至沸腾
(2)向含有酚酞的0.1 mol·L-1氨水中加入少量的NH4Cl晶体,则溶液颜色___________ 。
a.变蓝色 b.变深 c.变浅 d.不变
(3)向0.1 mol·L-1醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强度(I)随加入氨水的体积(V)变化的曲线关系是下图中的___________。

 +OH-。
+OH-。(1)下列情况能引起电离平衡正向移动的有
①加NH4Cl固体;②加NaOH溶液;③通入HCl;④加CH3COOH溶液;⑤加水;⑥加热至沸腾
(2)向含有酚酞的0.1 mol·L-1氨水中加入少量的NH4Cl晶体,则溶液颜色
a.变蓝色 b.变深 c.变浅 d.不变
(3)向0.1 mol·L-1醋酸溶液中逐滴加入氨水至过量时,溶液的导电能力将发生相应的变化,其电流强度(I)随加入氨水的体积(V)变化的曲线关系是下图中的___________。
A.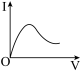 | B. | C.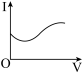 | D. |
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】常温下,将一元酸HA的溶液和KOH溶液等体积混合(忽略体积变化),实验数据如下表:
(1)HA为___________ (填“强酸”、“弱酸”或“无法确定”)
(2)x___________ 0.2(填:“<”、“=”、“>”)
(3)实验②反应后的溶液中离子浓度由大到小的顺序为___________
(4)实验①反应后的溶液中c(K+)___________ c(A-)+c(HA) (填:“<”、“=”、“>”)
(5)0.2 mol∙L−1的HA和0.1 mol∙L−1的KOH等体积混合充分反应后所得的溶液中c(HA)___________ c(A-) (填:“<”、“=”、“>”)
| 实验编号 | 起始浓度/ mol∙L−1 | 反应后溶液的pH | |
| c(HA) | c(KOH) | ||
| ① | 0.1 | 0.1 | 9 |
| ② | x | 0.2 | 7 |
(1)HA为
(2)x
(3)实验②反应后的溶液中离子浓度由大到小的顺序为
(4)实验①反应后的溶液中c(K+)
(5)0.2 mol∙L−1的HA和0.1 mol∙L−1的KOH等体积混合充分反应后所得的溶液中c(HA)
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】回答下列问题。
(1)在48mL0.1mol/L HNO3溶液中加入12mL0.4mol/LKOH溶液,所得溶液呈___________ (填酸性、碱性、中性)
(2)25℃时,a mol·L-1CH3COOH溶液的pH=b,用含a和b的代数式表示CH3COOH的电离平衡常数Ka=___________ (精确计算式)。
(3)硒酸(H2SeO4)在水溶液中的电离如下:H2SeO4=H++ HSeO ,HSeO
,HSeO
 H++SeO
H++SeO ,Ka=10×10-2 (25℃)。
,Ka=10×10-2 (25℃)。
①向H2SeO4溶液中滴加少量氢氧化钠稀溶液,该反应的离子方程式为___________ 。
②已知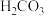 的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11,则KHCO3和KHSeO4两溶液混合反应的离子方程式为
的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11,则KHCO3和KHSeO4两溶液混合反应的离子方程式为___________ 。
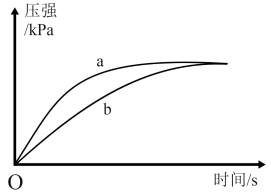
(4)已知25℃时,Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13,。在该温度下向两个锥形瓶中各加入0.5g NaHCO3粉末,塞紧橡胶塞,然后用注射器分别注入2mL2mol/LCH3COOH溶液和2mL2mol/LHSCN溶液,测得锥形瓶内气体的压强随时间的变化如图所示,则曲线___________ 表示HSCN溶液(填a或b)。
(1)在48mL0.1mol/L HNO3溶液中加入12mL0.4mol/LKOH溶液,所得溶液呈
(2)25℃时,a mol·L-1CH3COOH溶液的pH=b,用含a和b的代数式表示CH3COOH的电离平衡常数Ka=
(3)硒酸(H2SeO4)在水溶液中的电离如下:H2SeO4=H++ HSeO
 ,HSeO
,HSeO
 H++SeO
H++SeO ,Ka=10×10-2 (25℃)。
,Ka=10×10-2 (25℃)。①向H2SeO4溶液中滴加少量氢氧化钠稀溶液,该反应的离子方程式为
②已知
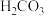 的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11,则KHCO3和KHSeO4两溶液混合反应的离子方程式为
的电离平衡常数Ka1=4.4×10-7,Ka2=4.7×10-11,则KHCO3和KHSeO4两溶液混合反应的离子方程式为(4)已知25℃时,Ka(CH3COOH)=1.8×10-5,Ka(HSCN)=0.13,。在该温度下向两个锥形瓶中各加入0.5g NaHCO3粉末,塞紧橡胶塞,然后用注射器分别注入2mL2mol/LCH3COOH溶液和2mL2mol/LHSCN溶液,测得锥形瓶内气体的压强随时间的变化如图所示,则曲线

您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】研究电解质在水溶液中的离子反应与平衡有重要的意义。
(1)25℃时对氨水进行如下操作,请填写下列空白。
①若向氨水中加入少量硫酸铵固体,则溶液中 将
将__________ (填“增大”“减小”或“不变”)。
②若向氨水中加入稀盐酸,使氨水恰好被中 和,则此时溶液显___________ (填“酸性”“碱性”或“中性”),用离子方程式表示其原因_________________ ,此溶液中离子的浓度大小顺序为___________
③在浓度为 的氨水中加入等体积
的氨水中加入等体积 的
的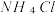 溶液,已知
溶液,已知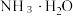 的电离常数为
的电离常数为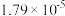 ,此时混合溶液显
,此时混合溶液显___________ (填“酸性”“碱性”或“中性”),此溶液中离子的浓度大小顺序为 ______
(2)常温下,几种弱酸的电离平衡常数如下表所示,回答下列问题:
①上述四种酸酸性由强到弱的顺序为___________ ;
②将少量的CO2通入NaClO溶液中,反应的离子方程式:___________ 。
(1)25℃时对氨水进行如下操作,请填写下列空白。
①若向氨水中加入少量硫酸铵固体,则溶液中
 将
将②若向氨水中加入稀盐酸,使氨水恰好被
③在浓度为
 的氨水中加入等体积
的氨水中加入等体积 的
的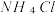 溶液,已知
溶液,已知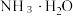 的电离常数为
的电离常数为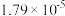 ,此时混合溶液显
,此时混合溶液显(2)常温下,几种弱酸的电离平衡常数如下表所示,回答下列问题:
| 化学式 | HCOOH | H2CO₃ | HCN | HClO |
| 电离平衡常数 | K=1.8×10⁻⁴ | K₁=4.3×10⁻⁷;K2=5.6×10⁻¹¹ | K=4.9×10⁻¹⁰ | K=4.7×10⁻⁸ |
②将少量的CO2通入NaClO溶液中,反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐1】已知氢硫酸是一种二元弱酸,请回答以下问题:
(1)已知 0.1mol/L NaHS 溶液显碱性,则c(S2-)___ c(H2S)(填“>”“<”或“=”)。
(2)常温下,向 0.2mol/L的 H2S溶液中逐滴滴入 0.2mol/L NaOH 溶液至中性,此时溶液中以下所示关系不正确的是___ (填字母)。
(3)已知常温下,CaS饱和溶液中存在平衡CaS(s) ⇌Ca2+(aq)+S2-(aq) △H>0。
①温度升高时,KSP(CaS ) =___ (填“增大”“减少”或“不变”,下同)。
②滴加少量浓盐酸时,c(Ca2+ )___ ,原因是___ (用文字和离子方程式说明)。
③若向CaS 饱和溶液中加入Cu(NO3)2 溶液中,生成一种黑色固体物质,写出该过程中反应的离子方程式:___ 。
(1)已知 0.1mol/L NaHS 溶液显碱性,则c(S2-)
(2)常温下,向 0.2mol/L的 H2S溶液中逐滴滴入 0.2mol/L NaOH 溶液至中性,此时溶液中以下所示关系不正确的是
| A.c(H+)·c(OH-)=1×10-14 |
| B.c(Na+)=c(HS-)+2c(S2-) |
| C.c(Na+)> c(HS-)+c(S2-)+ c(H2S) |
| D.c(H2S)> c(S2-) |
①温度升高时,KSP(CaS ) =
②滴加少量浓盐酸时,c(Ca2+ )
③若向CaS 饱和溶液中加入Cu(NO3)2 溶液中,生成一种黑色固体物质,写出该过程中反应的离子方程式:
您最近一年使用:0次
填空题
|
适中
(0.65)
名校
【推荐2】描述弱电解质电离情况可以用电离平衡常数表示,表1是常温下几种弱酸的电离平衡常数(Ka)和弱碱的电离平衡常数(Kb),表2是常温下几种难(微)溶物的溶度积常数(Ksp)。
表1
表2
请回答下列问题:
(1)表1所给的四种酸中,酸性最弱的是_____ (用化学式表示)。下列能使醋酸溶液中CH3COOH的电离程度增大,而电离平衡常数不变的操作是___ (填字母序号)。
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈_____ (选填“酸性”、“中性”或“碱性”),该溶液中存在的各离子浓度大小关系为_____ 。
(3)物质的量之比为1:1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子浓度从大到小的顺序为_____ 。
(4)工业中常将BaSO4转化为BaCO3后,再将其制成可溶性的钡盐(如BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.01mol•L﹣1,则溶液中CO32-物质的量浓度最少应为_____ 。
表1
| 酸或碱 | 电离平衡常数(Ka或Kb) |
| CH3COOH | 1.8×10﹣5 |
| HNO2 | 4.6×10﹣4 |
| HCN | 5×10﹣10 |
| HClO | 3×10﹣8 |
| NH3•H2O | 1.8×10﹣5 |
表2
| 难(微)溶物 | 溶度积常数(Ksp) |
| BaSO4 | 1×10﹣10 |
| BaCO3 | 2.6×10﹣9 |
| CaSO4 | 7×10﹣5 |
| CaCO3 | 5×10﹣9 |
请回答下列问题:
(1)表1所给的四种酸中,酸性最弱的是
A.升高温度 B.加水稀释
C.加少量的CH3COONa固体 D.加少量冰醋酸
(2)CH3COONH4的水溶液呈
(3)物质的量之比为1:1的NaCN和HCN的混合溶液,其pH>7,该溶液中离子浓度从大到小的顺序为
(4)工业中常将BaSO4转化为BaCO3后,再将其制成可溶性的钡盐(如BaCl2)。具体做法是用饱和的纯碱溶液浸泡BaSO4粉末,并不断补充纯碱,最后BaSO4转化为BaCO3。现有足量BaSO4悬浊液,在该悬浊液中加纯碱粉末并不断搅拌,为使SO42-物质的量浓度不小于0.01mol•L﹣1,则溶液中CO32-物质的量浓度最少应为
您最近一年使用:0次
填空题
|
适中
(0.65)
解题方法
【推荐3】现有以下浓度均为0.1mol·L-1的溶液:①KNO3溶液②CH3COONa溶液③NH4Cl溶液④NaOH溶液⑤氨水⑥CH3COOH溶液⑦盐酸⑧NaHCO3溶液⑨NaHC2O4溶液;已知常温下相关电离平衡常数如表:
回答下列有关小题:
(1)写出NaHCO3的电离方程式___ ;列出NH 的水解平衡常数表达式Kh(NH
的水解平衡常数表达式Kh(NH )=
)=___ ,计算常温下Kh(NH )=
)=___ 。
(2)②中各离子浓度由大到小的顺序为___ 。
(3)常温下:若将④和⑥混合,并使混合后溶液pH=7,则所需体积V④___ V⑥(填“>”“<”或“=”);若将④和⑦混合,并使混合后溶液pH=12,则V④:V⑦=__ ;将④和⑦等体积混合得w溶液,⑤和⑥等体积混合得Z溶液,混合后溶液pH值W___ Z(填“>”、“<”或“=”,下同);
(4)⑧和⑨混合如果能反应,写出离子反应方程式___ ,如果不能反应,则该小题不填。
| 弱电解质 | CH3COOH | NH3•H2O | H2CO3 | H2C2O4 |
| Ka或Kb | 1.8×10-5 | 1.8×10-5 | Ka1=4.3×10-7 | Ka1=5.6×10-2 Ka2=5.0×10-5 |
(1)写出NaHCO3的电离方程式
 的水解平衡常数表达式Kh(NH
的水解平衡常数表达式Kh(NH )=
)= )=
)=(2)②中各离子浓度由大到小的顺序为
(3)常温下:若将④和⑥混合,并使混合后溶液pH=7,则所需体积V④
(4)⑧和⑨混合如果能反应,写出离子反应方程式
您最近一年使用:0次



