1 . 某学生用已知物质的量浓度的盐酸来测定未知物质的量浓度的NaOH溶液时,选择酚酞作指示剂。请填写下列空白:
(1)某学生的操作步骤如下:
A.移取20.00mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序___________ 。
→___________→___________→___________→A→F。
(2)滴定终点的判断方法:___________ 。
(3)滴定结束时,酸式滴定管中的液面如图所示,则读数为___________ mL。
(5)某学生根据三次实验分别记录有关数据如表:
请选用其中合理数据求出该氢氧化钠溶液物质的量浓度:c(NaOH)=___________ mol/L。(计算结果保留4位有效数字)
(6)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是___________(填字母)。
(1)某学生的操作步骤如下:
A.移取20.00mL待测溶液注入洁净的锥形瓶中,并加入2~3滴酚酞试液。
B.用标准溶液润洗滴定管2~3次。
C.调节滴定管旋塞使尖嘴充满溶液,把盛有标准溶液的酸式滴定管固定好。
D.取标准盐酸溶液注入酸式滴定管至零刻度以上2~3cm。
E.调节液面至零刻度(或以下),记下读数V1。
F.用标准溶液滴定至终点,记下滴定管液面的刻度V2。
请写出操作步骤的正确顺序
→___________→___________→___________→A→F。
(2)滴定终点的判断方法:
(3)滴定结束时,酸式滴定管中的液面如图所示,则读数为

A. | B.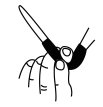 | C. | D. |
(5)某学生根据三次实验分别记录有关数据如表:
| 滴定次数 | 待测氢氧化钠溶液的体积/mL | 0.1000mol•L-1盐酸的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液体积 | ||
| 第一次 | 25.00 | 0.00 | 26.11 | 26.11 |
| 第二次 | 25.00 | 1.56 | 30.30 | 28.74 |
| 第三次 | 25.00 | 0.22 | 26.31 | 26.09 |
(6)由于错误操作,使得上述所测氢氧化钠溶液的浓度偏高的是___________(填字母)。
| A.中和滴定到达终点时俯视滴定管内液面读数 |
| B.碱式滴定管用蒸馏水洗净后立即取用25.00mL待测碱溶液注入锥形瓶进行滴定 |
| C.酸式滴定管用蒸馏水洗净后立即装标准溶液来滴定 |
| D.锥形瓶用待测液润洗 |
您最近一年使用:0次
解题方法
2 . 电解质的水溶液中存在电离平衡。
(1)NH3·H2O是常见的弱碱。
①NH3·H2O在水溶液中的电离方程式为_______ 。
②下列方法中,可以使氨水中NH3·H2O电离程度减小的是(填字母序号)________ 。
a.微热溶液 b.滴加浓盐酸 c.加水稀释 d.加入氯化铵晶体
(2)常温条件下,用0.1000mol/L NaOH溶液分别滴定体积均为 、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。_______ 。
②滴定醋酸的曲线是_______ (填“I”或“Ⅱ”),则V1______ V2(填“>”、 “<”“或“=”)。
(3)如图为盛放盐酸的滴定管中液面的位置。盐酸的体积读数:滴定后读数为_____ mL。 未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
①该滴定过程应选择______ (填“甲基橙”或“酚酞”)为指示剂,根据上述数据,可计算出该醋酸的浓度约为_____  。
。
②在上述实验中,下列操作会造成测定结果偏大的有______ 。(填字母序号)。
A.滴定前仰视读数,滴定后俯视读数
B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
C.滴定过程中,溶液刚出现变色,立即停止滴定
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
(1)NH3·H2O是常见的弱碱。
①NH3·H2O在水溶液中的电离方程式为
②下列方法中,可以使氨水中NH3·H2O电离程度减小的是(填字母序号)
a.微热溶液 b.滴加浓盐酸 c.加水稀释 d.加入氯化铵晶体
(2)常温条件下,用0.1000mol/L NaOH溶液分别滴定体积均为
 、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。
、浓度均为0.1000mol/L的盐酸和醋酸溶液,得到滴定过程中溶液pH随加入NaOH溶液体积而变化的两条滴定曲线。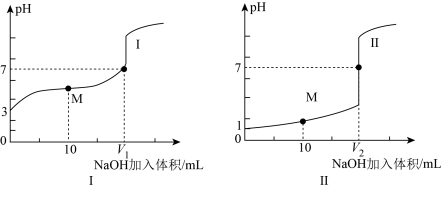
②滴定醋酸的曲线是
(3)如图为盛放盐酸的滴定管中液面的位置。盐酸的体积读数:滴定后读数为

 未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。
未知浓度的醋酸放入锥形瓶中,用0.1000mol/L NaOH标准溶液进行滴定。重复上述滴定操作2~3次,记录数据如下。| 实验编号 | NaOH溶液的浓度(mol·L-1) | 滴定完成时,NaOH溶液滴入的体积(mL) | 待测醋酸的体积(mL) |
| 1 | 0.1000 | 22.48 | 20.00 |
| 2 | 0.1000 | 25.72 | 20.00 |
| 3 | 0.1000 | 22.52 | 20.00 |
 。
。②在上述实验中,下列操作会造成测定结果偏大的有
A.滴定前仰视读数,滴定后俯视读数
B.碱式滴定管使用前,水洗后未用标准氢氧化钠溶液润洗
C.滴定过程中,溶液刚出现变色,立即停止滴定
D.锥形瓶水洗后未干燥
E.碱式滴定管尖嘴部分有气泡,滴定后消失
您最近一年使用:0次
3 . 25℃时,部分物质的电离平衡常数如表所示:
请回答下列问题:
(1)HCOOH、H2CO3、HCN的酸性由强到弱的顺序为___________ 。
(2)向Na2CO3溶液中加入足量HCN,反应的离子方程式为___________ 。
(3)写出HCOONa溶液中的电荷守恒式___________ 。
(4)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.00mol/L的NaOH标准溶液滴定:
①用NaOH固体配置100mL,1.00mol/L的NaOH溶液,需要用到的仪器除托盘天平,药匙,烧杯,玻璃棒,胶头滴管,还必须要___________ 。
②实验过程中,将25.00mLHCOOH放入锥形瓶,滴入酚酞2-3滴;NaOH溶液应装___________ 入(填“酸式滴定管”或“碱式滴定管”);滴定过程中,眼睛应注视___________ 。
③连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为___________ mL。
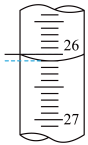
④某学生根据3次实验分别记录有关数据如下表:
依据上表数据计算该HCOOH溶液的物质的量浓度为___________ mol/L(计算结果保留到小数点后两位)。
⑤下列操作中可能使所测HCOOH溶液的浓度数值偏低的是___________ (填字母)。
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
| 化学式 | HCOOH | H2CO3 | HCN |
| 电离平衡常数 | 1.5×10-4 | Ka1=4.2×10-7 Ka2=4.9×10-11 | 3.0×10-8 |
(1)HCOOH、H2CO3、HCN的酸性由强到弱的顺序为
(2)向Na2CO3溶液中加入足量HCN,反应的离子方程式为
(3)写出HCOONa溶液中的电荷守恒式
(4)为了测定一元酸HCOOH溶液的浓度,现取25.00mLHCOOH溶液,用1.00mol/L的NaOH标准溶液滴定:
①用NaOH固体配置100mL,1.00mol/L的NaOH溶液,需要用到的仪器除托盘天平,药匙,烧杯,玻璃棒,胶头滴管,还必须要
②实验过程中,将25.00mLHCOOH放入锥形瓶,滴入酚酞2-3滴;NaOH溶液应装
③连续滴定3次,若其中一次滴定结束时,滴定管中的液面如图所示,则终点读数为

④某学生根据3次实验分别记录有关数据如下表:
| 实验序号 | 待测HCOOH溶液体积/mL | 1.00mol/LNaOH的体积/mL | ||
| 滴定前刻度 | 滴定后刻度 | 溶液的体积 | ||
| 1 | 25.00 | 0.00 | 12.49 | V1 |
| 2 | 25.00 | 0.56 | 14.56 | V2 |
| 3 | 25.00 | 0.22 | 12.73 | V3 |
⑤下列操作中可能使所测HCOOH溶液的浓度数值偏低的是
A.滴定前,用待测液润洗锥形瓶
B.一滴标准溶液附在锥形瓶壁上未洗下
C.选用甲基橙作指示剂
D.配置NaOH溶液时,称量NaOH固体速度过慢
E.读取NaOH溶液体积时,开始仰视读数,滴定结束时俯视读数
您最近一年使用:0次
名校
解题方法
4 . 滴定法是一种常见的定量实验分析方法,常见的有酸碱中和滴定法、氧化还原滴定法、沉淀滴定法等。常温下,用 的NaOH溶液滴定20.00mL
的NaOH溶液滴定20.00mL 醋酸
醋酸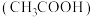 ,滴定曲线如图1所示。
,滴定曲线如图1所示。

1.在上述滴定过程中,不需要使用的玻璃仪器是 。
2.滴定过程中眼睛应注视_____ 。该实验使用的指示剂为_____ ,滴定终点的现象为_____ 。某次实验滴定终点时滴定管中液面位置如图2所示,则此时的读数为_____ mL。
3.如图1所示,c点的纵坐标为7,d点的横坐标为20.00mL,a、b、c、d四个点对应溶液中,_____ 点对应水的电离程度最大,c点溶液中,
_____  (填“>”“<”或“=”)
(填“>”“<”或“=”)
 的NaOH溶液滴定20.00mL
的NaOH溶液滴定20.00mL 醋酸
醋酸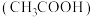 ,滴定曲线如图1所示。
,滴定曲线如图1所示。
1.在上述滴定过程中,不需要使用的玻璃仪器是 。
| A.移液管 | B.滴定管 | C.锥形瓶 | D.胶头滴管 |
3.如图1所示,c点的纵坐标为7,d点的横坐标为20.00mL,a、b、c、d四个点对应溶液中,

 (填“>”“<”或“=”)
(填“>”“<”或“=”)
您最近一年使用:0次
5 .  时,
时, 的
的 ,
, 。
。
(1)常温下, 加水稀释,稀释过程中,溶液的导电能力
加水稀释,稀释过程中,溶液的导电能力___________ (填“增强”或“减弱”);
(2) 溶液显酸性的原因是
溶液显酸性的原因是___________ 。
(3)利用草酸及草酸盐的性质可测定人体血液中钙离子的浓度。
实验流程:取血样 ,加适量的草酸铵[
,加适量的草酸铵[ ]溶液,析出草酸钙沉淀,将此沉淀洗涤后溶于强酸得草酸,再用硫酸酸化的
]溶液,析出草酸钙沉淀,将此沉淀洗涤后溶于强酸得草酸,再用硫酸酸化的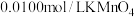 标准液平行滴定三次,平均消耗
标准液平行滴定三次,平均消耗 溶液
溶液 。即可计算出血液中钙离子的浓度。
。即可计算出血液中钙离子的浓度。
① 标准溶液应用滴定管
标准溶液应用滴定管___________ (填“酸式”或“碱式”)盛装,注入 ,标准溶液之前,滴定管需要
,标准溶液之前,滴定管需要___________ 、洗涤和润洗。
②请写出滴定过程中发生的离子反应方程式:___________ 。
③判断达到滴定终点的依据是___________ 。血液样品中 浓度为
浓度为___________  (保留2位有效数字)。
(保留2位有效数字)。
④下列操作会使测得的血液中钙离子的浓度偏高的是___________ 。
A.滴定前因装液较多,测量同学坐着没有起身,抬头读数
B.滴定过程中用蒸馏水将锥形瓶内壁上黏附的溶液冲下
C.若未等滴定管液面稳定就读数
D.酸式滴定管在滴定前有气泡,滴定后气泡消失
 时,
时, 的
的 ,
, 。
。(1)常温下,
 加水稀释,稀释过程中,溶液的导电能力
加水稀释,稀释过程中,溶液的导电能力(2)
 溶液显酸性的原因是
溶液显酸性的原因是(3)利用草酸及草酸盐的性质可测定人体血液中钙离子的浓度。
实验流程:取血样
 ,加适量的草酸铵[
,加适量的草酸铵[ ]溶液,析出草酸钙沉淀,将此沉淀洗涤后溶于强酸得草酸,再用硫酸酸化的
]溶液,析出草酸钙沉淀,将此沉淀洗涤后溶于强酸得草酸,再用硫酸酸化的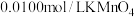 标准液平行滴定三次,平均消耗
标准液平行滴定三次,平均消耗 溶液
溶液 。即可计算出血液中钙离子的浓度。
。即可计算出血液中钙离子的浓度。①
 标准溶液应用滴定管
标准溶液应用滴定管 ,标准溶液之前,滴定管需要
,标准溶液之前,滴定管需要②请写出滴定过程中发生的离子反应方程式:
③判断达到滴定终点的依据是
 浓度为
浓度为 (保留2位有效数字)。
(保留2位有效数字)。④下列操作会使测得的血液中钙离子的浓度偏高的是
A.滴定前因装液较多,测量同学坐着没有起身,抬头读数
B.滴定过程中用蒸馏水将锥形瓶内壁上黏附的溶液冲下
C.若未等滴定管液面稳定就读数
D.酸式滴定管在滴定前有气泡,滴定后气泡消失
您最近一年使用:0次
解题方法
6 . 回答下列问题:
(1)化学中,酸的电离平衡常数(Ka)是评估酸性强弱的重要依据。几种酸的电离常数(25℃)如下表所示。
①写出CH3COOH的电离方程式:__________ 。
②写出H2S的Ka1的表达式:___________ 。
③常温下,浓度相同的三种溶液NaF、Na2CO3、CH3COONa,pH由大到小的顺序是_________ 。
④将过量H2S通入Na2CO3溶液,反应的离子方程式是_________ 。
(2)室温下,用0.100mol/L盐酸溶液滴定20.00mL0.100mol/L的氨水溶液,滴定曲线如图所示(忽略溶液体积的变化,①②填“>”、“<”或“=”)。

①a点所示的溶液中c(NH3·H2O)_________ c(Cl-)。
②b点所示的溶液中c(C1-)_______ c( )。
)。
③室温下pH=11的氨水与pH≈5的NH4Cl溶液中,由水电离出的c(H)之比为_______ 。
(1)化学中,酸的电离平衡常数(Ka)是评估酸性强弱的重要依据。几种酸的电离常数(25℃)如下表所示。
| 弱酸 | HF | CH3COOH | H2CO3 | H2S |
| 电离平衡常数 | Ka=7.2×10-4 | Ka=1.75×10-5 | Ka1=4.30×10-7 Ka2=5.61×10-11 | Ka1=9.1×10-8 Ka2=1.1×10-12 |
②写出H2S的Ka1的表达式:
③常温下,浓度相同的三种溶液NaF、Na2CO3、CH3COONa,pH由大到小的顺序是
④将过量H2S通入Na2CO3溶液,反应的离子方程式是
(2)室温下,用0.100mol/L盐酸溶液滴定20.00mL0.100mol/L的氨水溶液,滴定曲线如图所示(忽略溶液体积的变化,①②填“>”、“<”或“=”)。

①a点所示的溶液中c(NH3·H2O)
②b点所示的溶液中c(C1-)
 )。
)。③室温下pH=11的氨水与pH≈5的NH4Cl溶液中,由水电离出的c(H)之比为
您最近一年使用:0次
名校
解题方法
7 . 回答下列问题:
(1)下列溶液中, 由大到小的顺序是___________。
由大到小的顺序是___________。
(2)室温时,向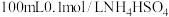 溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
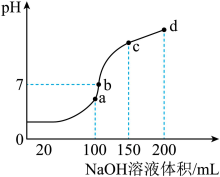
Ⅰ.试分析图中a、b、c、d四个点,水的电离程度最大的是___________ ;
Ⅱ.在b点,溶液中各离子浓度由大到小的排列顺序是___________ ;
Ⅲ.在cd段发生反应的离子方程式为___________ 。
(3)在标准状况下充满HCl的烧瓶做完喷泉实验后,得到稀盐酸,用标准碳酸钠溶液进行滴定。
Ⅰ.用标准 溶液滴定这种盐酸时,若用甲基橙作指示剂,达到滴定终点时,锥形瓶内溶液颜色变化为
溶液滴定这种盐酸时,若用甲基橙作指示剂,达到滴定终点时,锥形瓶内溶液颜色变化为___________ 。
Ⅱ.现配制三种浓度的标准 溶液,你认为最合适的是下列第
溶液,你认为最合适的是下列第___________ (填序号)种。
① ②
② ③
③
Ⅲ.若采用上述合适浓度的标准 溶液滴定,滴定时实验数据列表如下:
溶液滴定,滴定时实验数据列表如下:
则这种待测稀盐酸的物质的量浓度
___________ (用包含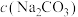 符号的算式表示)。
符号的算式表示)。
Ⅳ.下列实验中,由于错误操作导致所测出的盐酸浓度一定偏低的是___________ 。
A.滴定时,左手控制碱式滴定管的小球,右手握持锥形瓶,眼睛注视滴定管中的液面变化
B.酸式滴定管未用待测盐酸润洗
C.滴定时盛待测液的锥形瓶中有少量水
D.达到滴定终点时,俯视读数
(1)下列溶液中,
 由大到小的顺序是___________。
由大到小的顺序是___________。A.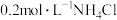 溶液 溶液 | B.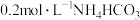 溶液 溶液 |
C.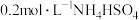 溶液 溶液 | D. 溶液 溶液 |
(2)室温时,向
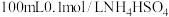 溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
溶液中滴加0.1mol/LNaOH溶液,得到溶液pH与NaOH溶液体积的关系曲线如图所示:
Ⅰ.试分析图中a、b、c、d四个点,水的电离程度最大的是
Ⅱ.在b点,溶液中各离子浓度由大到小的排列顺序是
Ⅲ.在cd段发生反应的离子方程式为
(3)在标准状况下充满HCl的烧瓶做完喷泉实验后,得到稀盐酸,用标准碳酸钠溶液进行滴定。
Ⅰ.用标准
 溶液滴定这种盐酸时,若用甲基橙作指示剂,达到滴定终点时,锥形瓶内溶液颜色变化为
溶液滴定这种盐酸时,若用甲基橙作指示剂,达到滴定终点时,锥形瓶内溶液颜色变化为Ⅱ.现配制三种浓度的标准
 溶液,你认为最合适的是下列第
溶液,你认为最合适的是下列第①
 ②
② ③
③
Ⅲ.若采用上述合适浓度的标准
 溶液滴定,滴定时实验数据列表如下:
溶液滴定,滴定时实验数据列表如下:| 试验编号 | 待测盐酸体积(mL) | 滴入碳酸钠溶液体积(mL) |
| 1 | 20.00 | 18.50 |
| 2 | 20.00 | 16.95 |
| 3 | 20.00 | 17.05 |

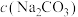 符号的算式表示)。
符号的算式表示)。Ⅳ.下列实验中,由于错误操作导致所测出的盐酸浓度一定偏低的是
A.滴定时,左手控制碱式滴定管的小球,右手握持锥形瓶,眼睛注视滴定管中的液面变化
B.酸式滴定管未用待测盐酸润洗
C.滴定时盛待测液的锥形瓶中有少量水
D.达到滴定终点时,俯视读数
您最近一年使用:0次
解题方法
8 . Ⅰ.温度t℃时,某NaOH稀溶液中c(H+)=10-amol·L-1,c(OH-)=10-b mol·L-1,已知a+b=12,请回答下列问题:
(1)该NaOH溶液中NaOH的物质的量浓度为__________ ,该NaOH溶液中由水电离出的c(OH-)为__________ 。
(2)给该NaOH溶液加热时,pH________ (填“变大”、“变小”或“不变”)。
Ⅱ.现用盐酸标准溶液来测定NaOH溶液的浓度。有以下实验操作:
①向溶液中加入1~2滴指示剂
②取20.00 mL标准溶液放入锥形瓶中
③用氢氧化钠溶液滴定至终点
④重复以上操作
⑤配制250 mL盐酸标准溶液
⑥根据实验数据计算氢氧化钠的物质的量浓度
(3)实验过程中正确的操作顺序是______ (填序号),上述操作②中使用的仪器除锥形瓶外,还需要______ ,用______ 作指示剂。
(4)滴定并记录V(NaOH)的初、终读数。数据记录如表所示:
某同学在处理数据过程中计算得到平均消耗NaOH溶液的体积V(NaOH)=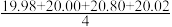 mL=20.20 mL。他的计算
mL=20.20 mL。他的计算______ (填“合理”或“不合理”),理由是____________ 。通过仪器测得第4次滴定过程中溶液pH随加入氢氧化钠溶液体积的变化曲线如图所示,则a______ (填“>”“<”或“=”)20.02。
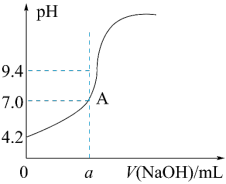
(1)该NaOH溶液中NaOH的物质的量浓度为
(2)给该NaOH溶液加热时,pH
Ⅱ.现用盐酸标准溶液来测定NaOH溶液的浓度。有以下实验操作:
①向溶液中加入1~2滴指示剂
②取20.00 mL标准溶液放入锥形瓶中
③用氢氧化钠溶液滴定至终点
④重复以上操作
⑤配制250 mL盐酸标准溶液
⑥根据实验数据计算氢氧化钠的物质的量浓度
(3)实验过程中正确的操作顺序是
(4)滴定并记录V(NaOH)的初、终读数。数据记录如表所示:
| 滴定次数 | 1 | 2 | 3 | 4 |
| V(HCl)/mL | 20.00 | 20.00 | 20.00 | 20.00 |
| V(NaOH)/mL(初读数) | 0.10 | 0.30 | 0.00 | 0.20 |
| V(NaOH)/mL(终读数) | 20.08 | 20.30 | 20.80 | 20.22 |
| V(NaOH)/mL(消耗) | 19.98 | 20.00 | 20.80 | 20.02 |
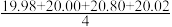 mL=20.20 mL。他的计算
mL=20.20 mL。他的计算
您最近一年使用:0次
9 . 酸碱滴定和氧化还原滴定是常见的两种滴定方法。
I.氧化还原滴定:化学兴趣小组欲准确测定某市售双氧水中 的含量:取双氧水
的含量:取双氧水 至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定,其反应的离子方程式为
至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定,其反应的离子方程式为 。
。
(1)滴定时,将高锰酸钾标准溶液注入___________ (填“酸”或“碱”)式滴定管中。
(2)滴定到达终点的现象是___________ 。
(3)根据实验测得,消耗 溶液,那么
溶液,那么 的浓度为
的浓度为___________ 。
Ⅱ.酸碱中和滴定:常温下,用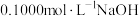 溶液分别滴定
溶液分别滴定 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:

(4)滴定盐酸的曲线是图___________ (填“1”或“2”)。
(5)滴定前 的电离度为
的电离度为___________ 。[电离度
 ×100%]
×100%]
(6)达到B、D状态时,反应消耗的 溶液的体积图1
溶液的体积图1___________ (填“>”“<”或“=”)图2;当 时,解释E点为碱性的原因
时,解释E点为碱性的原因___________ 。(离子方程式)
I.氧化还原滴定:化学兴趣小组欲准确测定某市售双氧水中
 的含量:取双氧水
的含量:取双氧水 至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定,其反应的离子方程式为
至锥形瓶中,加入稀硫酸酸化,用蒸馏水稀释。用一定浓度的高锰酸钾标准液滴定,其反应的离子方程式为 。
。(1)滴定时,将高锰酸钾标准溶液注入
(2)滴定到达终点的现象是
(3)根据实验测得,消耗
 溶液,那么
溶液,那么 的浓度为
的浓度为Ⅱ.酸碱中和滴定:常温下,用
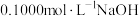 溶液分别滴定
溶液分别滴定 等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
等浓度的盐酸和醋酸溶液,得到两条滴定曲线,如图所示:
(4)滴定盐酸的曲线是图
(5)滴定前
 的电离度为
的电离度为
 ×100%]
×100%](6)达到B、D状态时,反应消耗的
 溶液的体积图1
溶液的体积图1 时,解释E点为碱性的原因
时,解释E点为碱性的原因
您最近一年使用:0次
10 . 回答下列问题。
(1)醋酸是常见的弱酸。
 醋酸在水溶液中的电离方程式为
醋酸在水溶液中的电离方程式为 ___________ 。
 下列方法中,可以使醋酸稀溶液中
下列方法中,可以使醋酸稀溶液中 电离程度增大的是
电离程度增大的是___________  填字母序号
填字母序号 。
。
a.滴加少量浓盐酸 b.微热溶液 c.加水稀释 d.加入少量醋酸钠晶体
(2)用 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。

 滴定醋酸的曲线是
滴定醋酸的曲线是___________  填“
填“ ”或“Ⅱ”
”或“Ⅱ” 。
。
 滴定开始前,三种溶液中由水电离出的
滴定开始前,三种溶液中由水电离出的 最大的是
最大的是___________ 。
 上述用
上述用 的
的 溶液滴定
溶液滴定 的盐酸,下列操作不正确的是
的盐酸,下列操作不正确的是___________ 。
A.用标准 溶液润洗碱式滴定管后,再装入标准碱溶液
溶液润洗碱式滴定管后,再装入标准碱溶液
B.用待测酸溶液润洗锥形瓶后,再装入待测酸溶液
C.滴定时两眼应注视滴定管中液面的变化,以免滴定过量
D.读数时,视线应与滴定管凹液面的最低点保持水平
(1)醋酸是常见的弱酸。
 醋酸在水溶液中的电离方程式为
醋酸在水溶液中的电离方程式为  下列方法中,可以使醋酸稀溶液中
下列方法中,可以使醋酸稀溶液中 电离程度增大的是
电离程度增大的是 填字母序号
填字母序号 。
。a.滴加少量浓盐酸 b.微热溶液 c.加水稀释 d.加入少量醋酸钠晶体
(2)用
 溶液分别滴定体积均为
溶液分别滴定体积均为 、浓度均为
、浓度均为 的盐酸和醋酸溶液,得到滴定过程中溶液
的盐酸和醋酸溶液,得到滴定过程中溶液 随加入
随加入 溶液体积而变化的两条滴定曲线。
溶液体积而变化的两条滴定曲线。
 滴定醋酸的曲线是
滴定醋酸的曲线是 填“
填“ ”或“Ⅱ”
”或“Ⅱ” 。
。 滴定开始前,三种溶液中由水电离出的
滴定开始前,三种溶液中由水电离出的 最大的是
最大的是 上述用
上述用 的
的 溶液滴定
溶液滴定 的盐酸,下列操作不正确的是
的盐酸,下列操作不正确的是A.用标准
 溶液润洗碱式滴定管后,再装入标准碱溶液
溶液润洗碱式滴定管后,再装入标准碱溶液B.用待测酸溶液润洗锥形瓶后,再装入待测酸溶液
C.滴定时两眼应注视滴定管中液面的变化,以免滴定过量
D.读数时,视线应与滴定管凹液面的最低点保持水平
您最近一年使用:0次



