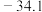名校
解题方法
1 . 2023年6月,科学家首次合成含铍-铍能的固态化合物,相关成果发表于《科学》杂质。该分子入选2023年最“炫”分子榜单,其结构如图所示,回答下列问题: 原子最外层电子的电子云轮廓图为
原子最外层电子的电子云轮廓图为_____ (填序号)。
A.球形 B.哑铃形
(2)下列电子排布式分别代表铍微粒,其中失去1个电子所需能量最多的是_____。
(3)“固态双铍化合物的化学式为_____ ,它不含_____ (填标号)。
A.极性键 B.非极性键 C.金属键 D. 键
键
(4)卤化铍的熔点如表所示:
① 中
中 原子的杂化方式为
原子的杂化方式为_____ ;
②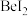
_____ (填“能”或“不能)溶于四氯化碳:
③ 、
、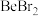 、
、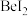 的熔点依次升高的原因是
的熔点依次升高的原因是_____ 。
(5) 易形成配离子
易形成配离子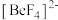 ,其中心阳离子的配位数为
,其中心阳离子的配位数为_____ ,配体是_____ (填化学符号),配离子的空间构型为_____ 。
(6)离子晶体中稳定配位多面体的理论半径比如表所示:
已知铍离子、氧离子的半径分别为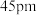 、
、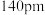 ,
, 的配位多面体是
的配位多面体是_____ 。
(7)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。这种氧化物的化学式为_____ ;设晶胞参数为 ,用
,用 表示阿伏加德罗参数的值,则
表示阿伏加德罗参数的值,则 晶体的密度为
晶体的密度为_____  (用含a和
(用含a和 的式子表示)。
的式子表示)。
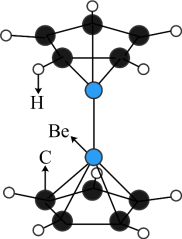
 原子最外层电子的电子云轮廓图为
原子最外层电子的电子云轮廓图为A.球形 B.哑铃形
(2)下列电子排布式分别代表铍微粒,其中失去1个电子所需能量最多的是_____。
A.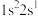 | B. | C.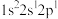 | D. |
(3)“固态双铍化合物的化学式为
A.极性键 B.非极性键 C.金属键 D.
 键
键(4)卤化铍的熔点如表所示:
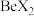 | 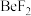 |  | 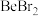 | 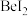 |
熔点/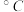 | 552 | 399 | 488 | 510 |
 中
中 原子的杂化方式为
原子的杂化方式为②
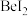
③
 、
、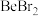 、
、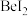 的熔点依次升高的原因是
的熔点依次升高的原因是(5)
 易形成配离子
易形成配离子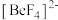 ,其中心阳离子的配位数为
,其中心阳离子的配位数为(6)离子晶体中稳定配位多面体的理论半径比如表所示:
| 配位多面体 | 配位数 | 半径比(r+/r-) |
| 平面三角形 | 3 | 0.15~0.225 |
| 四面体 | 4 | 0.225~0.414 |
| 八面体 | 6 | 0.414~0.732 |
| 立方体 | 8 | 0.732~1.000 |
| 立方八面体 | 12 | 1.000 |
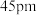 、
、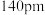 ,
, 的配位多面体是
的配位多面体是(7)Be的某种氧化物晶体是制备氟硼铍酸钾晶体的原料之一,其晶胞结构如图所示。这种氧化物的化学式为
 ,用
,用 表示阿伏加德罗参数的值,则
表示阿伏加德罗参数的值,则 晶体的密度为
晶体的密度为 (用含a和
(用含a和 的式子表示)。
的式子表示)。
您最近半年使用:0次
名校
解题方法
2 . 我国科学家研发的全球首套千吨级太阳能燃料合成项目被形象地称为“液态阳光”计划。该项目通过太阳能发电电解水制氢,再采用高选择性催化剂将二氧化碳加氢合成甲醇。回答下列问题:
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为_____ 。SiCl4可发生水解反应,机理如下: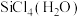 中Si采取的杂化类型为
中Si采取的杂化类型为_____ (填标号)。
(2)CO2分子中σ键和π键的比值_____ 。
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是_____ 。
(4)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2._____ 。
②设X的最简式的式量为 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为_____ nm(列出计算式, 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
(1)太阳能电池板主要材料为单晶硅或多晶硅。Si的价电子层的电子排布式为

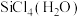 中Si采取的杂化类型为
中Si采取的杂化类型为(2)CO2分子中σ键和π键的比值
(3)甲醇的沸点(64.7℃)介于水(100℃)和甲硫醇(CH3SH,7.6℃)之间,其原因是
(4)我国科学家发展了一种理论计算方法,可利用材料的晶体结构数据预测其热电性能,该方法有助于加速新型热电材料的研发进程。化合物X是通过该方法筛选出的潜在热电材料之一,其晶胞结构如图1,沿x、y、z轴方向的投影均为图2.
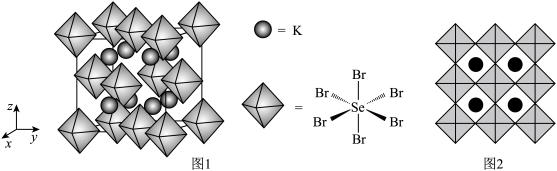
②设X的最简式的式量为
 ,晶体密度为
,晶体密度为 ,则X中相邻K之间的最短距离为
,则X中相邻K之间的最短距离为 为阿伏加德罗常数的值)。
为阿伏加德罗常数的值)。
您最近半年使用:0次
名校
解题方法
3 . 镓(Ga)用途非常广泛。
(1)GaAs的晶胞结构如图甲。将Mn掺杂到 的晶体中得到稀磁性半导体材料(图乙)。
的晶体中得到稀磁性半导体材料(图乙)。___________ 。
②GaAs晶胞中Ga和As原子之间最短距离为anm,且恰好为体对角线的 ,阿伏加德罗常数为NA,则该晶体的密度为
,阿伏加德罗常数为NA,则该晶体的密度为___________ g/cm3(列出表达式)。
③掺杂Mn之后,晶体中Mn、Ga、As的原子个数比为___________ (最简整数比)。
(2)GaN的制备:以Ga(CH3)3为原料,在一定条件下使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为___________ 。
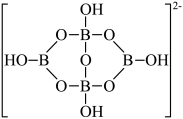
(3)与镓同主族的硼B具有缺电子性,B形成的[B4O5(OH)4]2-结构如图所示,则该离子存在的作用力有___________ (填选项),B原子的杂化方式为___________ 。
(1)GaAs的晶胞结构如图甲。将Mn掺杂到
 的晶体中得到稀磁性半导体材料(图乙)。
的晶体中得到稀磁性半导体材料(图乙)。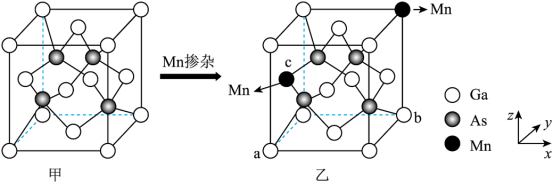
②GaAs晶胞中Ga和As原子之间最短距离为anm,且恰好为体对角线的
 ,阿伏加德罗常数为NA,则该晶体的密度为
,阿伏加德罗常数为NA,则该晶体的密度为③掺杂Mn之后,晶体中Mn、Ga、As的原子个数比为
(2)GaN的制备:以Ga(CH3)3为原料,在一定条件下使其与NH3发生系列反应得到GaN和另一种产物,该过程的化学方程式为
(3)与镓同主族的硼B具有缺电子性,B形成的[B4O5(OH)4]2-结构如图所示,则该离子存在的作用力有
您最近半年使用:0次
解题方法
4 . 硼及其化合物在科研、工业等方面有许多用途。
(1)基态B原子价层电子排布式是___________ 。
(2)六方氮化硼晶体也被称为“白石墨”,具有和石墨晶体相似的层状结构,如图所示。___________ 。
②分析六方氮化硼晶体层间是否存在化学键并说明依据:___________ 。
(3)氮化硼量子点(粒径大小为2~10nm)可用于检测金属离子,如Fe2+或Fe3+的检测原理如下图。___________ 。
②n=___________ (填数字)。
(4)NaBH4是一种重要的储氢材料,其晶胞结构由Ⅰ、Ⅱ两部分组成,如图所示。___________ 。
②已知阿伏加德罗常数为NA,该晶体的密度为___________ g·cm-3。(1nm=10-7cm)
(1)基态B原子价层电子排布式是
(2)六方氮化硼晶体也被称为“白石墨”,具有和石墨晶体相似的层状结构,如图所示。

②分析六方氮化硼晶体层间是否存在化学键并说明依据:
(3)氮化硼量子点(粒径大小为2~10nm)可用于检测金属离子,如Fe2+或Fe3+的检测原理如下图。

②n=
(4)NaBH4是一种重要的储氢材料,其晶胞结构由Ⅰ、Ⅱ两部分组成,如图所示。

②已知阿伏加德罗常数为NA,该晶体的密度为
您最近半年使用:0次
名校
解题方法
5 . 我国科学家合成了以 、
、 、
、 为核心元素的催化剂实现高效硝酸盐电还原为氨。催化剂晶体的典型晶胞结构如下图所示。下列说法正确的是
为核心元素的催化剂实现高效硝酸盐电还原为氨。催化剂晶体的典型晶胞结构如下图所示。下列说法正确的是
 、
、 、
、 为核心元素的催化剂实现高效硝酸盐电还原为氨。催化剂晶体的典型晶胞结构如下图所示。下列说法正确的是
为核心元素的催化剂实现高效硝酸盐电还原为氨。催化剂晶体的典型晶胞结构如下图所示。下列说法正确的是
A.基态 原子的价层电子排布式为 原子的价层电子排布式为 |
B.晶胞(a)中共有6个 原子 原子 |
C.晶体(b)的化学式为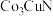 |
D.晶胞(a)中离 原子最近且等距的 原子最近且等距的 原子数目为8 原子数目为8 |
您最近半年使用:0次
名校
解题方法
6 . 锰(Mn)、钴(Co)、镍(Ni)等过渡金属元素化合物的应用研究是前沿科学之一,回答下列问题:
(1) 的价电子排布式为
的价电子排布式为_______ 。金属锰可导电、导热,有金属光泽和延展性,这些性质都可以用“_______ 理论”解释。
(2)已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列_______ (填序号),Mn原子的配位数为_______ 。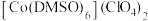 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为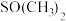 。DMSO中硫原子的杂化轨道类型为
。DMSO中硫原子的杂化轨道类型为_______ ,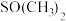 中键角
中键角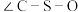
_______  中键角
中键角 (填“大于”“小于”或“等于”),
(填“大于”“小于”或“等于”), 的中心原子价层电子对数为
的中心原子价层电子对数为_______ ,元素S、Mn、N的电负性由大到小的顺序为_______ 。
(4)镍和苯基硼酸在催化剂作用下可以合成丙烯醇(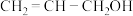 ),该物质与丙醛(
),该物质与丙醛(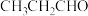 )相比,两者沸点相差较大,原因是
)相比,两者沸点相差较大,原因是_______ 。
(5) 的晶胞结构如图甲所示,其中离子坐标参数A为
的晶胞结构如图甲所示,其中离子坐标参数A为 ,B为
,B为 ,则C的离子坐标参数为
,则C的离子坐标参数为_______ 。一定温度下, 晶体可以自发地分散并形成“单分子层”,可以认为
晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,
作密置单层排列, 填充其中(如图乙),已知
填充其中(如图乙),已知 的半径为
的半径为 ,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为
,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为_______ g(用含a、NA的代数式表示)。
(1)
 的价电子排布式为
的价电子排布式为(2)已知金属锰有多种晶型,γ型锰的面心立方晶胞俯视图符合下列
A.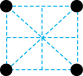 B.
B. C.
C.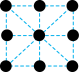 D.
D.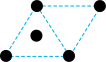
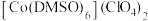 是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为
是一种紫色晶体,其中DMSO为二甲基亚砜,化学式为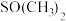 。DMSO中硫原子的杂化轨道类型为
。DMSO中硫原子的杂化轨道类型为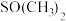 中键角
中键角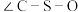
 中键角
中键角 (填“大于”“小于”或“等于”),
(填“大于”“小于”或“等于”), 的中心原子价层电子对数为
的中心原子价层电子对数为(4)镍和苯基硼酸在催化剂作用下可以合成丙烯醇(
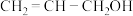 ),该物质与丙醛(
),该物质与丙醛(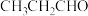 )相比,两者沸点相差较大,原因是
)相比,两者沸点相差较大,原因是(5)
 的晶胞结构如图甲所示,其中离子坐标参数A为
的晶胞结构如图甲所示,其中离子坐标参数A为 ,B为
,B为 ,则C的离子坐标参数为
,则C的离子坐标参数为 晶体可以自发地分散并形成“单分子层”,可以认为
晶体可以自发地分散并形成“单分子层”,可以认为 作密置单层排列,
作密置单层排列, 填充其中(如图乙),已知
填充其中(如图乙),已知 的半径为
的半径为 ,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为
,设阿伏加德罗常数值为NA,每平方米面积上具有该晶体的质量为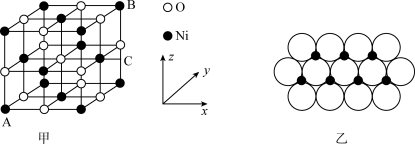
您最近半年使用:0次
2024-04-21更新
|
138次组卷
|
2卷引用:四川省绵阳南山中学2024届高三下学期三诊热身考试理综-化学试题
7 . CO2和CH4合成CH3COOH对实现“碳中和”目标具有重要意义。回答下列问题:
(1)25℃时,CH4和CH3COOH的燃烧热分别为890.3kJ·mol-1和873.7kJ·mol-1,写出CO2和CH4合成CH3COOH(l)的热化学方程式___________ 。
(2)在硫酸酸化的ZrO2催化剂表面发生反应时,涉及多个基元反应,反应经历pathA,pathB两个路径,其能量变化如下图所示。吸附在催化剂表面的物种用*标注,TS1、TS2、TS3表示过渡态。___________ (填“放出热量”或“吸收热量”)。
②上述基元反应pathA路径中,速率最慢的一步的反应方程式为___________ 。
③pathA和pathB路径相比,___________ 更容易进行。
(3)已知 能自发进行,
能自发进行,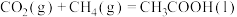
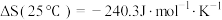 ,下列说法正确的是___________。
,下列说法正确的是___________。
(4)以CuO-ZrO2作催化剂,CO2、CH4投料比为1:1,300℃反应,平衡时CH4转化率为12%,CH3COOH选择性为95%,则CH3COOH的平衡产率为___________ 。(选择性指转化为目标产物的某反应物的质量与发生反应的该反应物的质量之比)
(5)立方ZrO2的晶胞如图,晶胞参数为apm,O2-和Zr4+间的最小距离为___________ pm,晶体密度为___________ g·cm-3。(列出计算式,阿伏加德罗常数的值用 表示)
表示)
(1)25℃时,CH4和CH3COOH的燃烧热分别为890.3kJ·mol-1和873.7kJ·mol-1,写出CO2和CH4合成CH3COOH(l)的热化学方程式
(2)在硫酸酸化的ZrO2催化剂表面发生反应时,涉及多个基元反应,反应经历pathA,pathB两个路径,其能量变化如下图所示。吸附在催化剂表面的物种用*标注,TS1、TS2、TS3表示过渡态。
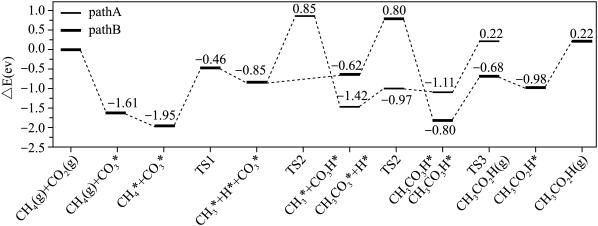
②上述基元反应pathA路径中,速率最慢的一步的反应方程式为
③pathA和pathB路径相比,
(3)已知
 能自发进行,
能自发进行,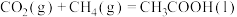
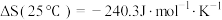 ,下列说法正确的是___________。
,下列说法正确的是___________。| A.25℃时,该反应能自发进行 |
| B.降低温度能提高CH4的平衡转化率 |
C. ,反应达平衡状态 ,反应达平衡状态 |
| D.温度越高反应速率越快 |
(4)以CuO-ZrO2作催化剂,CO2、CH4投料比为1:1,300℃反应,平衡时CH4转化率为12%,CH3COOH选择性为95%,则CH3COOH的平衡产率为
(5)立方ZrO2的晶胞如图,晶胞参数为apm,O2-和Zr4+间的最小距离为
 表示)
表示)
您最近半年使用:0次
2024-04-21更新
|
89次组卷
|
2卷引用:山西省平遥中学2023-2024学年高三二模考试化学试题
名校
解题方法
8 . Co、H、O形成晶体的晶胞结构如图甲;晶胞沿竖直方向向下的投影图如图乙,其中H被遮挡未画出。已知晶胞参数为 ,
, ,
,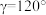 。下列说法错误的是
。下列说法错误的是
 ,
, ,
,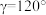 。下列说法错误的是
。下列说法错误的是
A.晶体的化学式为 |
B.晶体中存在 和 和 两种阴离子 两种阴离子 |
| C.晶体中Co的配位数为4 |
D.晶体密度为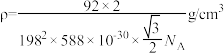 |
您最近半年使用:0次
名校
解题方法
9 . 高二化学组组织同学们制作晶体模型。8班张宇涵同学提交了金刚石的晶体结构模型,17班路雪同学提交了氯化钠的晶胞模型,如下图所示。下列说法不正确的是


A.金刚石晶体中,碳原子采取 杂化轨道成键,形成共价键三维骨架网络 杂化轨道成键,形成共价键三维骨架网络 |
B. 金刚石晶体中含 金刚石晶体中含 键 键 |
C.氯化钠晶体中,1个 周围有12个距离最近且相等的 周围有12个距离最近且相等的 |
D.氯化钠晶胞为立方体,若棱长为 ,则晶体密度为 ,则晶体密度为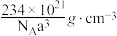 |
您最近半年使用:0次
10 . 中国第一辆火星车“祝融号”成功登陆火星。探测发现火星上存在大量做橄榄石矿物( ),回答下列问题:
),回答下列问题:
(1)基态 原子的价电子轨道表示式为
原子的价电子轨道表示式为______________ ,橄榄石中铁的化合价为______ ,橄榄石中,各元素电负性由大到小的顺序为____________
(2)已知一些物质的熔点数据如下表:
Na与Si均为第三周期元素,NaCl熔点明显高于SiCl4,原因是____________ 。
(3) 可以形成
可以形成 (
( ,4,5,6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足量AgNO3溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,第一次与第二次产生的沉淀的物质的量之比为1:2。则该溶液中溶质的化学式为
,4,5,6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足量AgNO3溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,第一次与第二次产生的沉淀的物质的量之比为1:2。则该溶液中溶质的化学式为_____________ 。
(4)硫酸铜溶液中逐渐滴加氨水至过量,离子反应依次为______________ 、___________ 。再向溶液中加入乙醇能够析出深蓝色的晶体,加入乙醇的作用:_________ 。
(5)某晶体的晶胞结构如图所示,已知晶胞参数分别为 、
、 、
、 ,
, 、
、 原子的坐标分别为
原子的坐标分别为 、
、 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。____________ 。
②C原子的坐标为____________ 。
③该晶体的密度为____________ g/cm3。(列出计算式即可,无需化简)
 ),回答下列问题:
),回答下列问题:(1)基态
 原子的价电子轨道表示式为
原子的价电子轨道表示式为(2)已知一些物质的熔点数据如下表:
物质 |
|
|
|
|
熔点/℃ |
|
|
|
|
(3)
 可以形成
可以形成 (
( ,4,5,6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足量AgNO3溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,第一次与第二次产生的沉淀的物质的量之比为1:2。则该溶液中溶质的化学式为
,4,5,6)等一系列配位数为6的配合物,向上述某物质的溶液中加入足量AgNO3溶液,有沉淀生成;过滤后,充分加热滤液有氨气逸出,且又有沉淀生成,第一次与第二次产生的沉淀的物质的量之比为1:2。则该溶液中溶质的化学式为(4)硫酸铜溶液中逐渐滴加氨水至过量,离子反应依次为
(5)某晶体的晶胞结构如图所示,已知晶胞参数分别为
 、
、 、
、 ,
, 、
、 原子的坐标分别为
原子的坐标分别为 、
、 ,阿伏加德罗常数的值为
,阿伏加德罗常数的值为 。
。
②C原子的坐标为
③该晶体的密度为
您最近半年使用:0次