1 . 环戊二烯是一种重要的有机合成原料,用其制备环戊烯涉及的反应如下:
(1)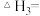
______ (用含“ ”和“
”和“ ”的式子表示),该反应在
”的式子表示),该反应在______ (填“高温”或“低温”)条件下能自发进行。
(2)下列操作中,能提高环戊二烯平衡转化率的是______ (填标号)。
A.增加环戊二烯的用量 B.恒温恒压下通入惰性气体 C.移除环戊烯
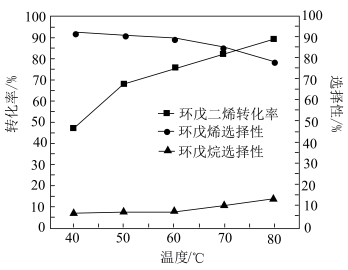
(3)保持其他条件不变,在相同时间内,环戊二烯转化率及环戊烯、环戊烷的选择性与温度的关系如下图所示:______ (填标号)。
A. B.
B. C.
C. 左右
左右
②随着温度的升高,环戊二烯转化率升高而环戊烯选择性降低,其原因是______ 。
(4)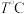 ,向恒容密闭容器中加入
,向恒容密闭容器中加入 环戊二烯
环戊二烯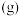 和
和
 ,反应达到平衡时,环戊二烯的转化率为
,反应达到平衡时,环戊二烯的转化率为 ,环戊烷物质的量为
,环戊烷物质的量为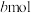 ,则用气体物质的量分数
,则用气体物质的量分数 表示的主反应的平衡常数
表示的主反应的平衡常数
______ (用含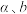 的计算式表示)。
的计算式表示)。
(5)用环戊二烯制备的二茂铁 可用作火箭燃料添加剂、汽油抗爆剂、橡胶熟化剂、紫外线吸收剂等。二茂铁的晶胞结构如图所示(未画出微粒),密度为
可用作火箭燃料添加剂、汽油抗爆剂、橡胶熟化剂、紫外线吸收剂等。二茂铁的晶胞结构如图所示(未画出微粒),密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则一个晶胞中含
,则一个晶胞中含 的数目为
的数目为______ 。
主反应: ;
;
副反应1: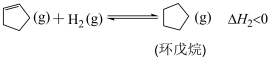 。
。
副反应2:
(1)
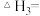
 ”和“
”和“ ”的式子表示),该反应在
”的式子表示),该反应在(2)下列操作中,能提高环戊二烯平衡转化率的是
A.增加环戊二烯的用量 B.恒温恒压下通入惰性气体 C.移除环戊烯
(3)保持其他条件不变,在相同时间内,环戊二烯转化率及环戊烯、环戊烷的选择性与温度的关系如下图所示:
A.
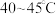 B.
B.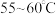 C.
C.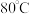 左右
左右②随着温度的升高,环戊二烯转化率升高而环戊烯选择性降低,其原因是
(4)
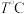 ,向恒容密闭容器中加入
,向恒容密闭容器中加入 环戊二烯
环戊二烯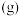 和
和
 ,反应达到平衡时,环戊二烯的转化率为
,反应达到平衡时,环戊二烯的转化率为 ,环戊烷物质的量为
,环戊烷物质的量为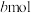 ,则用气体物质的量分数
,则用气体物质的量分数 表示的主反应的平衡常数
表示的主反应的平衡常数
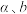 的计算式表示)。
的计算式表示)。(5)用环戊二烯制备的二茂铁
 可用作火箭燃料添加剂、汽油抗爆剂、橡胶熟化剂、紫外线吸收剂等。二茂铁的晶胞结构如图所示(未画出微粒),密度为
可用作火箭燃料添加剂、汽油抗爆剂、橡胶熟化剂、紫外线吸收剂等。二茂铁的晶胞结构如图所示(未画出微粒),密度为 ,设阿伏加德罗常数的值为
,设阿伏加德罗常数的值为 ,则一个晶胞中含
,则一个晶胞中含 的数目为
的数目为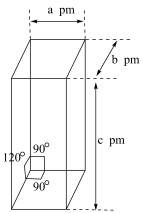
您最近半年使用:0次
2 . 氧化饰( )是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳饰矿(含
)是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳饰矿(含 、
、 、
、 等)为原料制备氧化饰,其工艺流程如图所示;
等)为原料制备氧化饰,其工艺流程如图所示; 形成复盐沉淀,步骤②中ⅱ)发生的反应为:
形成复盐沉淀,步骤②中ⅱ)发生的反应为:
② 能和很多金属离子形成较为稳定的配合物,如
能和很多金属离子形成较为稳定的配合物,如 能与
能与 结合成
结合成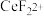
③ 在空气中易被氧化为
在空气中易被氧化为 。
。
④硫脲(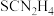 )具有还原性,酸性条件下易被氧化为
)具有还原性,酸性条件下易被氧化为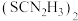 。
。
(1)“焙烧”前需将矿石粉碎成细颗粒,其目的是_______ 。
(2)焙烧后的固体产物中含有 和
和 物质的量之比为1∶1,步骤①发生反应的离子方程式为
物质的量之比为1∶1,步骤①发生反应的离子方程式为_______ 。
(3)加入硫脲的目的是将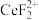 还原为
还原为 ,反应的离子方程式为
,反应的离子方程式为_______ 。
(4)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为_______ 。
(5)若常温下,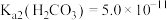 ,
, ,
, 恰好沉淀完全时
恰好沉淀完全时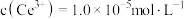 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中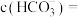
_______  。
。
(6)某研究小组利用硫化锌锂电池电解含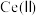 的溶液,可将
的溶液,可将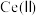 转化为
转化为 。该硫化锌锂电池放电时,负极材料晶胞组成变化如图所示。
。该硫化锌锂电池放电时,负极材料晶胞组成变化如图所示。 中,
中,
_______ 。
② 晶胞中,
晶胞中, 填充在
填充在 构成的部分正四面体空隙中,
构成的部分正四面体空隙中, 和
和 之间的核间距为a
之间的核间距为a ,设
,设 为阿伏加德罗常数的值,则晶胞的密度为
为阿伏加德罗常数的值,则晶胞的密度为_______  (列出计算式,
(列出计算式, 的摩尔质量为97
的摩尔质量为97 )。
)。
 )是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳饰矿(含
)是一种广泛应用的稀土氧化物,具有吸收强紫外线的能力,可以用于光催化降解有机污染物。现以氟碳饰矿(含 、
、 、
、 等)为原料制备氧化饰,其工艺流程如图所示;
等)为原料制备氧化饰,其工艺流程如图所示;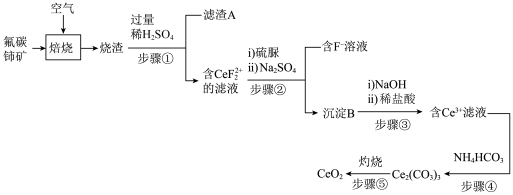
 形成复盐沉淀,步骤②中ⅱ)发生的反应为:
形成复盐沉淀,步骤②中ⅱ)发生的反应为:
②
 能和很多金属离子形成较为稳定的配合物,如
能和很多金属离子形成较为稳定的配合物,如 能与
能与 结合成
结合成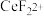
③
 在空气中易被氧化为
在空气中易被氧化为 。
。④硫脲(
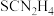 )具有还原性,酸性条件下易被氧化为
)具有还原性,酸性条件下易被氧化为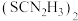 。
。(1)“焙烧”前需将矿石粉碎成细颗粒,其目的是
(2)焙烧后的固体产物中含有
 和
和 物质的量之比为1∶1,步骤①发生反应的离子方程式为
物质的量之比为1∶1,步骤①发生反应的离子方程式为(3)加入硫脲的目的是将
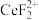 还原为
还原为 ,反应的离子方程式为
,反应的离子方程式为(4)步骤③加入盐酸后,通常还需加入另一种化学试剂X,根据题中信息推测,加入X的作用为
(5)若常温下,
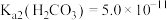 ,
, ,
, 恰好沉淀完全时
恰好沉淀完全时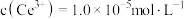 ,此时测得溶液的
,此时测得溶液的 ,则溶液中
,则溶液中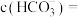
 。
。(6)某研究小组利用硫化锌锂电池电解含
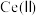 的溶液,可将
的溶液,可将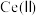 转化为
转化为 。该硫化锌锂电池放电时,负极材料晶胞组成变化如图所示。
。该硫化锌锂电池放电时,负极材料晶胞组成变化如图所示。
 中,
中,
②
 晶胞中,
晶胞中, 填充在
填充在 构成的部分正四面体空隙中,
构成的部分正四面体空隙中, 和
和 之间的核间距为a
之间的核间距为a ,设
,设 为阿伏加德罗常数的值,则晶胞的密度为
为阿伏加德罗常数的值,则晶胞的密度为 (列出计算式,
(列出计算式, 的摩尔质量为97
的摩尔质量为97 )。
)。
您最近半年使用:0次
3 . Fe有δ、γ、α三种同素异形体,其晶胞结构如图所示:___________ 个。
(2)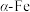 延展时,
延展时,___________ (填“可以”或“不可以”)转变为 。
。
(3)若δ—Fe晶体的晶胞边长为a cm, 表示阿伏加德罗常数的值,则δ—Fe单质的密度为
表示阿伏加德罗常数的值,则δ—Fe单质的密度为___________ 。

(2)
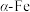 延展时,
延展时, 。
。(3)若δ—Fe晶体的晶胞边长为a cm,
 表示阿伏加德罗常数的值,则δ—Fe单质的密度为
表示阿伏加德罗常数的值,则δ—Fe单质的密度为
您最近半年使用:0次
名校
解题方法
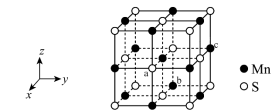
4 . 下图是MnS晶胞,其与NaCl晶胞属于同种类型。前者的熔点明显高于后者,其主要原因是___________ ;每个晶胞中平均分摊___________ 个S2-。
您最近半年使用:0次
名校
解题方法
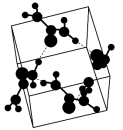
5 . 尿素晶体的晶胞如图所示。推测尿素晶体中存在的主要作用力为共价键和___________ 。每个尿素晶胞中含有___________ 个尿素分子。
您最近半年使用:0次
名校
解题方法
6 . 钙钛矿太阳能电池与锂硫电池集成,可实现太阳能直接对锂硫电池充电,其原理如图1所示。碳电极为共享电极,导电玻璃FTO基底上涂TiO2作为电子传输层。充电时,钙钛矿层吸收太阳光产生光生电子(e)和空穴(h),分离后输送到两个电极上。一种钙钛矿太阳能电池材料的晶胞结构如图2所示,已知abc0.569nm,90。下列说法正确的是

| A.共享碳电极为钙钛矿太阳能电池的负极 |
| B.锂硫电池放电时,Li向硫层迁移 |
C.充电时,共享碳电极上电极反应式为xS816e-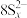 |
D.该钙钛矿晶体的密度为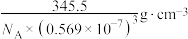 |
您最近半年使用:0次
解题方法
7 . 含氮物质在工业上应用非常广泛。将单质钡(Ba)、铼(Re)以一定比例混合,于特制容器中加热,依次通入N2、O2可制得某黑色晶体,该晶体晶胞如图所示,含有多个由Ba(+2)、Re(+4)、O(-2)和N(-3)组成的八面体与平面三角形,括号中为其化合价。
(1)基态Ba原子的简化电子排布式为___________ ,N、O、Ba简单氢化物的沸点由高到低的顺序为___________ (填化学式)。
(2)NO 中N原子的杂化方式为
中N原子的杂化方式为___________ ,下列离子或分子与 互为等电子体的是
互为等电子体的是___________ (填标号)。
a.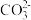 b.
b. c.SO3 d.
c.SO3 d.
(3)苯胺(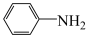 )中N原子与苯环形成p-π共轭,
)中N原子与苯环形成p-π共轭, 、
、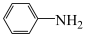 、
、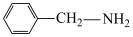 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是___________ 。
(4)该晶体中含有的八面体和平面三角形的个数比为___________ ,晶体的化学式为___________ 。
(5)晶胞参数为apm、apm、cpm, ,
,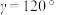 ,该晶体的密度为
,该晶体的密度为___________ g·cm-1(写出表达式)。

(1)基态Ba原子的简化电子排布式为
(2)NO
 中N原子的杂化方式为
中N原子的杂化方式为 互为等电子体的是
互为等电子体的是a.
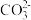 b.
b. c.SO3 d.
c.SO3 d.
(3)苯胺(
 )中N原子与苯环形成p-π共轭,
)中N原子与苯环形成p-π共轭, 、
、 、
、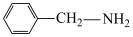 的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是
的碱性随N原子电子云密度的增大而增强,其中碱性最弱的是(4)该晶体中含有的八面体和平面三角形的个数比为
(5)晶胞参数为apm、apm、cpm,
 ,
,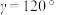 ,该晶体的密度为
,该晶体的密度为
您最近半年使用:0次
8 . 葡萄糖的银镜反应实验如下:
步骤1:向试管中加入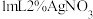 溶液,边振荡边滴加
溶液,边振荡边滴加 氨水,观察到有白色沉淀产生并迅速转化为灰褐色.
氨水,观察到有白色沉淀产生并迅速转化为灰褐色.
步骤2:向试管中继续滴加 氨水,观察到沉淀完全溶解.
氨水,观察到沉淀完全溶解.
步骤3:再向试管中加入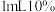 葡萄糖溶液,振荡,在
葡萄糖溶液,振荡,在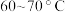 水浴中加热,观察到试管内壁形成了光亮银镜.
水浴中加热,观察到试管内壁形成了光亮银镜.
下列说法正确的是
步骤1:向试管中加入
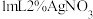 溶液,边振荡边滴加
溶液,边振荡边滴加 氨水,观察到有白色沉淀产生并迅速转化为灰褐色.
氨水,观察到有白色沉淀产生并迅速转化为灰褐色.步骤2:向试管中继续滴加
 氨水,观察到沉淀完全溶解.
氨水,观察到沉淀完全溶解.步骤3:再向试管中加入
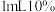 葡萄糖溶液,振荡,在
葡萄糖溶液,振荡,在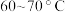 水浴中加热,观察到试管内壁形成了光亮银镜.
水浴中加热,观察到试管内壁形成了光亮银镜.下列说法正确的是

A.步骤1产生白色沉淀的离子反应方程式为 |
B.步骤2中沉淀溶解是因为生成了银氨配合物, 中含有 中含有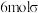 键 键 |
| C.步骤3中产生银镜,葡萄糖发生了氧化反应 |
| D.如图所示银的晶胞中有14个银原子 |
您最近半年使用:0次
名校
解题方法
9 . 我国科学家制备了一种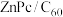 太阳电池,其结构示意图如下。
太阳电池,其结构示意图如下。___________ 区(填“s”“d”“ds”或“p”)。
(2) 分子中60个碳原子都是等价的,均以近似
分子中60个碳原子都是等价的,均以近似___________ 杂化的方式形成3个不共平面的 键,余下的1个p轨道电子互相重叠形成闭壳层电子结构,
键,余下的1个p轨道电子互相重叠形成闭壳层电子结构, 电子云分布在
电子云分布在 分子笼的内外层表面上。循环伏安测试表明:
分子笼的内外层表面上。循环伏安测试表明: 在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
(3)① 中基态
中基态 的电子排布式为
的电子排布式为___________ 。
② 中存在配位键的原因是
中存在配位键的原因是___________ 。
(4)某溶剂中, 可以和
可以和 形成分子间电荷转移复合物,反应方程式可表示为:
形成分子间电荷转移复合物,反应方程式可表示为: ,不同温度下生成电荷转移复合物的平衡常数如下表。
,不同温度下生成电荷转移复合物的平衡常数如下表。
反应: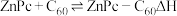
___________ 0(填“>”或。“<”), 中
中 是电子
是电子___________ (填“给体”或“受体”)。
(5) 晶体结构属于氯化钠型,其晶胞结构如图所示。
晶体结构属于氯化钠型,其晶胞结构如图所示。 的熔点和沸点比
的熔点和沸点比 的高,请解释原因
的高,请解释原因___________ 。
② 晶体的密度约为
晶体的密度约为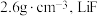 晶胞的体积约为
晶胞的体积约为___________  (列出计算式即可)。
(列出计算式即可)。
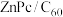 太阳电池,其结构示意图如下。
太阳电池,其结构示意图如下。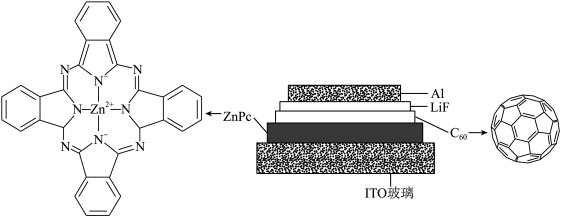
(2)
 分子中60个碳原子都是等价的,均以近似
分子中60个碳原子都是等价的,均以近似 键,余下的1个p轨道电子互相重叠形成闭壳层电子结构,
键,余下的1个p轨道电子互相重叠形成闭壳层电子结构, 电子云分布在
电子云分布在 分子笼的内外层表面上。循环伏安测试表明:
分子笼的内外层表面上。循环伏安测试表明: 在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。
在溶液中可以逐步可逆地接受6个电子形成负离子,却很难失去电子变为阳离子。(3)①
 中基态
中基态 的电子排布式为
的电子排布式为②
 中存在配位键的原因是
中存在配位键的原因是(4)某溶剂中,
 可以和
可以和 形成分子间电荷转移复合物,反应方程式可表示为:
形成分子间电荷转移复合物,反应方程式可表示为: ,不同温度下生成电荷转移复合物的平衡常数如下表。
,不同温度下生成电荷转移复合物的平衡常数如下表。| 温度 | 生成 的K 的K |
 | 1.2329 |
 | 0.9674 |
 | 0.4923 |
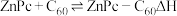
 中
中 是电子
是电子(5)
 晶体结构属于氯化钠型,其晶胞结构如图所示。
晶体结构属于氯化钠型,其晶胞结构如图所示。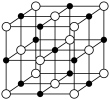
 的熔点和沸点比
的熔点和沸点比 的高,请解释原因
的高,请解释原因②
 晶体的密度约为
晶体的密度约为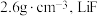 晶胞的体积约为
晶胞的体积约为 (列出计算式即可)。
(列出计算式即可)。
您最近半年使用:0次
10 . 高压不仅会引发物质的相变,还会导致新类型化学键的形成。如图所示,M、N、P为Na与 在50~300GPa的高压下反应生成的不同晶体晶胞,下列说法错误的是
在50~300GPa的高压下反应生成的不同晶体晶胞,下列说法错误的是
 在50~300GPa的高压下反应生成的不同晶体晶胞,下列说法错误的是
在50~300GPa的高压下反应生成的不同晶体晶胞,下列说法错误的是
A.M、N、P晶体的化学式分别为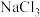 、 、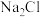 、 、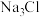 |
B.晶胞M、N、P中所含Cl原子的个数之比为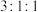 |
| C.晶胞M中与Na原子距离最近且等距的Cl原子有12个 |
D.1号的原子坐标为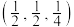 |
您最近半年使用:0次



