解题方法
1 . 晶体世界丰富多彩,复杂多样,各类晶体具有不同的结构特点,决定着他具有不同的性质和用途,回答下列问题:
(1)氢化铝钠(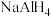 )是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。
)是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。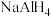 晶体中,与
晶体中,与 紧邻且等距的
紧邻且等距的 有
有_____ 个;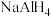 晶体的密度为
晶体的密度为_____  (用含a、
(用含a、 的代数式表示)
的代数式表示)_____ ,Mo原子周围与之等距离的Mo原子个数为_____ 。
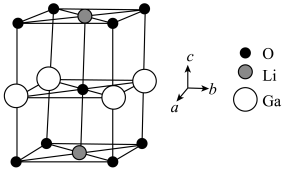
(3)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:_____ ,上述晶胞沿着a轴的投影图为_____ (填选项字母)。
(1)氢化铝钠(
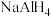 )是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。
)是一种新型轻质储氢材料,其晶胞结构如图所示,为长方体。 晶体中,与
晶体中,与 紧邻且等距的
紧邻且等距的 有
有 晶体的密度为
晶体的密度为 (用含a、
(用含a、 的代数式表示)
的代数式表示)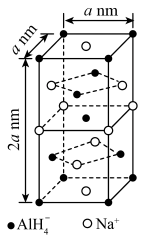

(3)Ga、Li和O三种原子形成的一种晶体基片在二极管中有重要用途。其四方晶胞结构如图所示:
A.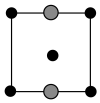 B.
B.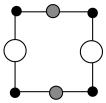 C.
C.
您最近半年使用:0次
解题方法
2 . 配合物在许多尖端领域如激光材料、超导材料、抗癌药物的研究、催化剂的研制、自组装超分子等方面有广泛的应用。回答下列问题:
(1)Ni与CO形成的配合物 为无色液体,易溶于
为无色液体,易溶于 、
、 等有机溶剂。
等有机溶剂。 为
为_____ (填“极性”或“非极性”)分子,分子中σ键与π键个数之比为_____ 。
(2)《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶可得到
溶液后,经提纯、结晶可得到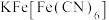 蓝色晶体。实验表明,
蓝色晶体。实验表明, 、
、 、
、 通过配位键构成了晶体的骨架。其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。
通过配位键构成了晶体的骨架。其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。_____ 实验,可确定该晶体结构(填标号)。
a.核磁共振 b.红外光谱 c.X射线衍射 d.质谱
②若 位于Ⅱ型立方结构的棱心和体心上,则
位于Ⅱ型立方结构的棱心和体心上,则 位于Ⅱ型立方结构的
位于Ⅱ型立方结构的_____ 上;一个Ⅱ型立方结构中含_____ 个 ;若
;若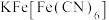 的摩尔质量为
的摩尔质量为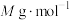 ,该蓝色晶体密度为
,该蓝色晶体密度为 ,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为
,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为_____ 。
(1)Ni与CO形成的配合物
 为无色液体,易溶于
为无色液体,易溶于 、
、 等有机溶剂。
等有机溶剂。 为
为(2)《诗经》言“缟衣茹藘(茜草)”,茜草中的茜素与矾土中的
 、
、 生成的红色配合物X是最早的媒染染料。
生成的红色配合物X是最早的媒染染料。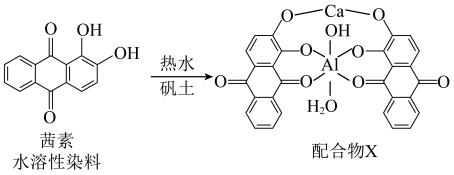
基态 的核外电子的运动状态有
的核外电子的运动状态有 的配体除
的配体除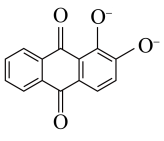 外还有
外还有
 溶液中滴加
溶液中滴加 溶液后,经提纯、结晶可得到
溶液后,经提纯、结晶可得到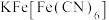 蓝色晶体。实验表明,
蓝色晶体。实验表明, 、
、 、
、 通过配位键构成了晶体的骨架。其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。
通过配位键构成了晶体的骨架。其局部结构如图1,记为Ⅰ型立方结构。将Ⅰ型立方结构平移、旋转、并置,可得到晶体的复晶胞(如图2,记为Ⅱ型立方结构,下层左后的小立方体g未标出)。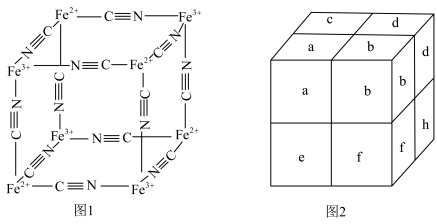
a.核磁共振 b.红外光谱 c.X射线衍射 d.质谱
②若
 位于Ⅱ型立方结构的棱心和体心上,则
位于Ⅱ型立方结构的棱心和体心上,则 位于Ⅱ型立方结构的
位于Ⅱ型立方结构的 ;若
;若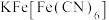 的摩尔质量为
的摩尔质量为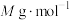 ,该蓝色晶体密度为
,该蓝色晶体密度为 ,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为
,Ⅱ型立方结构的边长为anm,则阿伏加德罗常数的值可表示为
您最近半年使用:0次
3 . 铋化锂晶胞结构如图所示。晶胞可以看作是由铋原子构成的面心立方晶格,锂原子填充在其中的四面体和八面体空隙处。设晶胞参数为apm,阿伏加德罗常数为 。下列叙述错误的是
。下列叙述错误的是
 。下列叙述错误的是
。下列叙述错误的是
A.若A的坐标为 ,C的坐标为 ,C的坐标为 ,则B的坐标为 ,则B的坐标为 |
| B.与Li距离最近的Bi的数目为6个 |
C.铋原子的半径为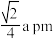 |
D.晶体密度的计算表达式为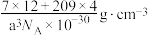 |
您最近半年使用:0次
名校
解题方法
4 . 含金的配合物在工业生产中有重要用途。一种金的配合物的晶体结构如图所示,下列说法错误的是

| A.该化合物的化学式为CsAuCl3 |
| B.Cs+的配位数为12 |
| C.Au是第ⅠB族的过渡金属 |
| D.1mol/L该配合物水溶液的电阻率较高 |
您最近半年使用:0次
名校
解题方法
5 . 当下新能源汽车电池的发展加大了对金属钻(Co)的需求。回答下列问题:
(1)基态Co原子价电子排布式为__________ ,Co2+有___ 个未成对电子。
(2)Co的第四电离能比Fe的第四电离能要小很多,原因是________________ 。
(3)Na3[Co(NO2)6]中的 中N原子为
中N原子为_______ 杂化,空间构型名称为_________ 形。
(4)一种Co(Ⅱ)的配合物结构如图所示,下列说法错误的是______(填序号)。
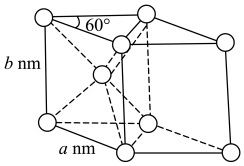
(5)金属钴晶胞结构及参数如图所示,该晶胞中Co的配位数为________ 。已知金属Co晶体密度为ρ g/cm3,则阿伏加德罗常数NA=___________ mol-1。
(1)基态Co原子价电子排布式为
(2)Co的第四电离能比Fe的第四电离能要小很多,原因是
(3)Na3[Co(NO2)6]中的
 中N原子为
中N原子为(4)一种Co(Ⅱ)的配合物结构如图所示,下列说法错误的是______(填序号)。
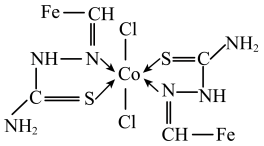
| A.配合物中的氯元素是Cl- |
| B.配合物中Co2+配位数为4 |
| C.结构中所有N原子有sp2、sp3杂化 |
D.结构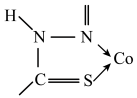 中所有原子共平面 中所有原子共平面 |
(5)金属钴晶胞结构及参数如图所示,该晶胞中Co的配位数为
您最近半年使用:0次
解题方法
6 .  、
、 、
、 、
、 是原子序数依次增大的短周期主族元素,基态
是原子序数依次增大的短周期主族元素,基态 原子核外的
原子核外的 个能级中容纳的电子数之比为
个能级中容纳的电子数之比为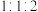 ,基态
,基态 原子有
原子有 个未成对电子,且
个未成对电子,且 、
、 、
、 三种元素形成的化合物甲的结构如图
三种元素形成的化合物甲的结构如图 所示,
所示, 、
、 形成的化合物的晶胞结构如图
形成的化合物的晶胞结构如图 所示。下列说法正确的是
所示。下列说法正确的是
 、
、 、
、 、
、 是原子序数依次增大的短周期主族元素,基态
是原子序数依次增大的短周期主族元素,基态 原子核外的
原子核外的 个能级中容纳的电子数之比为
个能级中容纳的电子数之比为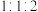 ,基态
,基态 原子有
原子有 个未成对电子,且
个未成对电子,且 、
、 、
、 三种元素形成的化合物甲的结构如图
三种元素形成的化合物甲的结构如图 所示,
所示, 、
、 形成的化合物的晶胞结构如图
形成的化合物的晶胞结构如图 所示。下列说法正确的是
所示。下列说法正确的是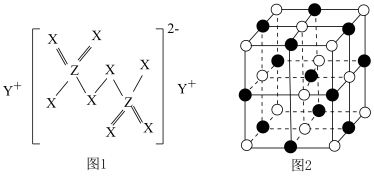
A. 、 、 为同周期元素 为同周期元素 |
B.基态 原子核外电子占据的最高能级的电子云轮廓图为哑铃形 原子核外电子占据的最高能级的电子云轮廓图为哑铃形 |
C.简单离子半径: |
D.图 所示的 所示的 个晶胞中含 个晶胞中含 个 个 离子 离子 |
您最近半年使用:0次
7 . 铌镍合金材料在生产中有广泛应用,它的晶胞如图所示。已知: 为阿伏加德罗常数的值,铌(Nb)和钒位于同族且与钒相邻,但是基态Nb原子最外层只有1个电子。下列叙述正确的是
为阿伏加德罗常数的值,铌(Nb)和钒位于同族且与钒相邻,但是基态Nb原子最外层只有1个电子。下列叙述正确的是
 为阿伏加德罗常数的值,铌(Nb)和钒位于同族且与钒相邻,但是基态Nb原子最外层只有1个电子。下列叙述正确的是
为阿伏加德罗常数的值,铌(Nb)和钒位于同族且与钒相邻,但是基态Nb原子最外层只有1个电子。下列叙述正确的是
A.基态Nb原子价层电子排布式为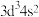 |
| B.镍、铌元素都位于周期表ds区 |
| C.晶胞中Nb、Ni原子数之比为3:1 |
D.晶体密度为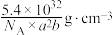 |
您最近半年使用:0次
名校
解题方法
8 . 氮及其化合物应用广泛。回答下列问题:
(1)基态 原子处于最高能级的电子云轮廓图为
原子处于最高能级的电子云轮廓图为___________ 形,能量最低的激发态 的核外电子排布式为
的核外电子排布式为___________ 。
(2)胍( )为平面形分子,存在大
)为平面形分子,存在大 键
键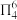 。胍属于
。胍属于___________ 分子(填“极性”或“非极性”), 原子的杂化轨道方式为
原子的杂化轨道方式为___________ ,①号 原子
原子 键角
键角___________ ②号 原子
原子 键角(填“>”“<”或“=”),胍易吸收空气中
键角(填“>”“<”或“=”),胍易吸收空气中 和
和 ,其原因是
,其原因是___________ 。
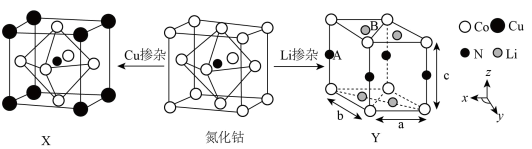
(3)氮化钴属于立方晶系,经 掺杂得催化剂
掺杂得催化剂 ,经
,经 掺杂得催化剂
掺杂得催化剂 。
。 属于立方晶系,晶胞参数为
属于立方晶系,晶胞参数为 ,距离最近
,距离最近 原子的核间距为
原子的核间距为___________  ,若
,若 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, 的密度为
的密度为___________  (用含
(用含 的代数式表示)。
的代数式表示)。 属于六方晶系,晶胞参数为
属于六方晶系,晶胞参数为 ,
, ,
,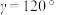 (
( 轴与
轴与 轴夹角),1个
轴夹角),1个 原子周围距离相等且最近的
原子周围距离相等且最近的 原子数目为
原子数目为___________ 。
(1)基态
 原子处于最高能级的电子云轮廓图为
原子处于最高能级的电子云轮廓图为 的核外电子排布式为
的核外电子排布式为(2)胍(
 )为平面形分子,存在大
)为平面形分子,存在大 键
键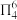 。胍属于
。胍属于 原子的杂化轨道方式为
原子的杂化轨道方式为 原子
原子 键角
键角 原子
原子 键角(填“>”“<”或“=”),胍易吸收空气中
键角(填“>”“<”或“=”),胍易吸收空气中 和
和 ,其原因是
,其原因是(3)氮化钴属于立方晶系,经
 掺杂得催化剂
掺杂得催化剂 ,经
,经 掺杂得催化剂
掺杂得催化剂 。
。
 属于立方晶系,晶胞参数为
属于立方晶系,晶胞参数为 ,距离最近
,距离最近 原子的核间距为
原子的核间距为 ,若
,若 表示阿伏加德罗常数的值,
表示阿伏加德罗常数的值, 的密度为
的密度为 (用含
(用含 的代数式表示)。
的代数式表示)。 属于六方晶系,晶胞参数为
属于六方晶系,晶胞参数为 ,
, ,
,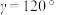 (
( 轴与
轴与 轴夹角),1个
轴夹角),1个 原子周围距离相等且最近的
原子周围距离相等且最近的 原子数目为
原子数目为
您最近半年使用:0次
名校
解题方法
9 . 含铜物质在生产生活中有着广泛应用。回答下列问题:
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。原子中电子有两种相反的自旋状态,分别用 和
和 表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为___________ ;
(2)已知 具有对称的空间构型,
具有对称的空间构型, 中的两个
中的两个 被
被 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为___________ ; 还可形成
还可形成 ,其中
,其中 代表
代表 。该配合物中,
。该配合物中, 模型为四面体的非金属原子共有
模型为四面体的非金属原子共有___________ 个。
(3)一种由 、
、 、
、 组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为 ,晶体中
,晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为___________ ;该晶体的化学式为___________ 。以晶胞参数为单位长度建立的坐标系可以表示晶胞中各原子的位置,称为原子的分数坐标,如 点,
点, 点原子的分数坐标分别为
点原子的分数坐标分别为 、
、 ,则
,则 点原子的分数坐标为
点原子的分数坐标为___________ ,晶胞中 、
、 间距离
间距离
___________  。
。 是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价
是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价 原子)。
原子)。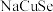 晶胞中0价
晶胞中0价 原子个数为
原子个数为___________ ,每个 晶胞完全转化为
晶胞完全转化为 晶胞,转移电子数为
晶胞,转移电子数为___________ 。
(1)一个原子轨道填充2个自旋方向相反(顺时针和逆时针)的电子。原子中电子有两种相反的自旋状态,分别用
 和
和 表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为
表示,称为电子的自旋磁量子数,则基态铜原子自旋磁量子数的代数和为(2)已知
 具有对称的空间构型,
具有对称的空间构型, 中的两个
中的两个 被
被 取代,能得到两种不同结构的产物,则
取代,能得到两种不同结构的产物,则 的空间构型为
的空间构型为 还可形成
还可形成 ,其中
,其中 代表
代表 。该配合物中,
。该配合物中, 模型为四面体的非金属原子共有
模型为四面体的非金属原子共有(3)一种由
 、
、 、
、 组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为
组成的晶体属四方晶系,晶胞参数如图所示,晶胞棱边夹角均为 ,晶体中
,晶体中 原子填充在
原子填充在 、
、 围成的四面体空隙中,则四面体空隙的占有率为
围成的四面体空隙中,则四面体空隙的占有率为 点,
点, 点原子的分数坐标分别为
点原子的分数坐标分别为 、
、 ,则
,则 点原子的分数坐标为
点原子的分数坐标为 、
、 间距离
间距离
 。
。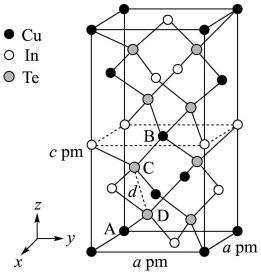
 是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价
是一种钠离子电池的正极材料,充、放电过程中正极材料立方晶胞(示意图)的组成变化如下图所示(晶胞内未标出因放电产生的0价 原子)。
原子)。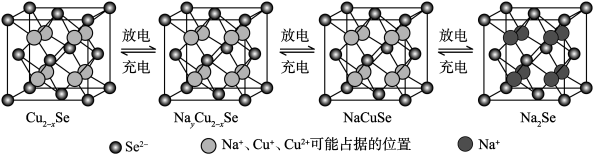
 晶胞中0价
晶胞中0价 原子个数为
原子个数为 晶胞完全转化为
晶胞完全转化为 晶胞,转移电子数为
晶胞,转移电子数为
您最近半年使用:0次
10 .  具有和石墨相似的层状结构,其二维平面结构如图所示,实线圈部分代表一个基本结构单元。研究表明,非金属掺杂(
具有和石墨相似的层状结构,其二维平面结构如图所示,实线圈部分代表一个基本结构单元。研究表明,非金属掺杂( 、
、 等)能提高其光催化活性。下列关于
等)能提高其光催化活性。下列关于 的说法不正确的是
的说法不正确的是
 具有和石墨相似的层状结构,其二维平面结构如图所示,实线圈部分代表一个基本结构单元。研究表明,非金属掺杂(
具有和石墨相似的层状结构,其二维平面结构如图所示,实线圈部分代表一个基本结构单元。研究表明,非金属掺杂( 、
、 等)能提高其光催化活性。下列关于
等)能提高其光催化活性。下列关于 的说法不正确的是
的说法不正确的是
A. 原子的第三电离能大于 原子的第三电离能大于 原子的第三电离能 原子的第三电离能 |
B.晶体中存在的微粒间作用力有极性键、 键、范德华力 键、范德华力 |
C.配位数为2的 原子与配位数为3的 原子与配位数为3的 原子数目之比为 原子数目之比为 |
D.每个基本结构单元中两个 原子(图中虚线圈)被 原子(图中虚线圈)被 原子替代所得物质化学式为 原子替代所得物质化学式为 |
您最近半年使用:0次



