名校
解题方法
1 . 现有mg含有Na2O杂质的Na2O2样品,某同学在实验室用如下装置(部分夹持仪器已省略)测定其杂质含量:
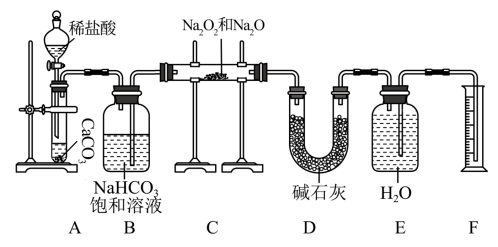
回答下列问题:
(1)装置A中反应的离子方程式为___________ ;该反应基本类型为___________ ,其中CaCO3属于___________ (填“酸”“碱”或“盐”)。
(2)图中有一处明显错误,请指出并改正:___________ 。
(3)装置B的作用是___________ ;装置D的作用是___________ ;若无装置D,样品中杂质的质量分数___________ (填“偏高”“偏低”或“无影响”)。
(4)写出装置C中Na2O2与CO2发生反应的化学方程式:___________ 。
(5)实验结束后,装置F中水的体积为V mL,已知氧气的密度为1.43 g· L-1,样品中杂质的质量分数为___________ (用含m、V的代数式表示,列出计算式即可)。

回答下列问题:
(1)装置A中反应的离子方程式为
(2)图中有一处明显错误,请指出并改正:
(3)装置B的作用是
(4)写出装置C中Na2O2与CO2发生反应的化学方程式:
(5)实验结束后,装置F中水的体积为V mL,已知氧气的密度为1.43 g· L-1,样品中杂质的质量分数为
您最近一年使用:0次
2022-01-18更新
|
110次组卷
|
2卷引用:内蒙古乌兰浩特第一中学2022-2023学年高一上学期期中考试化学试题
2 . 氯气在工业生产中有重要的用途。某课外活动小组利用下列装置在实验室中制备氯气,并进行有关氯气性质的研究。

(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
①写出实验室制氯气的化学方程式:_______ ;已知浓盐酸的质量分数为36.5%,密度为1.15g/mL,则该浓盐酸的物质的量浓度是_______ ;浓盐酸起酸性作用和还原剂作用的物质的量之比为_______ 。
②选择装置,将各仪器按先后顺序连接起来,应该是a→_______ →h(用导管口处的字母表示)。
(2)装置C中饱和食盐水的作用是_______ 。
(3)用E装置吸收多余氯气,写出E中发生反应的离子方程式:_______ ,实验结束后检验E中溶液含有氯离子的实验操作是_______ 。
(4)该小组同学设计并分别利用图2所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。G中的现象是_______ ,原因是_______ (用化学方程式表示)。


(1)该小组同学欲用图1所示仪器及试剂(不一定全用)制备并收集纯净、干燥的氯气。
①写出实验室制氯气的化学方程式:
②选择装置,将各仪器按先后顺序连接起来,应该是a→
(2)装置C中饱和食盐水的作用是
(3)用E装置吸收多余氯气,写出E中发生反应的离子方程式:
(4)该小组同学设计并分别利用图2所示装置探究氯气的氧化性,已知碘单质遇淀粉会变蓝。G中的现象是

您最近一年使用:0次
名校
解题方法
3 . 宋代《千里江山图》描绘了山清水秀的美丽景色,历经千年色彩依然,其中绿色来自孔雀石颜料[主要成分为Cu(OH)2∙ CuCO3],青色来自蓝铜矿颜料[主要成分为Cu(OH)2∙2CuCO3]。下列说法正确的是
| A.孔雀石、蓝铜矿颜料热稳定性较好 |
| B.孔雀石、蓝铜矿颜料在空气中易被氧化 |
| C.孔雀石、蓝铜矿颜料耐酸耐碱 |
| D.Cu(OH)2∙ CuCO3中铜的质量分数高于Cu(OH)2∙2CuCO3 |
您最近一年使用:0次
2024-01-08更新
|
74次组卷
|
3卷引用:内蒙古自治区乌兰浩特第一中学2023-2024学年高一上学期期末考试化学试题
名校
4 . 自古至今,铁及其化合物在人类生产生活中的使用发挥了巨大的作用。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是__________ (填化学式)。
(2)工业上,可利用硫酸亚铁溶液和氧气在催化剂条件下制作铁黄(FeOOH),一种不溶于水的黄色固体,写出该反应的离子方程式:______________________________ 。
(3)从某工业废渣wg(主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工艺流程如图(部分操作和条件略):

已知:二氧化硅不溶于硫酸。
①滤渣的主要成分为__________ (填化学式)。
②写出步骤Ⅴ的化学方程式:______________________________ 。
③请写出验证硫酸亚铁溶液中是否存在 的实验方法:
的实验方法:______________________________ 。
④若提取过程中铁元素的损耗忽略不计,最终获得ng的氧化铁。则废渣中铁元素的质量分数为__________ 。
(1)古代中国四大发明之一的司南是由天然磁石制成的,其主要成分是
(2)工业上,可利用硫酸亚铁溶液和氧气在催化剂条件下制作铁黄(FeOOH),一种不溶于水的黄色固体,写出该反应的离子方程式:
(3)从某工业废渣wg(主要含二氧化硅、氧化铁、氧化镁)中提取氧化铁的工艺流程如图(部分操作和条件略):

已知:二氧化硅不溶于硫酸。
①滤渣的主要成分为
②写出步骤Ⅴ的化学方程式:
③请写出验证硫酸亚铁溶液中是否存在
 的实验方法:
的实验方法:④若提取过程中铁元素的损耗忽略不计,最终获得ng的氧化铁。则废渣中铁元素的质量分数为
您最近一年使用:0次
名校
解题方法
5 . 钠的化合物在日常生活中的应用非常广泛,回答下列问题:
Ⅰ.为了测定 和NaHCO3的混合物中
和NaHCO3的混合物中 的质量分数,某同学用如下装置完成实验。
的质量分数,某同学用如下装置完成实验。
(1)实验前首先要进行的操作是_______ 。
(2)某同学称取65.4g混合物于锥形瓶中,打开止水夹,通入 ,一段时间后,关闭止水夹,称量装置C,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间
,一段时间后,关闭止水夹,称量装置C,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间 。停止通
。停止通 ,装置C的质量增加30.8g。
,装置C的质量增加30.8g。

①两次通入 的目的分别是
的目的分别是_______ 、_______ 。
②混合物中 的质量为
的质量为_______ g。
Ⅱ.侯德榜“联合制碱法”将制碱技术发展到个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。

资料:沉淀池中的反应为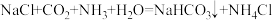 。
。
(3)操作1的名称为_______ ;煅烧炉中反应的化学方程式为_______ 。
(4)物质X可循环利用,其化学式为_______ 。
(5)工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与 反应可制得一种在生产、生活中常用于漂白、消毒的物质,同时有
反应可制得一种在生产、生活中常用于漂白、消毒的物质,同时有 生成,该反应的化学方程式是
生成,该反应的化学方程式是_______ 。
Ⅰ.为了测定
 和NaHCO3的混合物中
和NaHCO3的混合物中 的质量分数,某同学用如下装置完成实验。
的质量分数,某同学用如下装置完成实验。(1)实验前首先要进行的操作是
(2)某同学称取65.4g混合物于锥形瓶中,打开止水夹,通入
 ,一段时间后,关闭止水夹,称量装置C,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间
,一段时间后,关闭止水夹,称量装置C,打开旋塞,当锥形瓶中没有气泡生成时,关闭旋塞,再次打开止水夹,通入一段时间 。停止通
。停止通 ,装置C的质量增加30.8g。
,装置C的质量增加30.8g。
①两次通入
 的目的分别是
的目的分别是②混合物中
 的质量为
的质量为Ⅱ.侯德榜“联合制碱法”将制碱技术发展到个新的水平。该工艺以氯化钠为原料制取纯碱,主要流程如图所示(部分物质已略去)。

资料:沉淀池中的反应为
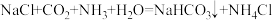 。
。(3)操作1的名称为
(4)物质X可循环利用,其化学式为
(5)工业可用纯碱代替烧碱生产某些化工产品,如用饱和纯碱溶液与
 反应可制得一种在生产、生活中常用于漂白、消毒的物质,同时有
反应可制得一种在生产、生活中常用于漂白、消毒的物质,同时有 生成,该反应的化学方程式是
生成,该反应的化学方程式是
您最近一年使用:0次
2022-11-04更新
|
151次组卷
|
2卷引用:内蒙古乌兰浩特市第四中学2022-2023学年高一上学期第三次月考化学试题
名校
解题方法
6 . 铁是人体必需的微量元素,铁摄入不足可能引起缺铁性贫血。黑木耳中含有比较丰富的铁元素,某研究型学习小组同学测定某地黑木耳中铁的含量。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。
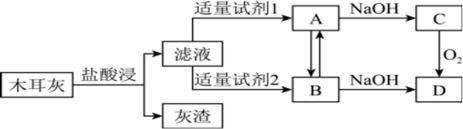
①浸泡液检测不出铁元素的原因是_______ 。
②试剂l应该是_______ 。
(2)A转化为B可加入的试剂有_______ 。
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为_______ 。
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为_______ L。
(1)称量黑木耳,将之洗净切碎,用蒸馏水浸泡,但浸泡液中未能检测到铁元素。高温灼烧黑木耳,使之完全灰化。将木耳灰用下图流程处理,对滤液中的溶质进行研究。

①浸泡液检测不出铁元素的原因是
②试剂l应该是
(2)A转化为B可加入的试剂有
a.酸性高锰酸钾 b.Cl2 c.H2O2溶液
(3)C生成D时的反应现象为
(4)已知在酸性条件下Fe2+可被氧气氧化为Fe3+,该反应每转移8mol电子,标准状况下消耗氧气的体积为
您最近一年使用:0次
名校
7 . A、B、C、D、E、F是原子序数依次增大的元素,其相关信息如下。
回答下列问题:
(1)元素A和E形成的化合物的电子式为___________ ,该化合物含有的化学键类型是___________ 。
(2)元素B在元素周期表中的位置为___________ ,其原子结构示意图为___________ 。
(3)元素D形成的单质在元素C形成的单质中燃烧的化学方程式为___________ ;元素D形成的单质久置于空气中最终得到的化合物的化学式为___________ 。
(4)下列事实,能证明元素E的非金属性强于S(硫)的非金属性的是___________(填字母)。
| 元素 | 特征 | 元素 | 特征 |
| A | 该元素的某种原子不含中子 | B | 简单氢化物的分子结构模型为 |
| C | 在人体中含量最多 | D | 该元素形成的化合物灼烧时火焰呈现黄色 |
| E | 该元素形成的单质常温下是黄绿色的有毒气体 | F | 由该元素形成的合金是目前我国用途最广的合金 |
(1)元素A和E形成的化合物的电子式为
(2)元素B在元素周期表中的位置为
(3)元素D形成的单质在元素C形成的单质中燃烧的化学方程式为
(4)下列事实,能证明元素E的非金属性强于S(硫)的非金属性的是___________(填字母)。
A.酸性: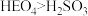 | B. 通入 通入 溶液能产生黄色沉淀 溶液能产生黄色沉淀 |
C.氢化物稳定性: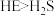 | D.常温下,E的单质为气态,S的单质为固态 |
您最近一年使用:0次
名校
解题方法
8 . W、X、Y、Z是原子序数依次增大的短周期主族元素,W与X、Y、Z不同周期,W为地壳中含量最多的元素,Y与W同主族,X的原子半径在短周期主族元素中是最大的。下列说法正确的是
| A.简单离子半径:X>Y>W |
| B.W与X形成的化合物中阴阳离子个数比为1∶1 |
| C.最简单氢化物的热稳定性:W<Y |
| D.Z形成的单质可用于自来水消毒 |
您最近一年使用:0次
2023-02-21更新
|
182次组卷
|
3卷引用:内蒙古乌兰浩特市第四中学2022-2023学年高一下学期开学考试化学试题
名校
解题方法
9 . A~G为中学常见的物质,其中A~F中含有同一种金属元素,各物质间有如下转化关系。其中B、G为地壳中含量排前两位的金属单质,D、F为碱,C、E为仅含两种元素的盐(部分条件已省略)。
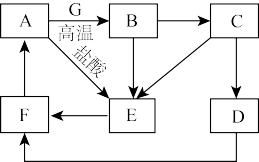
回答下列问题:
(1)A的化学式为___________ ;E溶液的颜色为___________ 色。
(2)E转化为F的离子方程式为___________ 。
(3)在溶液中D转化为F的现象为___________ 。
(4)某同学在老师的指导下展开了延伸学习,配制480mL C溶液。
C溶液。
①在配制C溶液时需加入少量铁屑,其目的是___________ 。
②在配制过程中,下列错误操作会导致所配溶液浓度(填“偏高”“偏低”或“无影响”)
a、用托盘天平称量时,左盘放砝码,并且使用游码:___________ ;
b、烧杯和玻璃棒未洗涤:___________ ;
c、定容时俯视刻度线:___________ 。

回答下列问题:
(1)A的化学式为
(2)E转化为F的离子方程式为
(3)在溶液中D转化为F的现象为
(4)某同学在老师的指导下展开了延伸学习,配制480mL
 C溶液。
C溶液。①在配制C溶液时需加入少量铁屑,其目的是
②在配制过程中,下列错误操作会导致所配溶液浓度(填“偏高”“偏低”或“无影响”)
a、用托盘天平称量时,左盘放砝码,并且使用游码:
b、烧杯和玻璃棒未洗涤:
c、定容时俯视刻度线:
您最近一年使用:0次
2023-01-07更新
|
198次组卷
|
4卷引用:内蒙古乌兰浩特市第四中学2022-2023学年高一下学期开学考试化学试题
10 . 设NA为阿伏加德罗常数的值,下列说法正确的是
| A.过量的铜与含0.2 mol HNO3的浓硝酸反应,转移电子的数目大于0.1NA |
| B.100 g质量分数17%H2O2溶液中含有H—O键数目为NA |
| C.标准状况下,11.2 L的HF中所含分子数为0.5NA |
| D.在K37C1O3+6H35Cl(浓)=KCl+3Cl2↑+3H2O反应中,若反应中电子转移的数目为10NA则有420 g氯气生成 |
您最近一年使用:0次
2020-12-02更新
|
123次组卷
|
2卷引用:内蒙古乌兰浩特市四中2022-2023 学年高三上学期第三次月考化学试题



