名校
解题方法
1 .  是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:
实验(一)制备 。
。
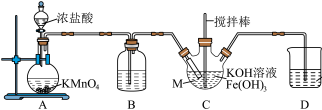
(1)仪器M的名称是_____ ,装置B的作用是_____ 。
(2)装置C中生成 的化学方程式为
的化学方程式为_____ 。
(3)实验得知装置D中吸收的 为装置A中生成
为装置A中生成 的25%,不考虑其他消耗,若装置D中生成的氧化产物只有
的25%,不考虑其他消耗,若装置D中生成的氧化产物只有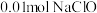 ,则生成
,则生成_____ 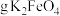 。
。
实验(二)探究 的性质。
的性质。

实验中观察到b中溶液变为蓝色,a中溶液由紫红色变为黄色,并产生气泡。
(4)酸R选择稀硫酸,不选择盐酸,其主要原因是_____ ;酸R选择稀硫酸时,从d口逸出的气体_____ (填“可以”或“不可以”)直接排放至大气中。
(5)当选用硫酸时,装置a中的离子方程式为_____ 。
(6)另设计一种方案确认有 产生:
产生:_____ 。
(7)向另一试管中的 溶液中滴加
溶液中滴加 溶液,溶液变为紫红色。不能证明氧化性:
溶液,溶液变为紫红色。不能证明氧化性: ,其原因是
,其原因是_____ 。
 是一种绿色净水剂,易溶于水。某小组在实验室条件下制备
是一种绿色净水剂,易溶于水。某小组在实验室条件下制备 并探究其性质。回答下列问题:
并探究其性质。回答下列问题:实验(一)制备
 。
。
(1)仪器M的名称是
(2)装置C中生成
 的化学方程式为
的化学方程式为(3)实验得知装置D中吸收的
 为装置A中生成
为装置A中生成 的25%,不考虑其他消耗,若装置D中生成的氧化产物只有
的25%,不考虑其他消耗,若装置D中生成的氧化产物只有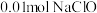 ,则生成
,则生成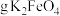 。
。实验(二)探究
 的性质。
的性质。
实验中观察到b中溶液变为蓝色,a中溶液由紫红色变为黄色,并产生气泡。
(4)酸R选择稀硫酸,不选择盐酸,其主要原因是
(5)当选用硫酸时,装置a中的离子方程式为
(6)另设计一种方案确认有
 产生:
产生:(7)向另一试管中的
 溶液中滴加
溶液中滴加 溶液,溶液变为紫红色。不能证明氧化性:
溶液,溶液变为紫红色。不能证明氧化性: ,其原因是
,其原因是
您最近一年使用:0次
2023-09-28更新
|
89次组卷
|
2卷引用:湖南省三湘创新发展联合体2023-2024学年高三上学期9月月考化学试题
名校
解题方法
2 . 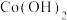 在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用
在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用 盐酸将其恰好完全溶解,得到
盐酸将其恰好完全溶解,得到 溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是

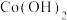 在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用
在空气中加热时,固体(不含其他杂质)质量随温度变化的曲线如图所示,取400℃时的产物[其中Co的化合价为+2、+3,分别表示为Co(II)、Co(III)],用 盐酸将其恰好完全溶解,得到
盐酸将其恰好完全溶解,得到 溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
溶液和4.48L(标准状况)黄绿色气体。下列说法错误的是
A.290℃时,若固体中只含有两种元素,则为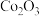 |
B.400℃时, |
| C.500℃时,固体中氧元素质量分数约为26.6% |
| D.生成的黄绿色气体可用于工业上生产“84”消毒液 |
您最近一年使用:0次
2022-10-18更新
|
529次组卷
|
3卷引用:湖南省长沙市湖南师范大学附属中学2022-2023学年高三上学期月考化学试题(二)
名校
解题方法
3 . 下列表示对应化学反应的离子方程式正确的是
A.用过量氨水吸收工业尾气中的 : :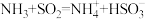 |
B.向NaClO溶液中加入少量 : :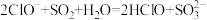 |
C.等物质的量的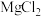 、 、 、HCl三种溶液混合: 、HCl三种溶液混合: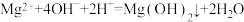 |
D. 溶液与 溶液与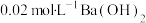 溶液等体积混合: 溶液等体积混合:  |
您最近一年使用:0次
解题方法
4 . 工业上用某矿渣(含有 )提取铜的操作流程如下:
)提取铜的操作流程如下:

已知: 。
。
回答下列问题:
(1)操作I的名称为___________ ;灼烧操作中常用的实验仪器有酒精灯、三脚架,还有___________ (夹持仪器不写)。
(2)固体混合物B的主要成分为___________ (写化学式);滤液A中铁元素的存在形式只能为 ,理由是
,理由是___________ (用离子方程式解释)。检验滤液A中 的试剂为
的试剂为___________ (填试剂名称)。
(3)滤液C中铝元素的主要存在形式为___________ (填离子符号),写出生成该离子的离子方程式:___________ 。
(4)某同学认为滤液 的水解程度是微弱的,
的水解程度是微弱的, 的水解不超过总量的10%,请设计实验验证该同学的观点是否正确:
的水解不超过总量的10%,请设计实验验证该同学的观点是否正确:___________ (所用材料: 试纸、
试纸、 的
的 溶液)。
溶液)。
(5)从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,主要步骤:称取一定质量的样品→___________ (填缺少的操作步骤,不必描述操作过程的细节)→过滤、洗涤、干燥→称量剩余固体铜的质量。
 )提取铜的操作流程如下:
)提取铜的操作流程如下:
已知:
 。
。回答下列问题:
(1)操作I的名称为
(2)固体混合物B的主要成分为
 ,理由是
,理由是 的试剂为
的试剂为(3)滤液C中铝元素的主要存在形式为
(4)某同学认为滤液
 的水解程度是微弱的,
的水解程度是微弱的, 的水解不超过总量的10%,请设计实验验证该同学的观点是否正确:
的水解不超过总量的10%,请设计实验验证该同学的观点是否正确: 试纸、
试纸、 的
的 溶液)。
溶液)。(5)从浓硫酸、浓硝酸、蒸馏水中选用合适的试剂,测定粗铜样品中金属铜的质量分数,主要步骤:称取一定质量的样品→
您最近一年使用:0次
2022-10-13更新
|
281次组卷
|
2卷引用:湖南省邵阳市部分校2022-2023学年高三上学期第一次联考化学试题
5 . 由硫铁矿烧渣(主要成分为Fe2O3、Fe3O4、Al2O3和SiO2)得到绿矾(FeSO4·7H2O),然后制取透明氧化铁颜料的流程如下:

已知:Ⅰ.透明氧化铁又称纳米氧化铁,粒子直径微小(10~90 nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
Ⅱ.Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)基态Fe2+的价层电子排布图为_______ 。
(2)“滤渣”中的主要成分是_______ 。
(3)流程中“ ”环节的目的是
”环节的目的是_______ 。
(4)“还原”过程中涉及的离子方程式为_______ 。
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以_______ 。
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:

称取3.47 g透明氧化铁,用稀硫酸溶解并定容至1 L,准确移取该溶液10.00 mL,加入足量KSCN溶液,再用蒸馏水定容至100 mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红的质量分数为_______ %(保留小数点后一位);若吸光度A减小,则氧化铁红的含量将_______ (填“增大”或“减小”)。

已知:Ⅰ.透明氧化铁又称纳米氧化铁,粒子直径微小(10~90 nm),包括氧化铁黄(FeOOH)和氧化铁红(Fe2O3),难溶于水,在碱性条件下非常稳定;
Ⅱ.Fe3+能将FeS2中的硫元素氧化为+6价。
回答下列问题:
(1)基态Fe2+的价层电子排布图为
(2)“滤渣”中的主要成分是
(3)流程中“
 ”环节的目的是
”环节的目的是(4)“还原”过程中涉及的离子方程式为
(5)“沉淀”采用分批加入KOH溶液,并不断搅拌,这样操作不但可以得到均匀、色泽纯正的氢氧化铁,而且还可以
(6)可用分光光度法测定制得的透明氧化铁中氧化铁黄和氧化铁红的含量。已知Fe(SCN)3的吸光度A(对特定波长光的吸收程度)与Fe3+标准溶液浓度的关系如图所示:

称取3.47 g透明氧化铁,用稀硫酸溶解并定容至1 L,准确移取该溶液10.00 mL,加入足量KSCN溶液,再用蒸馏水定容至100 mL。测得溶液吸光度A=0.8,则透明氧化铁中氧化铁红的质量分数为
您最近一年使用:0次
2022-09-30更新
|
221次组卷
|
2卷引用:湖南省长沙市第一中学2022-2023学年高三上学期月考(一)化学试题
名校
解题方法
6 . 固体盐X由四种常见元素组成,其中仅含一种金属元素,有如图转化关系:
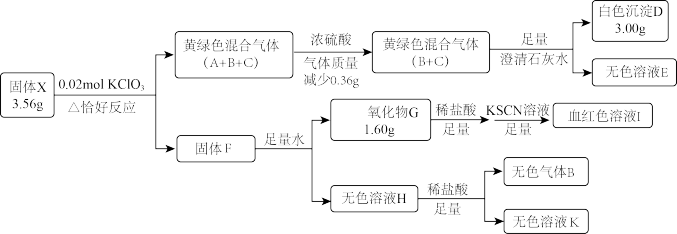
已知:H中溶质仅为一种常见正盐。黄绿色气体C密度为相同条件下H2的33.75倍。
请回答:
(1)X的组成元素为_______ ,固体F成分为_______ 。
(2)固体X在水中也可反应生成气体B,同时生成一种的相对较稳定的白色沉淀,请写出该反应化学方程式_______ 。
(3)气体C的化学式为_______ 。将气体C通入KOH溶液,微热,恰好完全反应,生成两种物质的量之比1∶5的盐,写出这两种盐的化学式_______ ,设计定量实验方案验证上述比例关系_______ 。(已知AgClO3溶于水,NaNO2能将ClO3-还原为Cl-)

已知:H中溶质仅为一种常见正盐。黄绿色气体C密度为相同条件下H2的33.75倍。
请回答:
(1)X的组成元素为
(2)固体X在水中也可反应生成气体B,同时生成一种的相对较稳定的白色沉淀,请写出该反应化学方程式
(3)气体C的化学式为
您最近一年使用:0次
名校
7 . 现有 的
的 ,将其加热并发生反应,并检测放出的气体1的质量,后向剩余固体a中加入足量的浓盐酸,并检测放出的气体2的质量。(已知,+4价的
,将其加热并发生反应,并检测放出的气体1的质量,后向剩余固体a中加入足量的浓盐酸,并检测放出的气体2的质量。(已知,+4价的 能和浓盐酸反应放出
能和浓盐酸反应放出 。
。 受热可分解为
受热可分解为 的+4、+2价的混合氧化物并放出
的+4、+2价的混合氧化物并放出 )。则下列说法中正确的是
)。则下列说法中正确的是
 的
的 ,将其加热并发生反应,并检测放出的气体1的质量,后向剩余固体a中加入足量的浓盐酸,并检测放出的气体2的质量。(已知,+4价的
,将其加热并发生反应,并检测放出的气体1的质量,后向剩余固体a中加入足量的浓盐酸,并检测放出的气体2的质量。(已知,+4价的 能和浓盐酸反应放出
能和浓盐酸反应放出 。
。 受热可分解为
受热可分解为 的+4、+2价的混合氧化物并放出
的+4、+2价的混合氧化物并放出 )。则下列说法中正确的是
)。则下列说法中正确的是A.气体1的物质的量最多为 |
B.若物质的量,气体 气体 气体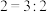 ,则固体的成分为物质的量之比可能为 ,则固体的成分为物质的量之比可能为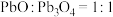 |
C.若物质的量,气体 气体 气体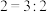 ,则固体a的成分为物质的量之比可能为 ,则固体a的成分为物质的量之比可能为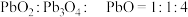 |
D.气体总物质的量可能为 |
您最近一年使用:0次
2022-08-17更新
|
479次组卷
|
2卷引用:湖南省邵阳市第二中学2022-2023学年高三上学期第三次月考化学试题
名校
解题方法
8 . 大多数离子液体含有体积很大的阴、阳离子(如图所示)。其中X、Y、Z为原子序数依次增大的短周期非金属元素,X、Z同主族。下列说法正确的是
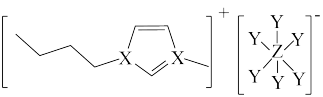

| A.原子半径:Z>X>Y | B.气态氢化物的稳定性:Z>X>Y |
| C.Z的氯化物的分子式一定为ZCl3 | D.此阴离子中Y、Z均满足8电子稳定结构 |
您最近一年使用:0次
2022-07-10更新
|
1346次组卷
|
7卷引用:湖南省株洲市攸县第二中学2022-2023学年高三上学期第三次月考化学试题
名校
解题方法
9 . 氧化铍(BeO)在航天航空等领域有着广泛的应用。一种以预处理后的硅铍矿(主要含BeO、Fe2O3、SiO2和FeO等)为原料提取BeO的流程如下图所示:

已知:Be(OH)2具有两性,在强碱性溶液中可转化为BeO 。下列说法错误的是
。下列说法错误的是

已知:Be(OH)2具有两性,在强碱性溶液中可转化为BeO
 。下列说法错误的是
。下列说法错误的是| A.“酸浸”步骤所得“滤渣①”的主要成分为Si |
| B.“滤液②”经处理后可获得副产品Na2SO4·10H2O |
C.“碱溶”时,主要反应为Be(OH)2+2OH-=BeO +2H2O +2H2O |
| D.“水解”时,适当增大溶液pH有利于提高BeO的提取率 |
您最近一年使用:0次
2022-05-23更新
|
1304次组卷
|
9卷引用:湖南省株洲市九方中学2022届高三下学期第二次模拟考试化学试题
湖南省株洲市九方中学2022届高三下学期第二次模拟考试化学试题湖南株洲南方中学2022-2023学年高三第四次月考化学试题广东省深圳市2021届高三4月第二次调研考试化学试题(已下线)卷05 工艺流程型选择题-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)专题13 物质的反应和转化-2022年高考真题模拟题分项汇编(已下线)第九章 化学实验基础及综合实验(测)-2023年高考化学一轮复习讲练测(全国通用)新疆喀什地区英吉沙县2022-2023学年高三上学期11月期中考试化学试题湖北省十堰市郧阳中学2023届高三11月月考化学训练题福建省福州第三中学2021-2022学年高一下学期期末考试化学试题
10 . 铂钌催化剂是甲醇燃料电池的阳极催化剂。一种以钌矿石[主要含Ru(CO3)2,还含少量的FeO、MgO、RuO4、CaO、SiO2]为原料制备钌(Ru)的流程如图。回答下列问题:
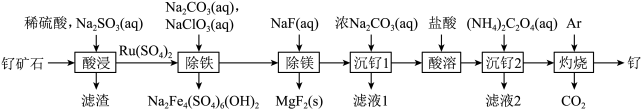
(1)Na2Fe4(SO4)6(OH)2中Fe的化合价为____ 。
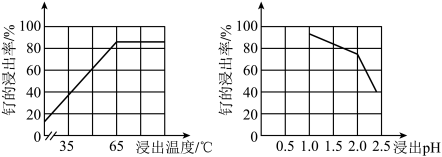
(2)“酸浸”时,Na2SO3的作用____ 。“滤渣”的主要成分有SiO2和____ (填化学式)。“酸浸”中钌的浸出率与浸出温度、pH的关系如图所示,“酸浸”的最佳条件是____ 。
(3)“除铁”的离子方程式为____ 。(提示:1molNaClO3参与反应,转移6mol电子)
(4)从“滤液2”中可提取一种化肥,其电子式为____ 。
(5)“灼烧”时Ar的作用是____ 。
(6)某工厂用10t钌矿石[含8.84tRu(CO3)2、165kgRuO4],最终制得3636kgRu,则Ru的产率为____ 。(保留三位有效数字)

(1)Na2Fe4(SO4)6(OH)2中Fe的化合价为
(2)“酸浸”时,Na2SO3的作用

(3)“除铁”的离子方程式为
(4)从“滤液2”中可提取一种化肥,其电子式为
(5)“灼烧”时Ar的作用是
(6)某工厂用10t钌矿石[含8.84tRu(CO3)2、165kgRuO4],最终制得3636kgRu,则Ru的产率为
您最近一年使用:0次
2022-05-10更新
|
1869次组卷
|
15卷引用:湖南省株洲市北附高级中学2022-2023学年高三上学期第五次月考化学试题
湖南省株洲市北附高级中学2022-2023学年高三上学期第五次月考化学试题河南省新乡市2022届高三第三次模拟理科综合化学试题河北省保定市2022届高三第二次模拟考试化学试题河南省名校联盟2022届高三下学期5月大联考理科综合化学试题(已下线)专题15工艺流程题-2022年高考真题+模拟题汇编(全国卷)(已下线)专题16工艺流程题-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题16工艺流程题-五年(2018~2022)高考真题汇编(全国卷)(已下线)专题15 工艺流程题-2022年高考真题模拟题分项汇编广东省广州市海珠外国语实验中学2022-2023学年高三上学期第二次阶段性考试化学试题福建省福州第一中学2022-2023学年高三上学期检考前适应性考试化学试题(已下线)专题29 无机化工流程综合分析-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)考前特训 [综合大题分类规范练](已下线)专题01 工艺流程专题-【大题精做】冲刺2023年高考化学大题突破+限时集训(新高考专用)山东新高考2022-2023学年高一上学期质量测评模拟演练化学试题 四川省泸州市泸县第一中学2023-2024学年高一上学期1月期末化学试题



