名校
1 . 向两份20 ml 0.1 mol/LBa(OH)2溶液中各加入定量的KAl(SO4)2和Al2(SO4)3溶液的导电性随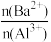 (混合前)的变化关系如图所示,下列分析不正确的是
(混合前)的变化关系如图所示,下列分析不正确的是
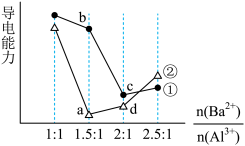
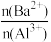 (混合前)的变化关系如图所示,下列分析不正确的是
(混合前)的变化关系如图所示,下列分析不正确的是
| A.a点溶液的pH值约为7 | B.b点溶液中大量存在的阳离子有Al3+和Ba2+ |
| C.c、d两点溶液中OH-均已完全反应 | D.②代表加入Al2(SO4)3的变化曲线 |
您最近一年使用:0次
2023-01-05更新
|
967次组卷
|
3卷引用:安徽省皖南八校2022-2023学年高三上学期第一次大联考化学试题
10-11高三·江西·阶段练习
名校
解题方法
2 . 两种硫酸盐按一定比例混合后共熔,可制得化合物X,且X溶于水能电离出K+、Cr3+、SO ,若将2.83gX中的Cr3+全部氧化为Cr2O
,若将2.83gX中的Cr3+全部氧化为Cr2O 后,溶液中的Cr2O
后,溶液中的Cr2O 可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为Cr2O
可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为Cr2O +6I-+14H+=2Cr3++3I2+7H2O。若向溶有2.83gX的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀。由此可推断出X的化学式为
+6I-+14H+=2Cr3++3I2+7H2O。若向溶有2.83gX的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀。由此可推断出X的化学式为
 ,若将2.83gX中的Cr3+全部氧化为Cr2O
,若将2.83gX中的Cr3+全部氧化为Cr2O 后,溶液中的Cr2O
后,溶液中的Cr2O 可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为Cr2O
可和过量KI溶液反应,得到3.81gI2,反应的离子方程式为Cr2O +6I-+14H+=2Cr3++3I2+7H2O。若向溶有2.83gX的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀。由此可推断出X的化学式为
+6I-+14H+=2Cr3++3I2+7H2O。若向溶有2.83gX的溶液中,加入过量的BaCl2溶液,可得到4.66g白色沉淀。由此可推断出X的化学式为| A.K2SO4•2Cr2(SO4)3 | B.K2SO4•Cr2(SO4)3 |
| C.2K2SO4•Cr2(SO4)3 | D.K2SO4• Cr2(SO4)3 Cr2(SO4)3 |
您最近一年使用:0次
2022-11-21更新
|
286次组卷
|
11卷引用:2012届安徽省宿州市高三第一次教学质量检测化学试卷
(已下线)2012届安徽省宿州市高三第一次教学质量检测化学试卷(已下线)2012届江西省白鹭洲中学高三第一次月考化学试卷(已下线)2015届江西省奉新县第一中学高三上学期第一次月考化学试卷辽宁省六校2021届高三上学期期中联考化学试题广东省中山纪念中学2021届高三上学期第一次月考化学试题(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点05 氧化还原反应-备战2022年高考化学一轮复习考点帮(浙江专用)宁夏石嘴山市第三中学2021-2022学年高三上学期期中考试化学(理)试题甘肃省天水一中2017-2018学年高一下学期入学考试化学试题豫中名校2022-2023学年高一上学期期中考试化学试题重庆市南开中学2022-2023学年高一上期期末考试化学试题
解题方法
3 . 某化学兴趣小组设计实验来测定某种天然黄铜矿(主要成分是CuFeS2,含SiO2杂质)的纯度。
(1)实验装置合理的连接顺序为____ 。

(2)现称取样品2.5g,研细后放在装置A的硬质玻璃管中煅烧。将黄铜矿研细的目的是____ ,装置B的作用是____ 。
(3)上述实验在反应后还要通入一段时间空气,其作用是____ (填标号,可以多选)。
a.除去SO2气体 b.有利于气体混合
c.除去反应后多余的氧气 d.使反应生成的SO2全部进入C装置中,使结果精确
(4)实验后取C中溶液的 于锥形瓶中,用0.05mol/L标准碘溶液进行滴定。滴定时主要发生的反应化学方程式是
于锥形瓶中,用0.05mol/L标准碘溶液进行滴定。滴定时主要发生的反应化学方程式是____ 。若达终点时,消耗标准溶液20.00mL,则黄铜矿的纯度为____ 。
(5)装置D可除去空气中的水蒸气,还能观察空气流速,若流速过快,可能会导致测定结果____ (填“偏高”“偏低”或“无影响”)。
(6)若将装置C中的溶液改为Ba(OH)2,测得的黄铜矿纯度会产生误差,假设实验操作均正确,可能的原因主要有____ (写出一点即可)。
(1)实验装置合理的连接顺序为

(2)现称取样品2.5g,研细后放在装置A的硬质玻璃管中煅烧。将黄铜矿研细的目的是
(3)上述实验在反应后还要通入一段时间空气,其作用是
a.除去SO2气体 b.有利于气体混合
c.除去反应后多余的氧气 d.使反应生成的SO2全部进入C装置中,使结果精确
(4)实验后取C中溶液的
 于锥形瓶中,用0.05mol/L标准碘溶液进行滴定。滴定时主要发生的反应化学方程式是
于锥形瓶中,用0.05mol/L标准碘溶液进行滴定。滴定时主要发生的反应化学方程式是(5)装置D可除去空气中的水蒸气,还能观察空气流速,若流速过快,可能会导致测定结果
(6)若将装置C中的溶液改为Ba(OH)2,测得的黄铜矿纯度会产生误差,假设实验操作均正确,可能的原因主要有
您最近一年使用:0次
名校
解题方法
4 . 碲被誉为“现代工业的维生素”,它在地壳中的丰度值很低。某科研小组从粗铜精炼的阳极泥(主要含有 )中提取粗碲的工艺流程如下图所示。下列说法
)中提取粗碲的工艺流程如下图所示。下列说法不正确 的是
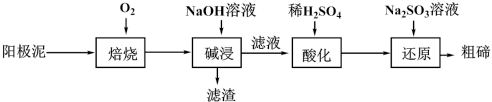
已知:①“焙烧”后,碲主要以 形式存在;②
形式存在;② 微溶于水,易溶于强酸和强碱。
微溶于水,易溶于强酸和强碱。
 )中提取粗碲的工艺流程如下图所示。下列说法
)中提取粗碲的工艺流程如下图所示。下列说法
已知:①“焙烧”后,碲主要以
 形式存在;②
形式存在;② 微溶于水,易溶于强酸和强碱。
微溶于水,易溶于强酸和强碱。| A.“焙烧”用到的主要仪器有:坩埚、泥三角、三角架、酒精灯、玻璃棒 |
| B.“碱浸”后所得的滤渣中含有Au、Ag,可用稀盐酸将其分离 |
C.“碱浸”时,反应的离子方程式为 |
D.“还原”时, 作还原剂 作还原剂 |
您最近一年使用:0次
2022-01-14更新
|
286次组卷
|
2卷引用:安徽省黄山市2021-2022学年高三上学期第一次理科综合测试化学试题
解题方法
5 . 二氧化铈 是一种重要的稀土氧化物。平板电视显示屏生产过程中会产生大量的废玻璃粉末(含
是一种重要的稀土氧化物。平板电视显示屏生产过程中会产生大量的废玻璃粉末(含 、
、 、
、 以及其他少量不溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
以及其他少量不溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:

回答下列问题:
(1) 中
中 元素的化合价为
元素的化合价为___________ 。为了提高废旧玻璃粉末浸出速率,除适当增加 溶液的浓度外,还可采取的措施有
溶液的浓度外,还可采取的措施有___________ (写出任一点)。
(2)向含 的滤渣中加入稀硫酸、
的滤渣中加入稀硫酸、 酸浸时发生反应的离子方程式为
酸浸时发生反应的离子方程式为___________ 。
(3)写出“碱浸、沉铈”过程中发生反应的化学方程式:___________ 。
(4)电解熔融的 可在阴极获得
可在阴极获得 ,写出阴极的电极反应式:
,写出阴极的电极反应式:___________ 。
(5)“碱浸、沉铈”后所得沉淀经过滤、洗涤、干燥后,称重得 纯净
纯净 ,最后熔融电解制得
,最后熔融电解制得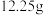 铈,则所制得铈的产率为
铈,则所制得铈的产率为___________ %。
 是一种重要的稀土氧化物。平板电视显示屏生产过程中会产生大量的废玻璃粉末(含
是一种重要的稀土氧化物。平板电视显示屏生产过程中会产生大量的废玻璃粉末(含 、
、 、
、 以及其他少量不溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
以及其他少量不溶于稀酸的物质)。某课题组以此粉末为原料回收铈,设计实验流程如下:
回答下列问题:
(1)
 中
中 元素的化合价为
元素的化合价为 溶液的浓度外,还可采取的措施有
溶液的浓度外,还可采取的措施有(2)向含
 的滤渣中加入稀硫酸、
的滤渣中加入稀硫酸、 酸浸时发生反应的离子方程式为
酸浸时发生反应的离子方程式为(3)写出“碱浸、沉铈”过程中发生反应的化学方程式:
(4)电解熔融的
 可在阴极获得
可在阴极获得 ,写出阴极的电极反应式:
,写出阴极的电极反应式:(5)“碱浸、沉铈”后所得沉淀经过滤、洗涤、干燥后,称重得
 纯净
纯净 ,最后熔融电解制得
,最后熔融电解制得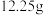 铈,则所制得铈的产率为
铈,则所制得铈的产率为
您最近一年使用:0次
6 . 铬及其化合物在工业上有重要的用途。铬元素的化合价可以是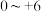 的整数价态。请根据如下转化关系图回答问题:
的整数价态。请根据如下转化关系图回答问题:
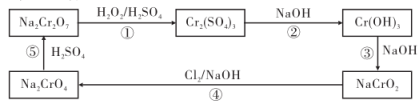
(1)框图中的含铬化合物中,铬元素为 价的盐有
价的盐有___________ 。
(2)反应①中氧化剂与还原剂的物质的量之比为___________ 。
(3)根据反应②、③,知 类似
类似 具有两性,请写出
具有两性,请写出 的酸式电离方程式:
的酸式电离方程式:___________ 。
(4)反应④的离子方程式为___________ 。
(5)目前处理酸性 废水多采用铁氧磁体法。该法是向废水中加入
废水多采用铁氧磁体法。该法是向废水中加入 将
将 还原成
还原成 ,调节
,调节 ,
, 、
、 全部转化成相当于
全部转化成相当于 (铁氧磁体,罗马数字表示元素价态)的沉淀。处理
(铁氧磁体,罗马数字表示元素价态)的沉淀。处理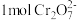 ,需加入
,需加入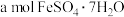 ,下列有关结论正确的是___________。
,下列有关结论正确的是___________。
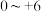 的整数价态。请根据如下转化关系图回答问题:
的整数价态。请根据如下转化关系图回答问题:
(1)框图中的含铬化合物中,铬元素为
 价的盐有
价的盐有(2)反应①中氧化剂与还原剂的物质的量之比为
(3)根据反应②、③,知
 类似
类似 具有两性,请写出
具有两性,请写出 的酸式电离方程式:
的酸式电离方程式:(4)反应④的离子方程式为
(5)目前处理酸性
 废水多采用铁氧磁体法。该法是向废水中加入
废水多采用铁氧磁体法。该法是向废水中加入 将
将 还原成
还原成 ,调节
,调节 ,
, 、
、 全部转化成相当于
全部转化成相当于 (铁氧磁体,罗马数字表示元素价态)的沉淀。处理
(铁氧磁体,罗马数字表示元素价态)的沉淀。处理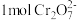 ,需加入
,需加入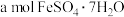 ,下列有关结论正确的是___________。
,下列有关结论正确的是___________。A.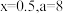 | B.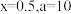 |
C.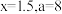 | D. |
您最近一年使用:0次
13-14高三·宁夏银川·阶段练习
名校
解题方法
7 . 足量铜与一定量的浓硝酸反应,得到硝酸铜溶液和二氧化氮、一氧化氮的混合气体2.24L(标准状况),这些气体与一定体积(标准状况)氧气混合后通入水中,所有气体完全被水吸收生成硝酸。若向所得硝酸铜溶液中加入4mol·L-1氢氧化钠溶液至铜离子恰好完全沉淀,则消耗氢氧化钠溶液的体积是50mL,下列说法正确的是
| A.混合气体中含二氧化氮1.12L |
| B.消耗氧气的体积为1.68L |
| C.此反应过程中转移的电子为0.3mol |
| D.参加反应的硝酸是0.4mol |
您最近一年使用:0次
2021-08-25更新
|
797次组卷
|
30卷引用:安徽省芜湖市2021届高三第二次月考化学试题
安徽省芜湖市2021届高三第二次月考化学试题(已下线)2015届宁夏银川一中高三第四次月考化学试卷2015届山东省滕州市三中上学期高三第四次月考理综化学试卷2016届河南省扶沟县高级中学高三上学期开学考试化学试卷2016届河南省三门峡市陕州中学高三上学期第一次精英对抗赛化学试卷2016届重庆市万州第二高级中学高三上学期期中测试理综化学试卷2016届河南省信阳市鸡公山风景区学校高三下2月月考化学试卷2015-2016学年安徽省六安一中高一下周末作业二化学试卷2015-2016学年安徽师大附中高一下学期期中考查化学试卷2017届广西桂林市第十八中学高三上第二次月考化学试卷2018届高三一轮复习化学:考点21-铜及其化合物性质探究(已下线)《考前20天终极攻略》-5月26日 元素及其化合物河南省漯河市临颍县南街高级中学2020届高三阶段性测试化学试题(已下线)专题13 氮及其化合物 (热点讲义)-2022年高三毕业班化学常考点归纳与变式演练 内蒙古自治区包钢第一中学2021-2022学年高三上学期10月月考化学试题2014-2015吉林省松原市扶余县一中高一上学期期末化学试卷2015-2016学年河北省冀州中学高一下开学考试化学试卷2015-2016学年山东省淄博六中高一下学科竞赛化学试卷福建省三明市第一中学2018-2019学年高二上学期开学考化学试题云南省新平县一中2018-2019学年高一上学期12月月考化学试题贵州省黔南布依族苗族自治州龙里中学2019-2020学年高一上学期期末考试化学试题辽宁省大连市一〇三中学2019-2020学年高一下学期期中考试化学试题江西省高安中学2020-2021学年高一上学期期末考试化学试题四川省邻水实验学校2020-2021学年高一下学期第一次月考化学试题福建省福州第三中学2020-2021学年高一下学期期中考化学试题(已下线)专题02 氮及其化合物【专项训练】-2020-2021学年高一化学下学期期末专项复习(人教版2019必修第二册)浙江省诸暨市第二高级中学2020-2021学年高二下学期期中考试化学试题重庆市第七中学校2021-2022学年高一下学期3月月考化学试题云南省普洱市镇沅彝族哈尼族拉祜族自治县第一中学2021-2022学年高一下学期4月份考试化学试题湖南省怀化市沅陵县第一中学2021-2022学年高一下学期第一次月考化学试题
8 . 化合物X在一定条件下可发生如图转化,有关叙述错误的是


A.溶液C到溶液D中发生的离子方程式为:Fe3++3SCN— Fe(SCN)3 Fe(SCN)3 |
| B.E为CO,物质的量为0.05mol |
| C.X为Fe(CO)4 |
| D.过量的稀硫酸若换成盐酸,会造成环境污染 |
您最近一年使用:0次
2021-06-30更新
|
2098次组卷
|
7卷引用:安徽省淮北市2021届高三第一次模拟考试化学试题
安徽省淮北市2021届高三第一次模拟考试化学试题(已下线)专题三 能力提升检测卷 (测) — 2022年高考化学一轮复习讲练测(新教材新高考)辽宁省实验中学2022届高三第一次阶段性考试化学试题(已下线)专题06 常见金属及其化合物-备战2022年高考化学学霸纠错(全国通用)(已下线)专题14物质的反应和转化-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题13物质的反应和转化-2022年高考真题+模拟题汇编(全国卷)(已下线)专题14物质的反应和转化-五年(2018~2022)高考真题汇编(全国卷)
9 . 在实验室采用如图装置制备气体,合理的是
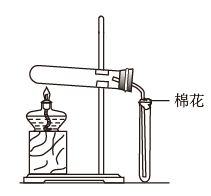
| 化学试剂 | 制备的气体 | |
| A | 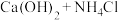 |  |
| B | 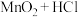 (浓) (浓) |  |
| C | 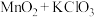 |  |
| D | 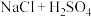 (浓) (浓) |  |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-06-09更新
|
21809次组卷
|
50卷引用:安徽省砀山县第四中学2022-2023学年高三上学期第一次月考化学试题
安徽省砀山县第四中学2022-2023学年高三上学期第一次月考化学试题安徽省亳州市第五完全中学2021-2022学年高三上学期期中考试化学试题安徽省六安市裕安区新安中学2022-2023学年高三上学期第三次月考化学试题2021年高考全国乙卷化学真题(已下线)第29讲 化学综合实验(精练)-2022年高考化学一轮复习讲练测(已下线)考点31 物质的制备 定量分析-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点34 物质的制备与合成-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)课时53 简单实验方案的设计与评价-2022年高考化学一轮复习小题多维练(全国通用)宁夏中卫市中宁县第一中学2021-2022学年高三上学期第一次月考化学试题内蒙古北京八中乌兰察布分校2021-2022学年高三上学期学科素养评估一化学试题(已下线)专题13 化学实验-备战2022年高考化学学霸纠错(全国通用)(已下线)第29讲 常见气体的制备与性质实验(讲) — 2022年高考化学一轮复习讲练测(新教材新高考)(已下线)2021年高考全国乙卷化学试题变式题(已下线)专题07 非金属及其化合物-2022年高考化学二轮复习重点专题常考点突破练(已下线)解密11 化学实验基础(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(浙江专用)(已下线)解密11 化学实验(讲义)-【高频考点解密】2022年高考化学二轮复习讲义+分层训练(全国通用)(已下线)专题05 化学基础实验—2022年高考化学二轮复习讲练测(全国版)-练习(已下线)秘籍04 实验仪器使用与基本操作-备战2022年高考化学抢分秘籍(全国通用)(已下线)卷01 小题仿真卷-【小题小卷】冲刺2022年高考化学小题限时集训(新高考专用)(已下线)押全国卷理综第9题 化学实验基础-备战2022年高考化学临考题号押题(课标全国卷)(已下线)查补易混易错点08 化学实验基础-【查漏补缺】2022年高考化学三轮冲刺过关(全国通用)(已下线)专题11 基本实验专练(已下线)专题11化学实验基础-三年(2020~2022)高考真题汇编(全国卷)(已下线)专题11化学实验基础-五年(2018~2022)高考真题汇编(全国卷)(已下线)微专题24 氯气、氨气、二氧化硫的实验室制备与应用-备战2023年高考化学一轮复习考点微专题(已下线)考点51 物质的制备-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)专题讲座(四) 常见气体的实验室制备、净化和收集(练)-2023年高考化学一轮复习讲练测(全国通用)(已下线)第27讲 物质的制备与性质实验(讲)-2023年高考化学一轮复习讲练测(新教材新高考)(已下线)专题23 化学实验基础性选择题-2023年高考化学毕业班二轮热点题型归纳与变式演练(新高考专用)(已下线)第一部分 二轮专题突破 专题18 物质检验、鉴别简单实验方案的设计及评价第四章 非金属及其化合物 第24讲 常见气体的实验室制备、净化和收集(已下线)素养卷07 微型物质制备方案设计-【小题小卷】冲刺2023年高考化学小题限时集训(新高考专用)(已下线)专题07 无机物的转化 微型工艺流程-2023年高考化学真题题源解密(全国通用)(已下线)微专题 常见气体的实验室制备、净化和收集(已下线)考点44 化学实验基础(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)(已下线)第3讲 物质制备实验的设计与评价黑龙江省大庆市肇州县第二中学2023-2024学年高三上学期11月月考化学试题河南省三门峡市实验高中2020-2021学年高二下学期6月月考化学试题河北省辛集中学 2020-2021学年高二下学期期末考试化学试题山西省实验中学2021-2022学年高二下学期开学分班素质测试化学试题四川省眉山市彭山区第一中学2021-2022学年高二上学期入学考试化学试题四川省邻水实验学校2021-2022学年高二上学期第一次月考化学试题陕西省西北农林科技大学附属中学2021-2022学年高一上学期期末考试化学试题甘肃省张掖市高台县第一中学2022-2023学年高一上学期期中考试化学试题湖南省郴州市汝城县第一中学2022-2023学年高一上学期期中考试化学试题山西省实验中学2021-2022学年高二上学期开学考试化学试题(已下线)专题04 常见气体的实验室制取(专题过关)-2022-2023学年高一化学下学期期中期末考点大串讲(人教版2019必修第二册)云南省开远市第一中学校2023-2024学年高一上学期9月半月考试化学试题章末知识整合吉林省通化市辉南县第六中学2023-2024学年高一下学期3月半月考化学试卷
14-15高三上·安徽·阶段练习
名校
解题方法
10 . 向体积均为10mL且物质的量浓度相同的两份NaOH溶液中分别通入一定量的CO2得到溶液甲和乙。向甲、乙两溶液中分别滴加0.1 mol·L-1盐酸。此时反应生成CO2体积(标准状况)与所加盐酸体积间的关系如图所示。则下列叙述中正确的是
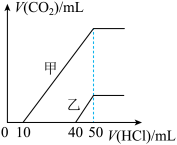

| A.乙溶液中含有的溶质是Na2CO3、NaHCO3 |
| B.当0<V(HCl)<10 mL时,甲溶液中发生反应的离子方程式为OH-+H+ =H2O |
| C.原NaOH溶液的物质的量浓度为0.5mol·L-1 |
| D.乙溶液中滴加盐酸后产生CO2体积的最大值为112 mL(标准状况) |
您最近一年使用:0次
2021-05-28更新
|
2622次组卷
|
25卷引用:2014届安徽省“江淮十校”协作体高三上学期第一次联考化学试卷
(已下线)2014届安徽省“江淮十校”协作体高三上学期第一次联考化学试卷2016届山东省威海市乳山市高三上学期期中测试化学试卷2017届河北省涞水县波峰中学高三8月月考化学试卷河南省豫南豫北名校2018届高三精英联赛化学试题1陕西省陕师大附中2018届高三第五次月考化学试题河南省豫南豫北名校2018届高三精英联赛化学试题2【全国百强校】天津市第一中学2019届高三上学期第一次月考化学试题【全国百强校】甘肃省天水市第一中学2019届高三上学期一轮复习第二次质量检测化学试题(已下线)2019年1月14日 《每日一题》高考二轮复习-钠及其化合物上海市十二校2015届高三12月联考化学试题天津一中2020届高三第二次月考化学试题福建省福州市第三中学2020-2021学年高三上学期第二次质量检测化学试题(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(全国通用)(已下线)考点13 钠及其化合物-备战2022年高考化学一轮复习考点帮(浙江专用)(已下线)考点13 钠及其化合物-备战2023年高考化学一轮复习考点帮(全国通用)(已下线)考点09 钠及其重要化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(新高考专用)(已下线)考点13 钠及其化合物(核心考点精讲精练)-备战2024年高考化学一轮复习考点帮(全国通用)2015-2016学年辽宁沈阳市第二中学高二下期末考化学卷【全国百强校】辽宁省沈阳市东北育才学校2018-2019学年高一上学期第二次月考化学试题河北省石家庄市第二十四中学2020-2021学年高二第二学期期中考试化学试题黑龙江省鹤岗市第一中学2020-2021学年高二6月月考化学试题广东省广州市三校2021-202学年高一上学期期末联考化学试题四川省南充高级中学2021-2022学年高一下学期开学考试化学试题陕西师范大学附属中学2023-2024学年高一上学期期中考试化学试题湖北省荆州市荆州中学2023-2024学年高一上学期期末考试化学试题



