名校
解题方法
1 . 铁有两种氯化物,都是重要的化工试剂。查阅有关资料如下:
氯化铁:熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点为670℃,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:
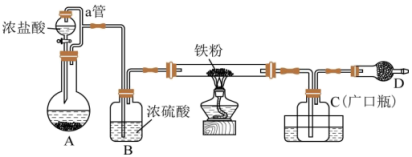
(1)装置A中,用KMnO4与浓盐酸反应制取氯气,写出反应的离子方程式:____________________ 。
(2)装置B的作用是______ ,导管a的作用是______ ,C放置在盛冷水的水槽中,冷水浴的作用是______ 。
(3)装置D中装的药品______ ,其作用是为了吸收未反应的Cl2防止污染环境。同时防止空气中的水进入装置C,使FeCl3潮解。
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.70 g产品溶于过量的稀盐酸中;②加入足量H2O2溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;
⑤称量所得红棕色固体为2.40 g。则该样品中铁元素的质量分数为______ %(结果精确到小数点后两位)。
(5)由(4)定量分析数据得出结论,并提出改进措施。
①用题目所给的装置制得的产物中,铁元素含量______ (填“相等”“偏高”或“偏低”),说明含有FeCl2杂质。
②若要得到较纯净的无水氯化铁,可采取的“装置”改进措施是____________________ 。
氯化铁:熔点为306℃,沸点为315℃;易吸收空气中的水分而潮解。工业上采用向500~600℃的铁粉中通入氯气来生产无水氯化铁。
氯化亚铁:熔点为670℃,可升华。工业上采用向炽热铁粉中通入氯化氢来生产无水氯化亚铁。
某化学活动小组用如图所示的装置(夹持装置略去)模拟工业生产制备无水氯化铁。请回答下列问题:

(1)装置A中,用KMnO4与浓盐酸反应制取氯气,写出反应的离子方程式:
(2)装置B的作用是
(3)装置D中装的药品
(4)定量分析。取装置C中的产物,按以下步骤进行测定:①称取4.70 g产品溶于过量的稀盐酸中;②加入足量H2O2溶液;③再加入足量NaOH溶液;④过滤、洗涤后灼烧沉淀;
⑤称量所得红棕色固体为2.40 g。则该样品中铁元素的质量分数为
(5)由(4)定量分析数据得出结论,并提出改进措施。
①用题目所给的装置制得的产物中,铁元素含量
②若要得到较纯净的无水氯化铁,可采取的“装置”改进措施是
您最近一年使用:0次
2 . 工业上“侯氏”制碱法制得的纯碱产品中常含有少量的NaCl。为测定纯碱产品中碳酸钠的含量,取23g样品置于烧杯中,加水将其溶解,然后逐滴滴入稀盐酸,当滴入200g稀盐酸时,两者恰好完全反应。生成的气体全部逸出,共收集到8.8g二氧化碳。求:
(1)所用稀盐酸中溶质的质量分数。_______
(2)23g样品中碳酸钠的质量分数(结果保留到0.1%)。_______
(1)所用稀盐酸中溶质的质量分数。
(2)23g样品中碳酸钠的质量分数(结果保留到0.1%)。
您最近一年使用:0次
解答题-实验探究题
|
适中(0.65)
|
名校
3 . 现用质量分数为98%、密度为1.84g·cm-3的浓H2SO4来配制500mL0.2mol·L-1的稀H2SO4.可供选择的仪器有:①玻璃棒、②烧瓶、③烧杯、④胶头滴管、⑤量筒、⑥容量瓶、⑦托盘天平、⑧药匙。请回答下列问题:
(1)上述仪器中,在配制稀H2SO4时用不到的有(填代号)_______ 。
(2)经计算,需浓H2SO4的体积为_______ 。现有①10mL、②50mL、③100mL三种规格的量筒,你选用的量筒是_______ 。(填代号)
(3)将浓H2SO4加入到适量蒸馏水中稀释后,冷却片刻,随后全部转移到_______ mL的容量瓶中,转移中应用玻璃棒_______ 。转移完毕,用少量蒸馏水洗涤烧杯和玻璃棒2~3次,并将洗涤液全部转移到容量瓶中,再加适量蒸馏水,振荡容量瓶,使溶液混合均匀。然后缓缓地把蒸馏水直接注入容量瓶,直到液面接近刻度线_______ 处。改用_______ 滴加蒸馏水,使溶液的_______ ,振荡、摇匀后,装瓶、贴签。
(4)在配制过程中,其他操作都准确,能引起误差偏高的有_______ (填代号)。
①洗涤量取浓H2SO4的量筒,并将洗涤液转移到容量瓶中
②稀释后的H2SO4溶液未等冷却至室温就转移到容量瓶中
③定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
④转移前,容量瓶中含有少量蒸馏水
⑤定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑥定容时,俯视刻度线
(1)上述仪器中,在配制稀H2SO4时用不到的有(填代号)
(2)经计算,需浓H2SO4的体积为
(3)将浓H2SO4加入到适量蒸馏水中稀释后,冷却片刻,随后全部转移到
(4)在配制过程中,其他操作都准确,能引起误差偏高的有
①洗涤量取浓H2SO4的量筒,并将洗涤液转移到容量瓶中
②稀释后的H2SO4溶液未等冷却至室温就转移到容量瓶中
③定容时,加蒸馏水超过刻度线,又用胶头滴管吸出
④转移前,容量瓶中含有少量蒸馏水
⑤定容摇匀后,发现液面低于刻度线,又用胶头滴管加蒸馏水至刻度线
⑥定容时,俯视刻度线
您最近一年使用:0次
4 . 用NA表示阿伏加德罗常数的值。下列说法正确的是
| A.100g质量分数为98%的浓硫酸中含有的氧原子数为4NA |
| B.0.1mol·L-1的NaOH溶液中含有的Na+数目为0.1NA |
| C.常温常压下,2.24L由CO和CO2组成的混合气体中含有的碳原子数为0.1NA |
| D.白磷与氯气反应可生成PCl3和PCl5,71g氯气与足量白磷充分燃烧时转移的电子数为2NA |
您最近一年使用:0次
2024-04-02更新
|
105次组卷
|
2卷引用:湖南省衡阳市祁东县成章高级中学2023-2024学年高一下学期入学考试化学试卷
5 . 下列有关阿伏加德罗常数( 表示阿伏加德罗常数的值)的说法正确的是
表示阿伏加德罗常数的值)的说法正确的是
A.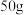 质量分数为 质量分数为 的乙醇溶液中氢原子数为 的乙醇溶液中氢原子数为 |
B.常温常压下, 中含有 中含有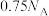 个原子 个原子 |
C.标准状况下, 水的体积约为 水的体积约为 |
D.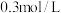 的 的 溶液中含有 溶液中含有 个 个 |
您最近一年使用:0次
名校
解题方法
6 . 向一定量的Fe、FeO、 的混合物中加入100mL1mol/L的盐酸,恰好便混合物完全溶解,放出336mL(标准状况下)的气体。所得溶液中加入KSCN溶液无红色出现,混合物中铁元素的质量分数为
的混合物中加入100mL1mol/L的盐酸,恰好便混合物完全溶解,放出336mL(标准状况下)的气体。所得溶液中加入KSCN溶液无红色出现,混合物中铁元素的质量分数为
| A.83.3% | B.57.8% | C.88.6% | D.78.6% |
您最近一年使用:0次
名校
7 . 下列有关实验原理或操作正确的是
| A.用20mL量筒量取15mL酒精,加水5mL,配制质量分数为75%酒精溶液 |
B.实验室配制500mL0.2mol/L的硫酸亚铁溶液,其操作是:用天平称15.2g绿矾 ,放入小烧杯中加水溶解,转移到500mL容量瓶,洗涤、稀释、定容、摇匀 ,放入小烧杯中加水溶解,转移到500mL容量瓶,洗涤、稀释、定容、摇匀 |
C.实验中需用2.0mol/L的 溶液950mL,配制时应选用的容量瓶的规格和称取 溶液950mL,配制时应选用的容量瓶的规格和称取 的质量分别为950mL、201.4g 的质量分别为950mL、201.4g |
D.在200mL某硫酸盐溶液中,含有 个硫酸根离子,同时含有 个硫酸根离子,同时含有 个金属离子,则该硫酸盐的物质的量浓度为2.5mol/L 个金属离子,则该硫酸盐的物质的量浓度为2.5mol/L |
您最近一年使用:0次
名校
解题方法
8 . 周南中学化学研究性学习小组请你参与“研究铁与水反应所得固体物质的成分、性质及再利用”实验探究,并回答下列问题:
探究一:设计如图所示装置进行“铁与水反应”的实验(夹持仪器略)。

(1)硬质玻璃管B中发生反应的化学方程式为___________ 。
(2)反应前A中投放碎瓷片的目的是___________ 。
(3)装置E中的现象是___________ 。
探究二:设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻管B冷却后,取少许其中的固体物质溶于___________ 后(写物质名称),将所得溶液分成两份。一份滴加几滴 溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为
溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为___________ (填序号)。
①一定有 ②一定有
②一定有 ③只有
③只有 ④只有
④只有
另一份用胶头滴管加入___________ (填试剂和现象),可以证明溶液中存在 。
。
探究三:设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(5)计算反应后B装置中铁元素的质量分数为___________ 。
探究一:设计如图所示装置进行“铁与水反应”的实验(夹持仪器略)。

(1)硬质玻璃管B中发生反应的化学方程式为
(2)反应前A中投放碎瓷片的目的是
(3)装置E中的现象是
探究二:设计如下实验方案确定反应后硬质玻璃管B中黑色固体的成分。
(4)待硬质玻管B冷却后,取少许其中的固体物质溶于
 溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为
溶液。若溶液变红色,推断硬质玻璃管B中固体物质的成分为①一定有
 ②一定有
②一定有 ③只有
③只有 ④只有
④只有
另一份用胶头滴管加入
 。
。探究三:设计如下流程测定反应后硬质玻璃管B中固体含铁元素的质量分数。

(5)计算反应后B装置中铁元素的质量分数为
您最近一年使用:0次
名校
9 . 溶液在日常生活、工农业生产和科学研究中具有广泛用途。
(1)60℃时,KNO3的溶解度为_______ 。
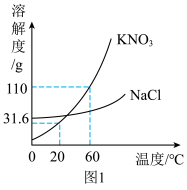
(2)20℃时,将20gKNO3加入到50g水中,充分溶解后所得溶液的质量为_______ g。
(3)除去KNO3溶液中混有的少量的NaCl,提纯的方法是_______ 。
(4)60℃,将KNO3和NaCl两种物质的饱和溶液降温至20℃,质量分数的大小关系为_______ 。
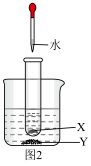
(5)探究温度对溶解度的影响,如图2所示。固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2,烧杯中盛放20℃Y的饱和溶液(有少量Y的固体则余),往试管中滴入适量水,烧杯中固体逐渐消失,写出X与Y可能的组合有_______ 。
(1)60℃时,KNO3的溶解度为

(2)20℃时,将20gKNO3加入到50g水中,充分溶解后所得溶液的质量为
(3)除去KNO3溶液中混有的少量的NaCl,提纯的方法是
(4)60℃,将KNO3和NaCl两种物质的饱和溶液降温至20℃,质量分数的大小关系为
(5)探究温度对溶解度的影响,如图2所示。固体X是NH4NO3或NaOH,固体Y是KNO3或Ca(OH)2,烧杯中盛放20℃Y的饱和溶液(有少量Y的固体则余),往试管中滴入适量水,烧杯中固体逐渐消失,写出X与Y可能的组合有

您最近一年使用:0次
名校
解题方法
10 . 下列图象能正确表示对应叙述的有

①向一定量硫酸和硫酸铜的混合溶液中逐滴加入氢氧化钠溶液
②向一定量的饱和氢氧化钙溶液中加入氧化钙
③向等质量、等质量分数的稀盐酸中分别加入锌和铁
④向一定量的盐酸和硫酸钠的混合溶液中逐滴加入氢氧化钡溶液

①向一定量硫酸和硫酸铜的混合溶液中逐滴加入氢氧化钠溶液
②向一定量的饱和氢氧化钙溶液中加入氧化钙
③向等质量、等质量分数的稀盐酸中分别加入锌和铁
④向一定量的盐酸和硫酸钠的混合溶液中逐滴加入氢氧化钡溶液
| A.1个 | B.2个 | C.3个 | D.4个 |
您最近一年使用:0次
2023-06-13更新
|
68次组卷
|
2卷引用:湖南省湘乡市第一中学2022-2023学年高一下学期开学考试化学试题



