1 . 下表是元素周期表的一部分,针对表中用字母标出的元素,回答下列问题:___________ (填标号);化学性质最不活泼的元素是___________ (填元素符号)。
(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是___________ (填化学式)。
(3)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序___________ (填化学式)。
(4)用电子式表示J与C形成化合物的过程:___________ 。
(5)请写出B的最高价氧化物对应的水化物与E发生反应的化学方程式:___________ 。

(2)A分别与G、H、I形成的最简单化合物中,稳定性最强的是
(3)B、C形成的最高价氧化物对应水化物的碱性从强到弱的顺序
(4)用电子式表示J与C形成化合物的过程:
(5)请写出B的最高价氧化物对应的水化物与E发生反应的化学方程式:
您最近一年使用:0次
2024-02-03更新
|
38次组卷
|
2卷引用:甘肃省白银市靖远县第四中学2023-2024学年高一下学期开学化学试题
名校
2 . 四种短周期元素在元素周期表中的位置如图所示,T是地壳中含量最高的金属元素。下列说法不正确的是
Q | |||
T | R | W |
| A.W的氢化物比R的氢化物稳定 |
| B.T的最高价氧化物对应的水化物可能为强碱 |
| C.Q的原子半径比T的小 |
| D.W和Q的原子序数相差10 |
您最近一年使用:0次
2022-01-07更新
|
448次组卷
|
6卷引用:甘肃省兰州市教育局第四片区2021-2022学年高一上学期期末考试化学试题
甘肃省兰州市教育局第四片区2021-2022学年高一上学期期末考试化学试题甘肃省民勤县第一中学2022-2023学年 高一下学期开学考试化学试题甘肃省武威市民勤县第一中学2023-2024学年高二上学期开学考试化学试题(已下线)专题33 元素的综合推断-2022年高考化学毕业班二轮热点题型归纳与变式演练(全国通用)(已下线)4.2.2 元素周期表和元素周期律的应用-2022-2023学年高一化学上学期课后培优分级练(人教版2019必修第一册)新疆生产建设兵团第二中学2022-2023学年高一上学期期末考试化学试题
3 . 密闭容器中有甲、乙、丙、丁四种物质,在一定条件下反应,测得反应前后各物质的质量分数如图所示。下列说法正确的是


| A.丙可能是单质 |
| B.丁一定是该反应的催化剂 |
| C.甲、乙的质量之和一定等于生成丙的质量 |
| D.若消耗3g的乙,则生成17g的丙 |
您最近一年使用:0次
2020-08-16更新
|
44次组卷
|
2卷引用:甘肃省庆阳第一中学2018-2019学年高一上学期开学考试化学试题
名校
4 . (1)3.01×1023个NH 含有电子的物质的量是
含有电子的物质的量是__ ;
(2)200mL2mol/L的Al2(SO4)3溶液中SO 的物质的量浓度为
的物质的量浓度为__ ;
(3)标准状况下,将224LNH3溶于330mL水形成溶液(密度为0.8g/ml),该溶液的物质的量浓度为__ mol/L;
(4)已知质量分数为98%的硫酸密度为1.84g/mL,试计算其物质的量浓度为___ mol/L。
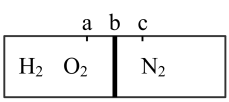
(5)如图所示在一个密闭容器中有一可自由滑动的隔板,室温下左端充入H2和O2的混合气,右端充入N2,开始时隔板在c处,电火花引燃左端气体充分反应后恢复至原来的温度,此时隔板在b处,且左端气体密度大于相同条件下空气密度,则原混合气体中H2和O2的体积比是___ ;原混合气体平均相对分子质量是___ 。
 含有电子的物质的量是
含有电子的物质的量是(2)200mL2mol/L的Al2(SO4)3溶液中SO
 的物质的量浓度为
的物质的量浓度为(3)标准状况下,将224LNH3溶于330mL水形成溶液(密度为0.8g/ml),该溶液的物质的量浓度为
(4)已知质量分数为98%的硫酸密度为1.84g/mL,试计算其物质的量浓度为
(5)如图所示在一个密闭容器中有一可自由滑动的隔板,室温下左端充入H2和O2的混合气,右端充入N2,开始时隔板在c处,电火花引燃左端气体充分反应后恢复至原来的温度,此时隔板在b处,且左端气体密度大于相同条件下空气密度,则原混合气体中H2和O2的体积比是

您最近一年使用:0次
2020-08-28更新
|
168次组卷
|
3卷引用:甘肃省武威第六中学2021届高三上学期第一次过关考试(开学考试)化学试题
甘肃省武威第六中学2021届高三上学期第一次过关考试(开学考试)化学试题(已下线)专题02 物质的量在化学实验中的应用(限时精练)-2022届高考化学一轮复习热点题型归纳与变式训练黑龙江省齐齐哈尔市恒昌中学校2022-2023学年高三上学期开学考试化学试题
解题方法
5 . 碱式氯化铝是某种高效净水剂的主要成分,实验室利用铝土矿(主要含Al2O3,还含少量Fe2O3、SiO2等杂质)制取碱式氯化铝的过程如下:

(1)溶解铝土矿需要使用质量分数为15%的盐酸,配制该盐酸所需的玻璃仪器有________
(2)盐酸溶解铝土矿的过程中,发生反应的离子方程式为____________ (写一个即可),其目的是__________________________________________________________ 。
(3)从不引入杂质去考虑,调节溶液的pH时加入的物质最好为__________ (填序号)。
A.NaOH B.Al C.氨水 D.Al2O3
(4)写出用pH试纸测定加入试剂X后所得溶液pH的操作:在白瓷板或玻璃片上放一小片pH试纸,________________________________________________ ,得出被测液的pH。
(5)实验室利用盐酸与大理石制取CO2的实验装置如图所示:

则各装置中导管从左到右的连接顺序为_________ ,装置C中盛放的试剂X为________ 。

(1)溶解铝土矿需要使用质量分数为15%的盐酸,配制该盐酸所需的玻璃仪器有
(2)盐酸溶解铝土矿的过程中,发生反应的离子方程式为
(3)从不引入杂质去考虑,调节溶液的pH时加入的物质最好为
A.NaOH B.Al C.氨水 D.Al2O3
(4)写出用pH试纸测定加入试剂X后所得溶液pH的操作:在白瓷板或玻璃片上放一小片pH试纸,
(5)实验室利用盐酸与大理石制取CO2的实验装置如图所示:

则各装置中导管从左到右的连接顺序为
您最近一年使用:0次
名校
6 . 短周期主族元素W、X、Y、Z的原子序数依次增大,W是地壳中含量最多的元素,W和Z位于同一主族,X的焰色反应为黄色,Y的最外层电子数比Z的最外层电子数少1,下列说法正确的是
| A.W、Z具有相同的最高正价 |
| B.X、Z形成的化合物水溶液呈碱性 |
| C.Y的最简单氢化物的热稳定性比Z的强 |
| D.原子半径:Z>Y> X> W |
您最近一年使用:0次
2020-03-27更新
|
147次组卷
|
3卷引用:甘肃省天水一中2020-2021学年高二上学期开学考试化学(文科)试题
7 . 观察与实验是学习化学的重要手段和方法,下列实验对应的描述不合理的是
| 实验内容 | 操作或现象 | 解释或结论 | |
| A | 铁丝在充满氧气的集气瓶中燃烧 | 火星四射,并有黑色固体生成 | 黑色固体是 |
| B | 将氧化铜与碳粉混合高温加热 | 有红色物质生成 | 说明碳有还原性 |
| C | 常温下,同时分别向同体积的盛有空气样品和呼出气体样品的集气瓶中滴加相同滴数的饱和澄清石灰水,振荡 | 盛有空气样品集气瓶中无浑浊现象,盛有呼出气体样品的集气瓶中变浑浊 | 人体呼出气体中 的含量高于吸入空气中 的含量高于吸入空气中 的含量 的含量 |
| D | 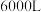 氧气在加压的情况下 氧气在加压的情况下 | 可装入容积为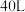 的钢瓶中 的钢瓶中 | 分子间有间隔 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2020-08-16更新
|
61次组卷
|
2卷引用:甘肃省庆阳第一中学2018-2019学年高一上学期开学考试化学试题
名校
解题方法
8 . A、B、C、D、E均为短周期元素,原子序数依次增大,请根据表中信息回答下列问题:
(1)G在元素周期表中的位置________ 。
(2)B最简单气态氢化物的结构式____ ,属于____ 化合物(填“离子”或“共价”);E的最高价氧化物的水化物电子式____ ,所含化学键类型________ 。
(3)C、D、E、F、G简单离子半径由大到小顺序为:____ (填离子符号)。
(4)用电子式表示G的氢化物的形成过程______ 。
(5)A元素的某氧化物与E元素的某含氧化合物反应生成单质的化学方程式是_______ 。
(6)E、F两元素最高价氧化物对应水化物相互反应的离子方程式:____ 。
| 元素 | 元素性质或结构 |
| A | 最外层电子数是其内层电子数的2倍 |
| B | B元素的单质在空气中含量最多 |
| C | C元素在地壳中含量最多 |
| D | D是同周期中原子半径最小的元素 |
| E | E元素在同周期中金属性最强 |
| F | F元素的最外层电子数等于周期序数 |
| G | G元素原子M层上电子数比L上少2个电子。 |
(2)B最简单气态氢化物的结构式
(3)C、D、E、F、G简单离子半径由大到小顺序为:
(4)用电子式表示G的氢化物的形成过程
(5)A元素的某氧化物与E元素的某含氧化合物反应生成单质的化学方程式是
(6)E、F两元素最高价氧化物对应水化物相互反应的离子方程式:
您最近一年使用:0次



