1 . 氢化钙(CaH2)是种白色细颗粒状固体,能与水发生剧烈反应,其反应的化学方程式为:CaH2+2H2O=Ca(OH)2+2H2↑,常用作登山运动员的能源提供剂。
(1)某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是___________ (填写化学式)。
为进步确定滤液中所含溶质的成分,他们进行了以下实验探究。
【提出猜想】
(2)猜想一:NaOH;
猜想二:NaOH和Na2CO3;
猜想三:___________ ;
猜想四:NaOH、Na2CO3、Ca(OH)2。
经过分析,大家一致认为上述猜想___________ 不需要验证,肯定是错误的,原因是___________ (用化学方程式表示)。
【实验探究】
(3)方案一:取一定量的滤液于试管中,往其中滴加少量稀盐酸,无明显实验现象。
方案二:取一定量的滤液于另一试管中,往其中滴加氯化钡溶液,观察到___________ 。
【讨论交流】
(4)根据实验现象,得出猜想___________ 是正确的。请解释方案一中无明显现象的原因是___________ 。
【拓展探究】
(5)上述小组同学将5g氢化钙样品(所含杂质不参与反应也不溶于水)加入到50g碳酸钠溶液中,充分混合后,恰好完全反应。实验测得反应过程中产生气体的质量为0.4g。计算:
①样品中CaH2的质量分数为___________ 。
②原碳酸钠溶液中溶质的质量为___________ 。
③反应后溶液中溶质的质量分数为___________ 。(计算结果保留一位小数)
(1)某化学实验小组为了探究氢化钙的性质,将一定量的CaH2加入到碳酸钠溶液中,立即产生大量气泡,且溶液变浑浊。充分反应后过滤,得到滤渣和滤液,滤渣的主要成分是
为进步确定滤液中所含溶质的成分,他们进行了以下实验探究。
【提出猜想】
(2)猜想一:NaOH;
猜想二:NaOH和Na2CO3;
猜想三:
猜想四:NaOH、Na2CO3、Ca(OH)2。
经过分析,大家一致认为上述猜想
【实验探究】
(3)方案一:取一定量的滤液于试管中,往其中滴加少量稀盐酸,无明显实验现象。
方案二:取一定量的滤液于另一试管中,往其中滴加氯化钡溶液,观察到
【讨论交流】
(4)根据实验现象,得出猜想
【拓展探究】
(5)上述小组同学将5g氢化钙样品(所含杂质不参与反应也不溶于水)加入到50g碳酸钠溶液中,充分混合后,恰好完全反应。实验测得反应过程中产生气体的质量为0.4g。计算:
①样品中CaH2的质量分数为
②原碳酸钠溶液中溶质的质量为
③反应后溶液中溶质的质量分数为
您最近一年使用:0次
名校
解题方法
2 . 下列实验方案能达到实验目的的是
| 选项 | 实验目的 | 实验方案 |
| A | 检验纯碱入中是否存在NaCl | 向待测液中加入AgNO3溶液 |
| B | 检验新制氯水的酸碱性 | 将pH试纸放在玻璃片上,用玻璃棒蘸取新制氯水点在试纸中部,再与标准比色卡对照 |
| C | 除去CO2气体中混杂的少量HCl气体 | 将混合气体依次通过盛有饱和NaHCO3溶液和浓硫酸的洗气瓶 |
| D | 测定NaHCO3和CaCO3固体混合物中的NaHCO3质量分数 | 准确称取ag样品和试管总质量。充分加热后冷却至室温,再称量总质量为bg |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2024-02-19更新
|
78次组卷
|
3卷引用:福建省师范大学附属中学2023-2024学年高一上学期期末考试化学试题
名校
解题方法
3 . 填空题
(1)① 中的质子数为
中的质子数为___________ ,电子数为___________ 。
② 中的质子数为
中的质子数为___________ ,电子数为___________ 。
③ 中的质子数为
中的质子数为___________ ,电子数为___________ 。
(2)含氧元素质量相同的 和
和 ,两者中硫原子个数比为
,两者中硫原子个数比为___________ ,两者的质量比为___________ 。
(3)把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要加水___________ g。
(4)镓属于活泼金属,镓( )元素与铝元素化学性质相似,请写出镓(
)元素与铝元素化学性质相似,请写出镓( )与稀硫酸反应的化学方程式为
)与稀硫酸反应的化学方程式为___________ 。
(1)①
 中的质子数为
中的质子数为②
 中的质子数为
中的质子数为③
 中的质子数为
中的质子数为(2)含氧元素质量相同的
 和
和 ,两者中硫原子个数比为
,两者中硫原子个数比为(3)把50g质量分数为98%的浓硫酸稀释为质量分数为20%的硫酸溶液,需要加水
(4)镓属于活泼金属,镓(
 )元素与铝元素化学性质相似,请写出镓(
)元素与铝元素化学性质相似,请写出镓( )与稀硫酸反应的化学方程式为
)与稀硫酸反应的化学方程式为
您最近一年使用:0次
4 . 将质量为15g锌片浸入100.2克硫酸铜溶液中,一段时间后,取出锌片,洗涤、干燥、称量,锌片的质量为14.8克。(写出计算过程)
(1)生成铜的质量为多少?_______
(2)剩余的溶液中生成硫酸锌的质量分数为多少?_________
(1)生成铜的质量为多少?
(2)剩余的溶液中生成硫酸锌的质量分数为多少?
您最近一年使用:0次
名校
5 . 截止2022年8月1日,全球累计确诊新冠肺炎人数已经超过5.2亿,过氧乙酸是广谱、高效、速效的消毒杀菌剂,其分子结构如图所示,下列有关说法不正确的是
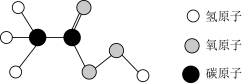

| A.1个过氧乙酸分子中共有9个原子 |
| B.过氧乙酸属于氧化物 |
| C.过氧乙酸分子中C、H、O原子个数比为2:4:3 |
| D.过氧乙酸中氧元素的质量分数最高 |
您最近一年使用:0次
名校
解题方法
6 . 铝镁合金是飞机制造、建筑等行业的重要材料。为测定某铝镁合金(不含其他元素)中铝的质量分数,将一定量铝镁合金与足量稀硫酸反应,设计了下列实验方案进行探究。回答下列问题:
(1)同学们拟选用下列实验装置中的某些装置完成实验:
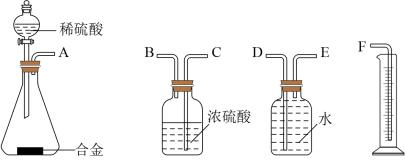
你认为最简易的装置的连接顺序是A→_______ ;连接好装置后首先应进行的操作是_______ 。
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接集气瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了如图所示的实验装置。

①装置中导管a的作用除了_______ 以外,从精确测量氢气体积的角度分析,还有一个作用是滴入锥形瓶的稀硫酸体积等于进入分液漏斗的气体体积,从而消除由于加入稀硫酸引起的氢气体积误差。
②已知金属与酸的反应是放热反应,为了较准确测量室温、一个标准大气压下氢气的体积,在读反应后量气管乙中液面的读数求氢气体积的过程中,除视线平视外还应注意_______ (填字母)。
A.冷却至室温再读数
B.乙管中液面不再上升时应该及时读数
C.读数时应上下移动量气管乙,使甲、乙中液面左右相平
D.读数时不必使甲、乙中液面左右相平
③若实验用铝镁合金的质量为5.1g,测得氢气体积为5.6L(已换算为标准状况),则合金中铝的质量分数为_______ (保留两位有效数字)。
(3)有同学提出把分液漏斗中的稀硫酸换成氢氧化钠溶液也可以测定铝镁合金中铝的质量分数和铝的相对原子质量,若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),锥形瓶中剩余固体的质量为cg,则铝的相对原子质量为_______ (用a、b、c表示)。
(1)同学们拟选用下列实验装置中的某些装置完成实验:

你认为最简易的装置的连接顺序是A→
(2)仔细分析实验装置后,同学们经讨论认为以下两点会引起较大误差:稀硫酸滴入锥形瓶中,即使不生成氢气,也会将瓶内空气排出,使所测氢气体积偏大;实验结束时,连接集气瓶和量筒的导管中有少量水存在,使所测氢气体积偏小。于是他们设计了如图所示的实验装置。

①装置中导管a的作用除了
②已知金属与酸的反应是放热反应,为了较准确测量室温、一个标准大气压下氢气的体积,在读反应后量气管乙中液面的读数求氢气体积的过程中,除视线平视外还应注意
A.冷却至室温再读数
B.乙管中液面不再上升时应该及时读数
C.读数时应上下移动量气管乙,使甲、乙中液面左右相平
D.读数时不必使甲、乙中液面左右相平
③若实验用铝镁合金的质量为5.1g,测得氢气体积为5.6L(已换算为标准状况),则合金中铝的质量分数为
(3)有同学提出把分液漏斗中的稀硫酸换成氢氧化钠溶液也可以测定铝镁合金中铝的质量分数和铝的相对原子质量,若实验用铝镁合金的质量为ag,测得氢气体积为bmL(已换算为标准状况),锥形瓶中剩余固体的质量为cg,则铝的相对原子质量为
您最近一年使用:0次
2022-08-17更新
|
324次组卷
|
6卷引用:福建省福清第一中学2023-2024学年高一下学期开学适应性练习化学试题
名校
7 . 为测定过氧化钠样品(只含 杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,下列说法正确的是
杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,下列说法正确的是
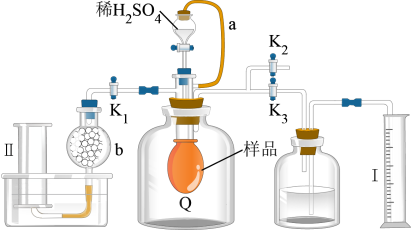
 杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,下列说法正确的是
杂质)的纯度,设计了如图所示的实验装置,图中Q为弹性良好的气球,称取一定量的样品放入其中,按图安装好仪器,下列说法正确的是
A.Q中发生反应的离子方程式为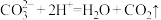 , ,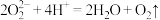 |
B.先关闭 、 、 ,打开 ,打开 ,用量筒I测量气体体积;再缓缓打开 ,用量筒I测量气体体积;再缓缓打开 ,用量筒II测量气体体积(残留的 ,用量筒II测量气体体积(残留的 忽略不计) 忽略不计) |
| C.没有导管a稀硫酸不易滴下来,而且会导致测量气体的体积偏大 |
D.若操作正确,量筒I中收集 水,量筒II中收集 水,量筒II中收集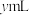 水, 水, 的质量分数为 的质量分数为 |
您最近一年使用:0次
2022-08-05更新
|
493次组卷
|
4卷引用:福建省福安市第一中学2023届高三上学期开学考试化学试题
福建省福安市第一中学2023届高三上学期开学考试化学试题福建省福清第一中学2023-2024学年高三上学期10月月考化学试题广东省2023届高三上学期开学联考化学试题(已下线)易错点05 钠及其化合物-备战2023年高考化学考试易错题
名校
8 . 下列实验方法能达到实验目的的是
| 选项 | 实验目的 | 实验方法 |
| A | 配制质量分数为5%的KNO3溶液 | 向盛有5.0gKNO3固体的烧杯中,加入100g水,搅拌 |
| B | 验证Al、Cu、Ag的金属活动性顺序 | 向CuSO4溶液和AgNO3溶液中各放入大小、形状相同的Al丝 |
| C | 鉴别CuSO4、BaSO4和CaCO3三种白色固体 | 分别取少量固体样品,加适量水,搅拌 |
| D | 检验氢气的纯度 | 用拇指堵住集满氢气的试管口,管口向下靠近火焰,移开拇指点火 |
| A.A | B.B | C.C | D.D |
您最近一年使用:0次
2021-11-03更新
|
128次组卷
|
3卷引用:福建省龙岩第一中学2021-2022学年高一上学期入学能力测试化学试题
名校
9 . 某校化学研究性学习小组设计如下实验方案,测定放置已久的NaHCO3样品中Na2CO3的质量分数。填写下列空白。
【方案一】气体吸收法:按下图装置进行实验。(碱石灰可吸收水、酸性气体)
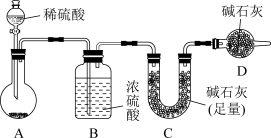
(1)实验前应先________ ;
(2)D装置的作用是_______ 。
(3)实验中除称量样品质量外,还需称_______ 装置(用字母表示)在反应前后质量的变化。
(4)根据此实验得到的数据,测定结果有较大误差。因为实验装置还存在一个明显缺陷,该缺陷是_____ 。
【方案二】沉淀法:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氢氧化钙溶液,过滤洗涤,干燥沉淀,称量固体质量,计算:
(5)洗涤沉淀的方法是_______
(6)已知称得样品5.7g,干燥后的沉淀质量为6.0g,则样品中碳酸钠的质量分数为______ %
【方案一】气体吸收法:按下图装置进行实验。(碱石灰可吸收水、酸性气体)

(1)实验前应先
(2)D装置的作用是
(3)实验中除称量样品质量外,还需称
(4)根据此实验得到的数据,测定结果有较大误差。因为实验装置还存在一个明显缺陷,该缺陷是
【方案二】沉淀法:称取一定量样品,置于小烧杯中,加适量水溶解,向小烧杯中加入足量氢氧化钙溶液,过滤洗涤,干燥沉淀,称量固体质量,计算:
(5)洗涤沉淀的方法是
(6)已知称得样品5.7g,干燥后的沉淀质量为6.0g,则样品中碳酸钠的质量分数为
您最近一年使用:0次
名校
解题方法
10 . Fe、FeO和Fe3O4的混合物,测得其中铁元素质量分数为80%。取该混合物7.0g,加足量稀硫酸完全溶解,生成FeSO4的质量为
| A.7.6g | B.15.2g | C.20.0g | D.40.0g |
您最近一年使用:0次



