名校
1 . 有四种短周期元素,它们的结构或性质等信息如表所述。
请根据表中信息填写:
(1)写出C元素的名称_______ ;D元素的元素符号_______ 。
(2)B元素在周期表中的位置:_______ ;A和B的简单离子半径关系是_______ >_______ (填离子符号)。
(3)基态A元素原子核外电子占据的最高能层包含的原子轨道数为_______ 。
(4)D原子的核外电子排布式为_______ ,其原子核外有_______ 个未成对电子。
(5)B和D的最高价氧化物对应的水化物能发生反应,其离子方程式是_______ 。
| 元素 | 结构或性质 |
| A | A是短周期中(除稀有气体外)原子半径最大的元素,该元素的某种合金是原子反应堆的导热剂 |
| B | B与A同周期,其最高价氧化物的水化物呈两性 |
| C | 元素的气态氢化物极易溶于水,且水溶液显碱性 |
| D | D是海水中除氢、氧元素外含量最多的元素,其单质或化合物也是自来水生产过程中常用的消毒杀菌剂 |
(1)写出C元素的名称
(2)B元素在周期表中的位置:
(3)基态A元素原子核外电子占据的最高能层包含的原子轨道数为
(4)D原子的核外电子排布式为
(5)B和D的最高价氧化物对应的水化物能发生反应,其离子方程式是
您最近一年使用:0次
解题方法
2 . 某种化合物是工业洗涤剂的中间体,其结构如下图所示。其中X、Y、Z、Q、W为原子序数依次增大的五种短周期元素,Q最外层电子数与Y核外电子总数相同,X的原子半径是元素周期表中最小的。回答下列问题:
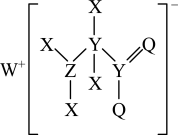
(1)写出Q元素在周期表中的位置:_______ ,Z单质的电子式:_______ 。
(2)Y、Z、Q三种元素所形成的最简单气态氢化物中,稳定性最强的是_______ (填化学式);X、Y、Z、Q四种元素组成的化合物中,既含离子键又含共价键的是_______ (填化学式)。
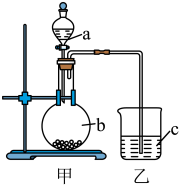
(3)利用如下图装置可比较Y、Z两元素得电子能力,b中发生反应的化学方程式为_______ 。

(1)写出Q元素在周期表中的位置:
(2)Y、Z、Q三种元素所形成的最简单气态氢化物中,稳定性最强的是
(3)利用如下图装置可比较Y、Z两元素得电子能力,b中发生反应的化学方程式为

您最近一年使用:0次
名校
解题方法
3 . 二草酸合铜(Ⅱ)酸钾(K2[Cu(C2O4)2])可用于无机合成、功能材料制备。实验室制备二草酸合铜(Ⅱ)酸钾可采用如下步骤:
Ⅰ.取已知浓度的CuSO4溶液,搅拌下滴加足量NaOH溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
Ⅱ.向草酸(H2C2O4)溶液中加入适量K2CO3固体,制得KHC2O4和K2C2O4混合溶液。
Ⅲ将Ⅱ的混合溶液加热至80~85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
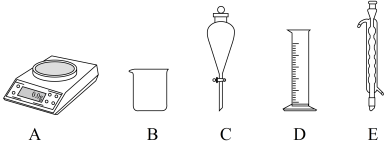
(1)由CuSO4•5H2O配制Ⅰ中的CuSO4溶液,下列仪器中不需要的有________ (填对应字母)。
(2)长期存放的CuSO4•5H2O中,会出现少量白色固体,原因是_______ 。
(3)Ⅰ中的黑色沉淀可能是________ (写化学式)。
(4)Ⅱ中原料配比为n(H2C2O4):n(K2CO3)=3:2,写出反应的化学方程式______ 。
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入K2CO3时应采取_______ 的方法。
(6)Ⅲ中应采用________ 进行加热。
(7)Ⅳ中“一系列操作”包括________ 。
Ⅰ.取已知浓度的CuSO4溶液,搅拌下滴加足量NaOH溶液,产生浅蓝色沉淀。加热,沉淀转变成黑色,过滤。
Ⅱ.向草酸(H2C2O4)溶液中加入适量K2CO3固体,制得KHC2O4和K2C2O4混合溶液。
Ⅲ将Ⅱ的混合溶液加热至80~85℃,加入Ⅰ中的黑色沉淀。全部溶解后,趁热过滤。
Ⅳ.将Ⅲ的滤液用蒸汽浴加热浓缩,经一系列操作后,干燥,得到二草酸合铜(Ⅱ)酸钾晶体,进行表征和分析。
回答下列问题:
(1)由CuSO4•5H2O配制Ⅰ中的CuSO4溶液,下列仪器中不需要的有

(2)长期存放的CuSO4•5H2O中,会出现少量白色固体,原因是
(3)Ⅰ中的黑色沉淀可能是
(4)Ⅱ中原料配比为n(H2C2O4):n(K2CO3)=3:2,写出反应的化学方程式
(5)Ⅱ中,为防止反应过于剧烈而引起喷溅,加入K2CO3时应采取
(6)Ⅲ中应采用
(7)Ⅳ中“一系列操作”包括
您最近一年使用:0次
名校
解题方法
4 . 常温下,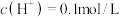 的某溶液中可能有
的某溶液中可能有 中的某几种,现取100mL该溶液进行如图实验。
中的某几种,现取100mL该溶液进行如图实验。

已知:单质碘是紫黑色固体,且氧化性 。
。
根据上述实验,回答下列问题:
(1)步骤①的实验操作名称是_____ ,步骤①中生成紫黑色固体单质的离子方程式是_____ 。
(2)此溶液中_____ (填“是”或“否”)存在 。若存在,则其物质的量浓度为
。若存在,则其物质的量浓度为_____ (若不存在,此问不作答)
(3)该溶液中一定不存在的离子有_____ 。
(4)根据整个实验过程推断 是否存在并说明理由。
是否存在并说明理由。_____ 。若存在,计算其物质的量浓度_____ 。(若不存在,此问不作答)
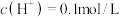 的某溶液中可能有
的某溶液中可能有 中的某几种,现取100mL该溶液进行如图实验。
中的某几种,现取100mL该溶液进行如图实验。
已知:单质碘是紫黑色固体,且氧化性
 。
。根据上述实验,回答下列问题:
(1)步骤①的实验操作名称是
(2)此溶液中
 。若存在,则其物质的量浓度为
。若存在,则其物质的量浓度为(3)该溶液中一定不存在的离子有
(4)根据整个实验过程推断
 是否存在并说明理由。
是否存在并说明理由。
您最近一年使用:0次
名校
5 . 实验室工作人员现用 晶体配制0.2
晶体配制0.2 的
的 溶液480mL。请回答下列问题:
溶液480mL。请回答下列问题:
(1)应称取 晶体的质量:
晶体的质量:_____ 。
(2)根据下列操作对所配溶液的浓度产生的影响,完成下列问题:
① 晶体失去了部分结晶水
晶体失去了部分结晶水
②用“左码右物”的称量方法称量晶体(使用游码)
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥使用
其中引起所配溶液浓度偏高的有_____ (填序号,下同),无影响的有_____ 。
(3)下列操作中,容量瓶所不具备的功能有_____ (填序号)。
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.稀释某一浓度的浓溶液
E.加热溶解固体溶质
(4)某同学改用固体 配制上述
配制上述 溶液的过程如图所示:
溶液的过程如图所示:

你认为该同学的错误步骤有_____(填序号)。
 晶体配制0.2
晶体配制0.2 的
的 溶液480mL。请回答下列问题:
溶液480mL。请回答下列问题:(1)应称取
 晶体的质量:
晶体的质量:(2)根据下列操作对所配溶液的浓度产生的影响,完成下列问题:
①
 晶体失去了部分结晶水
晶体失去了部分结晶水②用“左码右物”的称量方法称量晶体(使用游码)
③碳酸钠晶体不纯,其中混有氯化钠
④称量碳酸钠晶体时所用砝码生锈
⑤容量瓶未经干燥使用
其中引起所配溶液浓度偏高的有
(3)下列操作中,容量瓶所不具备的功能有
A.配制一定体积准确浓度的标准溶液
B.贮存溶液
C.测量容量瓶规格以下的任意体积的液体
D.稀释某一浓度的浓溶液
E.加热溶解固体溶质
(4)某同学改用固体
 配制上述
配制上述 溶液的过程如图所示:
溶液的过程如图所示:
你认为该同学的错误步骤有_____(填序号)。
| A.1处 | B.2处 | C.3处 | D.4处 |
您最近一年使用:0次
名校
解题方法
6 . 某学习小组为证实Ba(OH)2溶液和H2SO4溶液的反应是离子反应,设计了如下实验。请把该实验报告补充完整。
(1)【实验原理】溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察___________ ,据此判断溶液中自由移动的离子浓度的变化,从而证明反应是离子反应。
【实验装置】如图1所示。

【实验过程与记录】
(2)整个过程中混合溶液的导电能力(用电流强度I表示)可近似地用图2中的曲线___________ (填字母)表示。

(3)书写下列两种情况的离子方程式。
①向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至 恰好完全沉淀:
恰好完全沉淀: ___________ 。
②向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性:___________ 。
(4)已知:PbSO4难溶于水,但可溶于醋酸氨溶液中形成无色溶液,生成的(CH3COO)2Pb是难电离的物质,其化学方程式为PbSO4+2CH3COONH4= (CH3COO)2Pb+(NH4)2SO4,写出该反应的离子方程式:___________ 。
(1)【实验原理】溶液的导电性由溶液中离子的浓度及离子电荷数决定。观察
【实验装置】如图1所示。

【实验过程与记录】
| 实验步骤 | 实验现象 | 实验结论 |
| 连接好装置,向烧杯中加入25 mL一定浓度的Ba(OH)2溶液和2滴酚酞溶液,逐滴滴加一定浓度的H2SO4溶液直至过量,边滴边振荡 | Ba(OH)2溶液和H2SO4溶液的反应是离子反应 |

(3)书写下列两种情况的离子方程式。
①向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至
 恰好完全沉淀:
恰好完全沉淀: ②向NaHSO4溶液中,逐滴加入Ba(OH)2溶液至溶液显中性:
(4)已知:PbSO4难溶于水,但可溶于醋酸氨溶液中形成无色溶液,生成的(CH3COO)2Pb是难电离的物质,其化学方程式为PbSO4+2CH3COONH4= (CH3COO)2Pb+(NH4)2SO4,写出该反应的离子方程式:
您最近一年使用:0次
名校
7 . 利用如图装置可验证非金属元素的非金属性的变化规律:

(1)仪器A的名称为_____ 。
(2)请选择合适药品设计实验验证Cl、C、Si的非金属性的变化规律;装置A、C中所装药品分别为_____ 、_____ (填化学式)。
(3)C装置中发生的化学反应为:______ 。

(1)仪器A的名称为
(2)请选择合适药品设计实验验证Cl、C、Si的非金属性的变化规律;装置A、C中所装药品分别为
(3)C装置中发生的化学反应为:
您最近一年使用:0次
解题方法
8 . 铁及其化合物间的转化关系如下图所示,请回答下列问题:

(1)写出A和B的化学式:A_______ ;B_______ 。
(2)Fe(OH)2中铁元素的化合价是_______ 。
(3)检验 K+的实验方法是_______ (选填“焰色试验”或“化学沉淀法”)。
(4)合金钢具有各种特殊性能,如强度、硬度大,可塑性、韧性好。据此可知合金钢比纯铁具有更优良的_______ (选填“物理”或“化学”)性能。
(5)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂。主要用于饮用水处理,Na2FeO4属于_______ 类(选填“酸”、“碱”、“盐”)。
(6)工业炼铁的原理是Fe2O3+3CO 2Fe+3CO2,据此原理可知工业上铁的冶炼方法是
2Fe+3CO2,据此原理可知工业上铁的冶炼方法是_______ (填序号)。
①热分解法 ②热还原法 ③电解法

(1)写出A和B的化学式:A
(2)Fe(OH)2中铁元素的化合价是
(3)检验 K+的实验方法是
(4)合金钢具有各种特殊性能,如强度、硬度大,可塑性、韧性好。据此可知合金钢比纯铁具有更优良的
(5)高铁酸钠(Na2FeO4)是一种新型绿色消毒剂。主要用于饮用水处理,Na2FeO4属于
(6)工业炼铁的原理是Fe2O3+3CO
 2Fe+3CO2,据此原理可知工业上铁的冶炼方法是
2Fe+3CO2,据此原理可知工业上铁的冶炼方法是①热分解法 ②热还原法 ③电解法
您最近一年使用:0次
解题方法
9 . 氯气的实验室制备、收集及尾气处理装置如下图所示,请回答下列问题:

(1)完成下列化学方程式:MnO2+4HCl(浓) MnCl2+
MnCl2+_____ +2H2O
(2)图中仪器A的名称是_______ ;仪器B的名称是_______ (选填“圆底烧瓶、平底烧瓶、分液漏斗、长颈漏斗”)。
(3)氯气是一种_______ 色、有刺激性气味的气体。
(4)用向上排空气法收集氯气的原因是:氯气的密度比空气的密度_______ (选填“大”或“小”)。
(5)氯气的水溶液呈_______ (选填“酸”或“碱”)性。
(6)氯气有毒,烧杯中的溶液可用于吸收氯气,烧杯中盛装的是_______ (选填“NaOH”或“HCl”)溶液。
(7)氯气用途广泛,请列举一种氯气的用途_______ 。

(1)完成下列化学方程式:MnO2+4HCl(浓)
 MnCl2+
MnCl2+(2)图中仪器A的名称是
(3)氯气是一种
(4)用向上排空气法收集氯气的原因是:氯气的密度比空气的密度
(5)氯气的水溶液呈
(6)氯气有毒,烧杯中的溶液可用于吸收氯气,烧杯中盛装的是
(7)氯气用途广泛,请列举一种氯气的用途
您最近一年使用:0次
解题方法
10 . 某同学利用如下实验装置制备少量的漂白粉。回答下列问题:

(1)漂白粉的有效成分是_________ (填化学式)。
(2)仪器a的名称是_________ ,利用二氧化锰和浓盐酸制取氯气的化学方程式为_________ 。
(3)装置B中反应放热会使体系温度升高,导致氯气和石灰浆发生副反应产生杂质Ca(ClO3)2,为防止该副反应发生,可采取的措施是_________ 。
(4)C中发生反应的离子方程式为_________ 。

(1)漂白粉的有效成分是
(2)仪器a的名称是
(3)装置B中反应放热会使体系温度升高,导致氯气和石灰浆发生副反应产生杂质Ca(ClO3)2,为防止该副反应发生,可采取的措施是
(4)C中发生反应的离子方程式为
您最近一年使用:0次



